Введение
Параректальный свищ (свищ прямой кишки, анальная фистула) – это патологический ход между полостью прямой кишки и перианальной кожей, включающий наружное, внутреннее отверстие фистулы, а также эпителизированный трубчатый канал, расположенный в мягких тканях параректальной области [1].
Заболеваемость параректальными свищами, по данным Ю.А. Шелыгина с соавт., составляет 1,2–2,8 случая на 10 тыс. населения в год [1].
Клинически данная патология наиболее часто проявляется болезненными ощущениями, наличием дефекта кожного покрова в перианальной области (наружное свищевое отверстие при полной анальной фистуле) с поступлением из него выделений серозного или гнойного характера, периодическим обострением в форме образования болезненного уплотнения в параректальной клетчатке, что может значительно снижать качество жизни пациента, оказывать негативное влияние на психоэмоциональное и физическое здоровье [1]. Важным фактом остается то, что наиболее часто заболевание встречается у лиц трудоспособного возраста, преимущественно мужского пола [2].
Основным способом лечения параректальных свищей является хирургический. Главными задачами любого из методов хирургического лечения представляются полная ликвидация фистулы при сохранении нормальной анатомической структуры и функции анального сфинктера, минимизация риска развития рецидива. Метод оперативного лечения напрямую зависит от характера и расположения свища относительно тканей, окружающих прямую кишку [3]. На данный момент анальные фистулы классифицируются в зависимости: от наличия наружного свищевого отверстия (полные и неполные), от топографии фистулы относительно наружного сфинктера (интрасфинктерный, транссфинктерный и экстрасфинктерный), а также по степени «сложности» (простые и сложные). Одними из наиболее сложных для лечения являются транссфинктерные параректальные свищи, вовлекающие в патологический процесс более 30% анального сфинктера, и экстрасфинктерные фистулы [1]. Особенность лечения «сложных» свищей заключается в том, что при использовании традиционных методик, таких как рассечение свища в просвет кишки, иссечение свища с ушиванием сфинктера, часто развивается анальная инконтиненция [4].
Несмотря на наличие множества методов хирургического лечения, выделить один в качестве общепринятого золотого стандарта лечения «сложных» анальных фистул не представляется возможным. Высокая частота рецидивов, риск развития анальной инконтиненции, необходимость проведения повторных операций, по мнению авторов, свидетельствуют о необходимости создания новых способов хирургической коррекции этой патологии.
Цель исследования: оценить эффективность применения нового способа оперативного лечения транссфинктерных параректальных свищей в раннем и отделенном послеоперационном периодах.
Материалы и методы исследования
Проведено проспективное рандомизированное многоцентровое исследование на следующих базах: хирургическое и колопроктологическое отделение Клиник ФГБОУ ВО СамГМУ Минздрава России, хирургическое отделение лечебно-диагностического комплекса ООО «Медгард» в городе Самаре, хирургическое отделение № 2 Клинического госпиталя АО «Медицинская компания ИДК» в городе Самаре. В исследование были включены 104 пациента со «сложной» транссфинктерной анальной фистулой, срок проведения исследования – 4 года (с сентября 2021 года по сентябрь 2024 года).
Настоящее исследование проводилось в соответствии с утвержденным протоколом, этическими принципами Хельсинкской декларации Всемирной медицинской ассоциации (Сеул, 2008), трехсторонним Соглашением по надлежащей клинической практике (ICH GCP) и действующим законодательством РФ. Каждый пациент был информирован о проведении исследовательской работы, включении в изучаемые группы, было получено информированное добровольное согласие.
Критерии включения: возраст от 18 до 70 лет; наличие «сложной» полной транссфинктерной анальной фистулы криптогландулярной этиологии (в патологический процесс вовлечено более 30% наружного сфинктера); подписанное информированное добровольное согласие на участие в исследовании; оперативное вмешательство по поводу острого парапроктита проведено более 2 месяцев назад.
Критерии невключения: возраст моложе 18 и старше 70 лет; анальные фистулы других этиологий; интрасфинктерные, экстрасфинктерные, рецидивные параректальные фистулы; транссфинктерные свищи прямой кишки, вовлекающие менее 30% наружного сфинктера; гормонотерапия, химиотерапия, иммунодепрессивные состояния, наркомания, токсикомания, декомпенсированный сахарный диабет в анамнезе; отягощенный преморбидный фон; период беременности и лактации; сопутствующие онкологические заболевания; сепсис; наличие сопутствующих заболеваний прямой кишки и анального канала, влияющие на тонус сфинктера; воспалительные заболевания кишечника (язвенный колит, болезнь Крона); активный воспалительный процесс в параректальной клетчатке (острый парапроктит).
Первичный клинический исход – оценка выраженности болевого синдрома на 1-е, 3-и, 5-е и 10-е послеоперационные сутки при помощи визуально-аналоговой шкалы (VAS, ВАШ), сроков и вида заживления послеоперационных ран, а также учет ранних раневых осложнений.
Вторичный клинический исход – оценка функции запирательного аппарата прямой кишки и регистрация рецидива заболевания в случае обнаружения через 12 месяцев после оперативного вмешательства.
Распределение пациентов, включенных в исследование (n=104), осуществлялось методом конвертов при поступлении в стационар. Основная группа включала 54 пациента, которым хирургическое вмешательство проводилось по новому способу с применением нитей из сополимера L-лактида с ε-капролактоном (патент РФ на изобретение № 2753137 от 11.08.2021 г.). Контрольная группа включала 50 пациентов, которым была проведена операция LIFT (Ligation of Intersphincteric Fistula Tract, A. Rojanasakul, 2006). Все пациенты завершили исследование в полном объеме.
Распределение пациентов по гендерному признаку, возрасту, индексу массы тела (ИМТ) представлено в таблице 1.
Таблица 1
Распределение пациентов в изучаемых группах (n=104)
|
Показатели |
Основная группа (n=54) |
Контрольная группа (n=50) |
p-значение |
|||
|
Пол |
жен |
23 |
42,6% |
22 |
44,0% |
0,521 |
|
муж |
31 |
57,4% |
28 |
56,0% |
||
|
Возраст, полных лет |
Me (Q1; Q3) |
41,5 (34; 55,3) |
45,6 (38,5; 56,3) |
0,567 |
||
|
ИМТ, кг/м2 |
Me (Q1; Q3) |
25,2 (22,9; 29,3) |
25,7 (22,9; 29,8) |
0,567 |
||
Согласно представленным данным, статистически значимых различий между группами по гендерному признаку, возрасту и ИМТ не выявлено.
Все пациенты на амбулаторном этапе проходили стандартное предоперационное обследование согласно Российским клиническим рекомендациям по лечению свищей прямой кишки.
Все пациенты предъявляли схожие жалобы: на дискомфорт и наличие дефекта кожного покрова в перианальной области с мутными или гнойными выделениями, периодическое формирование болезненного уплотнения в данной области, сопровождающееся повышением температуры тела до субфебрильных значений. Длительность анамнеза в основной группе составила 7 (3; 10) месяцев, в контрольной – 8 (4; 12) месяцев. Для определения степени тяжести анальной инконтиненции в предоперационном периоде пациенты проходили анкетирование по Кливлендской шкале оценки анальной инконтиненции (Cleveland Clinic Continence Score questionnaire, Wexner score). По результатам анкетирования у всех пациентов изучаемых групп отсутствовали признаки анальной инконтиненции.
При изучении результатов лабораторных и инструментальных методов обследований отклонений от нормы не было.
Для объективной оценки состояния запирательного аппарата прямой кишки пациентам выполнена сфинктерометрия при помощи сфинктерометра Promedico Sphinctometer S 4402 (Германия). По результатам проведенной предоперационной сфинктерометрии патологии запирательного аппарата прямой кишки не выявлено.
Оперативное вмешательство, проведенное пациентам основной группы (n=54), включало следующие этапы:
1) ректальным зеркалом осуществляется ревизия анального канала с визуализацией внутреннего отверстия фистулы, проводятся прокрашивание и зондирование патологического хода пуговчатым зондом;
2) выполняются гидропрепаровка (0,5%-ным раствором новокаина) и мобилизация слизисто-подслизисто-мышечного лоскута стенки прямой кишки на 1/3 окружности анального канала до внутреннего отверстия фистулы и на 1,0 см выше него;
3) рубцово-измененные ткани в области внутреннего отверстия фистулы иссекаются, дефект ушивается рассасывающейся нитью «Vicril» 3/0 в подслизисто-мышечном слое;
4) окаймляющим разрезом иссекается дистальная часть фистулы от наружного отверстия до волокон сфинктера;
5) выполняется зондирование оставшейся части фистулы ершеобразным зондом-проводником (патент РФ на полезную модель № 205902 от 11.08.2021 г.), содержащим в просвете 3–4 самофиксирующиеся рассасывающиеся нити (metric 5) из сополимера L-лактида с ε-капролактоном. После удаления эпителиальной выстилки и тканевого детрита зонд выводится в проксимальном направлении с оставлением нитей в просвете фистулы (рис. 1) [5];
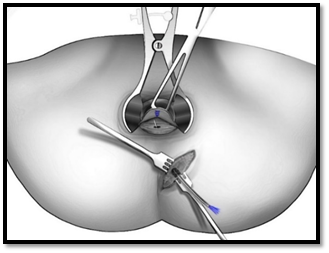
Рис. 1. Проведение ершеобразного зонда-проводника через фистулу
6) нити дополнительно фиксируются к волокнам сфинктера узловым Z-образным швом рассасывающейся нитью «Vicril» 3/0 со стороны раны в анальном канале (рис. 2);
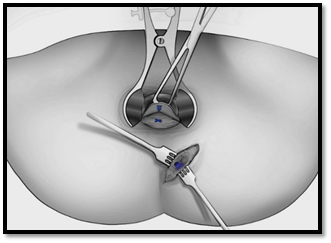
Рис. 2. Фиксация нитей со стороны раны анального канала Z-образным швом
7) осуществляется фиксация мобилизованного лоскута к перианальной коже без натяжения узловыми швами рассасывающейся нитью. Рана в перианальной области послойно ушивается отдельными узловыми швами рассасывающейся нитью с введением резинового выпускника в рану. В анальный канал вводится турунда с мазью «Диоксидин». На рану перианальной области накладывается асептическая повязка.
В контрольной группе (n=50) выполнялась стандартная операция LIFT, которая заключалась в выделении, перевязке и пересечении свищевого хода в межсфинктерном пространстве.
Эффективность оперативного лечения оценивалась в раннем послеоперационном периоде по следующим параметрам: степень выраженности болевого синдрома по визуально-аналоговой шкале боли, сроки и вид заживления раны, наличие раневых осложнений.
В отдаленном послеоперационном периоде (через 12 месяцев) критерием эффективности проведенного лечения были отсутствие рецидива заболевания и признаков анальной инконтиненции.
Для интерпретации полученных результатов в изучаемых группах нами введены критерии, представленные в таблице 2.
Таблица 2
Критерии оценки результатов лечения пациентов в изучаемых группах
|
Оценка результатов |
Критерий |
|
«Хорошие» |
· Отсутствие раневых осложнений в раннем послеоперационном периоде · Отсутствие признаков анальной инконтиненции · Отсутствие рецидива заболевания |
|
«Удовлетворительные» |
· Наличие раневых осложнений в раннем послеоперационном периоде · Отсутствие признаков анальной инконтиненции · Отсутствие рецидива заболевания |
|
«Неудовлетворительные» |
· Наличие/отсутствие раневых осложнений в раннем послеоперационном периоде · Наличие признаков анальной инконтиненции · Рецидив заболевания |
Статистические расчеты проводили с использованием пакетов прикладных программ SPSS 26 версия (USA) и Excel.
Проверку количественных показателей на соответствие нормальному распределению осуществляли с помощью критерия Шапиро–Уилка. В случае соответствия нормальному закону распределения показатели описывали с помощью среднего значения и стандартного отклонения (M(SD)), в ином случае показатели описывали медианой и квартилями (первым и третьим) (Me(Q1;Q3)). Качественные показатели описаны абсолютными значениями и долями (%).
В случае нормального распределения оценку статистической значимости различий в несвязанных группах проводили с применением критерия Стьюдента, при ином распределении использовали критерий Манна–Уитни. Для качественных переменных аналогичная задача решалась по результатам построения таблицы сопряженности с использованием критерия Пирсона или точечного критерия Фишера (для случая наличия в ячейках таблицы количества наблюдений, меньшего 5).
Для оценки значимости различий связанных выборок использовали критерий Вилкоксона (для 2 групп) и критерий Фридмана (для нескольких групп).
Расчеты проводились при уровне значимости 0,05.
Результаты исследования и их обсуждение
Результаты оценки выраженности болевого синдрома на 1-е, 3-и, 5-е и 10-е послеоперационные сутки представлены в таблице 3.
Таблица 3
Сравнение показателей выраженности болевого синдрома в основной и контрольной группах по VAS (ВАШ) (n=104)
|
Показатели |
Основная группа (n=54) |
Контрольная группа (n=50) |
p-значение |
|
1-е сутки после операции |
4 (3,8; 4,0) |
4 (3,0; 4,0) |
0,077 |
|
3-е сутки после операции |
2 (2,0; 3,0) |
2 (2,0; 3,0) |
0,994 |
|
5-е сутки после операции |
1 (1,0; 1,0) |
1 (1,0; 2,0) |
0,658 |
|
10-е сутки после операции |
0 (0; 0) |
0 (0; 0) |
0,277 |
При сравнении исследуемых групп по степени выраженности болевого синдрома статистически значимых различий не получено. Следует отметить, что обезболивание пациентов проводилось только путем введения нестероидных противовоспалительных препаратов (Кеторолак 2,0 мл в/м) в 1-е и 2-е послеоперационные сутки. Начиная с 3-х суток НПВС не применялись ввиду незначительного болевого синдрома.
В раннем послеоперационном периоде в обеих группах были зарегистрированы ранние раневые послеоперационные осложнения, которые представлены в таблице 4.
Таблица 4
Ранние раневые осложнения в группах сравнения (n=104)
|
Показатели |
Основная группа (n=54) |
Контрольная группа (n=50) |
p-значение |
|||
|
Кровотечение из п/о раны |
Нет |
51 |
94,4% |
45 |
90,0% |
0,477 |
|
Есть |
3 |
5,6% |
5 |
10,0% |
||
|
Нагноение п/о раны |
Нет |
51 |
94,4% |
42 |
84,0% |
0,113 |
|
Есть |
3 |
5,6% |
8 |
16,0% |
||
Сравнительный анализ исследуемых групп по виду и количеству ранних раневых осложнений показал, что статистических различий между группами нет.
Однако в количественном сравнении в основной группе отмечены меньшее количество осложнений в виде кровотечения из послеоперационной раны (3 (5,6%) эпизода в основной, 5 (10%) эпизодов в контрольной) и меньшее количество случаев нагноения послеоперационной раны (3 (5,6%) – в основной, 8 (16%) – в контрольной). Статистические различия не достигнуты в рамках текущей работы и, вероятнее всего, будут получены при изучении большего количества пациентов при дальнейших исследованиях.
Оценку сроков и вида заживления раны производили на основании записи врача-колопроктолога на амбулаторном этапе наблюдения за пациентами. Результаты сравнения исследуемых групп по этим показателям представлены в таблице 5.
Таблица 5
Сравнительная оценка изучаемых групп по сроку и виду заживления послеоперационных ран (n=104)
|
Показатели |
Основная группа (n=54) |
Контрольная группа (n=50) |
p-значение |
|||
|
Вид заживления раны |
Первичное |
51 |
94,4% |
42 |
84,0% |
0,078 |
|
Вторичное |
3 |
5,6% |
8 |
16,0% |
||
|
Срок заживления раны (дни) |
9,0 (8,0; 9,0) |
11,0 (10,0; 12,3) |
<0,001 |
|||
По данному показателю получены статистически значимые различия: заживление послеоперационных ран в основной группе происходило быстрее, чем в контрольной группе. Также стоит отметить, что в основной группе преобладало заживление первичным натяжением.
Средняя продолжительность госпитализации в основной и контрольной группах сопоставима (в основной – 4 (3,0; 4,3) дня, в контрольной – 4 (3,0; 5,3) дня).
Средняя длительность операции в основной группе составила 23,0 (20,0; 25,0) минуты, что незначительно дольше, чем в контрольной группе, – 17,0 (15,0; 20,0) минут. Увеличение длительности операции в основной группе связано с большим количеством этапов оперативного вмешательства.
Средние сроки реабилитации в основной группе оказались короче – 21,0 (20,0; 23,0) день, чем в контрольной – 25,0 (21,0; 30,0) дней, что связано с меньшим количеством ранних раневых послеоперационных осложнений.
Через 1 год после операции всем пациентам вновь выполнялась оценка функционального состояния запирательного аппарата прямой кишки. Пациенты в исследуемых группах (n=104) отмечали полный контроль за отхождением газов, жидкого и твердого кала (оценка по шкале Wexner). При проведении сфинктерометрии не было зарегистрировано случаев снижения тонуса сфинктера ниже референтных значений.
При анализе эффективности методик с точки зрения развития рецидива заболевания в изучаемых группах получены следующие данные: в основной группе в течение 1 года наблюдения возникло 5 (9,3%) рецидивов заболевания, в контрольной – 12 (24,0%). Таким образом, клиническая эффективность нового способа составляет 90,7%, традиционного способа (операция LIFT) – 76,0%. Показатели эффективности операции LIFT сопоставимы с литературными данными.
Итоговая оценка эффективности оперативного вмешательства в основной и контрольной группах представлена в таблице 6.
Таблица 6
Результаты оценки эффективности оперативного вмешательства в изучаемых группах (n=104)
|
Результат |
Основная группа (n=54) |
Контрольная группа (n=50) |
Всего |
|||
|
Хорошие |
46 |
85,2% |
34 |
68,0% |
80 |
76,9% |
|
Удовлетворительные |
3 |
5,6% |
4 |
8,0% |
7 |
6,7% |
|
Неудовлетворительные |
5 |
9,3% |
12 |
24,0% |
17 |
16,3% |
|
Всего |
54 |
100% |
50 |
100% |
104 |
100% |
|
р-значение |
0,046 |
|||||
Представленная таблица 6 демонстрирует, что в основной группе имеется наибольшее количество пациентов с «хорошим» результатом (46 – в основной, 34 – в контрольной). У 3 пациентов в основной группе и у 4 в контрольной получены «удовлетворительные» результаты. «Неудовлетворительные» результаты встречались преимущественно в контрольной группе – 12 случаев, тогда как в основной группе – лишь 5 случаев.
Лечение «сложных» параректальных свищей является непростой задачей в связи с высоким риском развития осложнений в раннем послеоперационном периоде и рецидива заболевания в дальнейшем [6]. Распространенность заболевания среди лиц трудоспособного возраста, выраженное снижение качества жизни при отсутствии лечения или при неудовлетворительном результате лечения обусловливают актуальность проблемы лечения данной категории пациентов.
К современным сфинктеросохраняющим операциям относятся: перемещение лоскута стенки прямой кишки, FiLaC, использование ауто- и аллотрансплантатов (Anal Fistula Plugs), применение мезенхимальных стволовых клеток, операция LIFT (Ligation Intersphincteric of the Fistula Tract).
В настоящее время активно применяется способ оперативного лечения «сложных» транссфинктерных параректальных свищей с использованием смещаемого лоскута слизистой прямой кишки для закрытия внутреннего отверстия свища – метод ERAF (Endorectal advancement Flap). Существуют различные вариации данного метода. Впервые данный способ лечения параректальных свищей описал Ashuast в конце XIX века [7]. Наиболее современным является вариант операции с выкраиванием «языковидного» полнослойного лоскута прямой кишки (Judd-Robles по D.R. Laird) [8]. Эффективность операции составляет 78,9%, нарушение функции анального держания встречается в 7,8% наблюдений [9]. По данным многоцентрового рандомизированного клинического исследования, применение данного метода позволяет добиться положительных результатов в 50–97% случаев и уменьшить частоту развития рецидива заболевания за счет закрытия внутреннего отверстия свища. Но использование данного способа сопровождается высоким риском развития слабости сфинктера в раннем послеоперационном периоде (до 55% пациентов) и анальной инконтиненции в отдаленном периоде [10].
Предложенный авторами способ лечения демонстрирует меньшее количество рецидивов заболевания (9,3%) и не оказывает влияния на запирательный аппарат прямой кишки.
В литературе описан сфинктеросохраняющий метод лечения «сложных» свищей с помощью диодного лазера – FiLaC, при котором облитерация просвета фистулы достигается за счет деструкции эпителиальной выстилки лазерным излучением.
По данным А.Г. Хитарьяна с соавт., оценка функции запирательного аппарата прямой кишки по шкале Wexner до и после оперативного вмешательства показала отсутствие отрицательного влияния FiLaC на функцию анального сфинктера [11].
Недостатками FiLaC являются оставление внутреннего отверстия фистулы, что значительно повышает вероятность развития рецидива, а также высокая стоимость оборудования, необходимого для выполнения оперативного лечения. При выполнении операции по предложенному нами способу внутреннее свищевое отверстие ликвидируется, что снижает риск развития рецидива заболевания.
Одним из современных сфинктеросохраняющих методов лечения параректальных свищей является обтурация просвета свищевого хода – Anal Fistula Plugs. Этот метод разработан E.K. Johnson, J.U. Gaw, D.N. Armstrong в 2006 году и заключается во введении в просвет свищевого хода биологических или синтетических материалов для закрытия просвета фистулы и формирования каркаса для собственных клеток пациента, обеспечивающего заживление свища [5]. Для этого применяются различные материалы: «BioDesign Surgisis», «Коллост»; «Permacol», а также разнообразные биосовместимые синтетические материалы на основе полигликолиевой кислоты и триметилкарбоната. [5]. Также в литературе имеется информация о введении фибринового клея в просвет свищевого хода после предварительного выскабливания свища [12]. Преимуществом обтурации свищевого хода биологическими, синтетическими материалами служит отсутствие признаков анальной инконтиненции в послеоперационном периоде в связи с отсутствием повреждения анального сфинктера, однако высокий процент рецидивов (до 65%) свидетельствует о несовершенстве методики [13].
Известен способ трансплантации культуры мезенхимальных стволовых клеток в фистулу после предварительной санации лазерным излучением [14]. Несмотря на эффективность, широкого распространения этот метод на данный момент не получил.
Применение данной группы методов хирургического лечения пациентов с параректальными свищами ограничено в связи с высокой стоимостью расходных материалов, техническими сложностями при выполнении операции, а также он характеризуется высоким процентом рецидивов заболевания (до 65%). Предложенный авторами способ отличается меньшей стоимостью реализации и значительно меньшим количеством рецидивов (9,3%).
Наиболее изученным и распространенным методом лечения «сложных» транссфинктерных анальных фистул, включенным в Российские клинические рекомендации по лечению пациентов со свищами прямой кишки, является операция LIFT, которая заключается в перевязке и пересечении свища в межсфинктерном пространстве. Применение данного способа оперативного лечения сопровождается минимальным болевым синдромом, отсутствием признаков анальной инконтиненции в послеоперационном периоде [15]. Однако, по данным многоцентрового рандомизированного исследования, рецидив параректального свища после использования данного метода наблюдается в 43% случаев [10].
Предложенный авторами новый способ оперативного лечения транссфинктерных параректальных свищей характеризуется слабо выраженным болевым синдромом, меньшим процентом рецидивов заболевания при отсутствии признаков анальной инконтиненции в послеоперационном периоде.
Выводы
1. При сравнении результатов лечения пациентов со «сложными» транссфинктерными анальными фистулами по предложенному авторами способу и после операции LIFT определено, что сроки госпитализации и послеоперационный болевой синдром сопоставимы. Также оба метода продемонстрировали свою безопасность с точки зрения воздействия на запирательный аппарат прямой кишки в послеоперационном периоде.
2. Применение предложенного авторами способа характеризуется минимальным количеством раневых осложнений, менее продолжительной послеоперационной реабилитацией и значительно меньшим количеством рецидивов заболевания в отдаленном периоде, что позволяет повысить качество жизни пациентов после перенесенной операции.
Библиографическая ссылка
Лисин О.Е., Яровенко Г.В., Каторкин С.Е., Журавлев А.В., Шестаков Е.В., Клюкин К.В., Купер В.Д. СРАВНИТЕЛЬНАЯ ОЦЕНКА ЭФФЕКТИВНОСТИ НОВОГО СПОСОБА ОПЕРАТИВНОГО ЛЕЧЕНИЯ ТРАНССФИНКТЕРНЫХ ПАРАРЕКТАЛЬНЫХ СВИЩЕЙ // Современные проблемы науки и образования. 2024. № 6. ;URL: https://science-education.ru/ru/article/view?id=33858 (дата обращения: 10.05.2026).
DOI: https://doi.org/10.17513/spno.33858



