Введение. На протяжении многих лет УЗИ является наиболее ценным методом визуализации почек. Его можно использовать независимо от скорости клубочковой фильтрации, он неинвазивный и применим у беременных. Биопсия почки под УЗ-контролем является рутинной процедурой в клинической практике как наиболее точный, однако инвазивный метод. Заболеваемость различными болезнями почек неуклонно растет, в связи с чем необходимы новые методы неинвазивной диагностики заболеваний почек.
Эластография сдвиговой волны позволяет получить информацию о жесткости тканей, этот метод уже доказал свою ценность для диагностики и оценки степени фиброзных изменений в печени. Следует отметить, что в отношении почек здоровых пациентов до последнего времени не существовало убедительных данных о жесткости.
Эластография использует ультразвуковые волны для оценки жесткости ткани. Метод позволяет провести точное количественное определение различий жесткости тканей, в отличие от пальпации, которая носит субъективный характер. Кроме того, соноэластография превосходит обычное УЗИ, которое не дает точной информации об упругих свойствах ткани, поскольку распространение ультразвука относительно равномерно в различных биологических средах.
Основной принцип эластографии заключается в создании напряжения в ткани и последующем измерении деформации, вызванной этим напряжением. Жесткость ткани количественно оценивается с помощью модуля Юнга, определяемого соотношением между приложенным напряжением и вызванной деформацией тканей, выражаемого, как правило, в паскалях или килопаскалях.
Методы, основанные на анализе сдвиговой волны, наиболее подходят для оценки жесткости почки, поскольку они позволяют выборочно исследовать различные отделы почки.
Наиболее важной проблемой является отсутствие нормальных пределов жесткости в здоровой почке, как это было определено для печени [1, 2, 3], щитовидной железы [4] и молочной железы. Измерения, проведенные в различных исследованиях, имеют значительные отличия, что подчеркивает необходимость дальнейшего изучения вопроса эластографии здоровых почек. Например, значения эластичности коры почки варьируют, по разным оценкам, от 15,4±2,5 кПа до 4,40 (3,68–5,70) кПа [5] для модуля Юнга в SSI или эластографии методом сдвиговой волны (SWE); и от 1,75 м/с[6] до 2,54±0,83 м/с [7] для скорости поперечной волны в ARFI. Исследование почек имеет важное значение, так как сообщалось о значительных различиях в эластичности между внешней и внутренней корой, между медуллярной и кортикальной частью почки, а также между корой и почечной лоханкой.
Цель исследования: оценить жесткость неизмененной паренхимы почек у пациентов, не имеющих заболеваний, определить нормативные показатели при выполнении эластографии и эластометрии методом сдвиговой волны (SWE), выработать стандартную технологию исследования, сводящую к минимуму вариабельность результатов.
Материал и методы исследования
Исследование было проведено в соответствии с Хельсинкской декларацией, пересмотренной в 2013 г. Информированное письменное согласие было получено от всех пациентов. Исследование проводилось проспективно с сентября 2022 года по декабрь 2023 года с участием пациентов, посещавших отделение ультразвуковой диагностики ЧУЗ «Клиническая больница «РЖД-Медицина» г. Ростов-на-Дону». Все пациенты прошли комплексное обследование, методика и порядок которого были подробно разъяснены обследуемым.
Перечень исследований состоял в следующем: на первом этапе всем пациентам до дня ультразвукового исследования выполняли подсчет скорости клубочковой фильтрации и проводили оценку стадии хронической болезни почек при ее наличии. В этом исследовании СКФ подсчитывали с использованием формулы CKD – EPI, согласно рекомендациям KDIGO 2012 года, точность расчета СКФ была заметно повышена за счет использования уравнения CKD – EPI по сравнению с формулой MDRD, особенно для значений, превышающих 60 мл/мин/1,73 кв. м. Более того, уравнение CKD-EPI находит предпочтение как в общей медицинской практике, так и в контексте общественного здравоохранения. Напротив, уравнение Кокрофта–Голта имеет тенденцию переоценивать функцию почек, что приводит к снижению точности СКФ. На следующий день после оценки СКФ с утра строго натощак пациентам выполняли ультразвуковое исследование почек в В-режиме по стандартной полипозиционной методике, включавшей измерение линейных размеров почек, паренхимы и оценку структурных изменений.
Следующим этапом выполняли допплерографию артерий почек с оценкой спектральных и скоростных характеристик магистрального и органного кровотока на уровне аорты, устьев почечных артерий, ворот почки, сегментарных артерий, междолевых и дуговых артерий, оценивали пиковую систолическую скорость кровотока, конечную диастолическую скорость кровотока и индекс резистентности на всех перечисленных участках.
Далее сертифицированный врач ультразвуковой диагностики, обладающий десятилетним опытом в области УЗИ брюшной полости и эластографии, выполнял SWE. Все исследования выполнялись с использованием системы визуализации Aixplorer US imaging system (SuperSonic Imagine, Aix-en-Provence, France), оснащенной конвексным датчиком (SC6-1, 1–6 МГц). Пациенты должны были опорожнить мочевой пузырь перед исследованием и задерживать дыхание на несколько секунд во время процедуры. Под контролем УЗИ в В-режиме в режиме реального времени проводили процедуру эластографии для определения модуля упругости обеих почек: при полипозиционном УЗИ выполняли эластографию паренхимы в 6 контрольных точках по отдельности: коркового слоя, мозгового слоя, сосочков пирамид, потом выполняли оценку суммарной жесткости паренхимы. Для обеспечения точности был использован ряд стандартизированных процедур: первоначально рамка для отбора проб эластографии (называемая Q-box) была минимизирована и имела фиксированный диаметр 4 мм. Впоследствии оптимальное размещение Q-box было достигнуто путем его размещения вблизи наружного слоя коркового вещества почки, рядом с капсулой почки, что позволило избежать включения мозгового слоя почки, затем выполнялось точное позиционирование в области мозгового слоя и сосочков пирамидок соответственно. Значения жесткости (Qmean) записывались для последующей интерпретации.
Точные критерии включения были определены следующим образом: нормальная скорость клубочковой фильтрации, отсутствие ультразвуковой патологии и аномалий почек в В-режиме, отсутствие нарушений магистрального и органного кровотока по данным допплерографии сосудов. Критериями исключения для пациентов были: заболевания почек воспалительного характера в анамнезе, изменения в общем анализе мочи, нефроптоз, мочекаменная болезнь, гидронефроз, индекс массы тела больше 25 и меньше 16, изменения спектральных и скоростных характеристик магистрального и органного кровотока при допплерографии, наличие аномалий развития почек.
Достоверность оценивали с использованием коэффициента внутриклассовой корреляции (ICC), были сгенерированы графики Блэнда–Альтмана для проверки смещения и соответствия. При оценке достоверности ICC руководствовались рекомендациями по толкованию мер, предложенными T.K. Koo, M.Y. Li в 2016 г., где ICC ниже 0,50 толкуется как низкая достоверность; 0,50–0,75 – умеренная достоверность; 0,75–0,90 – хорошая достоверность и выше 0,90 – отличная достоверность.
Результаты исследования и их обсуждение
29 пациентов были исключены из исследования из-за несоответствия критериям отбора. В частности, были исключены пациенты с множественными кистами почек (n=9), образованиями (ангиомиолипомы) (n=2), гидронефрозом (стриктуры лоханочно-мочеточниковых сегментов, перенесенные операции на мочеточниках и с явлениями инфравезикальной обструкции) (n=7), конкрементами (n=6), а также пациенты со снижением скорости клубочковой фильтрации (n=3). Кроме того, один человек столкнулся с трудностями в задержке дыхания во время диагностической оценки, и один человек имел высокий индекс массы тела, не позволявший адекватно оценить жесткость паренхимы, они тоже были исключены из исследования. Наконец, в данное исследование попали 168 пациентов: 74 женщины и 94 мужчины (возрастом от 18 до 51 года, 34,5±2,33).
По результатам исследования были получены следующие данные.
При эластографии сдвиговой волной паренхимы почек у пациентов жесткость коркового слоя (Qmean) – 9,2±1,3 кПа (ICC, 0,996, 95% ДИ, 0,993–0,997) (рис. 1, составлен авторами), жесткость медуллярного слоя – 8,3±1,2 кПа (ICC, 0,996, 95% ДИ, 0,994–0,997) (рис. 2, составлен авторами), жесткость сосочков пирамид – 13,4±1,4 кПа (ICC, 0,995, 95% ДИ, 0,992–0,997) (рис. 3, составлен авторами), средняя суммарная жесткость паренхимы – 10,3±1,3 кПа (ICC: 0,996, 95% ДИ, 0,993–0,998).
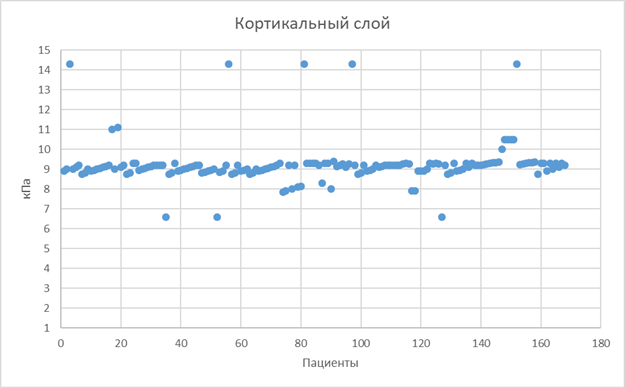
Рис. 1. График распределения жесткости кортикального слоя почки [составлен авторами]
На графике представлено распределение жесткости кортикального слоя почки у здоровых пациентов, жесткость выражена в кПа (n=168)
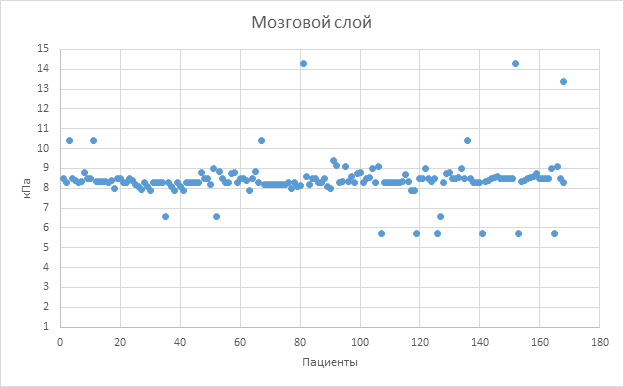
Рис. 2. График распределения жесткости мозгового слоя почки [составлен авторами]
На графике представлено распределение жесткости мозгового слоя почки у здоровых пациентов, жесткость выражена в кПа (n=168)
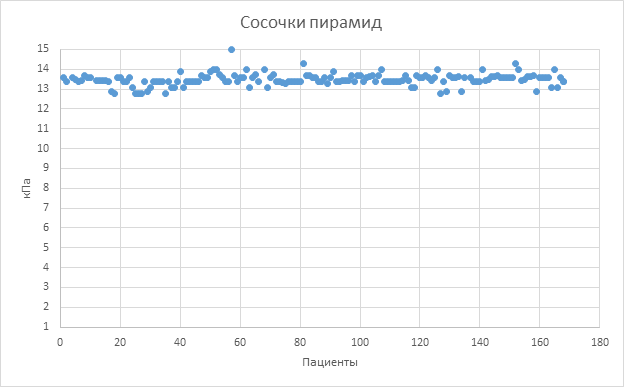
Рис. 3. График распределения жесткости сосочков пирамид [составлен авторами]
На графике представлено распределение жесткости сосочков пирамид почки у здоровых пациентов, жесткость выражена в кПа (n=168)
Следует отметить, что авторы испытали определенные сложности во время исследования, связанные с различными проблемами, которые были описаны авторами предыдущих работ. Первой проблемой были глубина расположения почки и неоднородность структур на пути ультразвукового луча от датчика до почки и обратно: максимальная глубина расположения зоны интереса в современных аппаратах составляет 8 см [8], в связи с чем пациентам с индексом массы тела более 25 адекватно выполнить эластографию почки не представлялось возможным, поэтому такие пациенты попали в группу исключения.
Еще один феномен – анизотропия, который присутствует во всех почечных отделах, особенно в мозговом слое [9, 10], и это важно при интерпретации результатов; направление ультразвукового луча по перпендикулярной оси на эти структуры приведет к повышению значения эластичности, поскольку поперечные волны распространяются быстрее; когда ультразвуковой луч направляется параллельно высокоанизотропной структуре, значения эластичности будут ниже, поскольку поперечные волны будут распространяться медленнее и рассеиваться в результате множественных отражений, создаваемых стромой, почечными канальцами и кровеносными сосудами [8]. Поэтому измерения жесткости в одной и той же части почки (субкапсулярной, корковой и мозгового вещества) целесообразны для получения достоверных и единообразных результатов [11, 12], что было применено авторами для получения стабильных и сопоставимых результатов исследования.
Одним из важных модификаторов скорости сдвиговой волны является васкуляризация почки. Так, в исследовании на животных, проведенном J.L. Genisson и соавторами, сообщалось о снижении эластичности почек после перевязки почечной артерии и, наоборот, повышении эластичности после перевязки почечной вены [8]. Более того, K. Asano и соавторы предположили, что при ХБП повышенная жесткость почек, измеренная при ARFI, может быть вызвана сосудистыми аномалиями при этом заболевании, а не фиброзом почечной паренхимы [7]. В связи с описанными данными исследователи исключили из данной работы пациентов с нарушением васкуляризации почки по данным допплерографии.
В нескольких исследованиях говорилось о линейном увеличении эластичности почечной ткани, связанном с повышенным давлением мочи, обусловленным обструкцией мочевыводящих путей [8]. Следовательно, при исследовании жесткости почки пациентов с неизмененной паренхимой допускать субъектов с расширением чашечно-лоханочной системы было нельзя, и они также были исключены.
Исходя из полученных данных, авторы разработали таблицу для стандартной технологии выполнения SWE, сводящей к минимуму погрешность, по аналогии со стандартами технологии эластографии печени, принятой во Всемирной федерации ультразвука в медицине и биологии (WFUMB) (табл. 1, составлена авторами и по данным WFUMB).
Таблица 1
Сравнительная таблица алгоритма выполнения SWE печени (по данным WFUMB) и алгоритма выполнения SWE почек (разработана авторами) [13]
|
Эластография печени по рекомендациям WFUMB |
Эластография почек по рекомендациям авторов |
|
Требуется строгое следование протоколу |
Требуется строгое следование протоколу |
|
Перед обследованием рекомендуется голод не менее 4 часов |
Перед обследованием рекомендуются голод не менее 4 часов и отказ от потребления жидкости не меньше 2 часов |
|
Обследование выполняется в положении на спине или на левом боку с поднятой рукой для увеличения межреберья |
Обследование выполняется в положении на спине или на левом/правом боку с поднятой рукой для увеличения межреберья |
|
Измерения выполняют межреберным доступом в месте наилучшего «окна» |
Измерения выполняют межреберным доступом или в месте наилучшего «окна» |
|
Эластография выполняется на расстоянии 1,5–2,0 см глубже капсулы печени во избежание артефакта реверберации. Лучшее место для исследования – на глубине 4,0–4,5 см от датчика |
Эластография выполняется в среднем сегменте почки для уменьшения артефакта анизотропии. Лучшее место для исследования – на глубине 4,0–4,5 см от датчика, но не более 8 см. Высокий индекс массы тела может не позволить выполнить SWE |
|
Излучатель обязательно располагать перпендикулярно капсуле печени |
Излучатель обязательно располагать перпендикулярно капсуле почки |
|
Q-box размещается таким образом, чтобы в зону интереса не попадали желчные протоки, крупные кровеносные сосуды и образования |
Q-box размещается таким образом, чтобы в зону интереса не попадали конкременты, крупные кровеносные сосуды и образования |
|
При выполнении транзиентной эластографии следует выбирать датчик в зависимости от телосложения пациента |
Выполнение транзиентной и компрессионной эластографии почек не актуально |
|
Десять результатов должны быть взяты |
6 измерений подходят для метода SWE при условии использования параметра оценки качества |
|
IQR/M (межквартильный размах/медиана) используется в качестве меры качества. Для измерений в кПа IQR/M должен быть <0,3 (30%), а для измерения в м/с — <0,15 (15%) для получения точных результатов |
IQR/M (межквартильный размах/медиана) используется в качестве меры качества. Для измерений в кПа IQR/M должен быть <0,3 (30%), а для измерения в м/с – <0,15 (15%) для получения точных результатов |
|
|
Патология сосудов и/или обструктивный процесс, острые воспалительные изменения могут исказить результат SWE |
Заключение
Данная работа является одним из этапов систематизации результатов предшествующих исследований, получения результатов анализа жесткости почек практически здоровых людей. Настоящее исследование позволило исключить возможные негативные факторы, описанные в предыдущих работах, которые, по мнению авторов, могут вызывать существенную вариабельность жесткости паренхимы. Полученные результаты свидетельствуют о возможности использования ультразвуковой эластографии сдвиговой волны для оценки жесткости паренхимы нативной почки у практически здоровых людей, получения высокодостоверных результатов нетравматичным методом и выработки стандартной методологии эластографии с минимальным уровнем погрешности. Полученные показатели жесткости помогут расширить возможности ультразвуковой эластографии для оценки диффузных и очаговых изменений в почках при различной патологии.
Библиографическая ссылка
Болоцков А.С., Маджугин М.Л., Дадаян А.Р., Фирсов М.С. ОЦЕНКА ЖЕСТКОСТИ ПАРЕНХИМЫ ПОЧЕК У ПРАКТИЧЕСКИ ЗДОРОВЫХ ПАЦИЕНТОВ МЕТОДОМ ЭЛАСТОГРАФИИ СДВИГОВОЙ ВОЛНОЙ // Современные проблемы науки и образования. 2024. № 5. ;URL: https://science-education.ru/ru/article/view?id=33646 (дата обращения: 31.05.2026).
DOI: https://doi.org/10.17513/spno.33646



