Введение
В настоящее время в мире используются интраокулярные линзы (ИОЛ), выполненные из гидрофильного или гидрофобного акрила. ИОЛ из гидрофильного акрила содержат большее количество воды. Например, гидрофильные ИОЛ фирмы Medicontur содержат в своем составе 25% воды, а гидрофобные – 0,4% воды. Все они имеют свои достоинства и недостатки [1, 2, 3]. Так, достоинством гидрофобных ИОЛ считается их медленное раскрытие в передней камере, что позволяет имплантировать их в капсульный мешок в полураскрытом состоянии, что облегчает процесс их имплантации [4]. Для имплантации гидрофобных ИОЛ чаще используют технику «wound assisted», когда край инжектора состыковывается с наружными краями разреза, а стенки тоннельного разреза являются «продолжением» внутреннего пространства картриджа при имплантации ИОЛ [5, 6, 7]. ИОЛ имплантируется в переднюю камеру, где медленно расправляется, за счет чего ее удобно имплантировать в капсульный мешок и центрировать под визуальным контролем. Гидрофильные ИОЛ более мягкие, и их имплантация техникой «wound assisted» более рискованна, это может привести к повреждению и разрыву ИОЛ, поэтому современные картриджи для их имплантации имеют тонкий носик, способный войти в переднюю камеру через разрез 1,8–2,2 мм, используемый для факоэмульсификации ядра. Гидрофильные ИОЛ раскрываются в передней камере быстро, и их имплантация в капсульный мешок требует больших усилий со стороны хирурга, особенно если мы имеем узкий зрачок и ИОЛ с плоскостной гаптикой. Даже при капсулорексисе средней величины, например 5 мм, и небольшой слабости связочного аппарата хрусталика имплантация ИОЛ с плоскостной гаптикой в капсульный мешок бывает затруднительна. Разработка в последние годы новых видов гидрофобных и гидрофильных ИОЛ с новыми современными картриджами, предварительной загрузкой в картридж, уменьшенным диаметром носика картриджа, который позволяет ввести его в переднюю камеру, уменьшают вероятность повреждения ИОЛ и делают имплантацию ИОЛ более безопасной процедурой [8, 9, 10].
Целью исследования было разработать оптимизированную технику имплантации ИОЛ в капсульный мешок для гидрофильных ИОЛ с плоскостной и S-образной гаптикой.
Материал и методы исследования
Для проведения данного исследования были сформированы две группы пациентов. В 1-ю, основную, группу были включены 30 пациентов (40 глаз) (мужчин – 14, женщин – 16) с осложненной катарактой и подвывихом хрусталика I степени, у которых имплантация ИОЛ выполнялась по новой, оригинальной технологии. Из них в 12 глазах наблюдалась гиперметропия слабой и средней степени, в 23 – рефракция, близкая к эмметропии, и в 5 глазах – миопия средней и высокой степени.
Пациенты 1-й группы были разделены на 2 подгруппы: 1а – пациенты, которым после факоэмульсификации была имплантирована по оптимизированной технологии ИОЛ с плоскостной гаптикой и увеличенной глубиной фокуса Teleon lentis comfort, в данную подгруппу вошли 20 пациентов (30 глаз); и 1b – которым после факоэмульсификации была имплантирована ИОЛ с S-образной гаптикой и расширенной глубиной фокуса Rayner RayOne EMV. В данную подгруппу вошли 10 пациентов (10 глаз).
Во 2-ю группу (группу сравнения) были также включены 30 пациентов (40 глаз) (мужчин – 13, женщин – 17) с осложненной катарактой и подвывихом хрусталика I степени, у которых имплантация ИОЛ выполнялась по стандартной технологии.
Пациенты 2-й группы также были разделены на 2 подгруппы: 2а, пациентам которой после факоэмульсификации была имплантирована по стандартной технологии ИОЛ с плоскостной гаптикой и увеличенной глубиной фокуса «Teleon lentis comfort». В данную подгруппу вошли 20 пациентов (30 глаз); 2b подгруппа, в которой после факоэмульсификации была имплантирована по стандартной технологии ИОЛ с S-образной гаптикой и расширенной глубиной фокуса «Rayner RayOne EMV», в данную подгруппу вошли 10 пациентов (10 глаз). Из них в 14 глазах наблюдалась гиперметропия слабой и средней степени, в 22 – рефракция, близкая к эмметропии, и в 4 глазах – миопия средней и высокой степени. Возраст пациентов 1-й группы составил от 39 до 82 лет (средний возраст – 72,8±8,2 года). Возраст пациентов 2-й группы составил от 37 до 80 лет (средний возраст – 70,2±10,8 года).
Во всех случаях для имплантации ИОЛ «Teleon lentis comfort» использовались картридж и инжектор производства швейцарской фирмы «Medicel AG» viscoject (вискоджект) 1.8, для использования через разрез 1,8 мм. Для имплантации ИОЛ «Rayner RayOne EMV» применялся оригинальный картридж данной фирмы, в которую ИОЛ была предзагружена.
Дооперационное и послеоперационное обследование у пациентов основной группы и группы сравнения включало в себя определение максимальной корригированной остроты зрения (МКОЗ), ВГД, дооперационной и интраоперационной величины зрачка при максимальном мидриазе, наличия ПЭС, УБМ – исследование состояния связочного аппарата хрусталика. Интраоперационно оценивались величина выполненного переднего капсулорексиса, разрывы передней и задней капсул хрусталика. Исследование остроты зрения без коррекции и с максимальной коррекцией проводили у пациентов на 2-е сутки и через 1 месяц после операции.
Статистическую обработку полученных данных осуществляли с помощью пакета программ «Statistica 10.0» («StatSoft», США). Поскольку распределение большинства признаков отличалось от нормального (проверяли по критерию Шапиро–Уилка), использовали непараметрические методы: описание групп представлено в виде медианы (Ме) и квартилей (Q25; Q75), при анализе изменений в группе использовали критерий Вилкоксона.
Некорригированная острота зрения до операции у пациентов основной группы составила 0,10 (0,10; 0,20) в группе контроля – 0,10 (0,08; 0,20). ВГД Р0 до операции у пациентов основной группы составило 14,50 (12,60; 18,30) мм рт. ст., у пациентов группы сравнения – 12,80 (11,65; 14,90) мм рт. ст.
По данным биомикроскопии у всех пациентов глаза были спокойными, роговица и влага передней камеры – прозрачными, зрачок круглой формы. Псевдоэксфолиации по краю зрачка были выявлены в 29 (72,5%) глазах пациентов 1-й группы, из них в 23 (57,5%) – пациентов 1а подгруппы и в 6 (15%) глазах – пациентов 1b подгруппы; в 27 (67,5%) глазах пациентов 2-й группы, из них в 22 (55%) глазах пациентов 2а подгруппы и 5 (12,5%) – пациентов 2b подгруппы. Зрачок диаметром 6,0–7,0 мм на максимальном медикаментозном мидриазе наблюдался в 18 (45%) глазах пациентов 1-й группы и 19 (47,5%) глазах – пациентов 2-й группы, диаметром 4,5–5,5 мм – в 22 (55%) глазах пациентов 1-й группы и 21 (52,5%) глазу – пациентов 2-й группы.
Техника имплантации ИОЛ с плоскостной гаптикой «Teleon lentis comfort» и с S-гаптикой «Rayner RayOne EMV»
После выполнения ФЭК вводили картридж в переднюю камеру и, продвигая ИОЛ по картриджу, помещали носик картриджа в капсульный мешок, на уровень передней капсулы. Продолжали инжектирование ИОЛ из картриджа в капсульный мешок, причем носик картриджа все время находился в передней камере, на уровне или ниже плоскости передней капсулы. Нижний гаптический элемент и оптическая часть ИОЛ помещались в капсульный мешок (рис. 1). После выхода оптической части ИОЛ из картриджа смещали носик картриджа вниз, в капсульный мешок, раскрывая его, при этом оптика линзы служила своеобразным протектором для раскрытия мешка. При выходе из картриджа верхний гаптический элемент, расправляясь, заходил в капсульный мешок (рис. 2). Интраокулярная линза расправлялась и центрировалась в капсульном мешке без ее дополнительной установки и правки хирургическими инструментами (рис. 3).
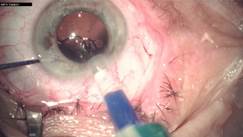
Рис. 1. Нижний гаптический элемент и оптика плоскостной гидрофильной ИОЛ имплантированы в капсульный мешок
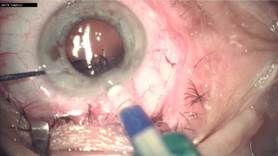
Рис. 2. Имплантация верхнего гаптического элемента ИОЛ в капсульный мешок
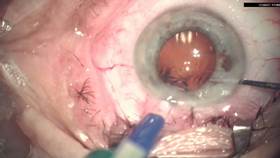
Рис. 3. ИОЛ имплантирована в капсульный мешок
По данной оптимизированной технологии пациентам 1-й группы 1а подгруппы имплантированы 30 ИОЛ с плоскостной гаптикой «Teleon lentis comfort» с диоптрийностью от 15 до 25,0 дптр; пациентам 1b подгруппы – 10 ИОЛ с S-гаптикой «Rayner RayOne EMV» с диоптрийностью от 16 до 22 дптр. Интраоперационно диаметр зрачка на максимальном медикаментозном мидриазе после факоэмульсификации ядра и удаления хрусталиковых масс составил 6,0–7,0 мм в 14 (35%) глазах и 4,0–5,5 мм – в 26 (65%) глазах пациентов 1-й группы. Дополнительной инструментальной репозиции интраокулярной линзы данным пациентам не проводилось, кроме доворота ИОЛ с плоскостной гаптикой «Teleon lentis comfort» для установки по вертикальной оси тем пациентам, у которых ИОЛ отклонилась от вертикальной оси. Это требование прописано в инструкции производителя по имплантации данной модели ИОЛ, которая требует вертикального расположения гаптических элементов интраокулярной линзы в глазу, согласно нанесенным на нее меткам.
Пациентам 2-й группы 2а подгруппы имплантированы 30 ИОЛ с плоскостной гаптикой «Teleon lentis comfort» по стандартной технологии с диоптрийностью от 13 до 25,5 дптр; пациентам 2b подгруппы – 10 ИОЛ с S-гаптикой «Rayner RayOne EMV» с диоптрийностью от 16 до 23 дптр по стандартной технологии. Интраоперационно, после факоэмульсификации ядра и удаления хрусталиковых масс величина зрачка на максимальном медикаментозном мидриазе была равна 6,0–7,0 мм в 15 (37,5%) глазах и 4,0–5,5 мм – в 25 (62,5%) глазах пациентов 2-й группы. Техника имплантации у пациентов 2-й группы заключалась в имплантации ИОЛ в переднюю камеру и, частично, в капсульный мешок. Нижний гаптический элемент и оптическая часть ИОЛ имплантировались в капсульный мешок, а верхний гаптический элемент располагался в передней камере, на передней капсуле и радужке. Далее имплантация верхнего гаптического элемента в капсульный мешок выполнялась с помощью шпателя.
Операционные осложнения. У пациентов 1-й группы 1а подгруппы при имплантации ИОЛ с плоскостной гаптикой «Teleon lentis comfort» в 3 случаях наблюдалась имплантация в капсульный мешок только половины верхнего гаптического элемента, вторая половина упиралась в переднюю капсулу кругового капсулорексиса, растягивая ее, и располагалась на передней капсуле хрусталика (рис. 4). В 2 этих случаях диаметр зрачка и капсулорексиса был равен 5,5 мм, в 1 случае диаметр зрачка был равен 5,5 мм, капсулорексиса – 5 мм. Ни в одном случае разрыва переднего кругового капсулорексиса не наблюдалось. При помощи шпателя половина верхнего гаптического элемента заправлялась в капсульный мешок (рис. 5). В 2 случаях, в глазах с миопией высокой степени, верхний гаптический элемент не зашел в капсульный мешок и находился в передней камере на передней капсуле и радужке, что потребовало его дополнительной репозиции в капсульный мешок шпателем.
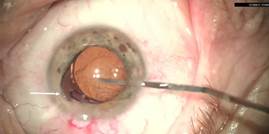
Рис. 4. Часть верхнего гаптического элемента находится на радужке (указано стрелкой)
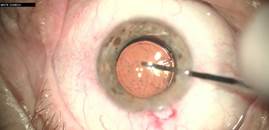
Рис. 5. Произведена репозиция ИОЛ в капсульный мешок при помощи шпателя
В 1 случае диаметр зрачка и капсулорексиса был равен 5,5 мм, во втором случае диаметр зрачка был равен 5,0 мм, капсулорексиса – 4,7 мм.
У пациентов 1-й группы 1b подгруппы при имплантации ИОЛ с S-гаптикой «Rayner RayOne EMV» в 1 случае (у пациента с миопией высокой степени) верхний гаптический элемент не зашел в капсульный мешок и находился в передней камере на передней капсуле и радужке, что потребовало его дополнительной репозиции в капсульный мешок шпателем. Диаметр зрачка в данном случае был равен 5,5 мм, капсулорексиса – 5 мм.
У пациентов 2-й группы 2а подгруппы при имплантации ИОЛ с плоскостной гаптикой «Teleon lentis comfort» по стандартной технологии в 4 случаях имплантация верхнего гаптического элемента в капсульный мешок с помощью шпателя не получилась из-за наличия псевдоэксфолиативного синдрома и слабости связочного аппарата хрусталика. В 1 случае диаметр зрачка и переднего капсулорексиса был равен 6 мм, в 2 случаях диаметр зрачка составил 5,5 мм, капсулорексиса – 5 мм, в 1 случае диаметр зрачка был равен 5,5 мм, капсулорексиса – 4,5 мм. Для раскрытия капсульного мешка потребовалась имплантация иридокапсулярного ретрактора вне зоны расположения верхнего гаптического элемента, и при развороте ИОЛ в сторону имплантированного ретрактора гаптический элемент был имплантирован в капсульный мешок.
Результаты исследования и их обсуждение
Исследование остроты зрения без коррекции и с максимальной коррекцией проводили у пациентов на 2-е сутки и через 1 месяц после операции. Послеоперационная корригированная острота зрения вдаль повысилась у пациентов обеих групп: в основной группе она составила 0,75, в группе сравнения – 0,70 (Z=1,88 р=0,060). ВГД Р0 на 2-е сутки после операции у пациентов основной группы составило 16,25 (14,40; 19,20) мм рт. ст., у пациентов группы сравнения – 17,60 (15,40; 19,80) мм рт. ст. У 4 пациентов 1-й группы и 6 пациентов 2-й группы в послеоперационном периоде наблюдалась умеренная гипертензия. Данным пациентам назначена гипотензивная терапия сроком на 1 месяц.
Роговица у всех пациентов в послеоперационном периоде была прозрачна, у 5 пациентов 1-й группы и 3 пациентов 2-й группы в послеоперационном периоде наблюдались единичные складки десцеметовой мембраны, которые были купированы на 3–5-е сутки консервативным лечением. Положение ИОЛ у всех пациентов было правильным, в капсульном мешке. Глазное дно – без особенностей.
Через 1 месяц после операции наблюдалось повышение корригированной остроты зрения у пациентов обеих групп: в 1-й группе она повысилась до 0,80, во 2-й группе – до 0,75 (Z=0,94 р=0,347). ВГД Р0 через 1 месяц после операции у пациентов основной группы составило 13,20 (11,10; 16,20) мм рт. ст., у пациентов группы сравнения – 14,20 (12,60; 17,30) мм рт. ст.
Внутриглазное давление у всех пациентов 1-й и 2-й группы было нормализовано. Роговица у всех пациентов через 1 месяц после операции была прозрачна. Положение ИОЛ у всех пациентов было правильным, в капсульном мешке. Глазное дно – без особенностей.
Обсуждение. Возможность оптимизации имплантации гидрофильных ИОЛ в капсульный мешок появилась только в последнее время, в связи с разработкой новых картриджей с диаметром носика значительно меньшим, чем величина основного разреза, и возможностью его введения в переднюю камеру и непосредственно в капсульный мешок [11, 12, 13].
У инжектора Viscoject LP604350С фирмы «Medicel AG» диаметр носика картриджа у выхода из картриджа равен 1,8 мм, по мере продвижения вверх толщина картриджа конусообразно увеличивается, и диаметра 2,2 мм он достигает в 5,4 мм от края картриджа. С учетом ширины операционного разреза 1,5–2,2 мм возможно погружение носика картриджа в переднюю камеру на глубину 3,9–3,2 мм.
Диаметр носика картриджа предзагруженной ИОЛ «Rayner RayOne EMV» равен 1,8 мм, по мере продвижения диаметр картриджа также конусообразно увеличивается, и наружный диаметр 2,2 мм находится на расстоянии 5,8 мм от выхода из картриджа. Учитывая ширину операционного разреза 1,5–2,2 мм, возможно погружение носика картриджа в переднюю камеру на глубину 4,3–3,6 мм. При имплантации плоскостной гидрофильной ИОЛ с помощью инжектора Viscoject фирмы «Medicel AG» и ИОЛ с S-гаптикой «Rayner RayOne» возможно продвижение картриджа в переднюю камеру и непосредственно в капсульный мешок. Нижний гаптический элемент, медленно выходя из картриджа, расправляет своды капсульного мешка, оптика ИОЛ помещается в центре капсульного мешка. Носик картриджа разворачивается вертикально вниз, оказывая небольшое давление на заднюю капсулу оптикой ИОЛ с медленным выходом верхнего гаптического элемента в капсульный мешок, и под воздействием эластичности ИОЛ помогает ему зайти непосредственно в капсульный мешок и там самостоятельно центрироваться. Данная техника создает возможность имплантации ИОЛ с плоскостной гаптикой в небольшой по размерам капсулорексис у пациентов с узким ригидным зрачком без применения ирис-ретракторов.
За счет ограниченной длины носика картриджа способность его погружения в капсульный мешок нормируется глубиной передней камеры, которая глубже у пациентов с миопией высокой степени. При глубине передней камеры 4 мм и более имплантация ИОЛ в капсульный мешок затруднена в связи с отсутствием возможности погружения носика картриджа в капсульный мешок.
Интраоперационные осложнения, возможные при имплантации верхнего гаптического элемента в капсульный мешок, возникают из-за недостаточного погружения носика картриджа в просвет капсульного мешка. Контроль положения носика картриджа в просвете капсульного мешка позволяет избежать данных осложнений у пациентов с гиперметропической и эмметропической рефракцией. У пациентов с миопией высокой степени не всегда возможна имплантация ИОЛ в капсульный мешок из-за увеличенной глубины передней камеры.
Выводы
1. Разработанная оптимизированная технология имплантации в капсульный мешок возможна только у тех ИОЛ, у которых диаметр носика картриджа меньше величины основного разреза и где возможно введение картриджа в переднюю камеру и капсульный мешок.
2. Введение картриджа непосредственно в капсульный мешок, медленный выход нижнего гаптического элемента и оптической части ИОЛ позволяют расправить капсульный мешок для безопасной имплантации в него верхнего гаптического элемента.
3. У пациентов с миопией высокой степени первичная имплантация ИОЛ в капсульный мешок не всегда возможна за счет увеличенной глубины передней камеры.
4. Интраоперационные осложнения, возможные при имплантации верхнего гаптического элемента, возникают из-за подъема носика картриджа из капсульного мешка в плоскость переднего капсулорексиса или в переднюю камеру, не зависят от величины капсулорексиса и устраняются без последствий для конечного результата.
Библиографическая ссылка
Пирогова Е.С. ОПТИМИЗИРОВАННАЯ ТЕХНИКА ИМПЛАНТАЦИИ ГИДРОФИЛЬНЫХ ИНТРАОКУЛЯРНЫХ ЛИНЗ С ПЛОСКОСТНОЙ И S-ОБРАЗНОЙ ГАПТИКОЙ В КАПСУЛЬНЫЙ МЕШОК // Современные проблемы науки и образования. 2024. № 4. ;URL: https://science-education.ru/ru/article/view?id=33600 (дата обращения: 11.04.2026).
DOI: https://doi.org/10.17513/spno.33600



