Введение
Псориаз (ПС) – хроническое иммуноассоциированное заболевание мультифакториальной природы с доминирующим значением в развитии генетических факторов, характеризующееся ускоренной пролиферацией кератиноцитов и нарушением их дифференцировки, дисбалансом между провоспалительными и противовоспалительными цитокинами, с частыми патогомоничными изменениями опорно-двигательного аппарата [1]. ПС является хроническим системным рецидивирующим заболеванием, проявляющимся гиперпролиферацией кератиноцитов и характеризующимся поражением различных органов и систем с преимущественным вовлечением в патологический процесс кожи [2, 3, 4].
По различным данным, во всем мире ПС страдают не менее 125 млн человек. Распространенность нозологии отличается широкой географической изменчивостью – от 0,91% в США до 8,5% в Норвегии [4]. По статистическим показателям на 2021 год, распространенность ПС в России составляет 243,7 на 100 тысяч населения, заболеваемость – 59,3 на 100 тысяч [1]. Описанные различия определяются разной степенью влияния факторов окружающей среды в климатических зонах, а также разнообразием генотипа человеческой популяции.
В настоящее время особое внимание исследователей и врачей различных специальностей направлено на проблему частой коморбидности псориаза с рядом заболеваний внутренних органов, в том числе печени и желчевыделительной системы. Печень является важнейшим органом детоксикации, нарушение этой функции приводит к эндотоксикозу, вызывает иммунный дисбаланс, активизирует воспалительные процессы, что способствует развитию и обострению псориаза. Печень и желчный пузырь участвуют в синтезе желчных кислот, выработке желчи, метаболизме витаминов, эти вещества играют значимую роль в поддержании иммунной системы и здоровья кожи [5]. Указанные механизмы объясняют частое сочетание псориаза с аутоиммунными заболеваниями печени и желчевыделительной системы, такими как аутоиммунный гепатит, первичный билиарный холангит (первичный билиарный цирроз печени), первичный склерозирующий холангит. Кроме того, современные стандарты лечения артропатической формы псориаза предполагают длительное назначение цитостатиков – метотрексата и циклоспорина. Эти препараты обладают потенциальной гепатотоксичностью, обусловленной иммуносупрессией и прямым повреждением печени, либо сочетанием указанных двух факторов. Кроме того, воспаление кожи при псориазе также дополнительно вызывает повышенное образование эндотоксинов и свободных радикалов, что запускает и поддерживает повреждение гепатоцитов с нарушением их функций [6].
В медицинской литературе приведены описания случаев идиопатических нарушений биохимических показателей функции печени у пациентов с псориазом. Так, при ретроспективном исследовании 518 таких больных в 4% случаев выявлено умеренное повышение активности печеночных ферментов, а в 8% наблюдений зарегистрированы высокие показатели цитолиза [7]. Автором H.Y. Ma с соавторами было установлено, что интерлейкин (ИЛ) 17 – критический медиатор фиброза печени различной этиологии – играет важную роль и в псориатическом процессе. Во время индуцированного фиброза печени при алкогольной болезни печени активируется продукция ИЛ-6, поддерживающего пролиферацию кератиноцитов при псориазе [8]. Функциональные нарушения гепатобилиарной системы подтверждают полисистемность псориаза и коррелируют с тяжестью его клинического течения [9]. Таким образом, комбинированная терапия псориаза предполагает применение гепатопротекторов и другой сопутствующей терапии в зависимости от особенностей коморбидности пациента. Учитывая проблему полипрагмазии, необходимо найти оптимальный гепатопротектор или их сочетание, терапевтическими мишенями которого являются звенья патогенеза как псориаза, так и заболевания печени. В связи с этим интерес представляют препараты, в состав которых входят урсодезоксихолевая кислота (УДХК) и адеметионин [10, 11].
УДХК оказывает прямое гепатопротективное действие ввиду защиты гепатоцитов от апоптоза, вызванного желчными кислотами, снижает гепатотоксичность гидрофобных солей желчи, является холеретиком, оказывает влияние на иммунологические реакции, подавляет продукцию цитокинов и интерлейкинов.
Адеметионин обладает несколькими гепатопротективными эффектами: оказывает холеретическое, холекинетическое, дезинтоксикационное, антиоксидантное и антифиброзное действие. Кроме того, имеет антидепрессивную активность. При лекарственном поражении печени адеметионин предотвращает появление или прогрессирование холестаза, нейтрализует свободные кислородные радикалы, снижает восприимчивость к окислительному стрессу, оказывает стабилизирующее влияние на клеточные мембраны гепатоцитов [12].
Важно отметить, что адеметионин повышает синтез протеогликанов и обеспечивает частичную регенерацию хрящевой ткани, что объясняет его выбор при псориатическом артрите. Назначение адеметионина приводит к снижению суставного болевого синдрома, сопоставимому с эффектом нестероидных противовоспалительных препаратов, при практически полном отсутствии побочных эффектов.
Цель исследования – применить мультидисциплинарный подход в лечении пациентов с артропатической формой псориаза.
Материал и методы исследования
Представляется клинический случай комплексного ведения коморбидного пациента с артропатической формой псориаза. Под наблюдением в Клиниках ФГБОУ СамГМУ Минздрава России в дерматовенерологическом отделении c 24.01.2024 по 08.02.2024 гг. находился пациент М., 39 лет. Поступил с жалобами на высыпания на коже головы, туловища, верхних и нижних конечностей, зуд, боль в голеностопных и коленных суставах.
Из анамнеза заболевания: больным себя считает с 2002 года, когда впервые появились высыпания на коже волосистой части головы. Изначально лечился самостоятельно различными шампунями с цинком и дегтем, с временным непродолжительным эффектом. Спустя несколько лет пациент стал замечать новые элементы на коже разгибательных поверхностей верхних и нижних конечностей. С 2018 года сыпь распространилась на туловище, а также начали беспокоить боли в суставах пальцев рук. После консультации дерматовенеролога установлен диагноз «псориаз» и назначено лечение (принимал внутрь метотрексат, местно мазь с мометазоном) с положительным эффектом, но у пациента появился постоянный дискомфорт в правом подреберье, и лечение он самостоятельно прекратил. В последующие годы отмечались обострения псориаза с периодичностью 2–3 раза в год в осенне-зимний период. Необходимо отметить, что имеется наследственная отягощенность, так как у отца пациента и сына псориаз. Последнее обострение началось за 2 недели до госпитализации в дерматовенерологическое отделение Клиник СамГМУ, когда появились бляшки на коже волосистой части головы, туловища, верхних и нижних конечностей, сопровождающиеся зудом. Отмечает появление болей в области голеностопных и коленных суставов в течение 7 лет. Со слов больного, обострение спровоцировано стрессом. Самостоятельно продолжал терапию топическими глюкокортикостероидами, без клинического улучшения. В связи с неэффективностью амбулаторного лечения был госпитализирован в дерматовенерологическое отделение Клиник СамГМУ для прохождения курса лечения.
При объективном обследовании выявлено, что процесс носит распространенный симметричный характер, занимает кожу волосистой части головы, туловища, преимущественно на разгибательных поверхностях верхних и нижних конечностей. Высыпания представлены мономорфными эпидермально-дермальными папулезными элементами округлых форм, розового цвета. Папулы плоские с шероховатой поверхностью, покрытые серебристо-белыми чешуйками, которые легко снимаются, размерами от 7 до 15 см в диаметре. На свежих папулах чешуйки раcполагаются в центре, по их периферии остается узкий яркий ободок. По мере прогрессирования процесса псориатические папулы распространятся по периферии, увеличиваются, образуя бляшки причудливых очертаний. В основании бляшек инфильтрация. Высыпания склонны к слиянию. При поскабливании элементов сыпи последовательно возникает обильное шелушение в виде серебристо-белых чешуек, напоминающих стеарин (феномен «стеаринового пятна»), после удаления чешуек остается влажная блестящая поверхность (феномен терминальной пленки), при дальнейшем поскабливании возникает капельное кровотечение (феномен кровяной росы) – псориатическая триада (рис. 1).
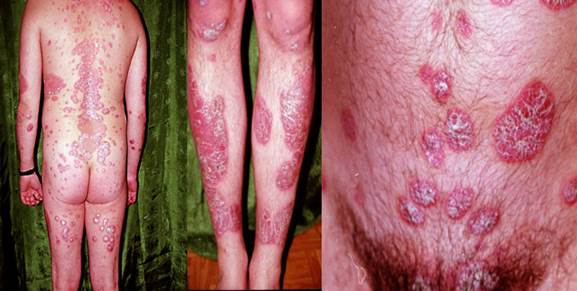
Рис. 1. Фотографии до лечения (из архива кафедры дерматовенерологии и косметологии ИПО ФГБОУ ВО СамГМУ Минздрава РФ)
По результатам проведенного обследования было установлено, что общий анализ крови не выявил явных изменений, кроме ускорения скорости оседания эритроцитов (СОЭ): лейкоциты 5,63•109/л (4,4–11,3•109/л) лейкоцитарная формула: палочкоядерные 1,0% (0–5%), сегментоядерные 62% (47–72%), эозинофилы 2% (0–5%), лимфоциты 28% (20–40%), моноциты 7% (2–10%), гемоглобин 15,20 г/дл (13,5–17,4 г/дл), эритроциты 4,76 • 1012л (4,37–5,79•1012/л), средний объем эритроцитов 96,0 фл (81,7–97,9 фл), тромбоциты 245,0•109/л (150–450•109/л). СОЭ по Панченкову 28 мм/час (0–15 мм/час).
Общий анализ мочи – без патологических изменений: удельный вес 1010, рН 6,71, белок, глюкоза, кетоны – отсутствуют, лейкоциты – 3–4 в поле зрения, эпителий – 1–2 в поле зрения, слизь.
По данным биохимического анализа крови выявлено, что, несмотря на полученные нормальные значения ряда показателей: общий белок 74,1 г/л (65–85 г/л), альбумин 47 г/л (35–52 г/л), глюкоза 5,2 ммоль/л (4,11–6,05 ммоль/л), билирубин общий 11,0 мкмоль/л (0–20,5 мкмоль/л), креатинин 66 мкмоль/л (44–80 мкмоль/л), аспартатаминотрансфераза (АсАТ) 41,6 Ед/л (0–40 Ед/л), щелочная фосфатаза (ЩФ) 64 Ед/л (40–130 Ед/л), имеются изменения аланинаминотрансферазы (АлАТ) 120,6 Ед/л (0–41 Ед/л) и гамма-глутамилтранспептидазы (ГГТ) 150 Ед/л (11–49 Ед/л). Таким образом, выявлены умеренный цитолиз (повышение АлАТ до 3 норм, при нормальном показателе АсАТ) и повышение ГГТ (3 нормы), что свидетельствует об активном поражении клеток печени, возможно токсического генеза, с развитием холестаза.
Для исключения вирусного гепатита назначено необходимое дообследование. Антитела к вирусу иммунодефицита человека (ВИЧ) 1, 2 – не обнаружены. HBsAg, антиHCVсум – отрицательные. Вирусный генез поражения печени у пациента исключен.
Для оценки степени гепатодепрессии проведено исследование гемостаза: протромбиновое время 12 сек (менее 17 сек), протромбиновый индекс 111% (более 70%). Печеночно-клеточной недостаточности не выявлено.
Важными и показательными являются полученные результаты гистологического исследования биоптата кожи: выраженный акантоз эпидермиса с характерным колбообразным расширением эпидермальных выростов книзу и истончением эпидермиса над верхушками вытянутых сосочков дермы, паракератоз, исчезновение зернистого слоя, скопление нейтрофильных лейкоцитов в зоне паракератоза. Описанные морфологические изменения биоптата подтверждают обострение псориаза.
Ввиду наличия артропатии и изменений в печеночных функциональных показателях крови для согласования дальнейшей тактики ведения пациент был направлен на консультацию к ревматологу и гастроэнтерологу.
При осмотре ревматологом было подвержено, что жалобы на высыпания на коже туловища, верхних и нижних конечностей и боли в мелких суставах кистей, голеностопных и коленных суставах, периодический кожный зуд являются клиническими проявлениями единого патологического процесса – артропатической формы псориаза, которым пациент страдает длительное время, однако регулярного базисного лечения не было. Ревматолог для лечения псориатического артрита назначил метотрексат 15 мг подкожно 1 раз в неделю в течение месяца и рекомендовал амбулаторное плановое обследование – магнитно-резонансную томографию (МРТ) илеосакральных сочленений, лабораторный контроль 1 раз в 2–3 недели – общий анализ крови с лейкоформулой, С-реактивный белок (СРБ), АлАТ, АсАТ, мочевина, креатинин крови.
За период госпитализации в дерматовенерологическое отделение пациент был также осмотрен гастроэнтерологом. После тщательного опроса выявлено наличие жалоб со стороны органов пищеварения – на периодическую изжогу, тяжесть и дискомфорт в правом подреберье без четкой связи с приемом пищи. В анамнезе заболевания следует отметить, что сам пациент наличие хронических заболеваний желудочно-кишечного тракта отрицал. Однако в связи с артралгией периодически принимал различные нестероидные противовоспалительные средства (НПВС), и больного часто (более 2 раз в неделю) беспокоила изжога, которую самостоятельно купировал антацидами. Не обследовался, курсового приема препаратов для лечения желудочно-кишечного тракта не было. При физикальном обследовании органов пищеварения были выявлены следующие изменения: умеренная болезненность в эпигастрии при пальпации, при перкуссии – увеличение размеров печени по Курлову: первый – 12 см, второй –- 11 см, третий – 10 см. Для уточнения диагноза гастроэнтерологом рекомендовано инструментальное дообследование – эзофагогастродуоденоскопия (ЭГДС) с исследованием на обнаружение Helicobacter pylori (HP) и ультразвуковое исследование (УЗИ) брюшной полости.
По результатам ЭГДС выявлены изменения слизистой пищевода и желудка: эрозивный рефлюкс-эзофагит (LA-C по Лос-Анджелесской классификации) и атрофия слизистой желудка (С1 по Kimura-Takemoto) на фоне поверхностного гастрита и дуоденогастрального рефлюкса (ДГР). Инфицирования НР не выявлено. По данным УЗИ органов брюшной полости обнаружены диффузные изменения печени по типу жирового гепатоза при отсутствии портальной гипертензии (воротная вена 11 мм); нарушения со стороны желчного пузыря – уплотнение стенки при нормальных размерах органа, наличие густой желчи; незначительная спленомегалия – площадь селезенки 57 см2; также выявлены диффузные изменения поджелудочной железы по типу липоматоза.
Таким образом, после физикального, лабораторного и инструментального обследований органов пищеварения у пациента выявлены изменения со стороны печени по типу стеатогепатита умеренной степени биохимической активности, хронический некалькулезный холецистит с явлениями дисхолии, хронический билиарнозависимый панкреатит, эрозивный рефлюкс-эзофагит и смешанный гастрит. Гастроэнтерологом рекомендовано включить в курс лечения комбинированную гепатопротективную терапию для коррекции цитолиза и холестаза, и были назначены препараты адеметионин и УДХК; для восстановления слизистой пищевода и желудка – рабепразол и ребамипид.
На основании проведенного комплексного обследования врачами дерматовенерологом, ревматологом и гастроэнтерологом был установлен клинический диагноз:
Основное заболевание: L40.5 Псориаз распространенный, артропатическая форма, стадия прогрессирования.
Сопутствующие заболевания:
Псориатический спондилоартрит 3-й степени активности, дактилит 3-го, 4-го пальцев правой кисти. Стеатогепатит умеренной степени биохимической активности. ГЭРБ II ст. Рефлюкс-эзофагит эрозивный. Хронический гастрит, смешанный (поверхностный с явлениями атрофии), обострение. ДГР. Хронический холецистит, некалькулезный, с явлениями дисхолии, ремиссия. Хронический панкреатит, билиарнозависимый, ремиссия.
В дерматовенерологическом отделении с учетом выявленной коморбидности и рекомендаций ревматолога и гастроэнтеролога назначено необходимое лечение: внутривенно капельно – преднизолон 30 мг/сут, хлоропирамин 20 мг/сут, адеметионин 800 мг/сут; подкожно – метотрексат 15 мг 1 раз в неделю; внутрь – рабепразол 40 мг/сут, ребамипид 300 мг/сут; наружно местно – салициловая мазь 2% + флуоцинолона ацетонид 0,025%, бетаметазон 0,05% + салициловая кислота 3% и селективная фототерапия 4 раза в неделю.
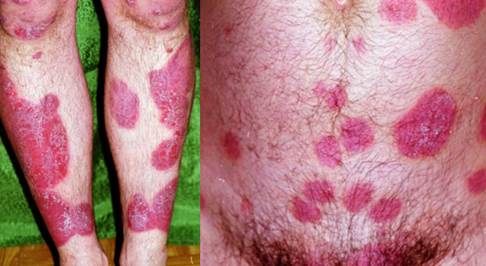
Рис. 2. Фотографии через 14 дней лечения (из архива кафедры дерматовенерологии и косметологии ИПО ФГБОУ ВО СамГМУ Минздрава РФ)
На фоне проводимого лечения у пациента на 14-й день (рис. 2) отмечалась положительная клиническая динамика – появления новых высыпаний не было, бляшки имели застойно-красный цвет, умеренно инфильтрированы и слабо шелушились, чешуйки покрывали высыпания полностью. Псориатическая триада сомнительная. Переносимость лекарственной терапии хорошая, побочных эффектов лечения не выявлено.
При выписке из дерматовенерологического отделения Клиник СамГМУ пациент активных жалоб не предъявлял, общее состояние расценено как удовлетворительное. Высыпания регрессируют, бляшки осели, шелушение отсутствует, инфильтрация значительно уменьшилась. Субъективных ощущений нет. Новых элементов нет. Болезненность в области голеностопных и коленных суставов беспокоит значительно меньше, зуда не отмечает.
Рекомендован амбулаторный курс медикаментозной терапии: метотрексат 10 мг – подкожно 1 раз в неделю, адеметионин 400 мг – по 1 т. 2 раза в день – 1 месяц, УДХК 250 мг – по 1 к. утром, 1 к. днем, 2 к. вечером перед сном – 4 месяца, ребамипид 100 мг – по 1 т. 3 раза в день – 2 месяца, рабепразол 20 мг – по 1 т. 2 раза в день – 2 месяца. Наружно: мазь клобетазол 0,05% 2 раза в неделю (суббота, воскресенье), крем кальципотриол 1 раз в день 5 дней в неделю (будни), эмоленты (увлажняющие) после душа в течение 3 минут регулярно, длительно.
Через 4 недели после выписки из стационара рекомендован повторный осмотр дерматовенерологом и гастроэнтерологом с результатами лабораторного исследования крови (показатели АлАТ, АсАТ, ГГТ, ЩФ и общего анализа крови) для оценки эффективности назначенной терапии и возможной коррекции лечения.
Результаты исследования и их обсуждение. Оценка эффективности лечения производилась через 4 недели после выписки из дерматовенерологического отделения. 11.03.2024 г. при осмотре пациента выявлена значимая положительная клинико-лабораторная динамика. На коже новых высыпаний не было, а имевшиеся при госпитализации высыпания побледнели, осели, шелушение отсутствовало, отмечались незначительная инфильтрация, умеренная эритема, поствоспалительная гиперпигментация (рис. 3) на теле, верхних и нижних конечностях. Зуд отсутствовал. Болезненность в суставах беспокоила значительно меньше.
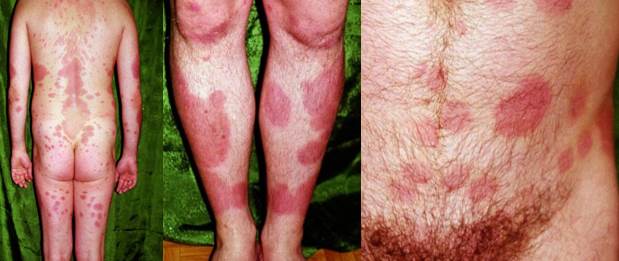
Рис. 3. Фотографии пациента через 4 недели после выписки (из архива кафедры дерматовенерологии и косметологии ИПО ФГБОУ ВО СамГМУ Минздрава РФ)
Также в ходе повторного наблюдения пациент не предъявляет ранее описанных жалоб на диспепсические расстройства. Следует отметить высокий комплаенс к проводимому медикаментозному курсу, хорошую переносимость метотрексата на фоне назначенной сопутствующей терапии (прием ингибитора протонной помпы, гастропротектора и комбинированной гепатопротективной терапии), снижение потребности в приеме НПВП в связи с артралгиями. Была отмечена положительная динамика в полученных лабораторных данных: уменьшение показателей цитолиза и холестаза: АлАТ 54,0 Ед/л (было 120,6 Ед/л), АсАТ 37,4 Ед/л (было 41,6 Ед/л), ГГТ 130 Ед/л (было 150 Ед/л), ЩФ 57 Ед/л (было 64 Ед/л). Общий анализ крови – без особенностей. Было рекомендовано продолжить ранее назначенный амбулаторный курс медикаментозной терапии без изменений.
Заключение
Таким образом, мультидисциплинарный подход в ведении пациентов с артропатической формой псориаза позволяет своевременно выявить коморбидность, определить оптимальный план обследования и назначить необходимую медикаментозную коррекцию, тем самым повысить приверженность (комплайнс) больного к длительному лечению и увеличить шансы на стойкую ремиссию.
Библиографическая ссылка
Арсеньева А.А., Пирогова Ю.Ю., Фатенков О.В., Орлов Е.В., Коннов П.Е. МУЛЬТИДИСЦИПЛИНАРНЫЙ ПОДХОД К ЛЕЧЕНИЮ АРТРОПАТИЧЕСКОЙ ФОРМЫ ПСОРИАЗА // Современные проблемы науки и образования. 2024. № 4. ;URL: https://science-education.ru/ru/article/view?id=33546 (дата обращения: 10.05.2026).
DOI: https://doi.org/10.17513/spno.33546



