Введение
Пациенты с грыжами составляют значительную часть контингента больных в отделениях общехирургического профиля. До 15–20% открытых абдоминальных вмешательств приводят к формированию послеоперационных грыж [1]. Особую сложность представляют собой вопросы лечения пациентов с большими дефектами брюшной стенки и потерей домена [1; 2]. В соответствии с международным дельфийским консенсусом выделяют три ключевых признака потери домена: грыжу не удается вправить из-за недостатка пространства, первичное фасциальное закрытие невозможно без использования специальных технических приемов, первичное фасциальное закрытие может привести к развитию абдоминального компартмент-синдрома (АКС) [2]. Для оценки ситуации рекомендуется использовать соотношение объемов грыжевого мешка и брюшной полости, измеренное с помощью компьютерной томографии, как это было предложено Tanaka E.Y. и Sabbagh C. [2; 3]. Мнения экспертов о том, какая доля перитонеального содержимого в грыжевом мешке точно соответствует потере домена, не всегда идентичны, однако чаще всего пороговым значением считают 20% [1; 2; 4].
Среди пациентов с большими послеоперационными грыжами немало коморбидных больных, для которых развитие ряда осложнений послеоперационного периода весьма опасно. Внедрение задней сепарации (в англоязычной литературе - TAR, transversus abdominis muscle release) позволило существенно расширить возможности реконструкции брюшной стенки [5; 6]. Тем не менее, даже в условиях ведущих хирургических центров с максимальным опытом таких операций, у большинства больных с большими грыжами после реконструкции брюшной стенки в послеоперационном периоде наблюдается интраабдоминальная гипертензия (ИАГ), а в ряде случаев - АКС [5; 6]. Это представляет собой жизнеугрожающую ситуацию [7], которая для клиник с меньшим опытом и ограниченными ресурсами может иметь негативные последствия и, по сути, недопустима. Спектр хирургических технологий, позволяющих осуществлять профилактику АКС, относительно невелик. Одним из наиболее часто используемых вариантов является bridging [1]. Данный термин, широко используемый как в англоязычной, так и в отечественной литературе, обозначает использование сетки в виде моста между краями грыжевого дефекта при невозможности надежного и/или безопасного ушивания листков влагалищ прямых мышц живота [1]. Такой подход не предусматривает выполнения реконструкции брюшной стенки и должен применяться лишь в тех ситуациях, когда иных вариантов завершения операции нет. К другим способам относят резекционные методики уменьшения объема содержимого брюшной полости. Опыт этих операций совсем небольшой [8], в существующих юридических реалиях в России любые осложнения таких вмешательств могут иметь серьезные последствия. С 1947 г. известна методика предоперационного растяжения брюшной стенки - прогрессивный предоперационный пневмоперитонеум (в англоязычной литературе PPP - preoperative progressive pneumoperitoneum). Результаты его применения впечатляют, хотя риск осложнений присутствует, есть сообщения и о летальности [9]. К сожалению, в России применение данного способа никак не регламентировано и находится за рамками правового поля. Другие варианты включают дозированное интраоперационное растяжение брюшной стенки с помощью специальных систем [10]. Авторами из Западной Европы получены хорошие результаты [10], однако указанная технология в РФ почти недоступна. Наиболее безопасно и детально исследовано за рубежом применение ботулотоксина типа A (в англоязычной литературе - BTA, botulinum toxin A) с целью предоперационной релаксации латеральных групп мышц [4; 11]. Методика эффективна и не содержит для пациента дополнительных рисков [4; 11]. В России имеются единичные публикации, в которых исследовано применение BTA перед выполнением протезирующей пластики; описанный авторами опыт однозначно положительный и вызывает большой научный и практический интерес [12]. Однако работ, основанных на комплексном подходе, включающем медикаментозную релаксацию латеральных групп мышц в сочетании с интраоперационным растяжением брюшной стенки с помощью карбоксиперитонеума и включением в план операции TAR, до настоящего времени в отечественной литературе не представлено.
Цель работы: изучение возможности и безопасности реконструкции брюшной стенки с помощью ботулотоксина типа А, лапароскопического подхода и сепарационной пластики у больных с большими послеоперационными грыжами и потерей домена.
Материал и методы исследования
В хирургическом отделении ГБУЗ НО «Городская больница № 35 Советского района г. Нижнего Новгорода» наблюдали 29 пациентов с большими послеоперационными грыжами. Больные были разделены на две группы. Первую группу составили 13 пациентов, включенных в описанный ниже протокол с их информированным согласием (подготовка пациента, введение ботулотоксина типа A в латеральные группы мышц брюшной стенки, лапароскопический подход, техника TAR). Контрольную (вторую) группу составили пациенты (n=16), последовательно оперированные по поводу больших послеоперационных грыж в этом же отделении в тот же временной интервал без использования указанного протокола подготовки, BTA и лапароскопии, которым также выполнена операция TAR в открытом варианте.
В первой группе выполняли комплексное обследование больных с оценкой операционно-анестезиологического риска и факторов, способствующих развитию ИАГ. Всем пациентам выполняли компьютерную томографию брюшной полости с измерением размеров грыжевого дефекта, объема грыжевого содержимого и брюшной полости по методу Tanaka [3]. Пример КТ у пациента с потерей домена приведен на рис. 1.
Ожирение представляет собой неустранимый в ходе операции фактор риска ИАГ, значение которого в этом отношении точно не определено [13]. Вид брюшной стенки пациентки с большой послеоперационной грыжей и морбидным ожирением представлен на рис. 2. Пациентам с индексом массы тела более 35 проводили предоперационную подготовку, направленную на снижение массы тела, путем назначения эндокринологом рекомбинантных агонистов глюкагоноподобного пептида 1 и/или установки внутрижелудочного баллона. После снижения индекса массы тела ниже 35 принимали окончательное решение об операции.
Далее в латеральные группы мышц выполняли инъекции BTA (Диспорт) под ультразвуковым контролем. Его максимальная разрешенная доза составляет 1000 ЕД. Использовали данный препарат в общей дозировке 500-600 ЕД для каждого пациента, разделенной поровну на 6 точек по передним аксиллярным линиям билатерально, соответственно в подреберной, мезогастральной и подвздошной областях, инфильтрируя при этом наружные, внутренние косые и поперечные мышцы живота. Техника и методика введения препарата соответствовали описанным в литературе [4; 11; 12]. Введение Диспорта показано на рис. 3. Каких-либо реакций на введение указанного медикамента не наблюдали, что также согласуется с публикациями коллег [4; 11; 12].
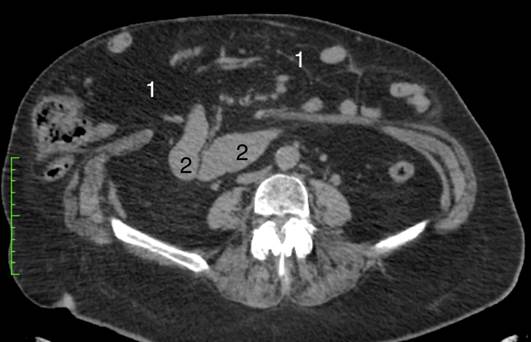
Рис. 1. КТ брюшной полости у пациента с потерей домена: 1 - содержимое грыжевого мешка; 2 - содержимое брюшной полости
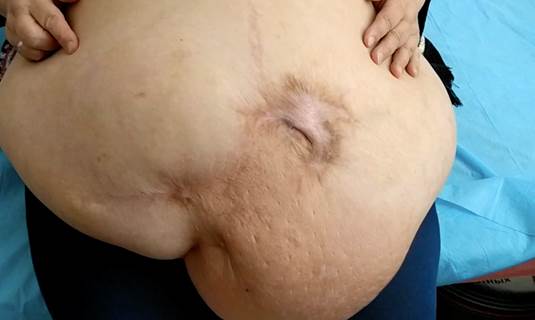
Рис. 2. Брюшная стенка у больной с большой послеоперационной грыжей, потерей домена и морбидным ожирением
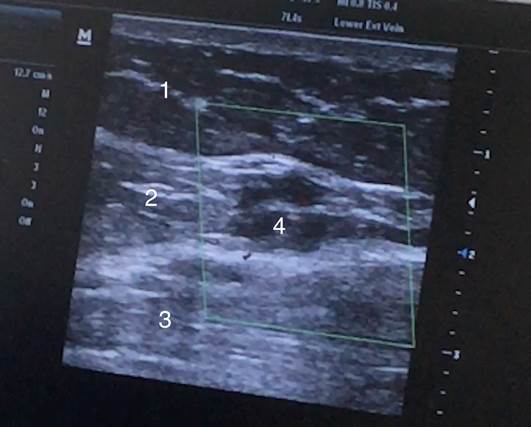
Рис. 3. Введение BTA под контролем УЗИ: 1 - подкожная клетчатка; 2 - мышцы латеральной группы; 3 - брюшная полость; 4 - введенный раствор BTA
После развития эффекта введения BTA пациентов приглашали на 2-й этап лечения. Операции выполняли в условиях тотальной внутривенной анестезии с миорелаксацией, интубацией трахеи и искусственной вентиляцией легких (ИВЛ). Операцию начинали лапароскопическим доступом, выполняя при этом все возможные у данного пациента этапы вмешательства, которые могли быть осуществлены с уверенностью и безопасно (адгезиолизис, преперитонеальная и ретромускулярная диссекция). Лапароскопический этап занимал от 60 до 120 минут в условиях карбоксиперитонеума с давлением 14 мм рт. ст. под контролем параметров ИВЛ, гемодинамики и газообмена.
Этап адгезиолизиса представлен на рис. 4. Преперитонеальная диссекция показана на рис. 5. Ретромускулярная диссекция отражена на рис. 6.
Затем выполняли открытый этап вмешательства, стандартный для всех пациентов - TAR [5; 6]. Техника операций на брюшной стенке содержала совокупность приемов, предложенных авторами TAR и принятых в клинической практике. Наиболее значимые моменты данного вмешательства детально изложены в литературе и доступны широкому кругу хирургов [5; 6].
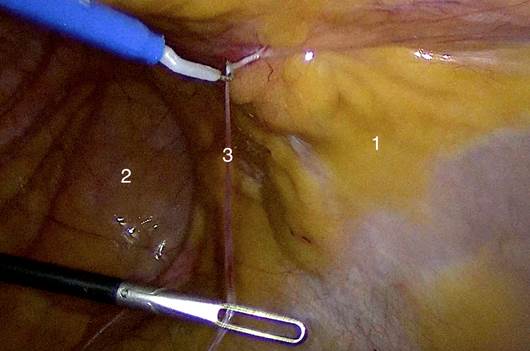
Рис. 4. Лапароскопический адгезиолизис: 1 – брюшина; 2 - полость грыжевого мешка; 3 - шнуровидная висцеропариетальная спайка
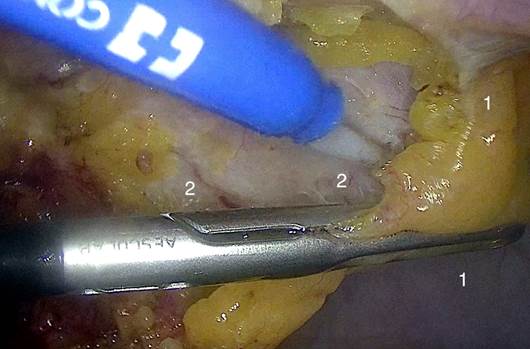
Рис. 5. Лапароскопическая преперитонеальная диссекция: 1 – брюшина; 2 - преперитонеальное пространство
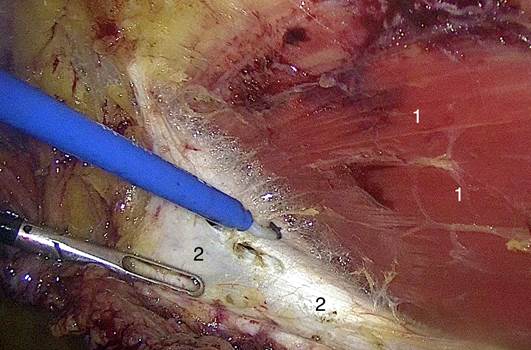
Рис. 6. Лапароскопическая ретромускулярная диссекция: 1 - прямая мышца живота; 2 - задний листок влагалища прямой мышцы живота
Основной этап TAR (пересечение поперечной мышцы живота) продемонстрирован на рис. 7.
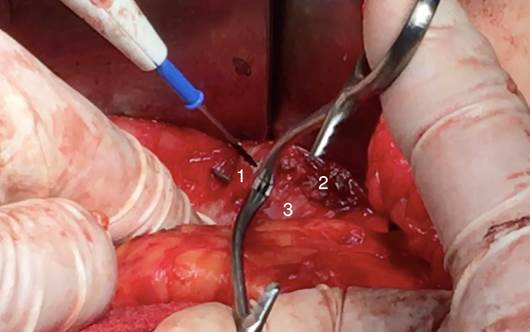
Рис. 7. Пересечение поперечной мышцы живота: 1 - волокна поперечной мышцы живота; 2 - пересеченные волокна поперечной мышцы живота; 3 - поперечная фасция
Далее непрерывным швом ушивали задние листки влагалищ прямых мышц живота (викрил 2/0). Ретромускулярно размещали полипропиленовую сетку (ES 3030, РФ) размерами и конфигурацией, соответствующими площади проведенной диссекции и требованиям Национальных рекомендаций РФ. Далее ушивали передние листки влагалищ прямых мышц живота непрерывным швом, стремясь к полной реконструкции брюшной стенки (PDS 0). Грыжевые мешки не иссекали, выполняли их пликацию. Ушивали рану.
Для исключения технических ошибок в период «кривой обучения» все этапы и навыки рассматриваемых вмешательств были полностью освоены и стандартизированы авторами данной работы в предшествовавших операциях и выполнялись хирургической бригадой, все члены которой владеют TAR в достаточной степени.
Статистический анализ значений проводили в программе Statistica 12.0. Поскольку распределение данных отличались от нормального, то для сравнения количественных показателей двух независимых выборок использовали критерий Mann – Whitney. Качественные признаки анализировали с помощью двустороннего точного критерия Fisher [14]. Статистически значимыми считали различия при уровне р<0,05. Распределение пациентов по полу и возрасту показано в таблице 1.
Таблица 1
Распределение больных по группам, полу и возрасту
|
|
Группа |
p, Fisher |
p, Mann - Whitney |
||
|
1 |
2 |
|
|
||
|
Пол |
Мужчины |
9 |
10 |
1 |
|
|
Женщины |
4 |
6 |
|||
|
Возраст |
Me |
56,2 |
50,2 |
|
0,1951 |
|
Me |
57 |
47,5 |
|||
|
IQR |
19 |
23 |
|||
|
Всего |
|
13 |
16 |
|
|
Таким образом, группы не имели статистически значимых отличий по полу и возрасту. Характеристика грыжевых дефектов представлена в таблице 2.
Таблица 2
Характеристика грыжевых дефектов
|
|
Группа |
p, Mann - Whitney |
p, Fisher |
||
|
1 |
2 |
|
|
||
|
Ширина грыжевых ворот |
Mean |
17,46 |
14,13 |
0,0736 |
|
|
Me |
17 |
12 |
|||
|
IQR |
5 |
8 |
|||
|
Площадь грыжевых ворот |
Mean |
336,07 |
250,25 |
0,083 |
|
|
Me |
289 |
258 |
|||
|
IQR |
212 |
134 |
|||
|
Площадь имплантируемой сетки |
Mean |
888,5 |
986,5 |
0,748 |
|
|
Me |
900 |
900 |
|||
|
IQR |
0 |
0 |
|||
|
Соотношение объема грыжевого мешка к объему перитонеального содержимого |
> 20% |
11 |
2 |
|
0,00015 |
|
< 20% |
2 |
14 |
|||
|
Mean |
0,47 |
0,18 |
0,0016 |
|
|
|
Me |
0,25 |
0,1 |
|||
|
IQR |
0,58 |
0,135 |
|||
Анализируемые группы не имели статистически значимых отличий по ширине и площади грыжевых ворот. Выявлено статистически значимое отличие в отношении феномена потери домена, который статистически значимо чаще встречался в первой группе, а соотношение объемов грыжевого мешка к объему перитонеального содержимого было в первой группе 0,25 (Me) и 0,1 (Me) во 2-й группе, p=0,0016. Таким образом, выполнение операций в первой группе было связано со значительными техническими трудностями, а осуществление профилактики АКС представляло собой весьма сложную задачу.
Результаты исследования и их обсуждение
У большинства пациентов в обеих группах удалось выполнить полное фасциальное закрытие дефекта, осуществив таким образом реконструкцию брюшной стенки. Только у 5 из 29 больных использован частичный bridging. Данные отражены в таблице 3. Несмотря на то, что контингент пациентов в первой группе был значимо сложнее для выполнения операции (пациенты имели потерю домена), чем во второй группе, реконструкция брюшной стенки в первой группе была осуществлена всем больным (статистически значимо чаще, p=0,04762).
Таблица 3
Характеристика выполненных операций
|
|
|
Группа |
p, Fisher |
|
|
1 |
2 |
|
||
|
Реконструкция брюшной стенки |
Полная |
13 |
11 |
0,04762 |
|
Неполная |
0 |
5 |
||
Подробные сведения о динамике ВБД представлены в таблице 4. Операции у всех 29 больных отвечали всем критериям безопасности с точки зрения профилактики АКС. Показатели внутрибрюшного давления в группах не имели статистически значимых отличий.
Таблица 4
Внутрибрюшное давление у оперированных пациентов
|
ВБД, мм рт. ст. |
|
Группа |
p, Mann - Whitney |
|
|
|
|
1 |
2 |
|
|
Исходное |
Mean |
4,15 |
4,56 |
0,3 |
|
Me |
4 |
4,5 |
||
|
IQR |
3 |
1 |
||
|
После операции |
Mean |
5,1 |
6,25 |
0,11 |
|
Me |
4 |
6 |
||
|
IQR |
2,55 |
2 |
||
|
1 сутки |
Mean |
6,42 |
5,5 |
0,57 |
|
Me |
3 |
5 |
||
|
IQR |
5,85 |
1,5 |
||
|
2 сутки |
Mean |
4,45 |
4,94 |
0,19 |
|
Me |
2 |
5 |
||
|
IQR |
4,25 |
2,5 |
||
В послеоперационном периоде наблюдали следующие осложнения: в первой группе парез кишечника и ретромускулярное жидкостное скопление с высокой температурой (антибиотикотерапия) и жидкостное скопление в ране (пункции под контролем УЗИ), во второй группе - высокая температура (антибиотикотерапия), нагноение раны (вакуумная терапия), инфицированная гематома (ревизия и удаление гематомы), венозный тромбоз (антикоагулянтная терапия) и сепсис (целевая антибиотикотерапия 4 препаратами). Все осложнения были купированы. Летальности в обеих группах не было. Данные об осложнениях представлены в таблице 5.
Таблица 5
Течение послеоперационного периода
|
Характер осложнений |
Класс по Clavien - Dindo |
Лечебные мероприятия |
Группа |
|
|
1 |
2 |
|||
|
Высокая температура |
II |
Антибиотикотерапия |
|
2 |
|
Ретромускулярное жидкостное скопление с высокой температурой |
II |
Антибиотикотерапия |
1 |
|
|
Венозный тромбоз |
II |
Антикоагулянтная терапия |
|
1 |
|
Парез кишечника |
II |
Стимуляция перистальтики |
1 |
|
|
Жидкостное скопление в ране с высокой температурой |
IIIA |
Антибиотикотерапия. Пункции под контролем УЗИ |
1 |
|
|
Нагноение раны |
IIIB |
Вакуумная терапия |
|
1 |
|
Инфицированная гематома |
IIIB |
Ревизия с удалением гематомы |
|
1 |
|
Сепсис |
IV |
Целевая антибиотикотерапия |
|
1 |
|
Всего |
|
|
5 |
6 |
По частоте осложнений послеоперационного периода и отдельным их классам статистически значимых отличий между группами не было (Fisher, p>0,05).
Результаты настоящего исследования не противоречат данным ранее опубликованных работ и согласуются с ними по смыслу. В частности, российские авторы убедительно продемонстрировали, что у больных с большими грыжами, оперированных после введения BTA, не отмечалось развитие АКС, а уровень внутрибрюшного давления не превышал 15 мм рт. ст. [12]. Полученные данные в ходе проведенной работы соответствуют данным наблюдениям. Вне всякого сомнения, такой подход представляется намного более безопасным, чем у ряда зарубежных коллег [5; 6], которые осознанно допускают развитие ИАГ в послеоперационном периоде с максимальными значениями до 36 мм рт. ст. Для стационаров с ограниченными ресурсами профилактика ИАГ и АКС особенно важна.
Ряд коллег рассматривают медикаментозную релаксацию латеральных групп мышц живота с помощью BTA в качестве альтернативы операциям TAR и Ramirez [12], стремясь несколько ограничить их применение. Другие сочетают эти технологии, а у определенной категории больных дополняют PPP указанной комбинацией методик [4]. Некоторые авторы используют BTA и PPP, а вопрос об применении TAR при необходимости решают в ходе операции [15]. Если без TAR реконструкцию выполнить проблематично или небезопасно, TAR используют без сомнений [15].
В рамках настоящего исследования использованы обе методики (BTA и TAR) в сочетании с растяжением брюшной стенки карбоксиперитонеумом. Не исключено, что для некоторых пациентов действительно было бы достаточно только BTA или TAR. На этот вопрос сложно дать однозначный ответ, ряд авторов применяет методики дифференцированно, в зависимости от особенностей пациента [4]. В этом отношении необходимо накопление опыта и проведение дальнейших исследований. Однако у лиц с большими грыжами и потерей домена (первая группа пациентов) именно при описанном комплексном подходе становится возможным безопасное выполнение полной реконструкции брюшной стенки. Следует обратить внимание, что использовать любые способы растяжения брюшной стенки (PPP или специальные системы) наиболее эффективно именно после введения BTA, о чем сообщают зарубежные авторы [4; 10].
Заключение
Применение ботулотоксина, лапароскопического подхода и задней сепарации позволяет осуществить полную реконструкцию брюшной стенки у пациентов с большими грыжами и потерей домена, при этом провести успешную профилактику развития абдоминального компартмент-синдрома.
Библиографическая ссылка
Паршиков В.В., Коновалова Е.А., Теремов С.А. ПЕРВЫЙ ОПЫТ ИСПОЛЬЗОВАНИЯ БОТУЛОТОКСИНА ТИПА A, ЛАПАРОСКОПИИ И ЗАДНЕЙ СЕПАРАЦИИ В ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ ПАЦИЕНТОВ С БОЛЬШИМИ ПОСЛЕОПЕРАЦИОННЫМИ ГРЫЖАМИ И ПОТЕРЕЙ ДОМЕНА // Современные проблемы науки и образования. 2024. № 4. ;URL: https://science-education.ru/ru/article/view?id=33532 (дата обращения: 11.04.2026).
DOI: https://doi.org/10.17513/spno.33532



