Послеоперационные осложнения в неотложной абдоминальной хирургии не потеряли своей актуальности, несмотря на современное развитие хирургии. Значительно чаще они встречаются после лапаротомий, в сравнении с лапароскопическими вмешательствами. Каждая релапаротомия, выполненная вследствие каких-либо осложнений, увеличивает продолжительность лечения и ухудшает прогноз [1–3].
Ряд авторов считает парез желудочно-кишечного тракта серьезной клинической проблемой, которая способствует развитию послеоперационных осложнений, в первую очередь у абдоминальных хирургических больных [4, 5]. Не купированная своевременно послеоперационная динамическая паралитическая кишечная непроходимость (послеоперационный парез кишечника) – довольно частая и весомая причина затяжной госпитализации. Симпатическая нервная система оказывает тормозящее действие на моторику кишечника, тогда как парасимпатическая ее усиливает. Баланс этих двух конкурирующих систем определяет количество ацетилхолина, высвобождаемого возбуждающими нервными импульсами в нервном сплетении кишечной стенки. Болевая перцепция в послеоперационном периоде подавляет парасимпатическую активность и чрезмерно активирует симпатическую нервную систему [6, 7].
Гуморальные механизмы регуляции вносят свой вклад в развитие пареза желудочно-кишечного тракта. Очень важны кинин-калликреиновая система (в частности, гистамин и брадикинин) и адреналин. Нарушения электролитного баланса, связанные со снижением объема циркулирующей крови, также способствуют развитию пареза [5, 6].
Опиоидные рецепторы играют важную роль в нейрогуморальной регуляции во всей центральной нервной системе и в желудочно-кишечном тракте в частности. Опиоидные обезболивающие препараты активируют μ-рецепторы в кишечнике, что приводит к снижению интенсивности моторики кишечника. Было доказано, что кумулятивная доза опиоидных препаратов является независимой переменной для развития паралитической кишечной непроходимости. Данный факт указывает на то, что по возможности следует использовать мультимодальный подход к обезболиванию, включающий ненаркотические препараты и селективную регионарную анестезию [4, 6, 7].
Инфекционное поражение раневого доступа является характерным и частым осложнением со стороны лапаротомии [2].
Послеоперационная пневмония продолжает привлекать к себе внимание хирургов, так как именно это осложнение очень часто сопровождает пациентов абдоминального хирургического профиля. Частота ее развития по некоторым данным варьируется от 1,5 до 15,8 %, а летальность – от 9 до 50 % [8, 9].
На сегодняшний день доказано, что ранняя послеоперационная активизация пациентов снижает послеоперационные осложнения в абдоминальной хирургии и является частью всех рекомендаций по расширенному восстановлению после операции [10, 11]. Отсюда понятно, насколько важным компонентом в комплексной профилактике послеоперационных осложнений в абдоминальной хирургии выступает адекватная анальгезия.
Цель исследования – предоставить сравнительный анализ течения послеоперационного периода в неотложной абдоминальной хирургии в зависимости от способа терапии раневой боли.
Материалы и методы исследования
Исследование проводилось с 2020 по 2023 г. на клинической базе кафедры факультетской хирургии им. проф. Ю.М. Лубенского ФГБОУ ВО КрасГМУ им. проф. В.Ф. Войно-Ясенецкого, в хирургических отделениях и ОРиИТ КГБУЗ «КМКБСМП им. Н.С. Карповича». В рамках исследования проведен анализ выраженности болевого синдрома со стороны операционной раны у 70 пациентов, которым была выполнена срединная лапаротомия в экстренном и срочном порядке по поводу травм и острых воспалительных заболеваний органов брюшной полости. Количество пациентов группы контроля составило 35 чел. – 16 (45,7±8,4 %) женщин и 19 (54,3±8,4 %) мужчин. Аналогичное количество больных включала и исследуемая группа, где женщин было 12 (34,3±8,0 %), а мужчин 23 (65,7 %±8,0 %). Обе исследуемые группы были сопоставимы по полу (р = 0,329), возрасту (р = 0,160), исходной тяжести общего состояния (табл. 1), характеру основной (табл. 2) и сопутствующей (табл. 3) патологии. Для участия в исследовании всеми пациентами было подписано добровольное информированное согласие.
Таблица 1
Основные признаки пациентов сравниваемых групп
|
Признак |
Контрольная группа, n = 35 |
Исследуемая группа, n = 35 |
p |
|
Пол |
16 (45,7±8,4 %) женщин |
12 (34,3±8,0 %) женщин |
0,3291 |
|
19 (54,3±8,4 %) мужчин |
23 (65,7 %±8,0 %) мужчины |
||
|
Возраст, Ме [P25; P75] |
53 [30; 64] |
60 [38; 68] |
0,1602 |
|
Тяжесть состояния при поступлении по SAPS II, Ме [P25; P75] |
15 [8; 20] |
20 [11; 20] |
0,2582 |
Примечание. 1 – при сравнении по критерию Пирсона χ2 (Пирсона Хи-квадрат); 2 – при сравнении по U-критерию Манна – Уитни.
Таблица 2
Структура пациентов по основной патологии
|
|
Контрольная группа, n = 35 |
Исследуемая группа, n = 35 |
|
Острая кишечная непроходимость |
13 (37,1±8,2 %) |
12 (34,3±8,0 %) |
|
Мезентериальный тромбоз |
1 (2,9±2,8 %) |
1 (2,9±2,8 %) |
|
Перфоративная гастродуоденальная язва |
8 (22,9±7,1 %) |
8 (22,9±7,1 %) |
|
Острый холецистит |
8 (22,9±7,1 %) |
8 (22,9±7,1 %) |
|
Травма органов брюшной полости |
3 (8,6±4,7 %) |
4 (11,4±5,4 %) |
|
Ущемленная вентральная грыжа |
1 (2,9±2,8 %) |
1 (2,9±2,8 %) |
|
Диагностическая лапаротомия |
1 (2,9±2,8 %) |
1 (2,9±2,8 %) |
Таблица 3
Структура пациентов по сопутствующей патологии
|
|
Контрольная группа, n = 35 |
Исследуемая группа, n = 35 |
|
Сахарный диабет |
5 (14,3±5,9 %) |
5 (14,3±5,9 %) |
|
Кардиологическая патология |
11 (31,4±7,8 %) |
13 (37,1±8,2 %) |
|
Вентральная грыжа |
1 (2,9±2,8 %) |
1 (2,9±2,8 %) |
|
Эрозивно-язвенные поражения верхних отделов ЖКТ |
2 (5,7±3,9 %); |
3 (8,6±4,7 %) |
|
Хроническая ишемия головного мозга |
1 (2,9±2,8 %) |
1 (2,9±2,8 %) |
|
Бронхиальная астма |
1 (2,9±2,8 %) |
1 (2,9±2,8 %) |
|
Хронический пиелонефрит |
– |
1 (2,9±2,8 %) |
Исследование проводилось в соответствии с Хельсинкской декларацией 1964 г. «Этические принципы проведения медицинских обследований с участием человека в качестве субъекта» с поправками 2013 г. и «Правилами клинической практики в Российской Федерации», утвержденными приказом Министерства здравоохранения Российской Федерации от 19.06.2003 № 266.
В исследование не включались пациенты с этапным ведением брюшной полости, больные с сочетанной травмой, пациенты, находящиеся в раннем послеоперационном периоде на аппарате искусственной вентиляции легких, пребывающие в бессознательном и терминальном состоянии, неконтактные или с выраженными когнитивными нарушениями и не способные к критическому мышлению. Наличие аллергии на ропивакаин являлось противопоказанием к участию в исследовании. Исключались также больные, не достигшие совершеннолетия.
Для профилактики послеоперационных осложнений пациенты обеих групп велись в послеоперационном периоде в соответствии с рекомендациями по расширенному восстановлению после операции [10, 11]:
- профилактика тромбоэмболических осложнений путем эластической компрессии нижних конечностей и применения низкомолекулярных гепаринов в соответствии со стратификацией риска по шкале Caprini;
- антибиотикопрофилактика (защищенными пенициллинами) и обработка кожи в соответствии со сроками проводимого вмешательства и индекса массы тела пациента;
- рестриктивная модель инфузионной терапии;
- профилактика послеоперационной тошноты и рвоты;
- отказ от рутинного использования назогастрального зонда и дренажей;
- раннее удаление уретрального катетера;
- раннее энтеральное питание в соответствии с тяжестью состояния и объемом оперативного вмешательства.
С целью купирования боли в первые дни после операции больные группы контроля получали опиоидные анальгетики и нестероидные противовоспалительные препараты (НПВП) в соответствии с рекомендациями по купированию болевого синдрома [12]. В исследуемой группе интраоперационно проводилась установка устройства, разработанного коллективом авторов (патент РФ 2797099 С1, 31.05.2023 (Бюл. № 16)) (рисунок). Данное устройство включает в себя следующие компоненты: 2 диализные трубки (полупроницаемые мембраны) необходимой длины (в зависимости от размера оперативного доступа) диаметром 6 мм, в которые устанавливаются полиуретановые катетеры (4–5 мм диаметром). Располагаются катетеры в диализных трубках таким образом, чтобы верхний край катетера не достигал верхушки диализной трубки, а нижний край значительно по длине превосходил аналогичный у мембраны, на катетеры наносятся незначительные перфорации иглой Дюфо или вырезаются ножницами. На верхний край трубки накладывается капроновая лигатура и герметично завязывается, аналогичным образом завязывается лигатура на нижний край мембраны, но уже поверх полиуретанового катетера. Данная манипуляция осуществляется для профилактики нежелательной утечки местного анестетика за счет герметизма в полости диализной трубки. При этом на верхнем участке края лигатур остаются достаточно длинными (около 10–15 см каждая). Имплантация производится перед закрытием раны в конце операции. Затем срединная лапаротомная рана ушивается, накладывается повязка. На этом хирургический этап заканчивается, выполняется завершающий этап сбора устройства. Соединяются между собой катетеры герметично за счет пластиковых и резиновых переходников медицинского назначения, к которым подключается эластомерная помпа с постоянной подачей местного анестетика. Сформированный комплекс диализных трубок с полиуретановыми трубками, описанный выше, размещается ретромускулярно (во влагалище прямых мышц живота) с двух сторон от срединной лапаротомной раны.
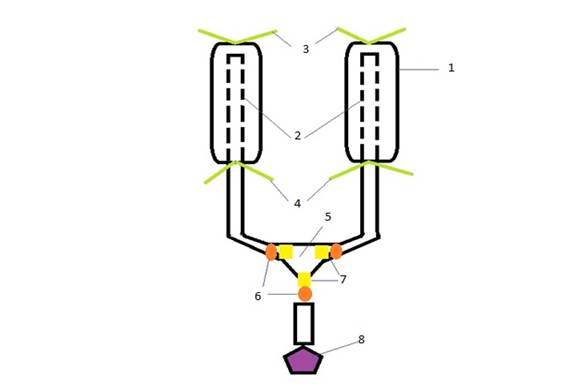
Схема устройства для местной анестезии срединной лапаротомной раны с использованием полупроницаемых мембран (1 – полупроницаемая мембрана, 2 – полихлорвиниловые катетеры, 3 – верхние лигатуры, 4 – нижние лигатуры, 5 – переходник, 6 – резиновые муфты, 7 – пластиковые муфты, 8 – инфузионнная (эластомерная) помпа)
Диагностика раневых осложнений проводилась с учетом клинической картины течения раневого процесса (наличие гиперемии, инфильтратов в области швов, характер экссудата при зондировании с направлением отделяемого на бактериологическое исследование), интраабдоминальных – по перистальтике, отхождению газов и наличию стула, по уровню внутрибрюшного давления (непрямой трансвезикальный метод), по дренажному отделяемому. Из экстраабдоминальных осложнений были выявлены только пневмонии, их диагностика осуществлялась при помощи оценки клинической картины врачом-пульмонологом с подтвержденной рентгенологической картиной. Других экстраабдоминальных осложнений в обеих группах выявлено не было.
Для расчета полученных данных использовалась программа Statistica, версия 12. Анализированные количественные данные не подчинялись закону нормального распределения по критериям Колмогорова – Смирнова с поправкой Лильефорса и Шапиро – Уилка, в связи с чем они представлены в виде медианы, 25 и 75 процентилей (Ме (P25; P75)). Различия между несвязанными группами проводились по критерию Манна – Уитни, а между связанными – по критерию Вилкоксона.
Качественные данные представлены в виде процентов и ошибки процентов (P±ОШ %). Результат сравнения различий качественного признака оценивался по критерию Хи-квадрат Пирсона и точному критерию Фишера. Если при сравнении статистических показателей между группами p < 0,05, то различия считались значимыми.
Результаты исследования и их обсуждение
Из 70 пациентов послеоперационный период осложнился только у 7 (10±3,6 %) человек.
Среди осложнений были выявлены следующие: один инфильтрат швов срединной лапаротомной раны, четыре пареза кишечника, две внутрибольничные пневмонии.
Инфильтрат области срединных швов был выявлен у 1 (2,9±2,8 %) больного контрольной группы на третьи сутки после операции. При ревизии швов в области инфильтрата зондом получен серозный экссудат, который взят на бактериологическое исследование, по результату которого отсутствовал рост микроорганизмов.
Парез кишечника проявлялся вздутием живота, отсутствием перистальтики кишечника и отхождения газов более 48 ч после операции [13]. У пациентов исследуемой группы послеоперационный парез кишечника был ликвидирован за 48 ч. У 4 (11,4±5,4 %) больных из контрольной группы парез кишечника сохранялся через 48 ч после операции (p = 0,114). Этим пациентам проводилась медикаментозная стимуляция желудочно-кишечного тракта до 72 ч. Указанные мероприятия оказались эффективными – купировалось вздутие живота, появилась активная перистальтика, начали отходить газы с последующим появлением самостоятельного стула в течение суток. При этом признаков внутрибрюшной гипертензии по проведенному измерению внутрибрюшного давления выявлено не было. Медиана внутрибрюшного давления на 4 сутки в контрольной группе составила 4,9 [4,7; 5,4] мм рт. ст., а в исследуемой – 4,8 [4,3; 5,1] мм рт. ст., однако эта разница между группами оказалась статистически незначимой (p = 0,268).
Внутрибольничные пневмонии были диагностированы у 2 (5,7±3,9 %) пациентов контрольной группы при наличии клиники фебрильной гипертермии, кашля, рентгенологически выявлена инфильтрация легочной ткани – диагноз подтвержден врачом-пульмонологом. Данный показатель статистически незначим (p = 0,493).
По итогу у 7 пациентов контрольной группы были выявлены послеоперационные осложнения, в исследуемой группе осложнения не выявлены (p = 0,011).
Койко-день в контрольной группе составил 10 [9; 14] дней, а в исследуемой группе – 10 [8; 13] дней. При этом отличия оказались статистически незначимыми (p = 0,515).
Учитывая то, что отличия в лечении пациентов в сравниваемых группах касались только способа обезболивания, авторы не могут исключить, что снижению количества осложнений способствовала адекватная анестезия в послеоперационном периоде, за счет инфузии анестетика через полупроницаемую мембрану. Диализная трубка, выполняющая роль мембраны, ввиду размера микропор позволяет беспрепятственно пропускать молекулы анестетика равномерно на всем протяжении раны, что исключает его депонирование в одних и полное отсутствие в других участках раны. Ретромускулярное (предбрюшинное) расположение катетеров (между прямыми мышцами и задними листками их влагалищ) позволяет выполнить блокаду прямых мышц живота, воздействуя на проходящие на этом уровне нервные волокна, которые иннервируют все слои брюшной стенки данного сегмента. Помимо этого, качественный обезболивающий эффект достигается за счет подачи анестетика непрерывно при помощи микроинфузионной помпы. Однако для более обоснованного заключения требуется более детальный анализ с большей выборкой пациентов.
При адекватном обезболивании пациенты интенсивнее включают брюшную стенку в акт дыхания, что приводит к увеличению экскурсии диафрагмы, а это снижает вероятность застойных явлений в легких [10, 11]. Кроме этого, за счет более ранней активизации пациентов улучшается системная микроциркуляция, это способствует адекватной регенерации поврежденных оперативным вмешательством тканей, а также более быстрому купированию воспалительного процесса [10, 11]. При полноценном мезентериальном кровотоке своевременно активизируется перистальтика кишечника, нормализуются процессы переваривания и всасывания. Это способствует профилактике пареза желудочно-кишечного тракта и более раннему переходу к полноценному энтеральному питанию [4, 10, 11]. Своевременное купирование парезов кишечника и отсутствие пневмоний в исследуемой группе авторы видят и в том, что у этих пациентов не применялись опиоиды, которые подавляют моторику желудочно-кишечного тракта и угнетают работу дыхательного центра [10].
Отсутствие осложнений, в первую очередь со стороны послеоперационной срединной раны, авторы связывают, помимо более адекватного кровотока на фоне ранней активизации, с непосредственным действием местного анестетика. Имеются данные о противовоспалительном эффекте данной группы препаратов [14]. Суть его заключается в подавлении активности лейкоцитов, которое приводит к снижению продукции медиаторов воспаления, что не влечет за собой подавление иммунитета на системном и местном уровнях, а лишь селективно подавляет их прайминг, препятствуя гиперергии. Доказано положительное влияние на проведение импульсов по нервным волокнам и между нейронами, а также на гладкую мускулатуру кишечника, что опять же объясняет отсутствие парезов кишечника в исследуемой группе [14]. Следует также отметить вазодилатирующий эффект местных анестетиков, который при анестезии области срединной лапаротомной раны способствует ее адекватной регенерации. Имеются данные, что профилактике инфицирования послеоперационной раны способствует антибактериальное действие [14] этой группы препаратов. Показано, что одним из анестетиков, обладающих наиболее выраженным противомикробным действием, как раз и является ропивакаин, причем чем выше его концентрация, тем более выражено антибактериальное действие препарата [14].
Заключение
Использование устройства для местной анестезии лапаротомной раны через полупроницаемую мембрану способствует уменьшению количества внутрибрюшных, экстраабдоминальных и раневых осложнений, в отличие от применения парентеральных анальгетиков, однако требуется более детальное изучение данной проблемы с набором большего количества групп исследования.
Библиографическая ссылка
Конторев К.В., Здзитовецкий Д.Э., Борисов Р.Н., Овсиенко Д.В. СНИЖЕНИЕ ПОСЛЕОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ В АБДОМИНАЛЬНОЙ ХИРУРГИИ ЗА СЧЁТ АДЕКВАТНОЙ АНЕСТЕЗИИ ЛАПАРОТОМНОЙ РАНЫ С ИСПОЛЬЗОВАНИЕМ ПОЛУПРОНИЦАЕМЫХ МЕМБРАН // Современные проблемы науки и образования. 2024. № 1. ;URL: https://science-education.ru/ru/article/view?id=33291 (дата обращения: 22.05.2026).
DOI: https://doi.org/10.17513/spno.33291



