Несмотря на многолетнюю историю вопроса, проблема оптимального способа восстановления непрерывности пищеварительной системы после гастрэктомии (ГЭ) до настоящего времени не нашла своего окончательного решения. Постгастрэктомические функциональные расстройства нарушают процессы пищеварения, ощутимо снижая качество жизни прооперированных больных, ухудшая их нутритивный статус, зачастую приводя к необходимости пожизненной диетической и медикаментозной коррекции и, в тяжелых случаях, инвалидизации [1, 2]. Нутритивная недостаточность после ГЭ развивается у 87% пациентов, из которых около 15% уже на момент постановки диагноза имеют потерю массы тела 10% и более за 6 месяцев [3]. В связи с этим, вопрос о выборе метода реконструкции пищеварительной системы после удаления желудка, обеспечивающего оптимальное качество жизни, компенсацию пищеварительных функций, поддержание приемлемого нутритивного статуса, не теряет своей актуальности [4,5].
Цель исследования – оценка непосредственных результатов ГЭ с реконструктивным этапом методом двойного тракта (РДТ) в сравнении с ГЭ по Ру.
Материалы и методы исследования. В исследование включены 55 пациентов, 29 пациентам выполнена ГЭ с РДТ (I группа), 26 – ГЭ по Ру (II группа). Критерии включения: возраст пациента старше 18 лет, гистологически верифицированная злокачественная опухоль желудка I – III стадий (T1-4a N0-3 M0), вид операции – гастрэктомия, наличие письменного информированного согласия на участие в исследовании. Отбор в исследование осуществлялся среди перенесших радикальное хирургическое лечение в отделении абдоминальной онкологии ГБУЗ «Клинический онкологический диспансер №1» Министерства здравоохранения Краснодарского края (ГБУЗ КОД №1 МЗ КК) в период 2020 – 2023 гг. Критерии исключения: наличие отдаленных метастазов, острых и хронических декомпенсированных сопутствующих заболеваний, туберкулез в активной стадии.
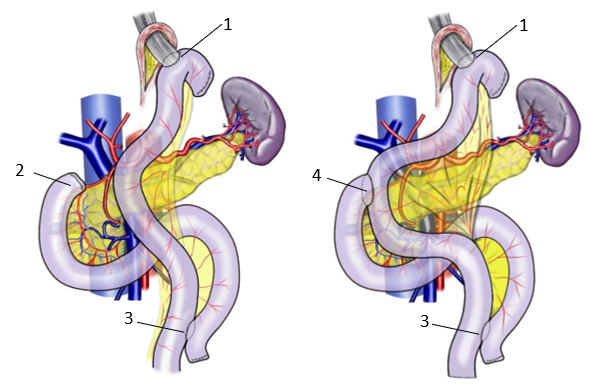
Характеристика пациентов представлена в таблице (таблица 1). ПриГЭ с РДТ (I группа) формировали эзофагоэнтероанастомоз (ЭЭА) на мобилизованной по Ру петле тощей кишки, соустье создавали с помощью циркулярного сшивающего аппарата «конец в бок» (рис. 1 Б, 1). На расстоянии 25 – 35 см (в зависимости от анатомической ситуации) однорядным непрерывным швом формировали анастомоз между двенадцатиперстной кишкой (ДПК) и алиментарной петлей по типу «конец в бок» (рис. 1Б, 4), реконструкцию завершали формированием межкишечного анастомоза между отводящей Ру-петлей и приводящей петлей тощей кишки, ушитой наглухо, по типу «бок в бок» (рис. 1 Б, 3), либо по типу «конец в бок». В группе контроля (ГЭ по Ру) формировали ЭЭА на мобилизованной по Ру петле тощей кишки аппаратным циркулярным швом (рис. 1 А, 1), культю ДПК ушивали наглухо (рис. 1А, 2), реконструкцию завершали формированием межкишечного анастомоза между Ру-петлей и приводящей петлей тощей кишки «бок в бок» (рис. 1 А, 3) или «конец в бок».
Таблица 1
Характеристика оперированных пациентов групп ГЭ с РДТ (I группа) и по Ру (II группа)
|
Показатель |
I группа (n=29) |
II группа (n=26) |
p |
|
Возраст, лет; средн. (СО) |
61,2 (9,5) |
57,5 (11,5) |
0,191 |
|
Масса тела, кг; средн. (СО) |
71,0 (11,1) |
75,5 (17,6) |
0,255 |
|
ИМТ, средн. (СО) |
25,3 (3,6) |
26,2 (5,8) |
0,464 |
|
Пол, n (%) |
|||
|
Мужской |
18 (62,1) |
16 (61,5) |
0,968 |
|
Женский |
11 (37,9) |
10 (38,5) |
|
|
Стадия по классификации TNM, n (%) |
|||
|
IA |
3 (10,3) |
4 (15,3) |
0,979 |
|
IB |
2 (6,9) |
2 (7,7) |
|
|
IIA |
4 (13,8) |
3 (11,5) |
|
|
IIB |
3 (10,3) |
3 (11,5) |
|
|
IIIA |
9 (31,0) |
6 (23,1) |
|
|
IIIB |
4 (13,8) |
4 (15,4) |
|
|
IIIC |
4 (13,8) |
4 (15,4) |
|
|
Локализация опухоли, n (%) |
|||
|
Кардиальный отдел, дно |
8 (27,6) |
5 (19,2) |
0,685 |
|
Тело желудка |
17 (58,6) |
16 (61,5) |
|
|
Антральный отдел |
1 (3,4) |
1 (3,8) |
|
|
Поражение, выходящее за пределы одной локализации |
3 (10,3) |
4 (15,3) |
|
|
Неоадъювантная химиотерапия, n (%) |
7 (24,1) |
6 (23,1) |
0,249 |
Примечание: СО – стандартная ошибка, ИМТ – индекс массы тела
Оценивали технические особенности операции, длительность операции, кровопотеря, длительность послеоперационного периода. При послеоперационном патологогистологическом исследовании оценивали количество удаленных лимфоузлов, количество лимфоузлов с метастазами, края резекции. Оценка осложнений проводилась с учетом Российской редакции классификации осложнений в хирургии, основанной на классификационной системе Clavien - Dindo - Strasberg, известной в литературе как классификация тяжести хирургических осложнений ACCORDION [6]. Для статистического анализа данных применены: анализ четырехпольных и многопольных произвольных таблиц сопряженности с использованием критерия хи-квадрат (χ2) Пирсона, H-критерий Краскела-Уоллиса, t-тест для независимых выборок. Пороговым критерием статистической значимости принято значение p<0,05. Для статистического анализа использовали программный пакет для статистической обработки данных IBM® SPSS Statistics 23.0 для Windows (IBM, США).
|
|
|
|
А |
Б |
|
Рис. 1. Схема реконструкции при ГЭ: А – по Ру; Б - с реконструкцией «двойной тракт» (РДТ). 1 – эзофаго-энтероанастомоз, 2 – культя ДПК, 3 – межкишечный анастомоз, 4 –дуодено-энтероанастомоз |
|
Результаты исследования и их обсуждение. По возрастному, половому составу, ИМТ, а также распределение по стадиям TNM, локализации опухоли, пациенты обеих групп не имели статистически значимых различий (табл. 1). Хирургическое лечение пациентов с раком желудка проводилось в соответствии с клиническими рекомендациями МЗ РФ. Объем лимфодиссекции соответствовал стандартному объему D2: удаление 1–7, 8а, 9, 10, 11р, 11d и 12а групп лимфатических узлов (+19, 20, 110 и 111 групп ЛУ при переходе опухоли на пищевод). Завершенный вид разработанной и стандартизированной методики операции ГЭ с РДТ представлен на рис. 2. Интраоперационных осложнений при выполнении реконструктивного этапа по типу РДТ не отмечалось, формирование дуодено-энтероанастомоза технически было возможно во всех случаях без технических сложностей.
По характеристикам доступа, частоте комбинированных операций, длительности операции, среднему показателю кровопотери различий между группами не было (таблица 2). Длительность операции не различалась между группами (166,4±23,0 мин в I группе и 164,4±34,8 мин во II группе, p=0,805), статистически значимых различий в кровопотере также не получено (229,3±54,3 мл vs 248,1±85,4 мл, p=0,330).
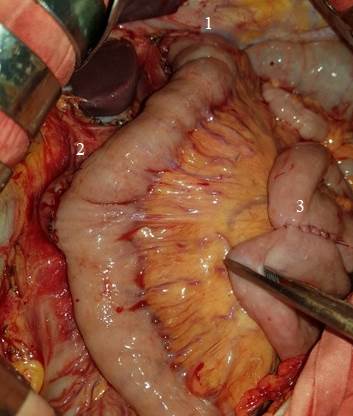
Рис. 2. Интраоперационная фотография реконструкции по методу РДТ при ГЭ: 1 – эзофаго-энтероанастомоз, 2 – дуодено-энтероанастомоз; 3 – межкишечный анастомоз
Длительность послеоперационного периода составила 7,4±1,2 сут. в I и 7,6±1,9 сут. во II группе (p=0,632). Летальных исходов не было в обеих группах. Осложнения наблюдались у 2-х пациентов I группы и 2-х – II группы. Во II группе отмечалось осложнение хирургического характера, потребовавшее реоперации (перфорация культи тонкой кишки). В остальных случаях имело место развитие пневмонии, причем в 2-х из них – вирусной этиологии (COVID-19). В связи с тем, что операции выполнялись пациентам с раком желудка, были оценены параметры онкологической безопасности технологии, которые также косвенно отражают степень радикальности операции. Количество удаленных при операции лимфоузлов в группе РДТ (18,7±7,1) статистически значимо не отличалось от показателя при стандартной ГЭ по Ру в группе контроля (19,8±4,5), не отмечено также различий в количестве лимфоузлов с метастазами и частоте R1 резекции.
Таблица 2
Характеристика результатов хирургического лечения
|
Показатель |
I группа (n=29) |
II группа (n=26) |
p |
|
Доступ, n (%) |
|||
|
Лапаротомия |
27 (93,1) |
23 (88,5) |
0,550 |
|
Абдомино-медиастинальный |
2 (6,9) |
3 (11,5) |
|
|
Комбинированный характер операции, n (%) |
8 (27,6) |
6 (23,1) |
0,702 |
|
Длительность операции, минут; средн. (СО) |
166,4 (23,0) |
164,4 (34,8) |
0,805 |
|
Кровопотеря, мл; средн. (СО) |
229,3 (54,3) |
248,1 (85,4) |
0,330 |
|
Длительность послеоперационного периода, сут.; средн. (СО) |
7,4 (1,2) |
7,6 (1,9) |
0,632 |
|
Количество удаленных лимфоузлов, n; средн. (СО) |
18,7 (7,1) |
19,8 (4,5) |
0,506 |
|
Количество лимфоузлов с метастазами, n; средн. (СО) |
4,3 (3,7) |
5,2 (4,9) |
0,593 |
|
Край резекции R1, n (%) |
2 (6,9) |
1 (3,8) |
0,339 |
|
Осложнения, n (%) |
|||
|
2 класс по Clavien - Dindo |
2 (6,9) |
1 (3,8) |
0,509 |
|
4 класс по Clavien - Dindo |
0 (0) |
1 (3,8) |
|
Метод реконструкции по типу двойного тракта (Double tract) был впервые описан K.Kajitani and J.Sato в Японии в 1965 г. (цит. по [7]). В последние десятилетия данная методика получила широкое распространение в азиатских странах при проксимальной резекции желудка (ПРЖ), во многих публикациях показано, что реконструкция ДТ после ПРЖ - простой, легко выполнимый метод с отличными послеоперационными результатами с точки зрения предотвращения симптомов рефлюкса и других свойственных для ПРЖ проблем [8]. При ГЭ методика РДТ применяется достаточно редко. R. Bandurski и соавторы сообщили об опыте применения РДТ после ГЭ у 75 пациентов, S.Maksimovic – 37 пациентов, M. Motamedi и соавторы - у 101 пациента, при этом о функциональных результатах, нутритивном статусе и качестве жизни в этих исследованиях не сообщается [9, 10, 11]. В отечественной литературе методика включения ДПК с «двойным пассажем» описана в работе [12].
В представленном исследовании предпринят анализ непосредственных результатов ГЭ с РДТ, выполняемой с применением ряда оригинальных технических приемов в отделении абдоминальной онкологии ГБУЗ КОД г. Краснодара. При этом автор не получил увеличения длительности операции, как это было отмечено в исследовании [13]. При выполнении ГЭ с РДТ не зарегистрирована статистически значимая разница по показателям осложнений и летальности. В представленном исследовании также не отмечено различий в кровопотере и длительности послеоперационной госпитализации, а также получена нулевая послеоперационная летальность, аналогично с литературными данными [13, 14]. Кроме того, продемонстрирована онкологическая безопасность восстановления непрерывности ЖКТ с восстановлением дуоденального пассажа, показано, что данная методика не влияет на качество лимфодиссекции, не приводит к увеличению частоты R+-резекции, и может использоваться у пациентов с раком желудка по аналогичным показаниям наравне с ГЭ по Ру.
Сопоставляя полученные в исследовании результаты с имеющимися в литературе аналогичными исследованиями, можно отметить метаанализ J. Hong и соавторов [15], в который авторы включили не только ГЭ, но и проксимальную и дистальную резекцию желудка с РДТ. Авторы пришли к выводам, что реконструкция РДТ сравнима с Ру по безопасности и хирургическим результатам, включая симптомы рефлюкса и послеоперационного восстановления, и демонстрируют определенные преимущества перед Ру с точки зрения приема пищи и поддержания массы тела. Полученные в исследовании результаты дают основание утверждать, что методика реконструкции РДТ при ГЭ характеризуется сопоставимой с традиционной реконструкцией по Ру хирургической и онкологической безопасностью. Это дает основание для проведения дальнейших исследований, направленных на объективную оценку отдаленных результатов данной операции, оценку функциональных последствий, влияния метода РДТ на качество жизни и нутритивный статус пациентов с раком желудка.
Заключение. Реконструкция методом двойного тракта при ГЭ сопоставима со стандартной реконструкцией по Ру по частоте осложнений, не приводит к увеличению длительности операции, кровопотери, длительности послеоперационного периода, а также не влияет на параметры радикальности операции. Технически процедура восстановления дуоденального пассажа отличается простотой и воспроизводимостью. Требуется дальнейшее изучение метода РДТ для оценки его потенциальных преимуществ в отдаленных функциональных результатах.
Библиографическая ссылка
Дербенев С.Н. РЕКОНСТРУКЦИЯ МЕТОДОМ ДВОЙНОГО ТРАКТА (DOUBLE-TRACT) В СРАВНЕНИИ С РЕКОНСТРУКЦИЕЙ ПО РУ ПРИ ГАСТРЭКТОМИИ: ОЦЕНКА НЕПОСРЕДСТВЕННЫХ РЕЗУЛЬТАТОВ // Современные проблемы науки и образования. 2024. № 1. ;URL: https://science-education.ru/ru/article/view?id=33287 (дата обращения: 22.05.2026).
DOI: https://doi.org/10.17513/spno.33287