В настоящее время представляет значительный интерес создание новой технологии лечения больных с дефектом большеберцовой кости, осложненным гнойной инфекцией. Это многофакторная проблема, требующая особого подхода. Сложность лечения пациентов с данной патологией связана с дополняющим его комплексом повреждений, таких как: сопутствующий перелом большеберцовой кости, гнойные раны, деформации, нарушения кровоснабжения и ряд других поражений. Реабилитация такой категории пациентов усугубляется изменением резистентности к большинству самых последних поколений антибактериальных средств, что способствует росту числа гнойных осложнений и часто заканчивается ампутацией [1]. В современных условиях ведения войны увеличивается частота тяжелых повреждений верхних и нижних конечностей, что требует применения многоэтапной хирургической тактики «damage control surgery». По данным военной статистики Istoria-mediajournal за 2020 год: от общего количества травм минно-разрывные и огнестрельные ранения нижних конечностей составляют 35%, верхних – 15% [2]. Многолетний опыт использования аппарата Илизарова и созданные на основе его применения методики управляемого чрескостного остеосинтеза (УЧО) имеют значительные возможности, реализация которых предполагает методичную работу по совершенствованию как компрессионно-дистракционных аппаратов, так и методик лечения [3, 4]. Существующие аппараты имеют ряд серьезных недостатков: они не всегда создают точную репозицию костных отломков, ее плавность и динамичность, в результате не обеспечивается оптимальный процесс регенерации кости [5–8]. Металлические конструкции аппаратов обладают чрезмерным весом и затрудняют рентгеновский контроль проведения остеосинтеза. На современном этапе в условиях анатомического эксперимента доказана необходимость [9] изготавливать определенные детали по размерам конструкции элементов аппарата в 3D. В настоящее время идет его внедрение в клиническую практику [10]. Анализ литературы также показал, что при лечении данной патологии нередко используется методика замещения дефекта большеберцовой кости аутотрансплантатом из малоберцовой кости на сосудистой ножке [11]. Однако данная костная пластика отличается высокой травматичностью, требует значительной резекции пораженного участка большеберцовой и малоберцовой костей. Ограничены возможности коррекции длины и деформации восстанавливаемой кости [12]. В «РНЦ «ВТО» им. академика Г.А. Илизарова разработан ряд методик замещения дефектов костей костным регенератом [12]. Но их применение требует остеотомии большеберцовой кости. При сопутствующем переломе большеберцовой кости данные методики не используются для получения костного регенерата с места перелома. Межберцовый регенераторный блок – это состояние стабилизации костным регенератом берцовых костей в центрированном положении, образующее единый конгломерат [13].
В условиях гнойной инфекции, возмещая посттравматический дефект большеберцовой кости за счет сопутствующего ему перелома с образованием в его области межберцового регенераторного блока, использовали прижимной элемент. Одновременно с этим при лечении воспользовались еще тремя новыми техническими решениями: методика «штекер» применена при сближении и контакте костных отломков в области диастаза; используя второй способ, удалось восстановить дефект мягких тканей; а с помощью третьего способа – ротационного модуля, основой которого является рентгенопрозрачное кольцо, изготовленное в 3D, устранили возникающее осложнение.
Цель исследования: показать возможности метода управляемого чрескостного остеосинтеза для лечения тяжелой категории больных путем разработки новых и модификации ранее разработанных способов лечения больных с дефектами большеберцовой кости при сопутствующем переломе в условиях гнойной инфекции.
Материал и методы исследования. Работа основана на изучении результатов управляемого чрескостного остеосинтеза при лечении пациента 29 лет с открытыми многооскольчатыми переломами костей левой голени (рис. 2а), полученными при автодорожной катастрофе.
Лечение пациента осуществлялось с помощью трех методик: «Способ замещения посттравматического дефекта большеберцовой кости» [14] (рис. 1а); «Способ замещения посттравматического дефекта большеберцовой кости с наличием дефекта мягких тканей» [15] (рис. 1б); «Способ сращения отломков диафизарной области длинной трубчатой кости при остеомиелитическом поражении» [16] (рис. 1в).
Перечисленные способы реализовывались на практике с использованием компрессионно-дистракционного аппарата [17] для устранения смещения отломков кости (рис. 1г).
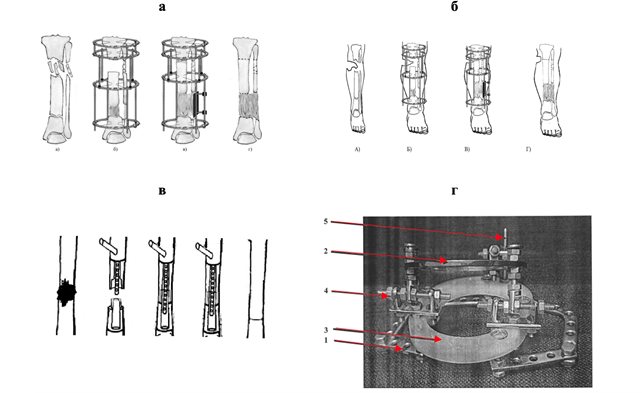
Рис. 1. Способы и средства, используемые при лечении пациента
Примечание к рисунку 1г: 1 – проксимальная, 2 – дистальная опоры (дуг, колец); 3 – рентгенопрозрачное кольцо; 4 – шарниры; 5 – дистракционные стержни
Хирургическое лечение хронического остеомиелита у пациента проводилось по методике А.И. Лапынина, А.А. Сафронова, В.И. Кима и иных «Способ оперативного лечения хронического остеомиелита» (Патент РФ на изобретение № 2676650/ 09.01.2019 г.).
Микробиологическое исследование раневого отделяемого раны пациента проводилось согласно приказу Минздрава России от 24.08.2020 г. № 889 на базе микробиологической лаборатории ФГБОУ ВО ОрГМУ Минздрава России.
Результаты исследования и их обсуждение
Анамнез: пациент А. 29 лет, ВИЧ-инфицированный, при автокатастрофе получил многооскольчатый перелом левой большеберцовой кости, который после удаления осколков кости преобразовался в посттравматический дефект длиной 12 см, а дистальнее его, на расстоянии 15 см, был зафиксирован перелом большеберцовой кости. По месту жительства больного не оперировали в течение 25 дней, предлагалась ампутация, от которой пострадавший отказался и был направлен в ГАУЗ «Городская клиническая больница №4» г. Оренбурга для уточнения дальнейшей тактики лечения пациента.
Результаты обследования: Травма была осложнена нагноением ран, флегмоной, посттравматическим остеомиелитом. Левый коленный сустав – под углом 170 градусов, движения качательные, болезненные. Левый голеностопный сустав – под углом 90 градусов, движения качательные, болезненные. Пульс на aa. dorsalis pedis et tibialis posterior слабого наполнения и напряжения. Движения пальцев качательные. Чувствительность на кожных покровах левой голени и стопы ослаблена.
Тактика лечения. К больному применена хирургическая тактика «damage control surgery». Разработан план этапного лечения. Первый этап – удаление костных отломков, нежизнеспособных мягких тканей, гнойного содержимого ран. После этого образуется посттравматический дефект большеберцовой кости на границе верхней и средней трети с сопутствующим ему переломом в нижней трети голени. Решено использовать остеосинтез компрессионно-дистракционным аппаратом, раны вести открыто, манипулируя компрессионно-дистракционным аппаратом, погрузить выступающие концы костных отломков в мягкие ткани задней поверхности голени. Вторым этапом запланировано комплексное консервативное лечение: переливание фракций крови, кровезаменителей, целенаправленная антибиотикотерапия. Третий этап: заместить дефект большеберцовой кости, устранить укорочение конечности, возместить дефект мягких тканей, восстановить целостность кожных покровов.
Проводимое хирургическое лечение у пациента на всех этапах осуществлялось под контролем рентгенографического исследования (рис. 2а–2д).
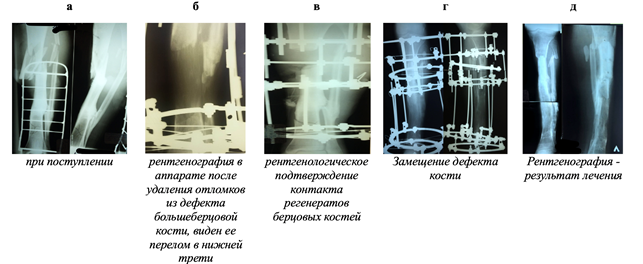
Рис. 2. Рентгенография пациента на различных этапах лечения
Пациенту при поступлении сделана операция: под общим наркозом удаление нежизнеспособных костных отломков, гнойного содержимого и участков мягких тканей (рис. 3а). После их удаления образовался посттравматический дефект 12 см в длину, произведен остеосинтез костей левой голени компрессионно-дистракционным аппаратом (рис. 3б).
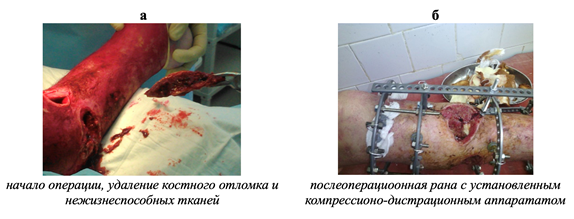
Рис. 3. Этапы хирургического лечения пациента
Согласно запатентованной методике, пациенту установили ротационный модуль между проксимальной и дистальной кольцевой опорой области торсионного смещения. Ротационный модуль (рис. 4) состоит из холостой (без спиц) рентгенопрозрачной кольцевой опоры, изготовленной в 3D (1). Параллельно плоскости к одной из ее сторон равномерно крепятся гайками (6) на консольных приставках (4) не менее трех резьбовых стержней (2). Перпендикулярно устанавливается на каждый из них с помощью консольной приставки (4) резьбовой стержень (5) для крепления к одной из баз аппарата внешней фиксации. С противоположной стороны резьбовыми стержнями кольцо ротационного модуля фиксируется к другой базе аппарата.

Рис. 4. Установленный на пациенте ротационный модуль прижимного устройства с базовым кольцом, изготовленным в 3D
Торсионная деформация устраняется за счет перемещения стержней по 0,25 мм в сутки в консольных приставках на холостом базовом кольце, изготовленным в 3D, за счет чего холостое кольцо с одной базой компрессионно-дистракционного аппарата вращаются вместе с одним из отломков кости и торсионная деформация дозированно устраняется.
У пациента для возмещения дефекта вместо остеотомии использовали перелом большеберцовой кости в ее нижней трети (рис. 2б). Для стимуляции ее костного регенерата на уровне перелома через 30 дней с момента дистракции выполнили остеотомию малоберцовой кости с целью сближения и контакта костных регенератов берцовых костей. Для этого с седьмого дня после остеотомии малоберцовой кости стали осуществлять дозированную дистракцию ее костных отломков в пределах 0,5–1,0 мм в сутки.
После получения костного регенерата малоберцовой кости длиной 5 см установили внешний прижимной элемент для сближения регенерата малоберцовой кости с регенератом большеберцовой кости (рис. 5). Пластиной внешнего прижимного элемента осуществляли упор на мягкие ткани и костный регенерат малоберцовой кости до ее погружения на 2,0 мм. Экспозиция такого напряжения была 1 час. Затем пластину с поверхности голени удаляли. На прежнее место ее устанавливали через 1 час и вновь создавали напряжение прижатия мягких тканей и костного регенерата малоберцовой кости пластиной до погружения до 2,0 мм. Данные манипуляции внешним прижимным элементом выполнялись в заданном режиме 8–9 раз в сутки с перерывом на дневной и ночной сон.

Рис. 5. Фотография внешнего прижимного устройства
В последующем дистракция осуществлялась по всем стержням с использованием внешнего прижимного элемента до сближения костных регенератов и их органотипической перестройки (рис. 2в). Срок дистракции составил 155 дней. На этот момент произошло сближение краев раны (рис. 6а). Окончательный демонтаж внешнего прижимного элемента выполнили при завершении фиксации в период органотипической перестройки костного регенерата. Прочность сращения проконтролировали путем клинической пробы и рентгенологически. После этого компрессионно-дистракционный аппарат был снят (рис. 2д). Срок фиксации составил 163 дня. Дополнительной иммобилизации не требовалось. Рана эпителизировалась (рис. 6б).
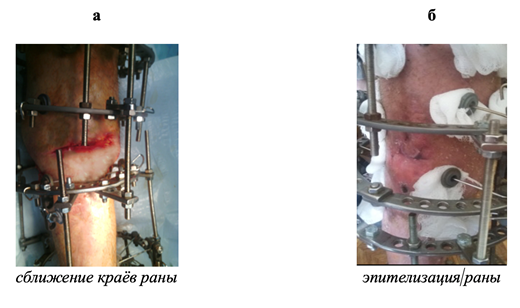
Рис. 6. Состояние раны после 155 дней дистракции
Пациент регулярно посещал занятия ЛФК. Движения в левом коленном суставе 180/90 градусов, голеностопном – 90/100 градусов. На момент демонтажа аппарата укорочения конечности не было.
Осложнения. Среди выделенных штаммов у больного превалировал Staphylococcus aureus (42,7%), а также микрофлора была представлена Proteus mirabilis (21,5%) и Streptococcus haemolyticus (14,3%) (табл.).
Соотношение показателей микрофлоры ран и свищей больного (%)
|
Состав микрофлоры |
При поступлении |
После операции |
||
|
1-й месяц |
3-й месяц |
5-й месяц |
||
|
Staphylococcus aureus |
42,7 |
36,3 |
50,0 |
– |
|
Proteus mirabilis |
21,5 |
27,3 |
22,5 |
– |
|
Streptococcus haemolyticus |
14,3 |
9,1 |
– |
– |
|
Pseudomonas aerugynosa |
– |
9,1 |
– |
– |
|
Другое |
21,5 |
18,2 |
27,5 |
– |
Обращает на себя внимание, что через месяц наблюдался довольно высокий процент выделения протея (от 21,5% до 27,3% случаев), причем количество выделенных штаммов возрастало в начале лечения. Прочие виды бактерий представлены в основном грамположительными палочками и единичными случаями выделения Alcaligenes faecalis, Enterobacter spp., Citrobacter spp., Staphylococcus epidermidis, Staphylococcus saprophyticus.
Результаты лечения: пациент передвигается без дополнительных средств опоры. Клиническая ось конечности правильная. Контрактура голеностопного сустава, тыльная флексия 80 градусов, подошвенная 110 градусов. Прогноз: благоприятный.
Обсуждение результатов лечения пациента. В послеоперационном периоде под влиянием напряжения в системе «аппарат – конечность» и целенаправленной антибиотикотерапии отмечалось уменьшение отделяемого из ран и свищевых каналов, изменялся его характер, четко прослеживался переход от гнойного содержимого к серозному с одновременным сокращением гноеродной микрофлоры. Активизация естественных антимикробных механизмов тканевой защиты, возникающая при чрескостном остеосинтезе, объясняется стимулирующим влиянием напряжения растяжения на неогенез тканей, адекватностью кровоснабжения и нагрузки. В основе механизма повышения естественной бактерицидной активности тканей лежат усиление интенсивности анаэробного гликолиза на начальных сроках лечения и оптимизация тканевой оксигенации в последующем. Кроме того, значительный вклад в описываемый феномен вносят суммарная бактерицидная активность сыворотки крови и клеточные реакции иммунитета (за счет усиления фагоцитоза, эффекторных функций лимфоцитов и др.). До настоящего времени молекулярные и клеточные механизмы данного явления остаются недостаточно изученными [1].
Воспаление мягких тканей в местах входа и выхода спиц является типичным при использовании методик управляемого чрескостного остеосинтеза. Причиной такого осложнения, как правило, служит нарушение техники остеосинтеза (имеются в виду недостаточная степень натяжения и жесткость крепления спиц на опорах), что приводит к их дестабилизации. В процессе дистракции было два эпизода, когда поочередно две спицы вырезались из кости. Появились гиперемия, прорезывание этими спицами мягких тканей, серозное отделяемое. Спицы удалили. Необходимо заметить, что при стабильной фиксации костных отломков места входа и выхода спиц окутываются эпидермальным валом, что является защитной реакцией организма, и разрушать на перевязках эту защиту нецелесообразно. Профилактикой воспаления является соблюдение техники проведения спиц: обязательное натяжение спиц спиценатягивателем, жесткое крепление на внешних опорах, использование спиц нужного диаметра и спиц с упорными площадками. Эффект от оперативного лечения за счет образования межкостного регенераторного блока на питающих ножках между берцовыми костями не только способствовал восстановлению опоры конечности и ликвидации укорочения, но и воздействовал на купирование гнойно-воспалительного состояния.
Усиление лечебного процесса происходило поочередно. Первый способ (изобретение) сочетался со второй методикой – комплексным клиническим лечением, использование которой расширяет лечебный диапазон. В последующем возникает необходимость подключения третьего способа при продолжении двух предыдущих. При появлении осложнения подключается действие четвертой технологии, также защищенной Патентом РФ. Без прерывания лечебного процесса применялись все методики как единое целое на фоне использования 3D-технологий. Данная аддитивная технология способствует применению управляемого чрескостного остеосинтеза при лечении больных, которым предлагалась только ампутация.
Выводы
1. Создание межберцового регенераторного блока способствует направленному костеобразованию из регенерата малоберцовой кости в регенерат большеберцовой. Предложенный, разработанный и внедренный способ замещения посттравматического дефекта при сопутствующем переломе большеберцовой кости может применяться в условиях гнойной инфекции.
2. Внедрение предложенных и использованных нами методик, а также сконструированного и примененного элемента прижатия и ротационного модуля способствовало динамической репозиции и сближению костных регенератов парных костей и мягких тканей. Восстановление костной структуры пострадавшей большеберцовой кости и мягких тканей голени достигнуто при образовании объединенного костного регенерата в области сопутствующего дистального перелома большеберцовой кости.
Библиографическая ссылка
Лапынин А.И., Гурьянов А.М., Лапынин Д.А., Ким В.И., Сафронов А.А., Захаров В.В., Даньшин Д.П., Дмитриев К.А., Реймер И.А., Булычева Е.В., Михайлова М.Е. АДДИТИВНОЕ ПРИМЕНЕНИЕ УПРАВЛЯЕМОГО ЧРЕСКОСТНОГО ОСТЕОСИНТЕЗА ДЛЯ ЗАМЕЩЕНИЯ ДЕФЕКТА БОЛЬШЕБЕРЦОВОЙ КОСТИ ПРИ СОПУТСТВУЮЩЕМ ЕЕ ПЕРЕЛОМЕ В УСЛОВИЯХ ГНОЙНОЙ ИНФЕКЦИИ // Современные проблемы науки и образования. 2023. № 6. ;URL: https://science-education.ru/ru/article/view?id=33134 (дата обращения: 15.05.2026).
DOI: https://doi.org/10.17513/spno.33134



