Артериальная гипотензия – частое нарушение в течение анестезии, которое может возникнуть на различных этапах, по разным причинам и с разными последствиями. Индукция анестезии с применением внутривенных анестетиков и наркотических анальгетиков снижает тонус симпатической нервной системы, уменьшает венозный возврат, а вентиляция с положительным давлением способствует усугублению гемодинамических нарушений. Гипотензия между вводной анестезией и разрезом является в значительной степени предотвратимым критическим инцидентом. Напротив, гипотензии во время операции избежать сложнее, поскольку она является многофакторной и возникает в результате кровопотери, изменения интенсивности воздействия, позиционирования пациента и сдавления магистральных сосудов. Устойчивые периоды гипотензии связаны с риском развития неблагоприятного исхода лечения в виде послеоперационных осложнений [1] и увеличения летальности [2].
Риск развития артериальной гипотензии зависит не только от анестезиологических и хирургических факторов, но и от сохранности механизмов поддержания артериального давления, среди которых наиболее важным в плане краткосрочной регуляции является артериальный барорефлекс [3]. При прогрессировании хронических заболеваний кардиореспираторной системы происходит нарушение рефлекторной регуляции в виде снижения чувствительности периферического хеморефлекса и снижения чувствительности артериального барорефлекса [4]. Проба с произвольным пороговым апноэ хорошо себя зарекомендовала в оценке функционального состояния кардиореспираторной системы как у здоровых добровольцев [5], так и в качестве предоперационного прогностического маркера гемодинамических нарушений [6]. Физиологическое обеспечение длительности произвольного порогового апноэ до сих пор является предметом дискуссий. Ключевая роль отводится чувствительности периферического хеморефлекса, однако другие факторы также могут оказывать влияние [7]. Тип метаболизма непосредственно влияет на потребление кислорода и продукцию углекислого газа и потенциально может вносить вклад в длительность апноэ.
Цель исследования: изучить влияние длительности ППА на течение анестезии у пациентов с различным дыхательным коэффициентом.
Материал и методы исследования
В исследование включены данные пациентов, оперированных на органах брюшной полости в ГБУЗ «ККБ № 2» с 1 января 2023 года по 31 августа 2023 года.
Критерии включения в исследование: пациенты старше 18 лет, подвергающиеся плановым оперативным вмешательствам на органах брюшной полости, физический статус которых соответствует I–III классам по ASA. Все пациенты подписывали добровольное информированное согласие на участие в исследовании.
Критерии исключения: острая массивная кровопотеря, аспирация, бронхоспазм, анафилактические реакции, злокачественная гипертермия, отказ от участия в исследовании.
Критерии невключения в исследование: отсутствие информированного согласия пациента, когнитивные нарушения.
Проба с максимальной задержкой дыхания на вдохе
Пробу с задержкой дыхания проводили следующим образом. Троекратно (с интервалом в 10 мин.) определяли длительность произвольного порогового апноэ (ППА), для чего после вдоха объемом, равным приблизительно 2/3 жизненной емкости легких, производится задержка дыхания. Длительность произвольного порогового апноэ измеряли от начала пробы до появления рефлекторных сокращений диафрагмы, определяемых пальпаторно. Рассчитывали среднее арифметическое значение длительности трех проб.
Оценка типа метаболизма
Определение типа метаболизма производили методом непрямой респираторной калориметрии (НРК) в открытом контуре (монитор «Тритон МПР 6-03 15») с расчетом дыхательного коэффициента (ДК). Все исследования проводили накануне операции. Пациенты воздерживались от приема пищи в течение 7 часов до исследования.
До начала проведения НРК обеспечивали обследуемому 30-минутный период покоя. Минимальная продолжительность периода покоя составляла 20 минут до достижения устойчивого состояния основного обмена. Критериями устойчивого состояния считали разброс показателей VО2 и VСО2 < 10%. Длительность исследования зависела от скорости достижения устойчивого состояния основного обмена и составляла около 30 мин. Данные, полученные в течение первых 5 минут, исключались из последующего анализа. Исследование основного обмена проводили в положении пациента лежа на спине в отдельном помещении, при температуре 22 °С, в тихой, спокойной обстановке без шума и других внешних раздражителей. Для оценки использовали мундштук с носовой клипсой.
При нефизиологических значениях ДК (>1,3 или <0,67) проводили повторное исследование после диагностики возможных технических проблем.
Анестезиологическое обеспечение
Всем пациентам оперативное вмешательство осуществлялось в условиях сочетания общей анестезии и эпидуральной анальгезии (катетер устанавливался на уровне Th 8 - Th 9, периоперационная анальгезия обеспечивалась введением раствора ропивокаина в концентрации 2 мг/мл).
Вводная анестезия обеспечивалась введением внутривенно пропофола дробно по 50 мг до достижения гипнотического эффекта (уровень биспектрального индекса менее 60) и фентанила, миорелаксация достигалась введением рокурония.
ИВЛ проводили аппаратом Datex Ohmeda (GE, США), во всех случаях дыхательный объем составлял 6-7 мл/кг должной массы тела, частота дыхания определялась уровнем напряжения углекислого газа в конечной порции выдоха (поддерживалась нормовентиляция).
Артериальное давление на всех этапах анестезии оценивалось инвазивным способом.
Формирование групп и подгрупп исследования
Вся исследуемая когорта была разделена на три группы в зависимости от уровня ДК. Группы были разделены на подгруппы в зависимости от уровня ППА (рис. 1).
Оцениваемые исходы
К первичным целевым точкам относили снижение артериального давления ниже 20% от исходного, максимальную выраженность снижения артериального давления в % от исходного, общую продолжительность эпизодов гипотензии (согласно дефиниции целевой точки).
Статистические методы исследования
Статистический анализ данных выполнялся с помощью программы MedCalc (MedCalc Software Ltd), версия 19.1.3.
Данные с нормальным распределением представлены в виде среднего значения ± стандартное отклонение, данные с распределением, отличным от нормального, представлены в виде медианы (25-75 перcентили).
Для сравнения исходных качественных переменных использовался точный тест Фишера, а для количественных переменных – критерий Крускала-Уоллиса. Во всех случаях уровень р менее 0,05 считали статистически значимым.
Для оценки влияния изучаемых переменных на выраженность артериальной гипотензии и общую длительность эпизодов гипотензии применяли множественный регрессионный анализ.
Для оценки роли изучаемых переменных в риске развития артериальной гипотензии применяли логистический регрессионный анализ. Прогностическая ценность полученной модели оценивалась с помощью ROC-анализа и определения площади под ROC-кривой (AUROC). Результат AUROC 0,70–0,79 считали имеющим удовлетворительную прогностическую ценность, результат 0,80–0,89 – хорошую прогностическую ценность, а результат 0,9 и более оценивали как обладающий отличной прогностической ценностью.
Результаты исследования и их обсуждение
Всего в исследование включены данные 92 пациентов (рис. 1). Значительная часть пациентов относилась к группе 2 (ДК 0,85-0,99) – больше половины.
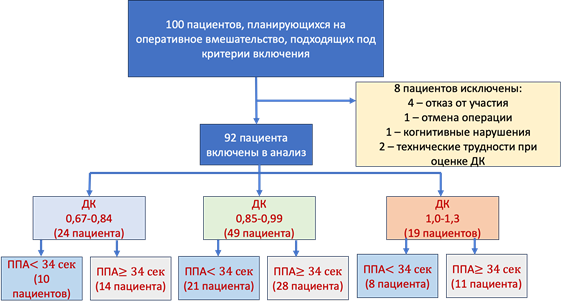
Рис. 1. Распределение пациентов в группы и подгруппы
По исходным характеристикам исследуемые группы различались по уровню ДК, что отражает дизайн исследования и деление на группы. По полу, возрасту, индексу массы тела, исходной тяжести по классификации ASA, пересмотренному индексу сердечно-сосудистого риска Lee статистически значимых различий отмечено не было (табл. 1).
Таблица 1
Характеристика исследуемых групп по исходным характеристикам
|
Параметр |
1 (ДК 0,67-0,84) |
2 (ДК 0,85-0,99) |
3 (ДК 1,00-1,30) |
p |
|
ДК |
0,75 (0,70-0,79) |
0,92 (0,88-0,95) |
1,045 (1,03-1,06) |
0,0001 |
|
Пол (жен.) |
54,2% |
53,0% |
52,6% |
0,99 |
|
ППА, сек. |
37 (27-56) |
40 (28-52) |
41 (27-54) |
0,26 |
|
ИМТ, кг/м2 |
26,1 (23-31,6) |
26,9 (23,5-30,9) |
26,4 (23,8-30,4) |
0,54 |
|
Возраст |
63 (53-68) |
59 (48-66) |
61 (49-65) |
0,35 |
|
Класс ASA 1 2 3 |
16,6% 58,4% 25,0% |
18,3% 55,1% 26,6% |
10,5% 63,1% 26,4% |
0,65 0,83 0,92 |
|
Пересмотренный индекс кардиального риска Lee |
2 (1-2) |
2 (1-2) |
2 (1-2) |
0,43 |
По интраоперационным параметрам, таким как длительность операции, интраоперационная кровопотеря, темп инфузии и потребность в вазопрессорах, группы также статистически значимо не различались (табл. 2).
Таблица 2
Характеристика исследуемых групп по интраоперационным характеристикам
|
Параметр |
1 (ДК 0,67-0,84) |
2 (ДК 0,85-0,99) |
3 (ДК 1,00-1,30) |
p |
|
Длительность операции |
225 (135-335) |
230 (155-330) |
220 (150-310) |
0,32 |
|
Гемоглобин, г/л |
113 (102-134) |
110 (101-125) |
116 (108-132) |
0,45 |
|
Интраоперационная кровопотеря, мл |
250 (150-300) |
300 (200-350) |
300 (150-350) |
0,51 |
|
Темп инфузии, мл/мин. |
11,1 (8-15,2) |
12,5 (8,3-18,8) |
10,2 (7,7-17,5) |
0,19 |
|
Потребность в вазопрессорах |
58% |
63% |
53% |
0,75 |
|
Потребность в гемотрансфузиях |
4% |
4% |
5% |
0,97 |
Во всех группах частота, длительность и выраженность артериальной гипотензии была выше в подгруппах пациентов с продолжительностью ППА менее 34 секунд, независимо от уровня ДК (табл. 3).
Таблица 3
Частота артериальной гипотензии, ее выраженность и продолжительность в подгруппах в зависимости от ППА и ДК
|
Группа |
1 (ДК 0,67-0,84) |
2 (ДК 0,85-0,99) |
3 (ДК 1,00-1,30) |
||||||
|
Подгруппа |
ППА |
ППА |
р |
ППА |
ППА |
р |
ППА |
ППА |
р |
|
Максимальное снижение АДср, % от исходного |
27 (17-38) |
15 (12-22) |
0,02 |
29 (19-35) |
15 (12-23) |
<0,0001 |
27 (21-34) |
15 (12-23) |
0,009 |
|
Общая длительность гипотензии, мин. |
23 (4-34) |
0 (0-12) |
0,01 |
22 (15-27) |
0 (0-17) |
0,0001 |
21 (12-26) |
0 (0-12) |
0,0011 |
|
Частота гипотензии, % |
70 |
21 |
0,035 |
71 |
39 |
0,04 |
75 |
27 |
0,07 |
Как показал многофакторный регрессионный анализ, параметрами, связанными с выраженностью гипотензии, являются длительность пробы с задержкой дыхания и количество баллов по шкале кардиального риска (табл. 4). Класс ASA, длительность операции и дыхательный коэффициент не оказали значимого влияния (скорректированный коэффициент детерминации R2-adjusted для модели составил 0,34, коэффициент множественной корреляции 0,68).
Таблица 4
Влияние переменных на выраженность гипотензии
|
Переменная |
k |
Ст. ошибка |
t |
P |
rpartial |
rsemipartial |
|
Константа |
34,9057 |
|||||
|
ППА |
-0,4064 |
0,06183 |
-6,572 |
<0,0001 |
-0,4856 |
0,4434 |
|
Пересмотренный индекс кардиального риска Lee |
2,8350 |
0,8090 |
3,504 |
0,0006 |
0,2840 |
0,2364 |
|
Длительность операции |
-0,01416 |
0,01113 |
1,272 |
0,2055 |
0,005 |
0,04 |
|
Класс ASA |
0,59 |
1,04 |
0,57 |
0,57 |
-0,003 |
0,002 |
|
Дыхательный коэффициент |
-0,28 |
6,34 |
-0,04 |
0,96 |
-0,003 |
0,002 |
Аналогичная закономерность была отмечена и при определении факторов, связанных с общей длительностью эпизодов гипотензии, ими оказались длительность ППА и количество баллов по шкале кардиального риска (табл. 5) (скорректированный коэффициент детерминации R2-adjusted для модели составил 0,25, коэффициент множественной корреляции 0,5). Остальные факторы, включая дыхательный коэффициент, статистически значимо не влияли на параметр.
Таблица 5
Влияние переменных на продолжительность гипотензии
|
Переменная |
k |
Ст. ошибка |
t |
P |
rpartial |
rsemipartial |
|
Константа |
36,6050 |
|||||
|
ППА |
-0,5801 |
0,1044 |
-5,569 |
<0,0001 |
-0,4284 |
0,3905 |
|
Пересмотренный индекс кардиального риска Lee |
3,4298 |
1,2973 |
2,644 |
0,0091 |
0,2196 |
0,1854 |
|
Длительность операции |
0,0035 |
0,0171 |
-0,207 |
0,8360 |
-0,0176 |
0,0145 |
|
Класс ASA |
-0,5403 |
1,5664 |
-0,411 |
0,6805 |
-0,0313 |
0,0228 |
|
Дыхательный коэффициент |
6,5475 |
9,5523 |
0,687 |
0,4994 |
-0,0555 |
0,0492 |
Логистический регрессионный анализ показал, что факторами, влияющими на риск развития артериальной гипотензии, были длительность ППА (ОШ 0,92 (95% ДИ 0,88-0,96)) и количество баллов по шкале кардиального риска (ОШ 2,42 (95% ДИ 1,35-2,34)) (табл. 6). Тест Хосмера-Лемешова для модели показал ее хорошие характеристики (хи-квадрат=4,3, р=0,8).
Таблица 6
Влияние переменных на риск развития гипотензии
|
Переменная |
Коэффициент |
СО |
Вальд |
P |
|
Пересмотренный индекс кардиального риска Lee |
0,88713 |
0,29737 |
8,8995 |
0,0029 |
|
ASA |
0,13421 |
0,34012 |
0,1557 |
0,6931 |
|
Длительность операции |
-0,0040366 |
0,0037397 |
1,1651 |
0,2804 |
|
Дыхательный коэффициент |
2,03933 |
2,18881 |
0,8681 |
0,3515 |
|
ППА |
-0,080524 |
0,023098 |
12,1537 |
0,0005 |
|
Константа |
0,42538 |
Площадь под ROC-кривой для полученной модели составила 0,79 (95% ДИ 0,71-0,86) (рис. 2).
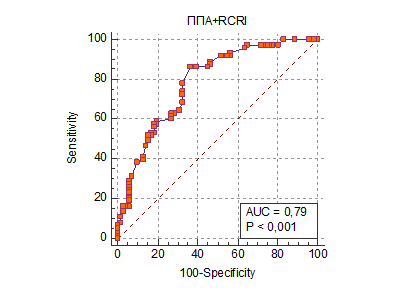
Рис. 2. Прогностическая значимость ППА в оценке риска гипотензии (снижение ниже 20% от исходного): ППА – произвольное пороговое апноэ, RCRI - пересмотренный индекс кардиального риска Lee, AUC – площадь под ROC-кривой
Основными результатами нашего исследования можно считать тот факт, что длительность произвольного порогового апноэ наряду с количеством баллов по шкале кардиального риска влияют на частоту артериальной гипотензии, ее выраженность и общую продолжительность эпизодов.
Частота артериальной гипотензии, наблюдаемая нами, оказалась достаточно высокой, что соотносится с данными литературы. Так, Maheshwari K. et al. сообщили о частоте артериальной гипотензии в 71% в некардиальной хирургии [8], а Mitsuru Ida et al. выявляли частоту в 96,8% [9].
Частота артериальной гипотензии была статистически значимо выше в группе пациентов с продолжительностью ППА менее 34 секунд. Нарушение рефлекторной регуляции кардиореспираторной системы увеличивает риск гемодинамических нарушений. Так Ranucci M. et al. показали, что дисфункция артериального барорефлекса является независимым предиктором гипотензии и острого повреждения почек и синдрома малого сердечного выброса после кардиальных операций [10]. Еще одна работа продемонстрировала, что пациенты со сниженной чувствительностью артериального барорефлекса в значительно большей степени склонны к развитию кардиоваскулярных осложнений и имеют большую длительность госпитализации [11].
Прогностическая ценность длительности ППА в комплексе предоперационной оценки была оценена в ряде работ, показавших, что частота критических инцидентов, в том числе гемодинамических, зависит от длительности ППА [6; 12; 13]. Наша работа показала, что эта закономерность сохраняется у пациентов с различным типом метаболизма, а дыхательный коэффициент, определенный в предоперационный период, не влияет на частоту, выраженность и длительность артериальной гипотензии. Это согласуется с данными, свидетельствующими об определяющей роли чувствительности периферического хеморефлекса в генезе ППА [5].
Не удивительной оказалась также роль шкалы кардиального риска в оценке вероятности артериальной гипотензии, это простой и широко используемый индекс, применяемый для прогнозирования серьезных сердечных осложнений после некардиальных операций. Он включает в себя шесть равнозначных компонентов: ишемическую болезнь сердца, сердечную недостаточность, цереброваскулярные заболевания, почечную недостаточность, сахарный диабет и хирургические вмешательства высокого риска [14; 15]. Несмотря на то, что способ был разработан в 1999 году, он до сих пор достаточно точно стратифицирует пациентов с различным периоперационным кардиальным риском [16-18]. Шкала, безусловно, имеет важные ограничения. Хотя индекс позволяет выявить пациентов с различным периоперационным кардиальным риском, он не позволяет точно предсказать абсолютный риск сердечно-сосудистых осложнений у отдельного пациента [19], возможно, из-за высокой чувствительности современных биохимических тестов, позволяющих лучше выявлять послеоперационное повреждение миокарда. Кроме того, некоторые компоненты индекса, такие как сахарный диабет, по мнению ряда авторов, необходимо исключить, поскольку они предоставляют минимальную прогностическую информацию [18]. Другие компоненты могут потребовать модификации для оптимизации шкалы. Например, почечную недостаточность лучше определять по скорости клубочковой фильтрации [18], а риск хирургических вмешательств может включать больше уровней сложности, чем в настоящее время [20]. Наконец, индекс, возможно, должен включать несколько других прогностически важных факторов риска, включая возраст, заболевания периферических артерий и функциональные возможности [16; 20]. Тем не менее, несмотря на указанные недостатки, наши данные продемонстрировали высокую надежность шкалы.
Безусловно, важным является не только оценка гемодинамических нарушений, но и вклад этих нарушений в риск неблагоприятного исхода. Как показывают многочисленные данные литературы, эта взаимосвязь есть [21]. Дальнейшее изучение роли ППА в выявлении этой взаимосвязи станет первым этапом на пути к поиску возможностей снижения риска.
Ограничения исследования. Основным ограничением исследования можно считать пилотный его характер, при проектировании дизайна не рассчитывался необходимый объем выборки. Первичными целевыми точками являлись гемодинамические нарушения в виде артериальной гипотензии, выраженной в процентах от исходного, и не учитывались абсолютные величины среднего артериального давления. Кроме того, не оценивалось влияние гемодинамических инцидентов на исход, что будет сделано в дальнейшем.
Заключение. Частота и длительность гипотензии более выражены у пациентов с длительностью ППА менее 34 секунд при всех типах метаболизма. Длительность ППА наряду с пересмотренным индексом кардиального риска связаны с выраженностью гипотензии и ее длительностью. Длительность ППА позволяет прогнозировать развитие артериальной гипотензии независимо от уровня предоперационного дыхательного коэффициента.
Библиографическая ссылка
Трембач Н.В., Федунец Д.Э., Дряев С.А., Мусаева Т.С., Вейлер Р.В., Трембач И.А., Заболотских И.Б. ВЛИЯНИЕ ДЛИТЕЛЬНОСТИ ПРОИЗВОЛЬНОГО ПОРОГОВОГО АПНОЭ НА ТЕЧЕНИЕ АНЕСТЕЗИИ ПРИ ОБШИРНЫХ АБДОМИНАЛЬНЫХ ОПЕРАЦИЯХ У ПАЦИЕНТОВ С РАЗЛИЧНЫМ ТИПОМ МЕТАБОЛИЗМА: ПИЛОТНОЕ ИССЛЕДОВАНИЕ // Современные проблемы науки и образования. 2023. № 6. ;URL: https://science-education.ru/ru/article/view?id=33083 (дата обращения: 15.05.2026).
DOI: https://doi.org/10.17513/spno.33083




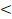 34 сек.
34 сек.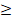 34 сек.
34 сек.