Нейрофиброматозы – группа наследственных заболеваний, характеризующихся появлением множественных доброкачественных и реже злокачественных опухолей центральной и периферической нервной системы [Ошибка! Источник ссылки не найден.]. Нейрофиброматоз I типа (ранее известный как периферический (НФ1)) – одно из наиболее часто встречающихся генетических заболеваний, его распространенность составляет 1:3000–4000 человек. Заболевание отличается высокой вариабельностью клинической картины: комбинация фенотипических проявлений и степень их выраженности могут значительно различаться как в общей популяции больных, так и между членами одной семьи [Ошибка! Источник ссылки не найден.].
Этиологическим фактором развития НФ I выступает патогенная мутация в гене NF1, расположенном на длинном плече 17-й хромосомы. Продукт гена, белок нейрофибромин, негативно регулирует активность онкогенов Ras за счет гидролиза их активных ГТФ-связанных форм в неактивные ГДФ-связанные. Соответственно, мутации в гене NF1 приводят к стимуляции Ras и усиленной пролиферации клеток с формированием доброкачественных (нейрофибром, глиом) и злокачественных опухолей [Ошибка! Источник ссылки не найден., Ошибка! Источник ссылки не найден., Ошибка! Источник ссылки не найден.]. Исследования на мышах также продемонстрировали решающую роль нейрофибрина в управлении мезенхимальных стволовых клеток для дифференцировки остеобластов [Ошибка! Источник ссылки не найден., Ошибка! Источник ссылки не найден.].
В 2021 году были утверждены диагностические критерии, которые позволяют поставить диагноз:
А) для пациентов без семейной истории – при наличии 2 признаков из следующих: 1) 6 или более пятен по типу «кофе с молоком» (CALM – café-au-lait macules) более 5 мм в допубертате и более 15 мм в постпубертате; 2) веснушки в подмышечной или паховой области; 3) 2 или более нейрофибромы любого типа или 1 плексиформная нейрофиброма;4) глиома зрительного нерва; 5) 2 или более узелка Лиша или 2 или более аномалии хориоидеи; 6) характерное поражение костей (клиновидная дисплазия или псевдоартроз); 7) гетерозиготный патогенный вариант в гене NF1;
Б) для пациентов с семейной историей достаточно лишь одного признака из перечисленных выше [Ошибка! Источник ссылки не найден., Ошибка! Источник ссылки не найден., Ошибка! Источник ссылки не найден.].
CALM определяются у 99 больных, а поражение костной системы выявлено у 60% пациентов с нейрофиброматозом 1-го типа. Наиболее часто наблюдаются деформации позвоночника. Поражение трубчатых костей (чаще всего большеберцовой кости) проявляется в их врожденном искривлении или истончении, при этом врожденный псевдоартроз отмечен у 4–5% пациентов [Ошибка! Источник ссылки не найден., Ошибка! Источник ссылки не найден., Ошибка! Источник ссылки не найден., Ошибка! Источник ссылки не найден.]. Кроме того, по данным литературы, у детей с НФ1 в 3,4 раза выше риск развития переломов, чем у пациентов контрольной группы без НФ1, что связано с развитием остеопороза [Ошибка! Источник ссылки не найден.]. Поражение верхних конечностей встречается редко, описано около 100 случаев. Псевдоартроз может возникать на костях предплечья как изолированно, так и поражать обе кости. С ростом ребенка (при отсутствии лечения) происходит прогрессирование деформации, что приводит к косметическим и функциональным нарушениям [Ошибка! Источник ссылки не найден., Ошибка! Источник ссылки не найден.].
Лечение данного контингента пациентов представляет сложную задачу в связи с высоким риском осложнений и отсутствием консолидации костных фрагментов. Основные задачи лечения: 1) успешное сращение ложного сустава и предотвращение повторного перелома; 2) стабилизация суставов предплечья (дистальный лучелоктевой, локтевой и лучезапястный суставы); 3) исправление осевой деформации и устранение разницы длины конечностей; 4) сохранение функционирующих зон рост у детей [Ошибка! Источник ссылки не найден., Ошибка! Источник ссылки не найден.]. В литературе представлены различные методики хирургического лечения: пластика ложного сустава неваскуляризованным аутотрансплантатом, микрохирургическая пересадка малоберцовой кости, формирование лучелоктевого синостоза, транспорт костных сегментов, основанный на принципах дистракционного остеогенеза [Ошибка! Источник ссылки не найден., Ошибка! Источник ссылки не найден., Ошибка! Источник ссылки не найден.]. Однако до сих пор нет единого мнения о том, какой тип костного трансплантата следует использовать. Губчатая кость обладает лучшим остеогенным потенциалом, но гораздо более восприимчива к резорбции. Однако кортикальные распорные трансплантаты обладают лучшей устойчивостью к резорбции и приемлемым остеогенным потенциалом, особенно при использовании в качестве васкуляризованного трансплантата. К недостаткам относятся связанные с этим болезненные ощущения в месте забора (обычно здоровая конечность), длительная операция и сложная микрохирургическая техника [Ошибка! Источник ссылки не найден.].
При любом варианте оперативного лечения необходима стабильная фиксация, возможно использование пластины, интрамедуллярного гвоздя, внешней фиксации или комбинации вышеперечисленных методов [Ошибка! Источник ссылки не найден., Ошибка! Источник ссылки не найден.]. Рекомендуемый хирургический протокол состоит из резекции ложного сустава, интрамедуллярного остеосинтеза и костной пластики, что позволяет достичь удовлетворительных результатов в 80% случаев [Ошибка! Источник ссылки не найден.].
Цель исследования – рассмотреть клинический случай лечения пациента с нейрофиброматозом, одним из симптомов которого являлась врожденная локтевая косорукость.
Материалы и методы исследования
В исследовании представлен пациент мальчик Д., 6 лет, которому проводились обследование и оперативное лечение в ФГБУ «НМИЦ детской травматологии и ортопедии им. Г.И. Турнера» Минздрава РФ. Представлены данные клинического обследования и инструментальных методов исследования, а также результаты хирургического лечения. Пациенту были выполнены рентгенографическое обследование, компьютерная томография и магнитно-резонансная томография в сосудистом режиме.
Клинический случай
Пациент Д., 6 лет, поступил в клинику реконструктивной микрохирургии и хирургии кисти ФГБУ «НМИЦ детской травматологии и ортопедии им. Г.И. Турнера» Минздрава РФ с жалобами на деформацию и укорочение правого предплечья. Из анамнеза известно, что ребенок от 3-й беременности, протекавшей без особенностей, 3-х естественных родов на сроке гестации 38 недель. Старшие дети здоровы, семейный анамнез не отягощен.
При клиническом осмотре отмечены пигментные пятна цвета «кофе с молоком» на коже спины, бедер, живота размерами от 5 до 10 мм. Движения в суставах левой верхней и нижних конечностях в полном объеме. Выявлены гипоплазия мягких тканей, укорочение правой верхней конечности за счет предплечья на 3 см. Сгибание в локтевом суставе в полном объеме, ограничение ротационных движений до 30°, гипермобильность локтевого сустава. Подвывих головки лучевой кости и саблевидная деформация ее диафиза. Движения в лучезапястном суставе и суставах правой кисти в полном объеме.
По данным лучевой диагностики отмечаются укорочение на 1,8 см (по отношению к лучевой) и деформация локтевой кости, истончение ее диафиза, ложный сустав в средней трети, угловая деформация лучевой кости в средней трети 25° (рис. 1а, 1б, 1в). При проведении магнитно-резонансной томографии в сосудистом режиме визуализированы лучевая и локтевая артерии (рис. 1г).
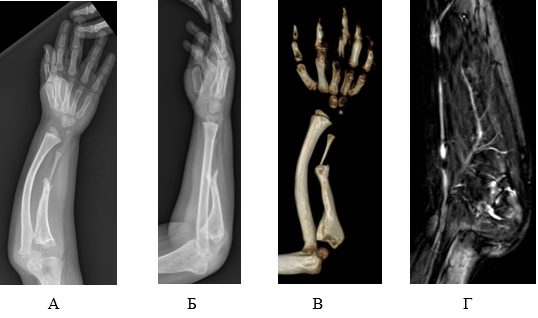
Рис. 1. Результаты лучевой диагностики у пациента Д., 6 лет (описание в тексте)
А, Б, В – рентегенограмма и компьютерная томография предплечья до начала оперативного лечения, Г – магнитно-резонансная томография в сосудистом режиме
Пациенту выставлен диагноз «нейрофиброматоз I типа, локтевая косорукость». После результатов обследования принято решение о проведении оперативного лечения с целью устранения имеющейся деформации предплечья. Первым этапом выполнены остеотомия локтевой кости, монтаж аппарата внешней фиксации (АВФ). Из Г-образного разреза на боковой поверхности предплечья в средней трети выделена локтевая кость. Произведена ее остеотомия на данном уровне с иссечением фрагмента костно-хрящевого тяжа длиной 5 мм от средней трети до дистального отдела. Наложены швы на рану. Далее проведены 2 перекрестные спицы в проксимальном отделе локтевой кости, 2 – в дистальном отделе лучевой кости и 1 спица – через 2–5-е пястные кости. Спицы фиксированы в двух кольцах дистракционного аппарата, скрепленных между собой 3 штангами.
Дистракция начата на 2-е сутки после операции по 0,25 мм 3 раза в сутки. После низведения дистального фрагмента локтевой кости диастаз составил 5,9 см (рис. 2а). Период коррекции составил 36 дней, остеосинтеза – 68 дней. В течение всего периода остеосинтеза проводилась лечебная физкультура, направленная на разработку движений в локтевом суставе и суставах пальцев кисти, по 20–30 минут 3–4 раза в сутки.
Вторым этапом выполнены демонтаж АВФ, микрохирургическая аутотрансплантация фрагмента малоберцовой кости в позицию локтевой кости. После демонтажа АВФ из зигзагообразного разреза на ульнарной поверхности предплечья выделены дистальный и проксимальный фрагменты локтевой кости, диастаз между ними составил 6,5 см. В проксимальном и дистальном углах разреза выделены локтевая артерии, v.basilica.
Выполнен продольный разрез по наружной поверхности голени в проекции малоберцовой кости с формированием «буйкового» лоскута. «Буйковый» лоскут необходим для оценки кровообращения аутотрансплантата в послеоперационном периоде. По задней поверхности кости на межкостной мембране обнаружена малоберцовая артерия с сопровождающими ее венами. Начиная с дистального отдела, в проксимальном направлении она выделена на протяжении 8 см, перевязаны все мышечные ветви. После остеотомии малоберцовой кости в двух местах и перевязки сопровождающих сосудов в дистальном и проксимальном отделах трансплантат заимствован из донорской области. После этого наложены послойно швы на рану голени.
Трансплантат перенесен на предплечье и сопоставлен с дистальным и проксимальным отделами локтевой кости, зафиксирован двумя продольно проведенными спицами. На контрольной рентгенограмме положение фрагментов и МОС удовлетворительное (рис. 2б). Наложены анастомозы конец в конец в проксимальном и дистальном отделах между локтевой и малоберцовой артерией, коммитантой веной и v.basilica. После снятия клипс получен устойчивый кровоток в трансплантате. Послойно наложены швы на рану, гипсовые лонгеты на правую верхнюю и левую нижнюю конечности.
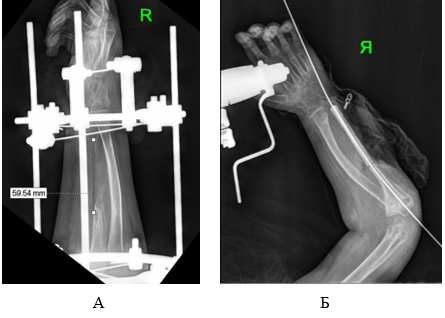
Рис. 2. Рентгенограмма предплечья пациента Д., 6 лет на этапе оперативного лечения: А – после низведения дистального отдела локтевой кости, Б – после микрохирургической аутотрансплантации фрагмента малоберцовой кости в диастаз локтевой кости
Швы сняты на 18-е сутки после операции. Раны зажили первичным натяжением. Осевая спица в проекции 5-й пястной кости удалена через 65 дней после контрольной рентгенограммы. Начата разработка движений в суставах верхней конечности. Пациенту разрешено использование руки в быту, с ограничениями по занятию спортом. При рентгенологическом исследовании через 6 месяцев выявлено, что сохраняется зона псевдоартроза в проксимальном отделе «локтевая кость – аутотрансплантат», в связи с чем принято решение о сохранении интрамедуллярной спицы (рис. 3а, 3б). Через 1 год после оперативного вмешательства выполнены рентгенологическое исследование и компьютерная томография предплечья. По полученным данным отмечены полная консолидация фрагментов, тенденция к регрессии саблевидной деформации лучевой кости (до 25° – после 17°) (рис. 3в, 3г, 3д), интрамедуллярная спица удалена, разрешена полная нагрузка на конечность.
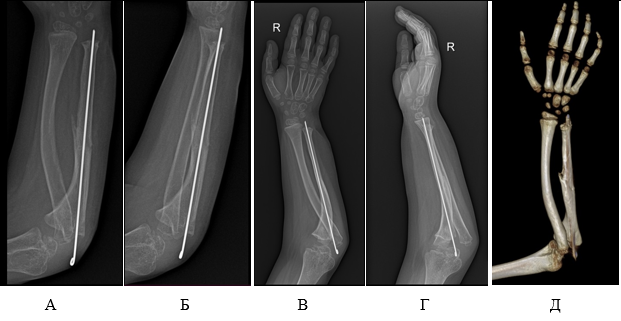
Рис. 3. Данные лучевой диагностики пациента Д.: А, Б – рентгенограмма предплечья через 6 месяцев после микрохирургической аутотрансплантации фрагмента малоберцовой кости В,Г,Д – рентгенограмма и компьютерная томография предплечья через 1 год после микрохирургической аутотрансплантации фрагмента малоберцовой кости
Обсуждение
Хирургическому лечению пациентов с локтевой косорукостью на фоне нейрофиброматоза посвящено незначительное количество работ в современной литературе. Однако актуальность этого вопроса неоспорима в связи с высокой частотой встречаемости данного заболевания [Ошибка! Источник ссылки не найден.]. У пациентов отмечена тенденция к увеличению деформации предплечья. Причинами прогрессирования являются врожденный псевдоартроз либо незначительная травма с последующими безуспешными попытками консервативного лечения [Ошибка! Источник ссылки не найден.]. По данным литературы описаны различные подтипы врожденного ложного сустава, одним из вариантов которого является формирование костных фрагментов, напоминающих «тающую сладость» [Ошибка! Источник ссылки не найден.], что и отмечено в данном исследовании. Лечение этого заболевания представляет собой трудную задачу, так как оно развивается у растущего ребенка. В литературе представлены различные варианты хирургического лечения псевдоартроза – с или без аутогенной костной пластики, использование внешней фиксации, свободная васкуляризированная трансплантация малоберцовой кости и формирование лучелоктевого синостоза. Никаких крупных когортных исследований или рандомизированных исследований не проводилось [Ошибка! Источник ссылки не найден.].
В настоящее время признано, что успех костной пластики в области псевдоартроза зависит от васкуляризации данной зоны. Адекватное кровоснабжение играет ключевую роль в заживлении костей. В случае нарушения микроциркуляции, как у пациентов с нейрофиброматозом, методикой выбора является микрохирургическая аутотрансплантация кровоснабжаемого костного трансплантата. В отличие от неваскуляризированной кости, кровоснабжение осуществляется посредством анастомоза между реципиентной и донорской артериями, что сохраняет микроциркуляцию в надкостнице, эндосте и обеспечивает первичное заживление, поскольку индуцируется живыми остеобластами. Таким образом, трансплантат не подвергается некрозу, происходит его реваскуляризация, что дает более высокий показатель успеха и ускорение консолидации фрагментов при некротических поражениях скелета [Ошибка! Источник ссылки не найден.].
Сроки консолидации в области ложного сустава костей предплечья составляют в среднем 3–8 месяцев [Ошибка! Источник ссылки не найден.]. В представленном исследовании через 2,5 месяца получена консолидация только в дистальном отделе, что позволило удалить осевую спицу. Через 6 месяцев полной консолидации фрагментов не выявлено. Однако наличие интрамедуллярной спицы позволило проводить реабилитацию пациента. Полная консолидация фрагментов отмечена только через 1 год после проведения оперативного вмешательства. Кроме того, выявлена тенденция к уменьшению угла деформации лучевой кости, что снижает необходимость проведения дополнительных вмешательств на лучевой кости с целью коррекции ее деформации.
Выводы
Обширные костные дефекты костей предплечья у детей с нейрофиброматозом 1-го типа остаются актуальной проблемой детской травматологии и ортопедии. Одной из сложных задач хирургического лечения данной группы пациентов являются замедленная консолидация фрагментов или развитие ложного сустава. Представленный клинический случай описывает отсутствие консолидации костных фрагментов в зоне «локтевая кость – аутотрансплантат» через 6 месяцев после оперативного лечения. С целью увеличения стабильности костных фрагментов возможно использование интрамедуллярной фиксации (осевой спицы, TEN, интрамедуллярного стержня). Наличие интрамедуллярной фиксации позволяет начать более раннюю реабилитацию (даже при отсутствии консолидации) и социализацию пациента, а также предотвращает развитие патологического перелома.
Библиографическая ссылка
Авдейчик Н.Ю., Голяна С.И., Гранкин Д.Ю., Сафонов А.В. ЛОКТЕВАЯ КОСОРУКОСТЬ ПРИ НЕЙРОФИБРОМАТОЗЕ I ТИПА (СЛУЧАЙ ИЗ ПРАКТИКИ) // Современные проблемы науки и образования. 2023. № 6. ;URL: https://science-education.ru/ru/article/view?id=33060 (дата обращения: 15.05.2026).
DOI: https://doi.org/10.17513/spno.33060



