Лепра на территории Российской Федерации распространена в нескольких южных областях Прикаспийской низменности и не несет эпидемической угрозы в связи с малой численностью больных и низкой контагиозностью самого заболевания. Подобная относительно благоприятная ситуация наблюдается не везде в мире, и ряд приграничных государств, а также стран с активными миграционными процессами имеют худшие эпидемиологические показатели по лепре, что сохраняет угрозу и в отношении Российской Федерации. Возраст больных лепрой на 2023 год в России в среднем приближен к 60 годам, и это не может не отражаться на общем состоянии пациентов и на течении основного заболевания; соответственно, параллельно возникает целый ряд проблем геронтологического профиля, важнейшей из которых представляется коморбидность [1, 2]. Особенностью последних десятилетий в подходе к диагностике и лечению пациентов с длительно текущими заболеваниями является рассмотрение не отдельных нозологических форм с точки зрения специфики течения и результатов терапии, а взгляд на пациента с позиции коморбидности, сочетания различных заболеваний и состояний инфекционной и неинфекционной природы, которые могут определять прогноз развития патологического процесса у данного пациента [1, 2].
Лепра (болезнь Гансена) представляет собой хроническое генерализованное инфекционное заболевание человека, вызываемое Mycobacterium leprae и Mycobacterium lepramatosis, характеризующееся длительным инкубационным периодом, разнообразными по клиническим проявлениям поражениями кожи и слизистых, верхних дыхательных путей, периферической нервной системы, костно-мышечного аппарата и внутренних органов [3].
Клинические разновидности течения лепрозного процесса соотносятся с классификацией Ридли–Джоплинга (1962 г.), в основу которой положен иммуногистологический принцип различия между типами заболевания, но достоверные различия клиники регистрируются в максимально пограничных типах – лепроматозный и туберкулоидный [4].
Лепроматозный тип лепры развивается у человека при отсутствии иммунного ответа на возбудителя – Mycobacterium leprae; данный сценарий является самым нежелательным и тяжелым с точки зрения клинических проявлений болезни и инвалидизирующих последствий даже после полного излечения. Лепроматозный тип при отсутствии своевременной терапии является визитной карточкой лепры, запечатленной в «ужасных» стигмах обезображенных лиц и конечностей. Кожные проявления начинаются, как правило, с пятен гипо- или гиперхромного характера, а в дальнейшем на фоне усиления инфильтрации кожи формируются папулы и узлы различного размера и цвета – от оттенков розового до синюшных и желтых. Локализация элементов сыпи не ограничивается кожей тела и конечностей, часто максимальные страдания пациенту доставляет изменение тканей лица, где, в первую очередь, на себя обращает внимание усиление рельефа в области естественных складок кожи за счет диффузной инфильтрации. Надбровные дуги, спинка носа, ушные раковины утолщаются, бугристый рельеф и мадароз на фоне стойкого пареза лицевого нерва придают лицу выражение атоничного безразличия. Глазные яблоки полуприкрыты кожей верхнего века, нижнее веко расслаблено и вывернуто (лагофтальм). Подобная же картина наблюдается в области нижней губы, которая с трудом прикрывает рот. Специфический лепроматозный ринит характеризуется воспалением слизистой с характерным отеком, гиперемией, а потом и мелкими эрозиями на фоне атрофии слизистой. Течение лепроматозного ринита может усугубляться появлением лепром, которые, по сути, являются специфическими гранулемами и после распада формируют рубцовые деформации по типу «плосковдавленного носа» – развивается facies leonina, или «львиное лицо» [4, 5]. Контагиозность при лепроматозном типе считается выше, чем при туберкулоидном, за счет высокого содержания возбудителя в покровных тканях и особенно в слизистой носа. Эволюция морфологических элементов проходит через стадии изъязвления и длительного рубцевания, которое может быть очень грозным осложнением, в особенности локализуясь на слизистых в области носа, глотки, мягкого и твердого нёба, гортани и языка. Перфорации носовой перегородки, разрушение костных структур лицевого отдела черепа сильно меняют облик больного и доставляют, кроме физических, еще и психологические страдания.
Помимо кожи и слизистых оболочек, в патологический процесс неминуемо вовлекаются периферические нервы, характер их поражения - восходящий и симметричный. Вначале чаще поражаются верхняя ветвь лицевого нерва и большой ушной нерв, также нередки поражения локтевого, срединного и малоберцового нервов. Нервные стволы пальпаторно уплотнены и гипертрофированы, нарушение иннервации вследствие отека и сдавления приводит к изменению трофики как самого нерва, так и иннервируемой им области [5]. Клинически можно видеть мононевриты и полиневриты лепрозной природы, которые сопровождаются морфофункциональными нарушениями чувствительных волокон, приводящими к потере поверхностной чувствительности, особенно в дистальных отделах конечностей (температурной, болевой и тактильной). Параллельно развиваются и двигательные нарушения, снижение мышечной силы, амиотрофии. Лепрозные невриты – один из самых грозных инвалидизирующих факторов, независимо от типа и формы патологического процесса они могут приводить к развитию нейротрофических язв и мутиляций, вовлекая глубокие хрящевые и костные структуры [5].
Туберкулоидный тип лепры отличается более скромными кожными проявлениями, как правило, пятнистого и папулезного характера, которые часто немногочисленны и не образуют кожных лепром. Элементы сыпи могут преобразовываться в фигурный туберкулоид вследствие отставания разрешения периферии от центральной части элемента. Подобные причудливые высыпания являются стадией эволюционных изменений бляшечной формы туберкулоида, с шелушением по периферии и атрофией в центральной зоне. Патологические проявления на коже при туберкулоидном типе редко носят деструктивный характер, обычно оставляя после себя гипо- или гиперхромные пятна. Тем не менее, пациенты в активной форме болезни являются бактериовыделителями и имеют не меньшее эпидемиологическое значение, чем при лепроматозном типе [6]. При специфических полинейропатиях картина не столь благоприятна, как при кожных проявлениях. Поражения нервов могут возникать даже раньше, чем высыпания на коже. В основе этого лежат специфика гранулематозной ткани при туберкулоидном типе и ранние вазомоторные расстройства по типу спастико-атонического состояния артериол. Изменение трофики и иннервации влечет за собой развитие остеомиелита как основной причины хронизации язвенных дефектов и мутиляций в дистальных отделах верхних и нижних конечностей. Изменение поверхностных видов чувствительности способствует высоким рискам травмирования конечностей в бытовых условиях и умножает инвалидизирующие факторы, к которым, помимо нейротрофических язв, относятся парезы и параличи, атрофия мелких мышц и формирование контрактур пальцев, остеомиелит и лизис дистальных фаланг пальцев (мутиляции). Формируется характерная для лепры конфигурация кисти по типу «тюленья лапа», «свисающая кисть», «обезьянья лапа» [7].
Пожалуй, самой тяжелой полинейропатией с выраженной деструкцией нервной ткани и тяжелыми клиническими последствиями проявляется недифференцированный тип (невритическая лепра). Кожные проявления носят пятнистый эритематозный или гипохромный характер, как правило, это единичные элементы. Неврологическая симптоматика здесь выходит на передний план и превалирует над кожной. Нервные стволы асимметрично вовлечены в процессы специфического воспаления не только инфекционного, но и аутоиммунного характера [7]. Недифференцированный тип может представлять собой трансформацию лепроматозного или туберкулоидного типов, при этом частым клиническим симптомом будет гипералгический неврит – выраженный болевой синдром по ходу нерва, причинами которого, прежде всего, являются демиелинизация, нарастание отека, закономерная ишемизация и компрессия нерва в анатомических туннелях. Следствия деструкции периферических нервных стволов, описанные выше у лепроматозного и туберкулоидного типов, также имеют место при недифференцированном типе лепры в более агрессивном и быстром варианте течения с эпизодами острых параличей [7].
Клиническая симптоматика у больных лепрой складывается не только из признаков основного заболевания, но и из проявлений коморбидной патологии. Коморбидность представляет собой сочетание нескольких заболеваний, которые существуют или развиваются на фоне основного заболевания и носят вторичный, подчиненный характер; при этом не исключается их влияние на течение и эффективность лечения основной патологии [8].
Коморбидные состояния у больных лепрой – это ситуация, когда у пациента протекают одновременно несколько заболеваний, одно усиливает другое, и их отрицательное влияние на организм не арифметически складывается, а геометрически умножается. Коморбидный пациент – это тяжелый пациент с множеством болезней, лечение которых может быть затруднено взаимоисключающими требованиями к контролю разных заболеваний. При этом мозаичность, стертость, переплетение жалоб и симптомов делают процесс диагностики заболеваний, лечения больных лепрой сложным и часто нестандартным, а лечение влечет за собой вынужденную полипрагмазию, развитие лекарственных осложнений, и это предопределяет затягивание лепрозного процесса [9].
В Астраханском регионе в настоящее время группа больных лепрой – это, прежде всего, лица пожилого и старческого возраста, как правило, имеющие несколько длительно протекающих заболеваний, каждое из которых характеризуется своими специфическими проявлениями, особенностями течения, осложнениями, различным прогнозом и требует соответствующей индивидуализированной терапии [10].
Цель данного исследования: представить проблему коморбидности у пациентов, больных лепрой, оценить структуру и попытаться осветить пути решения данной проблемы на пациентах, проходивших стационарное лечение в клиническом отделении ФГБУ «Научно-исследовательский институт по изучению лепры» Минздрава России.
Материал и методы исследования
За период с 2019 по 2021 гг. в клиническом отделении ФГБУ «Научно-исследовательский институт по изучению лепры» Минздрава России было отмечено 189 случаев стационарного лечения больных лепрой. Впервые диагноз лепры был поставлен у 8 человек, рецидив заболевания – у 5, остальные 176 пациентов – с диагнозом «лепра в стадии ремиссии», но с обострением осложнений лепры в виде хронических полинейропатий или трофических язв.
У всех пациентов был отдифференцирован тип заболевания (лепроматозный, туберкулоидный, недифференцированный), оценена частота встречаемости отдельных типов в обследованной когорте пациентов. Также была оценена частота встречаемости многобактериальной и малобактериальной лепры. Были даны гендерно-возрастная характеристика обследованных пациентов и оценка частоты встречаемости коморбидной патологии со стороны различных органов и систем.
Статистическая обработка данных проводилась с использованием программы STATISTICA 12.0, Stat Soft, Inc. Для проверки статистических гипотез использовали критерий хи-квадрат Пирсона (χ2).
Результаты исследования и их обсуждение
У обследованных пациентов многобактериальная лепра была установлена в 93 случаях, что было сопоставимо по частоте встречаемости (χ2=0,14; df=1; p=0,713) с малобактериальной лепрой, выявленной у 87 пациентов. Недифференцируемая лепра встречалась статистически значимо реже по сравнению с много- и малобактериальной лепрой (χ2=0,56; df=1; p<0,001 и χ2=0,56; df=1; p<0,001, соответственно) – у 9 пациентов. Лепроматозный тип лепры был диагностирован у 168 пациентов. Туберкулоидный тип лепры встречался статистически значимо реже – у 21 пациента (χ2=81,71; df=1; p<0,001). По гендерному признаку статистически значимых различий выявлено не было: мужчин среди обследованных пациентов было 87 человек, женщин – 102 человека (χ2=0,79; df=1; p=0,373). По возрасту группа была неоднородна – преобладали пациенты в возрасте от 71 до 80 лет – 93 человека (49,2%), статистически значимо меньше были представлены пациенты в возрасте от 71 до 80 лет – 39 человек (20,6%), в возрасте от 81 до 90 лет – 30 человек (15,9%) и в возрасте 51 до 60 лет – 21 человек (11,1%). Пациенты в возрасте от 40 до 50 лет – 3 человека (1,6%) и от 91 года и старше – 3 человека (1,6%).
Помимо основного заболевания, все пациенты имели одно или несколько сопутствующих заболеваний. Так, у 58 пациентов (30,7%) наблюдались заболевания сердечно-сосудистой системы: 57 человек (30,2%) страдали артериальной гипертензией, 39 человек (20,6%) – ишемической болезнью сердца. У 26 пациентов (13,8%) отмечалась патология гепатобилиарной системы с выраженными нарушениями функции печени, но лишь 6 из них имели в анамнезе вирусный гепатит В, С. Гепатобилиарная патология была представлена лекарственными поражениями печени (15 человек) и неалкогольной жировой болезнью печени (5 человек). Заболеваниями желудка и кишечника страдали 19 человек (10%): хроническим гастритом – 12 человек, язвенной болезнью 12-перстной кишки – 1 человек, синдромом раздраженного кишечника – 6 человек. Заболевания почек наблюдались у 19 человек (10%): почечнокаменная болезнь (нефролитиаз) наблюдалась у 8 человек, поликистозная болезнь почек – у 2 человек, хронический пиелонефрит – у 9 человек. Пациенты с заболеваниями бронхолегочной системы были немногочисленны – 4 человека, страдавших хронической обструктивной болезнью легких. Сахарный диабет 2-го типа наблюдался у 4 пациентов.
У 38 пациентов наблюдались сочетания нарушений зрения различного генеза: катаракта (24 человека – 12,7%), глаукома (3 человека – 1,6%), ретинопатии (31 пациент – 16,4%) (рис.).
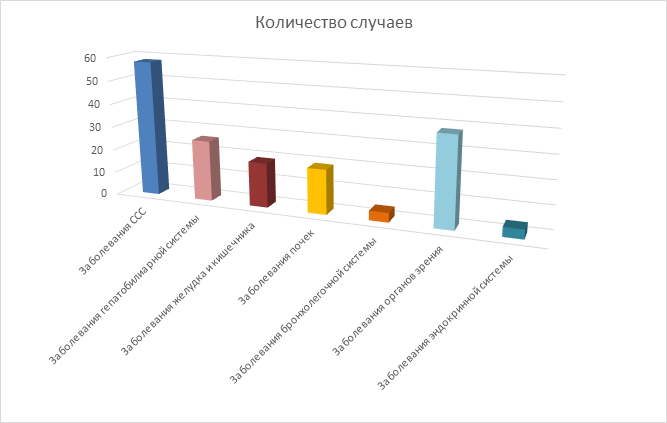
Структура коморбидной патологии у обследованных пациентов
Основной диагноз «лепра» и сопутствующие коморбидные заболевания во всех случаях были подтверждены традиционными клинико-анамнестическими, лабораторными и инструментальными методами.
У больных лепрой клинические проявления сопутствующих заболеваний часто были ведущими при сборе анамнеза и жалоб. При поступлении в клинику общими жалобами больных были шум в ушах, головная боль, головокружение, бессонница, снижение зрения, тяжесть в правом подреберье, дискомфорт в эпигастральной области, явления диспепсии.
У больных лепрой с сопутствующими заболеваниями число принимаемых препаратов часто достигало 9–10, из них 3 противолепрозных препарата, остальные – это препараты, действие которых направлено на лечение коморбидных заболеваний.
Из общего числа больных с сопутствующими заболеваниями на фоне проводимой терапии у 6,4% регистрировались побочные реакции. Частота возникновения побочных реакций зависела от лекарственной нагрузки и во всех случаях устранялась лишь после отмены части фармацевтических препаратов. Характер побочного действия препаратов среди лиц старческой возрастной группы проявлялся спектром токсических реакций, среди которых доминировали вазопрессорные, нейротоксические и диспепсические явления. Кроме того, количественное увеличение получаемых лекарственных форм не способствовало комплаентности пациентов, а напротив, вызывало негативный настрой к терапии в целом и личности врача в частности [11].
Все пациенты, проходившие стационарное лечение в клиническом отделении ФГБУ «Научно-исследовательский институт по изучению лепры» Минздрава России, были проинформированы как об основном заболевании (лепра), так и о сопутствующих, находились под врачебным наблюдением в течение длительного периода (до нескольких лет).
Ввиду геронтологических особенностей у данной категории больных вне активной стадии основного заболевания причинами, снижающими качество жизни, выступают именно сопутствующие болезни и синдромы, да и причиной смерти таких пациентов уже давно не является лепра. Причины смерти сопоставимы с таковыми в основной популяции «здорового» населения. Специфика лечения лепры подразумевает применение длительных курсов комбинированных химиотерапевтических препаратов, нуждающихся в дополнительной протекции и гормонотерапии во время обострения лепрозных реакций. Пренебречь курсом лечения означает оставить болезни шанс на возвращение. Часто в силу клинико-лабораторного разнообразия и тяжести лепрозного процесса коморбидная патология либо остается в тени основного заболевания и диагностируется только в запущенной форме, либо и вовсе неверно интерпретируется и становится угрозой для жизни больного. Этиотропное лечение лепры предполагает применение комбинированной терапии (рифампицин, дапсон, клофазимин) в сочетании с антибактериальными средствами (офлоциклин, миноциклин, кларитромицин) до момента очищения скарификатов кожи от возбудителя с троекратным контролем. Согласно клиническим рекомендациям, оправдано применение иммуномодулирующих, нестероидных противовоспалительных средств для лечения соматических болевых синдромов. Коррекция микроциркуляции и стимуляция синтеза нейротрансмиттеров осуществляются путем назначения витаминов группы В, тиоктовой кислоты, антиоксидантов и нейротрофических нутриентов, антихолинэстеразных препаратов. Обострение лепрозного процесса – лепрозных реакций 1-го и 2-го типов – предполагает назначение гормональной терапии. Добавив к данному списку препараты для купирования коморбидных состояний, мы получаем внушительный комплекс средств с различным механизмом действия и побочными явлениями, что затрудняет проведение полноценной медикаментозной терапии, отражаясь на результатах и сроках лечения и реабилитации пациентов [11, 12].
Заключение
Необходима разработка оптимальной стратегии ведения коморбидного больного с учетом возможной вынужденной полипрагмазии, совместимости препаратов, высокого риска развития лекарственных осложнений и снижения на этом фоне приверженности больных к лечению.
Остаются открытыми вопросы ресурсного обеспечения коморбидных больных лепрой. Часто целевое использование средств при закупке медицинских препаратов исключительно для специализированной терапии лепры не представляется возможным, поскольку лечение сопутствующей патологии в специализированных лечебных учреждениях не всегда осуществимо.
Библиографическая ссылка
Шелепова Т.Н., Набиева А.Р., Воронина Л.П., Луценко А.В., Самотруева М.А. ПРОБЛЕМА КОМОРБИДНОСТИ В КЛИНИКЕ ЛЕПРЫ // Современные проблемы науки и образования. 2023. № 6. ;URL: https://science-education.ru/ru/article/view?id=33037 (дата обращения: 29.04.2026).
DOI: https://doi.org/10.17513/spno.33037



