Гастроинтестинальные гормоны секретин и холецистокинин участвуют в регуляции секреторной деятельности поджелудочной железы и влияют на желчевыделение, что определяет их важную роль в развитии острого воспаления поджелудочной железы.
Исследованиями выявлен факт угнетающего воздействия опиоидных препаратов на секрецию желудка, поджелудочной железы, а также на выработку желчи у лабораторных животных, которым данные средства вводили внутрибрюшинно, в стерильном физиологическом растворе. Получены результаты, указывающие на существенное понижение стимулирующего действия секретина на желчеотделительную функцию печени, при этом наиболее выраженный эффект был получен при использовании препаратов, взаимодействующих с периферическими µ- и κ-опиоидными рецепторами. Подобный, но менее выраженный эффект обеспечивало применение препаратов, стимулирующих периферические δ-опиоидные рецепторы [1].
Экспериментально установлено, что транскраниальная электростимуляция увеличивает концентрацию эндогенных опиатов в структурах мозга и ликворе, а также вызывает существенное увеличение содержания ß-эндорфина в плазме крови животных и человека. ß-эндорфин и другие эндогенные лиганды, взаимодействуя с опиоидными рецепторами нескольких типов (µ, χ, σ, ϐ, έ), формируют сложную систему опиоидной регуляции, оказывающей влияние на различные функции организма – от нервно-психической деятельности до функционирования висцеральных органов. В частности, установлена способность транскраниальной электростимуляции усиливать противовоспалительный эффект комплексной терапии воспалительных заболеваний различных систем организма [2].
С учетом результатов ранее выполненных исследований мы предположили, что проведение физиотерапевтических процедур транскраниальной электростимуляции больным острым панкреатитом будет стимулировать выработку эндогенных опиатов, которые, в свою очередь, понизят уровень секретина и холецистокинина в сыворотке крови, оптимизируют течение воспалительного процесса в поджелудочной железе, уменьшат риск развития серьезных осложнений в брюшной полости и повысят эффективность комплексных лечебных мероприятий у данной категории пациентов.
Цель исследования – определение влияния физиотерапевтического метода транскраниальной электростимуляции на уровень ß-эндорфина, гастроинтестинальных гормонов секретина и холецистокинина у больных с острым воспалением поджелудочной железы.
Материалы и методы исследования. В работе представлена оценка динамики ß-эндорфина, секретина и холецистокинина у 40 пациентов с острым панкреатитом, находившихся на стационарном лечении в хирургическом стационаре ГБУЗ «НИИ-ККБ №1 им. проф. С.В. Очаповского» Министерства здравоохранения Краснодарского края. Диагноз заболевания был определен на основе анамнеза, лабораторных и инструментальных методов исследования.
Критериями включения больных острым панкреатитом для проведения исследования были:
1) возраст пациентов от 35 до 65 лет;
2) неосложненный вариант течения заболевания;
3) отсутствие указаний на наличие эпилепсии, тиреотоксического зоба, перенесенных травм головы, доброкачественных и злокачественных образований головного мозга;
4) состояние ремиссии при наличии хронических болезней сердечно-сосудистой, дыхательной и костно-мышечной систем;
5) наличие информированного согласия на участие в исследовании.
Критерии исключения лиц с острым воспалением поджелудочной железы из когорты исследования:
1) возраст менее 34 и более 66 лет;
2) деструктивные формы заболевания с различными осложнениями, требующими оперативного лечения;
3) наличие доброкачественных и злокачественных образований головного мозга, травм головы, эпилепсии, тиреотоксического зоба;
4) обострение хронических заболеваний сердечно-сосудистой, дыхательной и костно-мышечной систем.
Из 40 лиц с клиническим диагнозом К85 «Острый панкреатит» были сформированы 2 группы: группа сравнения из 20 пациентов (13 женщин, 7 мужчин), лечебный процесс которых был основан на стандарте оказания специализированной медицинской помощи, и основная группа из 20 больных (11 женщин, 9 мужчин), которым стандартную терапию дополняли физиотерапевтическими процедурами транскраниальной электростимуляции.
Транскраниальную электростимуляцию выполняли на аппарате «Трансаир-03» (Россия), при этом устанавливали электроды на голове пациента. В области лба прикрепляли фланелевую прокладку площадью 40 см2, в областях сосцевидных отростков располагали две фланелевые прокладки общей площадью 32 см2, а толщина каждой из трех прокладок равнялась 0,5 см. Для стерилизационной обработки прокладок использовали кипячение, а непосредственно перед началом воздействия поверхность прокладки, контактирующую с кожными покровами больного, покрывали тонким слоем контактного электропроводного геля «ENRAF-NONIUS» (Netherlands). Нанесение геля гарантировало обеспечение равновеликой электропроводности по всей площади соприкосновения в течение установленной продолжительности процедуры. Дозовые параметры процедуры были следующими: вид импульсного тока – биполярный, сила тока соответствовала индивидуальному сенсорно-толерантному уровню: от 1,2 до 3 мА. В начале процедуры в течение 5 минут осуществляли плавный выход на интенсивность тока, которая была оптимальной для конкретного пациента. Затем в течение 40 минут больному проводили электроимпульсное воздействие с интенсивностью тока, выбранной по его субъективной переносимости для данного дня. Если в течение воздействия пациент отмечал субъективное ослабление ощущений в области электродов, силу тока увеличивали до появления вибрации и покалывания стартового уровня. Продолжительность первой физиотерапевтической процедуры составляла 25 минут, остальные ежедневные воздействия в течение курса продолжались 45 минут. Курс включал от 7 до 8 процедур, выполненных в первую половину дня, с 8 до 12 часов.
Лабораторные исследования сыворотки крови для определения уровня секретина, холецистокинина и β-эндорфина выполняли в течение 24 часов после госпитализации пациента и на 7–8-е сутки пребывания в стационаре. Забор крови осуществляли из локтевой вены пациента, натощак, в объеме 10 мл. Из шприца вводили 10 мл крови в стерильную пробирку, которую помещали в центрифугу аппарата «Rotofix 32A» (Германия) на 10 минут, со скоростью вращения 3000 оборотов в минуту. Полученную сыворотку переносили в специализированные криопробирки и замораживали при t –20оС. Исследования проводили в клинико-диагностическом центре КубГМУ. Для анализа использовали тест-системы для иммуноферментного определения в сыворотке крови человека концентрации секретина «CEB075Hu ELISA Kit for Secretin (SCT), 96Т» (КНР) и холецистокинина «CEA802Hu ELISA Kit for Cholecystokinin (CCK), 96Т» (КНР). Уровни содержания гастроинтестинальных гормонов в сыворотке крови у здоровых лиц: секретин: среднее значение 10 пг/мл; холецистокинин: диапазон 0–126,4 пг/мл. Для анализа концентрации β-эндорфина использовали тест-систему «CEA806Hu ELISA Kit for Beta-Endorphin (bEP), 96Т» (КНР). Количественное содержание β-эндорфина в сыворотке крови определяли в пг/мл, а значения этого показателя для здоровых лиц, являвшихся донорами, составило 42,1+3,27 пг/мл [3].
Полученные в результате исследования данные обрабатывали с помощью программы «Stattech», выражая уровень секретина, холецистокинина и β-эндорфина в виде медианы (Ме), 25-м и 75-м процентилями (Q1–Q3), и проводили межгрупповое сравнение. Статистически достоверными считали различия при p<0,05.
На заседании Независимого этического комитета при ФГБОУ ВО КубГМУ Минздрава России проведение данного научно-практического исследования получило одобрение, зафиксированное в протоколе № 92 от 13.10.2020 г. Все пациенты основной группы подписали информированное согласие на проведение дополнительного лечения в виде транскраниальной электростимуляции.
Результаты исследования и их обсуждение
Результаты исходного уровня β-эндорфина в сыворотке крови у больных острым панкреатитом не различались (р=0,626): у лиц основной группы Me (Q1–Q3) равнялись 34,410 (27,755–42,970), а в группе сравнения составили 30,390 (26,797–42,142). Сопоставление начальной концентрации β-эндорфина у обследованных пациентов с уровнем этого эндогенного опиата, определенного в группе здоровых лиц, установило более низкие значения данного показателя у больных с острым воспалением поджелудочной железы, что, вероятнее всего, связано с нахождением обследованных лиц в состоянии острого стресса, вызванного абдоминальной патологией.
При оценке данных заключительного этапа были выявлены статистически значимые различия межгруппового сравнения исследуемых показателей (p<0,001): у пациентов основной группы определили 46,600 (40,898–51,672), тогда как в группе сравнения вычислили 27,755 (22,767–35,170).
Использование медикаментозных средств, указанных в клинических рекомендациях [4, с. 25–30] и стандарте оказания специализированной медицинской помощи для купирования болевого синдрома и проявлений воспалительного процесса, позволило получить клинический эффект, но у пациентов основной группы, дополнительно получавших физиотерапевтические процедуры транскраниальной электростимуляции, субъективные показатели и результаты клинических исследований были доподлинно лучше, чем у лиц из группы сравнения.
Заключительное определение уровня β-эндорфина в сыворотке крови выявило увеличение данного показателя в основной группе выше значений группы здоровых лиц, тогда как в группе сравнения результаты практически остались на исходном уровне.
Распределение сывороточного β-эндорфина у больных группы сравнения и основной группы представлено на рисунке 1.
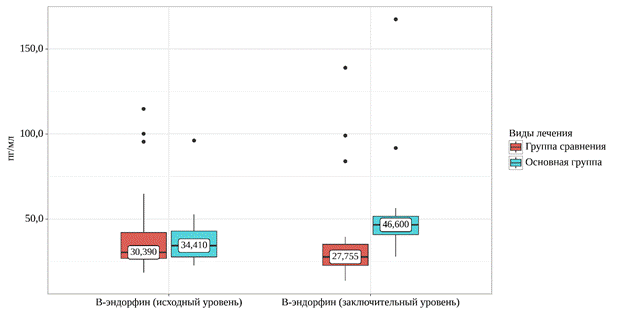
Рис. 1. Распределение сывороточного β-эндорфина у больных группы сравнения (стандартная терапия) и основной группы (стандартная терапия + ТЭС) в пг/мл. Примечание: исходный уровень – первые сутки, заключительный уровень – седьмые или восьмые сутки госпитализации
Полученные нами результаты измерения сывороточного холецистокинина у больных острым панкреатитом основной группы и группы сравнения приведены в таблице 1. Исходные различия концентрации холецистокинина между основной группой и группой сравнения были статистически не значимы (р=0,490). На заключительном этапе в группе сравнения наблюдали тенденцию снижения уровня, которая была недостоверной, тогда как в основной группе выявили достоверное снижение концентрации сывороточного холецистокинина.
Таблица 1
Анализ динамики уровня холецистокинина у пациентов группы сравнения (n=20) и основной с ТЭС-терапией (n=20) группы
|
Показатель |
Этапы наблюдения |
p |
|||
|
Исходный |
Заключительный |
||||
|
Me |
Q1–Q3 |
Me |
Q1–Q3 |
||
|
Холецистокинин, пг/мл (группа сравнения) |
32,145 |
27,610 – 39,755 |
29,045 |
26,310–33,310 |
0,452 |
|
Холецистокинин, пг/мл (основная группа) |
36,255 |
29,355 – 44,822 |
24,530 |
18,312–28,442 |
< 0,001* |
|
p |
0,490 |
0,029* |
– |
||
Примечание. * – различия показателей статистически значимы (p<0,05)
Исследование динамики уровня секретина показало, что исходные значения этого пептидного гормона в группах не различались, а Ме существенно превышала средние значения этого показателя у здоровых лиц. При заключительном обследовании в группе сравнения концентрация секретина уменьшилась на 26,7% по отношению к исходным значениям, тогда как в основной группе определили более выраженное снижение уровня данного пептида – на 55,7% (табл. 2).
Таблица 2
Анализ динамики уровня секретина у пациентов группы сравнения (n=20) и основной с ТЭС-терапией (n=20) группы
|
Показатель |
Этапы наблюдения |
p |
|||
|
Исходный |
Заключительный |
||||
|
Me |
Q1–Q3 |
Me |
Q1–Q3 |
||
|
Секретин, пг/мл (группа сравнения) |
60,645 |
27,992–83,617 |
44,010 |
26,848–72,435 |
0,430 |
|
Секретин, пг/мл (основная группа) |
61,740 |
38,608–94,550 |
27,995 |
17,955–38,390 |
< 0,001* |
|
p |
0,745 |
0,028* |
– |
||
Примечание. * – различия показателей статистически значимы (p<0,05)
Секретин – пептидный гормон, вырабатываемый S-клетками слизистой оболочки двенадцатиперстной кишки, проксимального отдела тощей и дистального отдела тонкой кишок, оказывающий регуляторное воздействие на секрециюподжелудочной железы. S-клетки продуцируют неактивную формуполипептида, которая трансформируется в активный секретин под действиемсоляной кислоты желудочного сока при рН менее 4. Выработку секретина стимулируют жирные кислоты,этиловый спирт, компоненты специй, являющиеся факторами риска развития алкогольно-алиментарной формы острого панкреатита. Усиливают стимуляцию продукции секретина желчные кислоты. Выраженную гиперсекретинемию с концентрацией секретина в плазме крови более 5000 пг/мл выявляли у лиц с островковой карциномой поджелудочной железы и обширными метастазами в печень. У пациентов с синдромом Золлингера–Эллисона уровень секретина в плазме крови натощак обычно составлял 920 пг/мл, что значительно превосходило концентрацию этого гормона у здоровых людей или большинства пациентов с язвенной болезнью двенадцатиперстной кишки (10 пг/мл), при условии временного прекращения терапии блокаторами Н2-рецепторов или ингибиторами протонной помпы в течение нескольких дней [5].
В исследовании авторов у пациентов с острым воспалением поджелудочной железы исходный уровень секретина превышал концентрацию этого гастроинтестинального гормона в сыворотке крови у здоровых лиц в шесть раз. Проведение стандартных лечебных мероприятий позволило снизить содержание этого пептида у больных группы сравнения на четверть, тогда как дополнительное выполнение трансцеребральных электроимпульсных процедур пациентам основной группы обеспечило понижение у них уровня секретина более чем наполовину. Таким образом, увеличение содержания ß-эндорфина в плазме крови больных острым панкреатитом на 35,3%, вызванное проведением транскраниальной электростимуляции, понизило у них концентрацию секретина на 55,7%, что сопоставимо с эффектами угнетения активности секретина введением синтетических опиатов и подтверждает взаимодействие эндогенного ß-эндорфина с опиоидными рецепторами, через которые действовали фармакологические препараты.
Заключение. Выполнение больным острым панкреатитом физиотерапевтических процедур транскраниальной электростимуляции позволяет наряду с увеличением концентрации ß-эндорфина понизить в сыворотке крови уровень гастроинтестинальных гормонов секретина и холецистокинина и более существенно уменьшить выраженность системного воспалительного ответа, чем стандартное лечение.
Библиографическая ссылка
Клиндухова М.О., Каде А.Х. ВЛИЯНИЕ ТРАНСКРАНИАЛЬНОЙ ЭЛЕКТРОСТИМУЛЯЦИИ НА УРОВЕНЬ СЕКРЕТИНА И ХОЛЕЦИСТОКИНИНА У БОЛЬНЫХ ОСТРЫМ ПАНКРЕАТИТОМ // Современные проблемы науки и образования. 2023. № 5. ;URL: https://science-education.ru/ru/article/view?id=32982 (дата обращения: 29.04.2026).
DOI: https://doi.org/10.17513/spno.32982



