Артериальная гипертензия (АГ) у больных раком может быть вызвана противоопухолевыми препаратами (например, ингибиторами сосудистого эндотелиального фактора роста (VEGFi, vascular endothelial growth factor inhibitors), ингибиторами тирозинкиназ области кластера точки разрыва – локуса онкогена Абельсона (BCR-ABL TKI, breakpoint cluster region–Abelson oncogene locus tyrosine kinase inhibitors), фторпиримидинами, цисплатином и др.), препаратами различной направленности (кортикостероидами, нестероидными противовоспалительными препаратами) и другими факторами, такими как стресс, болевой синдром, употребление алкоголя, почечная недостаточность, нелеченое апноэ во сне, ожирение и малая физическая активность [1].
Онкологическим больным с впервые диагностированной АГ коррекция других факторов необходима перед решением вопроса о приостановке терапии онкологических нозологий как наиболее эффективной стратегии профилактики кардиотоксичности, вызванной адъювантной или неоадъювантной химиотерапией (ХТ). При этом рассматривается отказ от ХТ у онкологических больных с высоким риском развития кардиотоксичности или ограничение кумулятивной дозы [2].
Однако отмена ХТ или снижение доз химиотерапевтических препаратов не является эффективной стратегией в лечении онкологических нозологий при возникновении сердечно-сосудистых заболеваний. В связи с этим можно рассмотреть сочетанную фармакологическую терапию при онкологических заболеваниях и развившейся кардиотоксичности на фоне ХТ, которая представляется как оптимальный вариант ведения пациентов с данной коморбидностью [3].
Нелеченая АГ является одним из первостепенных факторов риска возникновения сердечной недостаточности при лечении антрациклиновыми препаратами, ибрутинибом и VEGFi. Учитывая, что многие препараты для лечения рака, вызывающие гипертонию, также вызывают сердечную дисфункцию, связанную с терапией рака, лечение гипертонии ингибиторами ангиотензинпревращающего фактора (иАПФ) или блокаторов рецепторов ангиотензина II (БРА) в качестве терапии первой линии рекомендуется для уменьшения риска развития сердечной дисфункции на фоне фармакологического лечения онконозологий. При этом комбинированная терапия иАПФ или БРА и дигидропиридиновыми блокаторами кальциевых каналов (БКК) рекомендуется онкологическим больным с систолическим артериальным давлением (АД) ≥ 160 мм рт. ст. и диастолическим АД ≥ 100 мм рт. ст., при достижении уровней целевых показателей АД < 140/90 мм рт. ст. возможен переход на монотерапию иАПФ или БРА.
У пациентов с резистентной гипертензией, развившейся на фоне фармакологического лечения онкологии, следует рассмотреть возможность применения калийсберегающих диуретиков, пероральных или трансдермальных нитратов, а также гидралазин. При высоком симпатическом тонусе, стрессовом воздействии или болевом синдроме следует рассмотреть возможность назначения бета-блокаторов, включая карведилол или небиволол. Калийсберегающие и тиазидные диуретики могут быть рассмотрены у онкологических больных с кардиотоксичностью в виде АГ и нарушением функции почек [1].
Рассмотренные варианты терапии АГ, индуцированной ХТ, предложенные Европейским обществом кардиологов (ESC), оппонируют Евразийским клиническим рекомендациям по кардиоонкологии [1, 3]. ESC считает, что дигидропиридованные БКК следует рассматривать как препараты первой линии в лечении АГ, индуцированной препаратами моноклональных антител, в то время как иАПФ и БРА отмечены в качестве фармакологических групп препаратов, способствующих повышению ВБП и ОВП [1]. При этом Евразийская ассоциация кардиологов отводит решающее место в антигипертензивной терапии при кардиотоксичности иАПФ/БРА [3].
В связи с этим выбор адекватной и эффективной схемы лечения VEGF-индуцированной АГ остается спорным в кардиоонкологии и требует проведения дополнительных исследований для определения однозначности в понимании первоочередности выбора линий терапии.
Цель – изучить эффективность нефиксированных комбинаций антигипертензивной терапии при развитии бевацизумаб-индуцированной артериальной гипертензии в эксперименте у нормотензивных крыс линии Wistar для определения первой линии терапии артериальной гипертензии, вызванной препаратами моноклональных антител.
Материалы и методы исследования
Гипотензивный эффект изучен у самцов крыс линии Wistar с нормотензивными показателями АД до проведения исследования. Медико-биологическая клиника Курского государственного медицинского университета Министерства здравоохранения Российской Федерации предоставила животных для эксперимента. Для крыс были созданы комфортные условия, предназначенные для их адекватной жизнедеятельности и проведения исследовательской работы: специализированная комната для животных и лаборатория, температура окружающей среды составила +23±2 °C, вентиляция поддерживалась на уровне 12 объемов в час, режим сна и бодрствования 12×12, регулярные специализированные пищевой и водный режимы. Для исключения влияния временного фактора на гемодинамику у крыс измерения проводились в первую половину суток (10 часов). Проводимые эксперименты осуществлялись при непосредственном соблюдении Европейской конвенции по защите экспериментальных животных (86/609 EEC).
Бевацизумаб-индуцированная артериальная гипертензия у крыс линии Wistar смоделирована введением внутрибрюшинно препарата моноклональных антител модифицированным методом [4], в оригинальном методе бевацизумаб вводился крысам по 10 мг/кг в неделю, вызывая стойкое повышение артериального давления. В проведенном исследовании вводился бевацизумаб по формуле пересчета для животных с нестандартным весом:
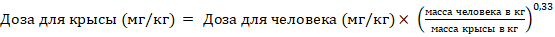 (*)
(*)
В соответствии с приведенной формулой было установлено, что при весе крыс 400±40 г вводимая доза бевацизумаба составляет ≈ 15 мг/кг в неделю, а кумулятивная доза при внутрибрюшинном введении – 60 мг/кг, что приходится на 4 инъекции для каждого животного. Для экспериментальной работы применялся препарат авастин (бевацизумаб), концентрат для приготовления раствора инфузий, серия выпуска B7271.
Осуществлялась запись гемодинамических показателей: систолического артериального давления (САД), диастолического артериального давления (ДАД), частоты сердечных сокращений (ЧСС) у крыс-самцов линии Wistar аппаратно-программным комплексом для электрофизиологических исследований MP150 («Biopac Systems, Inc.», США) с последующей обработкой данных программой «AcqKnowledge 4.4».
Для обеспечения чистоты эксперимента с целью уменьшения влияния стрессовых воздействий был проведен период адаптации, в течение которого животные находились в специализированном пенале, при этом на хвост надевался датчик с манжетой. Такое положение каждая крыса занимала 10 мин каждый день на протяжении недельного периода.
Крысы-самцы линии Wistar перед регистрацией гемодинамических параметров направлялись на 20 мин в специальную нагревательную вентилируемую камеру с температурным режимом 40 °C. Впоследствии осуществлялись 10 последовательных измерений АД и ЧСС на хвосте на протяжении 300 с, далее производился расчет средних арифметических значений.
После достижения стабильной бевацизумаб-индуцированной АГ вводились нефиксированные комбинации антигипертензивных препаратов (АГП): 1 комбинация – иАПФ + диуретик (лизиноприл + гидрохлоротиазид), 2 комбинация – БРА + БКК (телмисартан + амлодипин).
Антигипертензивная терапия препаратами проводилась внутрижелудочно через зонд ежедневно 1 раз в день в течение 20 дней. Перед каждым введением готовилась суспензия из исследуемых препаратов в 1 % крахмальном киселе, при этом объем внутрижелудочного введения для всех животных составлял 5 мл/кг массы тела, контрольная группа получала внутрижелудочно только 1 % крахмальный кисель. Дозы препаратов для крысы рассчитывались путем переноса рекомендованных для человека доз по коэффициентам учета разницы в площади поверхности тела [5]. В связи с тем, что в эксперименте использовались животные с нестандартной массой тела (400±40 г) на начало исследования, перенос доз с человека на крысу производился по формуле (*).
В исследовании было 3 группы крыс, по 20 крыс-самцов (возраст – 8 месяцев) в каждой группе: группа, не получавшая лечения (контроль), и 2 группы, получавшие комбинированную терапию, терапия исследуемыми препаратами начиналась через 2 недели после 1-й инъекции бевацизумаба и продолжалась в течение 20 дней. Давление у животных непрямым методом (на хвосте) измерялось за день до 1-й инъекции бевацизумаба (исходное базовое давление) и далее один раз в неделю до выведения животных из эксперимента. На следующий день после 3-й инъекции бевацизумаба начинали внутрижелудочное введение исследуемых препаратов.
Группа № 1 – бевацизумаб в дозе 15 мг/кг в неделю в течение четырех недель.
Группа № 2 – бевацизумаб 15 мг/кг в неделю + комбинация лизиноприл в дозе 0,8 мг/кг/сутки с гидрохлортиазидом в дозе 2 мг/кг/сутки.
Группа № 3 – бевацизумаб 15 мг/кг в неделю + комбинация телмисартан в дозе 3,1 мг/кг/сутки с амлодипином в дозе 0,4 мг/кг/сутки.
Обеспечена статистическая обработка цифровых экспериментальных данных с использованием программного обеспечения STATISTICA 12.6. Полученные точки измерения гемодинамических параметров соответствовали нормальному распределению (критерий Шапиро – Уилка, р < 0,001), поэтому группы с равной дисперсией подвергались оценке критерием Стьюдента, что позволило определить достоверность различий результатов по разным временным точкам. Достоверные различия принимались между сравниваемыми показателями при p ≤ 0,05.
Результаты исследования и их обсуждение
Гемодинамические показатели были измерены у крыс после прохождения адаптационного периода и до начала введения бевацизумаба (день «0»). Первое измерение гемодинамики проведено до осуществления периода адаптации для фиксации значений САД, ДАД и ЧСС при искусственных иммобилизационных стрессовых условиях с целью получения начальных значений рассматриваемых показателей, в последующем проходил недельный адаптационный период. По его окончанию и до начала введения бевацизумаба (день «0») были измерены гемодинамические показатели у крыс (табл. 1).
Таблица 1
Гемодинамические показатели ненаркотизированных крыс с бевацизумаб-индуцированной артериальной гипертензией до начала лечения (М±m, n = 20)
|
№ п/п |
День измерения |
Показатель |
Группа животных |
||
|
№ 1 Контроль |
№ 2 Лизиноприл + Гидрохлортиазид |
№ 3 Телмисартан + Амлодипин |
|||
|
1 |
До начала введения бевацизумаба / день «0» |
САД |
126,5±2,9 |
127,9±3,1 |
130,3±3,0 |
|
ДАД |
84,1±1,8 |
86,3±1,7 |
81,9±2,2 |
||
|
ЧСС |
339±5 |
344±6 |
355±9 |
||
|
2 |
+2 дня после 1-й инъекции бевацизумаба 15 мг/кг |
САД |
134,5±3,9 |
144,6±5,3 |
138,4±5,0 |
|
ДАД |
102,6±2,7* |
101,7±3,5* |
109,0±3,2* |
||
|
ЧСС |
357±7 |
336±10 |
385±12 |
||
|
3 |
+2 дня после 2-й инъекции бевацизумаба 15 мг/кг |
САД |
151,5±4,4* |
159,2±6,3* |
151,3±4,1* |
|
ДАД |
110,4±4,7* |
114,4±5,7* |
117,0±4,5* |
||
|
ЧСС |
360±12 |
330±15 |
355±14 |
||
|
4 |
+5 дней после 2-й инъекции бевацизумаба 15 мг/кг |
САД |
165,8±5,2** |
166,8±6,0** |
158,6±4,9** |
|
ДАД |
130,4±4,4** |
132,3±5,4** |
127,9±6,4** |
||
|
ЧСС |
348±12 |
328±18 |
370±15 |
||
Примечание. * – при р < 0,05 по сравнению с показателями в день «0»; ** – при р < 0,01 по сравнению с показателями в день «0».
Из табл. 1 видно, что адаптация крыс перед началом эксперимента прошла успешно и показатели давления и ЧСС близки к нормальным значениям во всех экспериментальных группах.
Через два дня после 1-й инъекции бевацизумаба во всех группах экспериментальных животных наблюдалось повышение артериального давления, и если САД повышалось, но это повышение не достигало достоверных значений (р > 0,05), то ДАД во всех трех группах было достоверно выше, чем в день «0» (р < 0,05). ЧСС существенно не изменялась.
Через 9 дней после 1-й инъекции бевацизумаба или через 2 дня после 2-й инъекции бевацизумаба отмечается достоверное повышение как САД, так и ДАД во всех экспериментальных группах (р < 0,05) по сравнению с исходными значениями в день «0», при этом ЧСС достоверно не изменяется.
В контрольной точке измерения АД перед началом антигипертензивной терапии – через 12 дней после 1-й инъекции бевацизумаба или через 5 дней после 2-й инъекции бевацизумаба уровень АД во всех экспериментальных группах повысился с высокой степенью достоверности (р < 0,01). При этом САД повышалось на величину от 28 до 39 мм рт. ст., а ДАД повышалось на величину от 40 до 44 мм рт. ст. Достоверных изменений ЧСС не наблюдалось.
На этом первый этап эксперимента закончился, и на 15-й день после 1-й инъекции бевацизумаба или на следующий день после 3-й инъекции бевацизумаба начался этап изучения эффективности нефиксированных комбинаций антигипертензивных препаратов для лечения бевацизумаб-индуцированной артериальной гипертензии. 2-я группа животных получала лизиноприл в дозе 0,8 мг/кг/сутки с гидрохлортиазидом в дозе 2 мг/кг/сутки, 3-я группа животных получала комбинацию телмисартан в дозе 3,1 мг/кг/сутки с амлодипином в дозе 0,4 мг/кг/сутки, а 1-я группа животных была контрольной и получала 1 % крахмальный кисель в эквиобъемных дозах со 2-й и 3-й группами. Данные гемодинамических показателей у крыс после начала лечения исследуемыми комбинациями лекарственных препаратов на фоне продолжающихся инъекций бевацизумаба представлены в табл. 2.
Таблица 2
Гемодинамические показатели ненаркотизированных крыс с бевацизумаб-индуцированной артериальной гипертензией после начала лечения (М±m, n = 20)
|
№ п/п |
День измерения |
Показатель |
Группа животных |
||
|
№ 1 Контроль |
№ 2 Лизиноприл + Гидрохлортиазид |
№ 3 Телмисартан + Амлодипин |
|||
|
1 |
До начала введения бевацизумаба / день «0» |
САД |
126,5±2,9** |
127,9±3,1** |
130,3±3,0** |
|
ДАД |
84,1±1,8** |
86,3±1,7** |
81,9±2,2** |
||
|
ЧСС |
339±5 |
344±6 |
355±9 |
||
|
2 |
Контрольное измерение / день 12 после 1-й инъекции бевацизумаба |
САД |
165,8±5,2 |
166,8±6,0 |
158,6±4,9 |
|
ДАД |
130,4±4,4 |
132,3±5,4 |
127,9±6,4 |
||
|
ЧСС |
348±12 |
328±18 |
370±15 |
||
|
3 |
+1 день после начала лечения / после 3-й инъекции бевацизумаба 15 мг/кг |
САД |
154,5±6,3 |
145,3±5,3* |
139,6±4,8* |
|
ДАД |
125,6±7,7 |
116,5±4,2* |
111,2±3,7* |
||
|
ЧСС |
347±11 |
336±10 |
365±10 |
||
|
4 |
+8 дней после начала лечения |
САД |
157,3±6,4 |
131,7±4,3** |
120,1±3,1** |
|
ДАД |
127,4±3,7 |
99,7±5,7** |
94,2±3,3** |
||
|
ЧСС |
342±12 |
353±9 |
363±12 |
||
|
5 |
+15 дней после начала лечения |
САД |
157,3±4,1 |
123,0±2,8** |
118,6±3,3** |
|
ДАД |
127,4±4,4 |
92,3±3,0** |
79,8±2,5** |
||
|
ЧСС |
350±9 |
331±14 |
347±6 |
||
|
6 |
+19 дней после начала лечения |
САД |
168,2±6,4 |
120,3±3,1** |
115,4±2,9** |
|
ДАД |
133,1±6,0 |
88,3±2,2** |
76,5±3,4** |
||
|
ЧСС |
332±11 |
351±12 |
359±12 |
||
Примечание. * – при р < 0,05 по сравнению с показателями контрольного измерения; ** – при р < 0,01 по сравнению с показателями в день контрольного измерения.
Из табл. 2 следует, что у контрольной (нелеченой) группы животных АД до конца периода наблюдения оставалось очень высоким и, несмотря на продолжающиеся инъекции бевацизумаба, достоверно не изменялось по сравнению с контрольной точкой артериальной гипертензии на 12 день после 1-й инъекции бевацизумаба. В группах, получавших лечение нефиксированными комбинациями антигипертензивных средств, АД начало снижаться уже на 2-й день после начала лечения (р < 0,05), а уже на 8 день терапии АД во 2-й и 3-й группах существенно не отличалось от показателей, зафиксированных в день «0» до начала введения бевацизумаба. К моменту завершения наблюдения АД в группах, получавших лечение нефиксированными комбинациями антигипертензивных препаратов, постепенно снижалось и в целом соответствовало уровню давления, зарегистрированному в день «0», т.е. до начала моделирования бевацизумаб-индуцированной артериальной гипертензии. Следует отметить, что у животных в 3-й группе, получавших комбинацию телмисартан 3,1 мг/кг/сутки + амлодипин 0,4 мг/кг/сутки, АД снижалось быстрее, чем во 2-й группе, получавшей комбинацию лизиноприл в дозе 0,8 мг/кг/сутки с гидрохлортиазидом в дозе 2 мг/кг/сутки. При этом следует отметить что САД в 3-й группе на 19-й день лечения было в среднем на 15 мм рт. ст. ниже (р < 0,05), чем в день «0» до начала введения бевацизумаба. ДАД в 3-й группе также было в среднем на 5 мм рт. ст. ниже (р > 0,05), чем в день «0» до начала введения бевацизумаба. В свою очередь у крыс, получавших лизиноприл в дозе 0,8 мг/кг/сутки с гидрохлортиазидом в дозе 2 мг/кг/сутки (2-я группа), АД снижалось немного медленнее, чем в 3-й группе, и к 19 дню лечения в сравнении с показателями в день «0» в среднем САД было ниже на 7 мм рт. ст. (р < 0,05) а ДАД оставалось выше приблизительно на 2 мм рт. ст. (р < 0,05). В отношении ЧСС наблюдаемые колебания в течение всего периода наблюдения не были статистически значимыми.
В целом можно отметить, что при использовании комбинации телмисартан 3,1 мг/кг/сутки + амлодипин 0,4 мг/кг/сутки нормализация АД была более быстрой, и цифры САД и ДАД в конце периода наблюдения были более низкими по сравнению с группой, получавшей комбинацию лизиноприл в дозе 0,8 мг/кг/сутки с гидрохлортиазидом в дозе 2 мг/кг/сутки, и выявлены следующие тенденции. САД в 3-й группе в сравнении со 2-й группой максимально снизилось к 8 дню лечения (8,81 %), в то время как ДАД отразило наибольшее снижение на 15 день после лечения (13,54 %). Причем наименьшая динамика между сравниваемыми комбинациями по САД наблюдается на 15-й день коррекции гипертензивного статуса (3,58 %). По ДАД наименьший показатель при сравнении комбинаций по эффективности друг с другом зафиксирован на 1-й день после начала коррекции АГ. После достижения максимальных значений снижения САД и ДАД в сравнительной характеристике групп антигипертензивной терапии отмечаются незначительные темпы по продолжающейся коррекции САД к 15-му дню (3,58 %) и 19-му дню (4,07 %) после начала лечения, ДАД демонстрирует снижение к 19-му дню после начала лечения (13,36 %), что позволяет отметить большее влияние комбинации телмисартан 3,1 мг/кг/сутки + амлодипин 0,4 мг/кг/сутки на темпы снижения ДАД. И тем не менее обе комбинации эффективно не только снижали повышенное АД в результате применения у крыс бевацизумаба в дозе 15 мг/кг в неделю, но и не позволили повыситься АД на фоне продолжающихся инъекций бевацизумаба.
Более значимая эффективность в терапии бевацизумаб-индуцированной артериальной гипертензии продемонстрирована на нефиксированной комбинации телмисартан 3,1 мг/кг/сутки + амлодипин 0,4 мг/кг/сутки при изначальных кардиотоксических явлениях, которые опосредованы гладкомышечными клетками сосудов, и, таким образом, дигидропиридиновые блокаторы кальциевых каналов оказывают прямое сосудорасширяющее действие через гладкие мышцы артериол, тем самым снижая проявления кардиотоксичности в виде АГ [6].
Применение иАПФ (зофеноприл) у крыс продемонстрировало эффективность в коррекции доксорубицин-индуцированной кардиотоксичности, что отразилось в снижении САД на 23,43 % (с 175±2 до 134±3 мм рт. ст.) [7]. Исследование на животных [8] продемонстрировало снижение кардиотоксичности доксорубицина и при применении другого препарата из класса иАПФ – каптоприла, а также бета-блокатора карведилола, при этом отмечается антиоксидантное и антиапоптотическое действие данной фармакотерапии. Стоит обратить внимание, что накоплено определенное количество данных по коррекции АГ при антрациклиновой ХТ, в то время как эффективность коррекции АГ при применении моноклональных антител в онкологической практике требует дальнейшего исследования, частью которого и явилась представленная научная работа.
Заключение
Инъекции бевацизумаба крысам в дозе 15 мг/кг один раз в неделю в совокупной дозе 60 мг/кг приводят к стойкому повышению артериального давления. Использование нефиксированных комбинаций антигипертензивных средств лизиноприл + гидрохлортиазид и телмисартан + амлодипин позволяют нормализовать артериальное давление, повышенное в результате применения бевацизумаба, и не допустить его повышения при продолжении введения бевацизумаба. В случае отсутствия противопоказаний применение нефиксированной комбинации телмисартан + амлодипин при бевацизумаб-индуцированной артериальной гипертензии является более рациональным.
Полученные результаты исследования на крысах линии Wistar согласуются с выводами Европейского общества кардиологов об эффективности применения дигидропиридиновых блокаторов кальциевых каналов в комбинированной терапии АГ у онкологических пациентов, в связи с чем данная группа препаратов может быть рассмотрена в качестве терапии первой линии. Изучение роли дигидропиридиновых антагонистов кальция в терапии кардиотоксичности химиотерапии следует продолжать по причине перспективности влияния данного класса препаратов в кардиоонкологической области на кальциевые каналы T-типа и определения самого эффективного лекарственного препарата из рассматриваемой фармакологической группы.
Библиографическая ссылка
Гладченко М.П., Маль Г.С., Артюшкова Е.Б., Хлямов С.В., Елисеева Р.С. ЭФФЕКТИВНОСТЬ НЕФИКСИРОВАННЫХ КОМБИНАЦИЙ АНТИГИПЕРТЕНЗИВНОЙ ТЕРАПИИ ПРИ ЛЕЧЕНИИ БЕВАЦИЗУМАБ-ИНДУЦИРОВАННОЙ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ У КРЫС ЛИНИИ WISTAR // Современные проблемы науки и образования. 2023. № 4. ;URL: https://science-education.ru/ru/article/view?id=32918 (дата обращения: 20.05.2026).
DOI: https://doi.org/10.17513/spno.32918



