Инфаркт миокарда (ИМ) продолжает лидировать среди причин смертности населения экономически развитых стран мира [1]. Особенно тревожит развитие ИМ у больных, имеющих хроническую патологию, например хроническую обструктивную болезнь легких (ХОБЛ), так как в этом случае нередко наблюдаются атипичное течение, диагностические трудности, снижение комплаентности больных и развитие полиорганной патологии [2]. К проявлениям полиорганного поражения можно отнести почечную дисфункцию.
По данным ряда авторов, почечная дисфункция у больных с сердечно-сосудистыми заболеваниями встречается чаще, чем в популяции, и ассоциирована с повышенным риском осложнений [3; 4]. Это позволило обосновать концепцию кардиоренального синдрома, подразумевающего развитие дисфункции почек при патологии сердца и наоборот [5; 6].
В многочисленных исследованиях доказана ассоциация хронической обструктивной болезни легких (ХОБЛ) и почечной дисфункции [7; 8]. Наряду с этим работы, посвященные изучению функции почек при сочетании ИМ и ХОБЛ, единичны [9]. В связи с этим представляется обоснованным определение функции органов выделения (креатинин, СКФ) у больных инфарктом миокарда в сочетании с ХОБЛ.
Цель исследования: определить наличие почечной дисфункции в остром периоде инфаркта миокарда у больных с хронической обструктивной болезнью легких.
Материал и методы исследования. Обследованию подверглись 195 жителей г.Астрахани, у которых на фоне ХОБЛ стабильного течения развился ИМ (ИМ+ХОБЛ). Группу сравнения составили 130 больных ИМ без ХОБЛ, получавших стационарное лечение в тот же период. Имелась группа контроля, представленная 110 жителями Астраханского региона, сопоставимыми с основной группой по полу и возрасту.
Диагностика ИМ основывалась на данных ЭКГ и повышения кардиоспецифичного белка тропонина в соответствии с Клиническими рекомендациями по ведению больных с острым коронарным синдромом с подъемом сегмента ST и без подъема сегмента ST (2020). Критериями включения в исследование являлись: ИМ I типа (острая стадия), наличие документированной ХОБЛ стабильного течения и согласия на участие в исследовании; отсутствие на момент обследования заболеваний и патологических состояний, потенциально способных повлиять на результаты исследования.
К критериям исключения отнесены: ИМ II-V типа; перенесенный ранее ИМ; ХБП со СКФ<30 мл/мин./м2, бронхиальная астма и другие заболевания легких, кроме ХОБЛ; сахарный диабет; артериальная гипертензия выше 2-й степени; стенокардия напряжения выше II функционального класса в анамнезе, острый инфекционный процесс; онкопатология; психические заболевания; значительное снижение когнитивных способностей. Клинико-анамнестическая характеристика обследованных представлена в таблице 1.
Таблица 1
Клинико-анамнестическая характеристика обследуемых пациентов
|
Показатель |
ИМ+ХОБЛ (n=195) |
ИМ без ХОБЛ (n=130) |
p |
|
Возраст, лет (Mе; Q1-Q3) |
56,0 [52,0; 60,0] |
56,0 [50,0; 62,0] |
0,718 |
|
Пол, муж.:жен. |
189:6 |
89:41 |
|
|
Q-ИМ, n (%) |
146 (74,9) |
101 (77,7) |
0,598 |
|
Поражение 2 и более КА |
145 (74,4) |
59 (45,4) |
<0,001 |
|
Наличие осложнений в остром периоде ИМ |
84 (41,3) |
32 (24,6%) |
<0,001 |
Примечание: р – статистическая значимость сравнений между группами, n – количество пациентов.
Всем пациентам была выполнена коронароангиография при ИМ с подъемом сегмента ST – первичное чрескожное вмешательство с установкой стента. Получаемое по поводу ИМ лечение соответствовало клиническим рекомендациям [10].
Проводимое научное исследование получило одобрение Регионального независимого этического комитета (от 18.01.2016, протокол № 12).
Оцениваемыми параметрами были: уровни мочевины, креатинина, скорость клубочковой фильтрации (СКФ), рассчитанная по формуле CKD-EPI, наличие протеинурии.
Статистическую обработку данных проводили посредством программы SPSS 26.0. Числовые значения представлены в виде медианы (Ме) и интерквартильного размаха (Q1; Q3). Сопоставление количественных признаков в двух группах наблюдения осуществлялось методом Манна-Уитни, трех – методом Краскела-Уоллиса.
Результаты исследования и их обсуждение
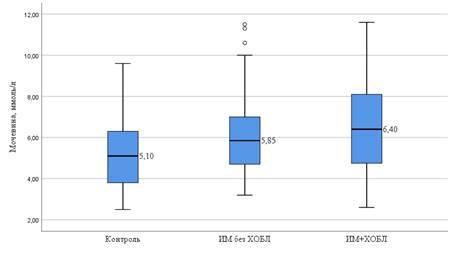
Рис. 1. Уровень мочевины (моль/л) в группах наблюдения
У больных ИМ, независимо от наличия или отсутствия ХОБЛ, уровень мочевины не имел статистически значимых различий между собой (p=0,514) и составил 5,9 [4,7-7,0] моль/л в группе больных ИМ без ХОБЛ и 6,4 [4,8-8,1] моль/л – в группе больных ИМ+ХОБЛ (рис. 1). В обеих группах уровень мочевины статистически значимо превышал значения в контрольной группе (p=0,004 – для группы больных ИМ без ХОБЛ, p<0,001 – для больных ИМ+ХОБЛ).
Уровень креатинина в наблюдаемых группах также превышал значения, полученные в группе контроля (рис. 2).
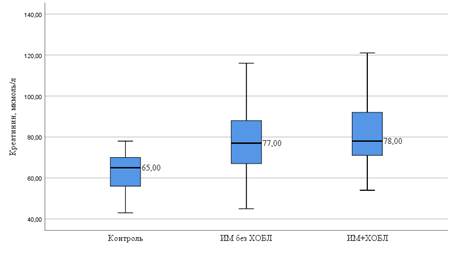
Рис. 2. Уровень креатинина (мкмоль/л) в группах наблюдения
У больных ИМ без ХОБЛ уровень креатинина составил 77,0 [67,0-88,0] мкмоль/л, у больных ИМ+ХОБЛ – 78,0 [77,0-95,0] мкмоль/л. В обоих случаях полученные значения статистически значимо превосходили таковые в контроле (p<0,001), а значения у больных ИМ+ХОБЛ были статистически значимо выше, чем у больных ИМ без ХОБЛ (p<0,001).
У больных ИМ без ХОБЛ СКФ составила 103,7 [91,1-119,2] мл/мин./1,73 м2, у больных ИМ+ХОБЛ – 110,15 [89,2-116,5] мл/мин./1,73 м2 (рис. 3).
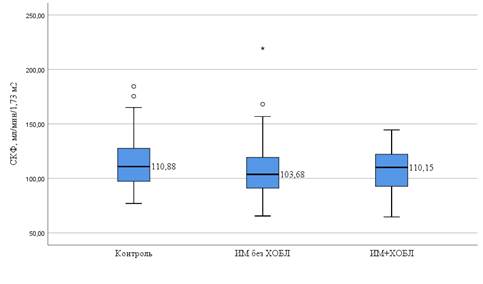
Рис. 3. СКФ (мл/мин./1,73 м2) в группах наблюдения
На рисунке 4 представлены данные о количестве пациентов с СКФ менее 90 мл/мин./1,73 м2 и протеинурией в группах наблюдения.
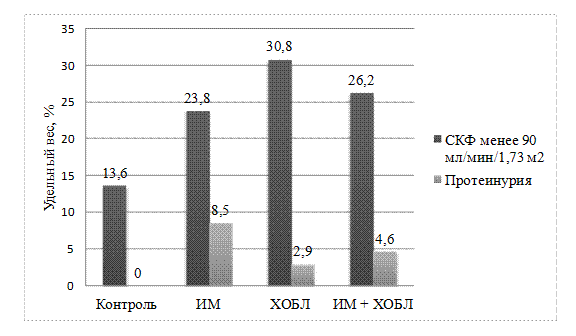
Рис. 4. Удельный вес лиц с СКФ менее 90 мл/мин./1,73 м2 и протеинурией в группах наблюдения
Авторы сопоставили количество и удельный вес лиц с СКФ менее 90 мл/мин./1,73 м2 и протеинурией. Было установлено, что в группе больных ИМ без ХОБЛ количество лиц с СКФ менее 90 мл/мин./1,73 м2 было 31 (23,8%), в группе больных ИМ+ХОБЛ – 51 (26,2%). При этом количество лиц с СКФ менее 90 мл/мин./1,73 м2 в группе больных ИМ+ХОБЛ было статистически значимо больше, чем в контроле (p=0,032). Количество лиц с протеинурией составило 11 (8,5%) среди больных ИМ и 9 (4,6%) – среди больных ИМ+ХОБЛ (p=0,006).
Авторами были проанализированы показатели функции почек в зависимости от глубины поражения миокарда. Для этого были сопоставлены значения при не-Q-ИМ и Q-ИМ. Полученные данные представлены в таблице 2 и на рисунке 5.
Таблица 2
Показатели функции почек у больных ИМ без ХОБЛ и ИМ+ХОБЛ с различной глубиной поражения миокарда
|
Показатели |
ИМ без ХОБЛ |
ИМ+ХОБЛ |
p |
||
|
Не Q-ИМ (n=29) |
Q-ИМ (n=101) |
Не Q-ИМ (n=49) |
Q-ИМ (n=146) |
||
|
Мочевина, ммоль/л
|
5,5 [4,7-6,2] p1=1,0 |
6,2 [4,8-7,2] p1=0,003 p2=1,0 |
5,9 [4,8-7,6] p1=0,016 p3=1,0 |
6,4 [4,7-8,3] p1<0,001 p2=1,0, p3=1,0 |
<0,001
|
|
Креатинин, мкмоль/л |
76,0 [68,0-94,0] p1<0,001
|
77,0 [67,0-88,0] p1<0,001 p2=1,0 |
80,0 [77,0-88,0] p1<0,001 p3=0,594 |
82,0 [77,0-97,0] p1<0,001 p2=1,0, p3<0,001 |
<0,001
|
|
СКФ, мл/мин./1,73 м2 |
105,1 [91,1-118,8] p1=0,328 |
103,7 [91,4-119,2] p1=0,183 p2=1,0 |
109,7 [98,9-118,0] p1=1,0 p3=1,0 |
102,5 [88,7-115,4] p1<0,001 p2=1,0, p3=1,0 |
0,001
|
Примечание: р – уровень статистической значимости различий при множественном сравнении (критерий Краскела-Уоллиса), р1 – с группой соматически здоровых лиц, р2 – с больными не Q-ИМ в данной группе, р3 – с соответствующей подгруппой больных ИМ без ХОБЛ.
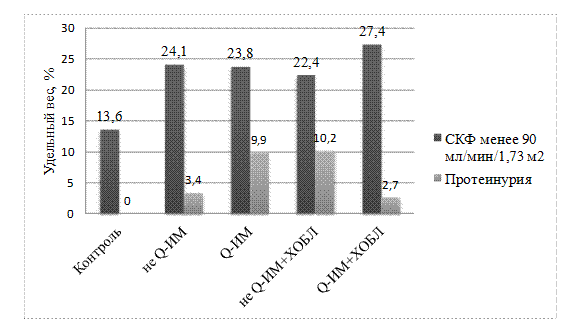
Рис. 5. Удельный вес лиц с СКФ менее 90 мл/мин./1,73 м2 и протеинурией у больных ИМ без ХОБЛ и ИМ+ХОБЛ в зависимости от глубины поражения миокарда
Авторами не было выявлено различий в показателях функции почек в зависимости от наличия зубца Q на ЭКГ.
Доказано, что почечная дисфункция является независимым предиктором сердечно-сосудистых заболеваний и летальности от кардиальных причин. Встречаемость патологии сердечно-сосудистой системы у больных с нарушенной почечной функцией на 64% выше, чем у здоровых лиц [5]. Именно сердечно-сосудистая патология является лидирующей причиной смертности у больных с патологией почек [11]. Осетрова Н.Б. (2020) ссылается на литературные данные, в соответствии с которыми существует обратная зависимость между показателями СКФ и величиной сердечно-сосудистого риска. Так, у пациентов с СКФ ниже 30 мл/мин./1,73м2 риск сердечно-сосудистых осложнений в 5,5 раз выше, чем у пациентов с более высокими значениями СКФ [6].
В свою очередь, почечная дисфункция у больных с инфарктом миокарда встречается чаще и является предиктором осложненного течения и неблагоприятного исхода [3].
Такая взаимосвязь сердечно-сосудистой и выделительной систем объясняется общностью ряда патогенетических звеньев. Доказано, что развитие кардиоваскулярной патологии, в частности ИМ, сопровождается эндотелиальной дисфункцией. В то же время фенестрированные эндотелиальные клетки являются компонентом капиллярных петель почечных нефронов, а треть всей эндотелиальной выстилки организма сосредоточена в сосудах и микроциркуляторном русле почек. Ренальная функция к тому же зависит от уровня кровотока в почечных артериях, а он, в свою очередь, обусловлен сердечным выбросом.
Как и ИБС, ХОБЛ также сопровождается нарушением функции почек. В работе Агранович Н.В. хроническая болезнь почек была впервые диагностирована у 47,1% больных ХОБЛ, причем при тяжелом течении выявлялись более высокие уровни маркеров воспаления – СРБ и ФНО-α в крови [12].
По данным Болотовой Е.В., у 37,3% лиц с ХОБЛ имеется снижение СКФ в пределах 89-60 мл/мин./1,73 м2, у 26,7% – до 59-45 мл/мин./1,73 м2, а у 3,3% больных ХОБЛ – менее 44 мл/мин./1,73 м2 [13]. Отсутствие в данном исследовании таких низких значений СКФ можно объяснить тем, что из него исключались пациенты с выраженной АГ, а именно у таких больных поражение почек встречается наиболее часто.
О взаимосвязи нарушения работы почек и неблагоприятного течения ИБС свидетельствуют результаты ретроспективного исследовании Wereski R.: дисфункция почек стала независимым предиктором повторного ИМ при ИМ 1-го и 2-го типов [4].
Уязвимость коморбидных пациентов в плане развития почечной дисфункции подтверждена в исследовании Boiko О. (2022). При сравнении трех групп – с ХОБЛ, сердечно-сосудистой патологией и коморбидных пациентов – наиболее выраженное снижение СКФ определялось также среди лиц с коморбидной патологией [9].
Заключение. Авторами были выявлены изменения показателей функции почек у больных инфарктом миокарда на фоне ХОБЛ, которые проявлялись более низкими, чем в группе контроля и пациентов с инфарктом миокарда, значениями скорости клубочковой фильтрации. Показатели функции почек не продемонстрировали статистически значимых различий в зависимости от наличия зубца Q на ЭКГ.
Библиографическая ссылка
Прокофьева Т.В., Полунина О.С., Белякова И.С. ФУНКЦИЯ ПОЧЕК ПРИ ИНФАРКТЕ МИОКАРДА У БОЛЬНЫХ С ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНЬЮ ЛЕГКИХ // Современные проблемы науки и образования. 2023. № 4. ;URL: https://science-education.ru/ru/article/view?id=32650 (дата обращения: 17.05.2026).
DOI: https://doi.org/10.17513/spno.32650



