Глаукома - многофакторное заболевание, которое характеризуется повреждением ганглиозных клеток сетчатки и снижением количества аксонов нервных клеток зрительного нерва. Основным фактором прогрессирования глаукомы является повышенное внутриглазное давление (ВГД). Подход к лечению глаукомы заключается в эффективном снижении ВГД для компенсации структурных и функциональных показателей [1]. На протяжении десятилетий традиционные методы снижения ВГД включали местные гипотензивные препараты, лазерную трабекулопластику и операции с формированием новых путей оттока внутриглазной жидкости. В современной практике появились новые методы, основанные на концепции малоинвазивной хирургии глаукомы (Minimally Invasive Glaucoma Surgery - MIGS), которые являются безопасными и эффективными при различных вариантах глаукомного процесса [2; 3]. Одной из методик MIGS является гониоассоциированная транслюминальная трабекулотомия (gonioscopy-assisted transluminal trabeculotomy - GATT), которая представляет собой трабекулотомию ab interno, метод, предложенный Grover et al. как инновационный метод хирургического лечения глаукомы [4]. GATT снижает ВГД за счет улучшения оттока внутриглазной жидкости через шлеммов канал, сохраняя неповрежденной конъюнктиву и склеру. Авторами были отмечены хорошие результаты контроля ВГД и снижение количества применяемых лекарств от глаукомы в послеоперационном периоде [5]. Если затронуть безопасности выполнения GATT, то стоит отметить, что угрожающие зрению послеоперационные осложнения встречаются редко [6]. Из распространенных осложнений отмечают гифему. О таких послеоперационных осложнениях, как иридодиализ, отслойка сосудистой оболочки, отслойка десцеметовой мембраны, не сообщалось. В настоящий момент существует проблема влияния хирургии глаукомы на плотность эндотелиальных клеток (ПЭК) роговицы, что не менее важно при выполнении MIGS [7].
В отличие от большинства процедур MIGS, GATT не включает имплантацию микростента или шунта в переднюю камеру, но тем не менее сама хирургическая манипуляция потенциально может повлиять на состояние ПЭК. Целью данной работы являлось исследование краткосрочного изменения ПЭК, связанного с GATT, в качестве изолированной процедуры или в сочетании с факоэмульсификацией катаракты на глазах с различными вариантами глаукомного процесса.
Цель исследования: изучить эффективность и безопасность применения пластики угла передней камеры у пациентов с катарактой и глаукомой.
Материалы и методы исследования. Произведен анализ хирургического лечения 68 пациентов (68 глаз), средний возраст которых составил 59,6 ± 19,8 года. У всех пациентов была диагностирована первичная открытоугольная глаукома с длительностью течения более 2 лет. Всем пациентам до этого ранее не проводились хирургические манипуляции по поводу глаукомы. В качестве терапии использовались гипотензивные инстилляционные препараты. Пациенты были разделены на 3 группы, в 1-ю группу вошли пациенты, которым была проведена операция по методике GATT (n=39), во 2-ю группу - пациенты, которым была проведена GATT в сочетании с факоэмульсификацией катаракты (n=23), 3-я группа была взята как группа контроля, в нее вошли пациенты, перенесшие стандартную факоэмульсификацию катаракты. GATT выполняли в 4 квадрантах в 76,9% случаев, в 3 квадрантах в 7,6% случаев, в 2 квадрантах в 12,8% случаев и в 1 квадранте в 2,5% случаев соответственно. При максимальной гипотензивной терапии ВГД до оперативного вмешательства во всех группах составило 33,9 ± 7,8 мм рт. ст. Все операции были выполнены на базе Центра офтальмологии НМХЦ им Н.И. Пирогова. Основными критериями оценки результатов хирургического лечения были показатели ВГД, количество применяемых антиглаукомных препаратов и ПЭК, которую оценивали с помощью автоматизированного эндотелиального микроскопа до оперативного вмешательства и в первый месяц после операции. Компьютерную периметрию осуществляли на анализаторе полей зрения Octopus (HAAG-STREIT, Швейцария) по пороговой стратегии: для оценки центрального поля зрения в пределах 30º от точки фиксации взгляда использовали программу 30-2. Анализировали следующие параметры: индексы MD и MS и sLV. Дополнительно применялась программа LowVision у пациентов с остротой зрения, сниженной до сотых. Также оценивали послеоперационные осложнения, в качестве наличия или отсутствия гифемы. Пациенты с заболеваниями роговицы, травмами, а также глаза, на которых уже проводились лазерные или хирургические антиглаукомные вмешательства в течение 6 месяцев до процедуры GATT, были исключены из исследования.
Результаты исследования и их обсуждение. В исследование были включены 39 пациентов, перенесших процедуру GATT, демографические показатели и характеристика глаукомного процесса представлена в таблице 1.
Таблица 1
Основные демографические показатели и характеристика глаукомного процесса пациентов 1-й группы (M±σ)
|
Параметры |
Показатели |
|
Возраст (лет)* |
59,6 ± 19,8 |
|
Пол (мужчины/женщины) |
26/13 |
|
Предоперационное внутриглазное давление (мм рт. ст.)* |
33,9 ± 7,8 |
|
Количество применяемых препаратов от глаукомы* |
3,6 ± 0,5 |
|
ПЭК до операции (клеток/мм²)* |
2181,6 ± 481,2 |
Примечание: ПОУГ - первичная открытоугольная глаукома; ПЭК - плотность эндотелиальных клеток.
*Данные представлены как среднее значение ± стандартное отклонение (M±σ).
До операции в 1-й группе показатель ВГД составил 33,9 ± 7,8 мм рт. ст., в первый день после хирургического лечения показатель ВГД снизился до 18,5±3 мм рт. ст. (p<0,05 в сравнении с данными до операции), а через неделю до 13,4±2,3 мм рт. ст. (p<0,05 в сравнении с данными до операции), на первом месяце показатель ВГД составил 10,3±2,8 мм рт. ст. (p<0,05 в сравнении с данными до операции), на 3-м месяце 10,2 ± 2,2 мм рт. ст. (p<0,05 в сравнении с данными до операции). Все послеоперационные значения ВГД в 1-й группе были значительно ниже, чем в дооперационном периоде. На рисунке 1 представлены показатели ВГД пациентов 1-й и 2-й групп, показатели были сопоставимы, что говорит об эффективном применении методики - как самостоятельной процедуры, так и в комбинации с факоэмульсификацией катаракты.
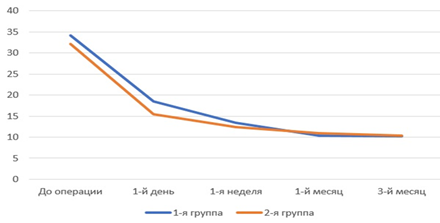
Рис. 1. Показатели внутриглазного давления пациентов 1-й и 2-й групп до операции и в послеоперационном периоде
Показатели периметрии по индексам MD, MS и sLV пациентов с ПОУГ, участвующих в исследовании, представлены в таблице 2. Анализ изменений периметрического индекса MD, характеризующего общее снижение чувствительности, показал уменьшение общей депрессии светочувствительности сетчатки у пациентов с глаукомой. При анализе изменений среднестатистического показателя sLV отмечено уменьшение количества относительных дефектов светочувствительности.
Таблица 2
Функциональные показатели у пациентов с ПОУГ (M±σ)
|
Параметры |
Показатели |
|
MD, dB* |
11,63±3,47* |
|
MS, dB* |
16,95±3,23* |
|
sLV* |
8,45±1,77* |
Примечание: МD (mean deviation) - среднее отклонение дефекта в анализируемой группе от возрастной нормы; MS (mean sensitivity) - средняя внутригрупповая светочувствительность, sLV (corrected loss variance) - корректированная внутригрупповая вариабельность снижения светочувствительности. *Данные представлены как среднее значение ± стандартное отклонение (M±σ).
При анализе показателей ПЭК в 1-й группе до операции были зафиксированы значения 2181,6 ± 481,2 клеток/мм², а через 1 месяц после хирургии 2152,8 ± 425,39 кл/мм² (рис. 2), разница в 28,8 клеток/мм² (1,31%) не была статистически значимой, что может говорить о сохранности ПЭК (р=0,467).
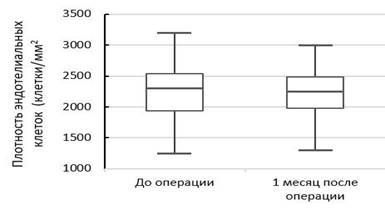
Рис. 2. Изменение плотности эндотелиальных клеток в 1-й группе до и через 1 месяц после операции
Во 2-й группе (рис. 3) средний показатель ПЭК до операции составил 2136,9 ± 418,6 клеток/мм², а через 1 месяц после комбинированной хирургии составил 2047,5 ± 421,6 клеток/мм².
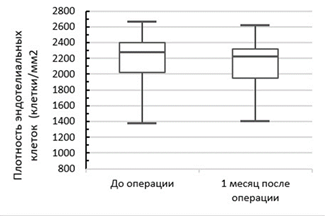
Рис. 3. Изменение плотности эндотелиальных клеток в группе GATT в сочетании с факоэмульсификацией катаракты до операции и через 1 месяц
Анализируя полученные данные, стоит отметить, что значительная потеря ПЭК была обнаружена только у четырех пациентов со снижением показателей больше 20% по сравнению с исходными значениями, среди них двоим пациентам была проведена стандартная GATT, а двоим - GATT в комбинации с ФЭК.
Количество применяемых антиглаукомных препаратов через 1 месяц после операции уменьшилось с 3.6 ± 0.5 до 1,1 ± 0,83 в 1-й группе (p<0,05 в сравнении с данными до операции), а во 2-й группе с 3.5 ± 0.5 до 1,05 ± 0,63 (p<0,05 в сравнении с данными до операции). В послеоперационном периоде из осложнений одним из главных являлась гифема, она наблюдалась у пациентов 1-й группы в 58,9%, у пациентов 2-й группы в 43,4%, со средней продолжительностью резорбции гифемы 3 дня в обеих группах.
Новые методы хирургического лечения глаукомы должны обеспечивать не только хорошие показатели ВГД, как при традиционной хирургии, но и иметь высокий профиль безопасности. Ряд авторов отмечает, что при глаукоме характерно снижение количества эндотелиальных клеток из-за различных факторов, таких как применяемая терапия, характер глаукомного процесса [8]. В ходе исследования у пациентов с первичной открытоугольной глаукомой, которым была проведена операция GATT в комбинации с ФЭК или без нее, не было обнаружено достоверных изменений показателей ПЭК. Данные об изменениях показателей ПЭК при проведении MIGS в литературе единичны, а влияние каждой методики различно. Lass J.H. et al. в своем 5-летнем наблюдении показали, что после имплантации микростента CyPass было отмечено повреждение эндотелия роговицы, которое было связано с положением стента в углу передней камеры [9]. В свою очередь, Samuelson T.W. et al. показали результаты имплантации микрошунта iStent, микростента Hydrus и Xen, которые не привели к значительной потере эндотелиальных клеток по сравнению с контрольными группами через 2 года наблюдения [10]. Рядом авторов было отмечено, что при стандартной трабекулэктомии показатели ПЭК снижаются на 3-11,4% в период от 3 до 24 месяцев после хирургического вмешательства [11; 12]. Tojo N. et al. в своем исследовании отметили, что при имплантации Ex-Press шунта, особенно если он расположен ближе к эндотелию, значительно уменьшается показатель ПЭК в среднем на 15,1% за 2 года [13]. Имплантация дренажных устройств для лечения глаукомы провоцирует эндотелий к непрерывному истощению и к высокому риску в случаях контакта с роговицей [14].
Заключение. В ряде случаев пациентам с глаукомой требуются повторные вмешательства для компенсации ВГД, а поскольку количество эндотелиальных клеток ограниченно, их сохранение является серьезной проблемой во время выбора тактики хирургического лечения. После выполнения GATT нами не были отмечены существенные изменения ПЭК, как и в сочетании с ФЭК, показатели существенно не отличались. Это показывает высокий профиль безопасности, который можно обосновать некоторыми параметрами: точные движения в передней камере, короткое время операции и низкая частота интраоперационных и послеоперационных осложнений. В настоящее время часто встречаются пациенты с низким количеством ПЭК, и чтобы выбирать наилучший вариант для каждого пациента с учетом результатов как безопасности, так и эффективности, требуется дифференцированный подход. В данном исследовании было показано, что применение методики GATT является одним из безопасных вариантов MIGS, и необходимы дальнейшие исследования для изучения долгосрочных изменений ПЭК после GATT.
Библиографическая ссылка
Файзрахманов Р.Р., Калинин М.Е., Павловский О.А., Босов Э.Д. РЕЗУЛЬТАТЫ ПРИМЕНЕНИЯ ПЛАСТИКИ УГЛА ПЕРЕДНЕЙ КАМЕРЫ У ПАЦИЕНТОВ С ГЛАУКОМОЙ И КАТАРАКТОЙ // Современные проблемы науки и образования. 2023. № 3. ;URL: https://science-education.ru/ru/article/view?id=32634 (дата обращения: 19.05.2026).
DOI: https://doi.org/10.17513/spno.32634



