Келоидные и гипертрофические рубцы являются доброкачественными фибропролиферативными заболеваниями, возникают в ответ на повреждение кожи, затрагивающее ее дермальный слой [1]. Оба вида поражений связаны с выраженным снижением качества жизни пациентов, их измененным физическим и ментальным статусом. К общим факторам, провоцирующим возникновение келоида, относятся: наследственная предрасположенность (изучена возможность генетической связи через антигены лейкоцитов человека (HLA) В14, В21, Вw16, Вw35, DR5 и DQw); нарушение функции желез внутренней секреции, вызывающее гормональный дисбаланс. Местными факторами, имеющими значение для развития келоида, являются тканевая гипоксия, нарушения межклеточных взаимодействий. Келоидные рубцы формируются, как правило, после глубоких и обширных травм, длительно и вялотекущих воспалительных процессов, но иногда могут возникать и спонтанно на неизмененной коже без видимых причин. Келоидные рубцы встречаются одинаково у мужчин и женщин, кроме того, распространены у людей с темной кожей (особенно африканского, латиноамериканского или китайского происхождения) [2]. При этом доказано, что келоиды обычно возникают в течение 3-12 месяцев после травмы кожи у предрасположенных людей. Повышенную склонность к образованию келоидов имеют анатомические области тела с замедленным протеканием репаративных процессов, а также с высоким натяжением кожи: передняя стенка грудной клетки, молочные железы, мочки уха, углы нижней челюсти, лопатки, локти, колени [3]. Согласно современным представлениям, механизм развития келоидных рубцов связан с циклическим растяжением индуцированного выброса Ca2 + через механочувствительные каналы в дермальных фибробластах человека [4].
Официальные показатели заболеваемости и распространенности келоидных и гипертрофических рубцов в России отсутствуют. По данным современных исследований, образование рубцов наблюдается у 1,5-4,5% лиц в общей популяции.
По этиологии келоидные рубцы делятся на истинные и ложные. По морфологии разделяются на фибробластические (активные), фиброзные (стабильные). К факторам риска, способствующим росту гипертрофических рубцов и келоидов, относят местные факторы (натяжение раны/рубца), сопутствующие заболевания (например, артериальная гипертония), генетические факторы (например, однонуклеотидные полиморфизмы) и факторы образа жизни. С келоидогенезом связано несколько моногенных заболеваний, таких как синдром Рубинштейна - Тайби, при котором у 24% пациентов развиваются спонтанно формирующиеся келоидные рубцы, а также наблюдаются мутации гена CREB, кодирующего белок транскрипционный коактиватор [4]. Для проведения дифференциальной диагностики келоидных рубцов осуществляется осмотр пораженной кожи, лучше под контролем дерматоскопии.
Заживление ран представляет собой сложный динамический процесс, подразделяющийся на три отдельные фазы: воспаления, пролиферации и ремоделирования, которые часто перекрываются. Патогенез гипертрофических и келоидных рубцов изучен не полностью. Однако нарушение регуляции на любой из этих фаз может предрасполагать к их развитию. Хотя гипертрофические и келоидные рубцы являются различными образованиями, они лежат в спектре одного и того же патофизиологического процесса. Классические провоспалительные цитокины интерлейкин (IL)-6, IL-8 и противовоспалительные цитокины IL-10 участвуют в заживлении ран. Предполагается, что нарушение регуляции этих цитокинов может способствовать развитию келоидов. В месте повреждения присутствует трансформирующий фактор роста (TGF)-β, фактор, который стимулирует пролиферацию фибробластов, синтез коллагена и способствует дифференцировке фибробластов в миофибробласты. TGF-β является полифункциональным цитокином, регулирующим клеточную пролиферацию, апоптоз, иммунные реакции, ремоделирование внеклеточного матрикса [5]. TGF-β имеет несколько изоформ, от 1 до 3 из которых вовлечены в этот аномальный процесс. TGF-β1 и 2 активируют фибробласты, а TGF-β3 является антагонистом рецепторов, который снижает активность фибробластов. Предполагается, что TGF-β1 и ИЛ-6 стимулируют дифференцировку нормальных фибробластов дермы в миофибробласты. Последние характеризуются повышенной способностью продуцировать компоненты внеклеточного матрикса и ассоциированы с целым рядом заболеваний с выраженными фибротическими изменениями в легких, печени, коже и почках. Таким образом, миофибробласты усиленно продуцируют коллаген, волокна которого, беспорядочно расположенные, определяются в дерме при келоидных рубцах. Утолщенные коллагеновые волокна образуют беспорядочные переплетения в дерме, приводя к образованию уплотнений. Помимо этого, коллагеновые агрегаты окружаются эндотелиальными клетками, эритроцитами, тромбоцитами, мастоцитами с признаками формирования новых сосудов. В области келоидных рубцов повышено содержание коллагена I, III, VI, XII, XIV типов. Коллаген XII типа рассматривается как маркер миофибробластов, коллаген VI типа обладает множественными функциями и связан с активацией миофибробластов – стимулирует их дифференцировку и супрессирует апоптоз. Особенно выделяют присутствие в области келоидных рубцов коллагена XIV типа, который определяется на участках повышенного механического воздействия [6]. По сравнению с нормальной кожей келоидные рубцы увеличивают выработку коллагена до 20 раз. Другие факторы, которые регулируются дифференцированно, включают матриксные металлопротеиназы, фактор роста тромбоцитарного происхождения (PDGF), инсулиноподобный фактор роста (IGF-1), эпидермальный фактор роста, фактор роста эндотелия сосудов (VEGF), фактор некроза опухоли-α и фактор роста соединительной ткани. В целом эти белки способствуют созданию среды, в которой наблюдается повышенная пролиферация фибробластов и перепроизводство коллагена и ECM, а также снижение апоптоза фибробластов [7; 8]. На сегодняшний день, по данным современных исследований, описаны четыре характерных морфологических признака келоидов, которые включают: наличие хаотично расположенных гиалинизированных коллагеновых волокон, наличие выступающего края, «похожего на язык», под неизмененным эпидермисом и сосочковой дермой; горизонтальная полоса клеточного фиброза в верхней части сетчатого слоя дермы и выраженная фасциальная полоса [9]. На основании этих характерных особенностей коллаген в келоидах часто называют «келоидным коллагеном». Келоиды содержат большее количество зрелого коллагена (типа I), чем незрелого коллагена (типа III). В дополнение к коллагену наблюдается повышенное содержание фибронектина, гликозаминогликанов, хондроитинсульфата и протеогликанов, но снижается эластичность и декорин. Экспрессия α-гладкомышечного актина неоднородна в келоидах.
Современные стратегии профилактики образования рубцов представляют большой научно-практический интерес и в основном направлены на регрессию воспаления. Одним из таких подходов является прессотерапия [10]. Ранее было обнаружено, что использование давящей одежды, бинтов, специальных форм из лейкопластыря или специализированных устройств сводит к минимуму образование рубцов. Теоретически терапия давлением уменьшает кровоснабжение раны, что приводит к ослаблению выделения воспалительных цитокинов, снижению синтеза коллагена и образования рубцов. Кроме того, считается, что применение давления увеличивает апоптоз клеток в области келоида, уменьшает ангиогенез, что также способствует уменьшению вероятности образования патологических рубцов. Лечение гипертрофических рубцов зависит от тяжести контрактуры рубца: если она тяжелая, хирургическое вмешательство является первым выбором. Если нет, показана консервативная терапия. Доступными в настоящее время методами лечения первой линии гипертрофических и келоидных рубцов являются силиконовые пленки или гели. Гель наносят на область рубца 2 раза в день в течение 3-12 месяцев. Гели применяются на лицо, шею, область суставов, где силиконовые покрытия невозможно зафиксировать. Препарат может назначаться детям с рождения. Эффективность терапии вариабельна. Учитывая тот факт, что хирургическое лечение келоидных рубцов (наиболее сложного варианта развития патологического рубцевания) в 50–100% случаев приводит к еще более тяжелым рецидивам, особую роль приобретают методы их медикаментозной коррекции. Консервативные методы лечения, включая гелевые пластыри, фиксацию лентой, наружные средства для местного и инъекционного применения, пероральные средства и косметическую терапию, следует назначать в каждом конкретном случае. Существует несколько типов инъекционных препаратов, которые можно использовать для лечения. Одним из методов лечения гипертрофических и келоидных рубцов первой линии являются внутриочаговые инъекции кортикостероидов, их часто также делают в сочетании с силиконовым покрытием. Стероиды способны тормозить размножение нормальных и некоторых типов опухолевых клеток, обладают противовоспалительным эффектом, иммуносупрессивным и сосудосуживающим свойствами, которые могут помочь уменьшить боль и зуд. Стероиды снижают синтез коллагена и гликозаминогликанов, ингибируют пролиферацию фибробластов и вызывают дегенерацию коллагена и фибробластов. Использование кортикостероидов для внутрирубцового введения позволяет достичь более высоких концентраций стероидов в рубце с минимальной системной абсорбцией. Внутрирубцовые инъекции кортикостероидов обычно делаются с триамцинолоном в дозе от 10 до 40 мг / мл каждые 4-6 недель. Обычно системные побочные эффекты не наблюдаются, поскольку используются низкие дозы. Однако сообщалось, что повторное введение стероидных инъекций может быть связано с гипертонией, сердечной недостаточностью, неконтролируемым диабетом и бактериальными и грибковыми инфекциями [3]. Внутриочаговые инъекции в ряде случаев приводят к развитию ранних осложнений, таких как кровотечение, кровоподтеки, инфицирование, нарушение заживления ран, стерильные абсцессы, а также отсроченных эффектов, таких как кожная и подкожная липоатрофия, лейкодермия, телеангиэктазии и локализованные или отдаленные стероидные акне. На практике, как показали результаты ряда исследований, многократное ежедневное местное нанесение крема, содержащего кортикостероиды, оказывало положительное воздействие на существующие келоиды и уменьшало рецидивы при нанесении даже на старые келоидные рубцы. Однако ограничением является то, что крем легко стирается [9].
Терапия противоопухолевыми препаратами может рассматриваться как альтернативный метод лечения, когда пациенту невозможно применить другие методы. 5-Фторурацил представляет собой аналог пиримидина, который ингибирует фермент тимидилатсинтазу, причем внутриочаговый способ введения является предпочтительным. Его использование в качестве варианта терапии при келоидных рубцах основано на том факте, что он ингибирует пролиферацию фибробластов, индуцирует апоптоз фибробластов без некроза, задерживает прогрессирование клеточного цикла и ингибирует TGF-β-индуцированный синтез коллагена I типа. При использовании глюкокортикостероидов или противоопухолевых препаратов часто используется комбинация с другими методами лечения. Внутриочаговые инъекции ботулинического токсина типа А могут улучшить и предотвратить гипертрофические рубцы и келоиды, подавляя натяжение рубца и активность фибробластов. Недавние рандомизированные контролируемые исследования показали, что послеоперационные инъекции ботокса предотвращали рубцы, улучшали внешний вид и уменьшали ширину гипертрофических рубцов и келоидов [11]. Основными побочными эффектами этого метода терапии являются выраженная болезненность инъекций и местная гиперпигментация. Экспериментальным вариантом лечения является терапия мезенхимальными стволовыми клетками (МСК). Благодаря высвобождению факторов роста из экзосом МСК, в частности трансформирующего фактора роста β, возможно изменение выраженности воспалительных реакций и развитие противофиброзного действия [12].
Криотерапия - это метод, который показал эффективность при небольших келоидах. Криотерапию в качестве монотерапии используют для лечения келоидов высотой не более 6 мм [13]. Жидкий азот может подаваться также с помощью специального оборудования или через криозонд с инъекционной иглой. Преимущества криодеструктивных методов лечения: большая точность воздействия, отсутствие заметной общей реакции, сравнительно высокая результативность лечения.
Цель исследования: описать клинический случай келоидного рубца у женщины 48 лет.
Клинический случай
На прием к дерматовенерологу пациентка женского пола в возрасте 48 лет с келоидным рубцом была направлена хирургом, к которому она обращалась по поводу обширного рубца на коже левого плеча, возникшего после термического ожога. Ожоговые травмы сопровождаются иммунной и воспалительной реакцией, метаболическими изменениями, которые могут быть сложными для лечения и приводить к образованию постоянных рубцов и неблагоприятным последствиям. Однако при тяжелых ожогах воспалительный процесс может становиться неконтролируемым, приводя к хроническому воспалению. Рубец причинял пациентке выраженный дискомфорт при движении конечностью, а также рассматривался как косметический дефект. Со слов пациентки, самостоятельно применяла увлажняющие средства, без выраженного эффекта. На момент обращения к хирургу ей было предложено хирургическое иссечение рубца, пациентка от предложенного метода лечения отказалась.
По данным объективного осмотра: на левом плече имеется выраженная рубцовая деформация кожи яркого, темно-розового цвета с неровными асимметричными краями, визуализированными сосудами древовидной формы, размером 8,0х4,0 см. На поверхности рубца справа прослеживается атрофия, в то время как слева наблюдаются отчетливые гипетрофические разрастания. При пальпации выступающий над кожей красный рубец плотный. Кожа вокруг рубца не изменена, болезненности нет (рис. 1).
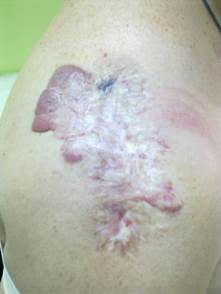
Рис. 1. Келоидный рубец на левом плече
Пациентке рекомендовано лечение в целях коррекции келоидного рубца в виде внутрирубцового введения инъекций триамцинолона ацетонида (кеналог) в дозе от 10 до 40 мг / мл каждый месяц в течение полугода. Инъекции выполнялись с различных точек. Курс терапии длился 4 месяца.
Данный клинический случай свидетельствуют о необходимости обращать внимание на особенности формирования рубцовой ткани у пациента на ранних сроках. Для келоидных рубцов характерно:
• начало формирования через несколько недель или месяцев после полного заживления раны;
• достаточно высокая скорость роста;
• отсутствие тенденции к уменьшению;
• распространение за пределы первоначальной раны;
• невозможность сформировать складку кожи на месте рубца;
• присутствие болезненности, зуда, жжения;
• бугристая и плотная консистенция рубца.
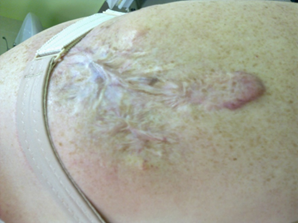
Рис. 2. Келоидный рубец на левом плече после лечения
Наиболее наглядной и широко используемой в клинической практике для оценки келоидных рубцов является The Vancouver Burn Scar Assessment Scale (Ванкуверская шкала оценки рубца). Общий результат по данной шкале может быть от 0 до 14 баллов (эластичность и высота над уровнем здоровой кожи, васкуляризация, пигментация), при этом результат 0 соответствует нормальной коже. При обращении пациентки показатели оценки по Ванкуверской шкале состояния рубца на левом плече составили 9 баллов, а после лечения инъекциями кортикостероидов составили 4 балла (рис. 1, 2). У больной была отмечена положительная динамика на фоне лечения, выражающаяся в исчезновении субъективных ощущений, уплощении рубца, образовании на месте келоида атрофического рубца.
Для профилактики образования и лечения молодых рубцов практикуют использование прессотерапии в виде давящих повязок с местными препаратами силикона, правильное применение которых может улучшить внешний вид келоида. Лечение келоидов начинается с внешнего осмотра и определения количества и размера келоидов для оценки факторов риска развития келоидов, индивидуальных у каждого пациента. Если имеется один келоидный рубец или рубцы небольшие, то, вероятно, основной причиной развития патологического рубца является натяжение кожи. Однако при наличии множественных или больших келоидов следует учитывать генетические и системные факторы, особенно при локализации келоидных рубцов в разных областях тела. Единичные или небольшие келоидные рубцы можно лечить консервативной терапией. На стадии старого рубца врач в первую очередь должен убедиться, что его рост закончен и рубцовая ткань стабильна. Тогда задача состоит в том, чтобы сделать его менее заметным (полностью убрать келоидный рубец невозможно, поскольку коррекция рубцовой деформации ведется строго в границах рубца, а минимальное воздействие на здоровую окружающую ткань может спровоцировать возобновление роста келоида). Пациенты с келоидными рубцами, получившие лечение, должны быть проинформированы и настроены на лечение рубцов и последующее наблюдение в долгосрочной перспективе. Тщательное наблюдение позволяет выявлять и лечить небольшие рецидивы, которые хорошо реагируют на местную стероидную терапию. Таким образом, пациенты должны находиться под наблюдением более 18-24 месяцев. Последующее наблюдение может прекратиться, когда рубец станет плоским и мягким. Консервативные методы могут использоваться как профилактические средства для предотвращения нежелательного образования рубцов и окончательного лечения, а также промежуточной терапии до тех пор, пока не будет произведено дальнейшее хирургическое восстановление, или в качестве дополнительного лечения после хирургической ревизии рубца.
Заключение. На сегодняшний день имеются разные технологии лечения келоидных рубцов, выбор оптимального способа остается актуальным вопросом врача-дерматовенеролога.
Библиографическая ссылка
Селицкая О.В. КЕЛОИДНЫЕ РУБЦЫ: СОВРЕМЕННЫЕ АСПЕКТЫ ПАТОГЕНЕЗА И ЛЕЧЕНИЯ // Современные проблемы науки и образования. 2023. № 3. ;URL: https://science-education.ru/ru/article/view?id=32613 (дата обращения: 19.05.2026).
DOI: https://doi.org/10.17513/spno.32613



