Исследование выполнялось в рамках федеральной целевой программы «Развитие фармацевтической и медицинской промышленности Российской Федерации на период до 2020 года и дальнейшую перспективу». Государственный контракт от 14.11.2017 №14.N08.11.1042.
Патофизиология формирования язвенной болезни желудка четко не определена, однако патогенетические теории развития предъязвенного фона, такие как кислотно-пептическая, нестероидная, хеликобактерная, гастрическая, стрессовая, общепризнанны [1–3]. Например, увеличение секреции глюкокортикоидов приводит к дистрофическим изменениям поверхностного эпителия слизистой оболочки, ослаблению секреции защитных мукополисахаридов, нарушению синтеза рибонуклеиновой кислоты, усилению процессов распада, тормозящих регенерацию. Определенный вклад в развитие дистрофических изменений вносят сосудистые нарушения, обусловленные набуханием эндотелия, мукоидным отеком, изменением эластических и аргирофильных волокон стенок сосудов. Все перечисленные механизмы провоцируют ульцерогенез. Для экспериментального моделирования глюкокортикоидных язвенных повреждений предложена методика комбинирования глюкокортикоида преднизолона с 80 % раствором этилового спирта [4]. Этанол повреждает эндотелий сосудов, что приводит к снижению кровотока и развитию ишемии, ингибирует антиоксидантную систему, что способствует образованию свободных радикалов [5–7]. Этанол-преднизолоновая модель позволяет со 100 % статистической вероятностью воссоздать эрозивно-язвенное повреждение слизистой желудка [8]. Цели исследования – изучение противоязвенной активности готовой лекарственной формы на основе динитрата 2-фенил-9-диэтиламиноэтилимидазо[1,2-а]бензимидазола при введении преднизолона в виде спиртового раствора на 80 % этиловом спирте с использованием в качестве препаратов сравнения ранитидина и омепразола.
Материалы и методы исследования
В эксперименте использовалась готовая лекарственная форма динитрата 2-фенил-9-диэтиламиноэтилимидазо[1,2-а]бензимидазола (лабораторный шифр ГЛФ РУ-64, таблетки 60 мг). Таблетки светло-зеленого цвета без запаха, двояковыпуклые, серия № 001 от 01.03.2018 [9]. Препараты сравнения: ранитидин (Хемофарм А.Д., Сербия, серия М703084), омепразол (субстанция омепразола Sigma Аldrich, США). Эксперименты выполнены на крысах-самцах линии Wistar (возраст 10–12 недель) массой 180–250 г. Животные содержались в соответствии с требованиями постановления Главного государственного санитарного врача РФ от 29.08.2014 № 51 «Об утверждении СП 2.2.1.3218-14 «Санитарно-эпидемиологические требования к устройству, оборудованию и содержанию экспериментально-биологических клиник (вивариев)». Язвенное поражение вызывалось введением преднизолона (Гедеон Рихтер, Румыния, серия № 960920), растворенного в спирте из расчета 20 мг/кг, и 80 % этилового спирта (необходимую концентрацию получали путем разведения спирта этилового 96 % водой дистиллированной с использованием ареометра лабораторного) в дозе 0,6 мл на 100 г массы тела животных. Доза для ГЛФ РУ-64 равна ЕD50, рассчитана на основании данных, полученных на модели этанол-преднизолонового повреждения для фармацевтической субстанции (5 мг/кг). Для ранитидина (28 мг/кг) и омепразола (3,7 мг/кг) дозы рассчитаны исходя из суточной дозы для человека с использованием соответствующих коэффициентов пересчета (для человека – 39, для крыс – 6). За 24 ч до моделирования патологии животные подвергались пищевой депривации со свободным доступом к воде. Исследуемая ГЛФ РУ-64 и препараты сравнения вводились профилактически за 1 час до введения комбинации этанола и преднизолона. Эвтаназию животных проводили через 12 ч после введения комбинации этанола и преднизолона. Исследования выполнялись в соответствии с Национальным стандартом РФ ГОСТ Р 53434-2009 «Принципы надлежащей лабораторной практики» и приказом Минздрава России от 01.04.2016 г. № 199н «Об утверждении правил надлежащей лабораторной практики» [10]. После эвтаназии из брюшной полости экспериментальных животных извлекали желудки и промывали их 0,9 % раствором хлорида натрия. Оценку повреждения осуществляли макроскопическим способом, подсчитывали площадь язвенного поражения и проводили макрофотографию. Для микроскопического изучения желудки фиксировались в 10 %-ном нейтральном формалине и заливались парафином. Гистологические срезы изготавливались на санном микротоме. Оценка глубины повреждения слизистой оболочки желудка проводилась с использованием инструментов программного обеспечения "Leica Application Suite".
Для анализа глубины язвенной альтерации использовали систему баллов [11]. В каждой группе высчитывали сумму баллов, после чего рассчитывали среднюю арифметическую величину, которая отображает среднюю степень изъязвления в группе (СИ). СИ – степень изъязвления, является средним арифметическим значением всех рассчитанных баллов. Также проводился расчет индекса изъязвления. В индексе изъязвления (ИИ) отражены как процент частоты животных с язвами, так и степень дистрофических нарушений в желудке. Рассчитывается как произведение степени изъязвления на % животных с язвами, деленное на 100.
Обработку полученных данных выполняли с использованием вариационной статистики: нормальность распределения вычисляли, используя критерий Колмогорова – Смирнова, рассчитывали среднее значение (М) и стандартную ошибку среднего значения (m), для параметрического распределения применяли критерий Стьюдента, а для непараметрического распределения использовали U-критерий Манна – Уитни.
Таблица 1
Распределение экспериментальных животных по группам
|
№ группы |
Вводимые вещества, доза |
|
Группа (контрольные; n= 10♂) |
преднизолон 20 мг/кг + этанол 80 % |
|
Группа (опытные; n = 10♂) |
преднизолон 20 мг/кг + этанол 80 % + ГЛФ РУ-64 – 5 мг/кг |
|
Группа (сравнение 1; n = 10♂) |
преднизолон 20 мг/кг + этанол 80 % + Ранитидин – 28 мг/кг |
|
Группа (сравнение 2; n = 10♂) |
преднизолон 20 мг/кг + этанол 80 % + Омепразол – 3,7 мг/кг |
Результаты исследования и их обсуждение
Эксперименты показали, что интрагастральное введение этанол-преднизолоновой смеси вызывает эрозивно-язвенное повреждение слизистой желудка. На рис. 1 представлена картина наиболее характерных макроскопических изменений слизистой желудка в контрольной группе и в группах, получавших ГЛФ РУ-64, препараты сравнения ранитидина и омепразола.
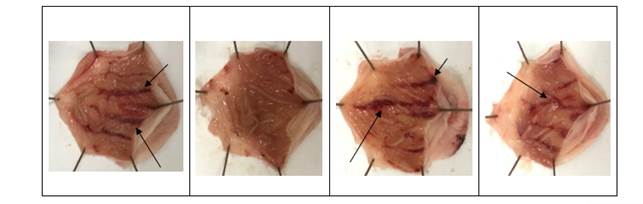
Рис. 1. Макрофотографии слизистой желудка исследуемых групп при повреждении этанол-преднизолоновой смесью
Изучаемая ГЛФ РУ-64 в дозе 5 мг/кг на 40 % снижала количество животных с поражением слизистой желудка, а площадь повреждения слизистой уменьшалась на 81,6 % по сравнению с контрольной группой. В 3-й группе, получавшей ранитидин в дозе 28 мг/кг, количество животных с поражением слизистой желудка уменьшалось на 20 %, а площадь повреждения на 66 % по сравнению со значениями контрольной группы. В 4-й группе, получавшей омепразол в дозе 3,7 мг/кг, количество животных с поражением слизистой желудка, так же как и в 3-й группе, уменьшалось на 20 %, а площадь повреждения на 63 % по сравнению с контрольной группой. Следует отметить, что достоверных отличий между эффектами изучаемой ГЛФ РУ-64 и препаратами сравнения по показателю абсолютных значений площади поврежденной слизистой не зафиксировано. В то же время расчет индекса изъязвления, который указывает не только на площадь поражения, но и на частоту эрозивно-язвенных изменений у животных, показал, что в группе ГЛФ РУ-64 индекс изъязвления снижался на 77 %, в группе препарата сравнения ранитидина на 47 %, в группе омепразола на 49 % (табл. 2).
Таблица 2
Макроскопические данные влияния ГЛФ РУ-64 на слизистую оболочку желудка при введении преднизолона 20 мг/кг в сочетании с этанолом (80 %), М±m
|
Группа (вещество) |
Доза |
Площадь повреждения (мм2/особь) |
% особей с поражением слизистой |
Степень изъязвления (СИ) |
Индекс изъязвле-ния (ИИ) |
% снижения ИИ |
|
Этанол + преднизолон
|
20 мг/кг в 80 % спирте |
64,09±14,61 |
100
|
3,90±0,10 |
3,90 |
– |
|
ГЛФ РУ-64 |
5 мг/кг |
11,82±7,07* |
60 |
1,50±0,47* |
0,90 |
77 |
|
Этанол + преднизолон
|
20 мг/кг в 80 % спирте |
|||||
|
Ранитидин |
28 мг/кг |
21,75±4,76* |
80 |
2,60±0,48* |
2,08 |
47 |
|
Этанол + преднизолон
|
20 мг/кг в 80 % спирте |
|||||
|
Омепразол |
3,7 мг/кг |
23,73±5,55* |
80 |
2,50±0,48* |
2,0 |
49 |
|
Этанол + преднизолон
|
20 мг/кг в 80 % спирте |
|||||
|
Примечание: * – достоверность относительно контроля Р < 0,05. |
||||||
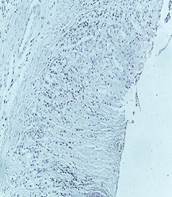
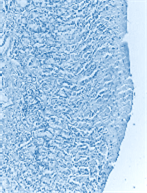
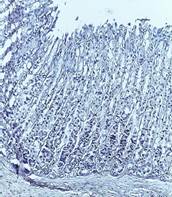
Микроскопическое изучение продемонстрировало, что сочетание преднизолона с этанолом приводит к процессу формирования поверхностных дефектов слизистой оболочки с лейкоцитарной инфильтрацией, деструкцией желез, кровоизлияниями и некрозом тканей. Микрофотографии наиболее типичных изменений и их описание представлены на рис. 2.
|
|
|
|
|
|
Группа № 1 Преднизолон 20 мг/кг + Этанол 80 %
|
Группа № 2 Преднизолон 20 мг/кг + Этанол 80 % + ГЛФ РУ-64 5 мг/кг |
Группа № 3 Преднизолон 20 мг/кг + Этанол 80 % + Ранитидин 28 мг/кг |
Группа № 4 Преднизолон 20 мг/кг + Этанол 80 % + Омепразол 3,7 мг/кг |
|
Дефект слизистой до подслизистого слоя с выраженным отеком. Отмечается обширная деструкция желез с участками гомогенных некротических масс |
Общий план строения слизистой сохранен, отмечается поверхностный отек и десквамация эпителия |
Поверхностный дефект слизистой с периферическими мелкоочаговыми кровоизлияниями, полнокровием сосудов подслизистой |
Отмечался выраженный отек слизистой с расширением просвета желез и пространств между ними. Также отмечались участки поверхностной десквамации эпителия |
Рис. 2. Результаты патоморфологической оценки влияния ГЛФ РУ-64 на процесс формирования язвенных повреждений слизистой оболочки желудка при введении преднизолона 20 мг/кг в сочетании с этанолом (80 %)
Морфометрические измерения глубины повреждения показали, что деструктивные процессы при профилактическом введении ГЛФ РУ-64 по показателю глубины формируемых дефектов были достоверно менее выражены, по сравнению с данными групп, получавших препараты сравнения ранитидин и омепразол. Средний процент снижения глубины повреждения при введении ГЛФ РУ-64 в дозе 5 мг/кг составил 78 %. Ранитидин и омепразол также достоверно относительно контроля снижали глубину повреждения слизистой оболочки – на 54 и 53 % соответственно. По результатам гистологических исследований деструктивные процессы в слизистых оболочках были выявлены только у 30 % животных, получавших ГЛФ РУ-64 (табл. 3).
Таблица 3
Показатели морфометрической оценки влияния ГЛФ РУ-64 на создание язвенной альтерации слизистой оболочки желудка при использовании преднизолона 20 мг/кг в сочетании с этанолом (80 %) (n = 50)
|
Группа |
Глубина повреждения, мкм |
Средний % снижения глубины повреждения |
|
Контроль Преднизолон 20 мг/кг + этанол 80 % |
141,95± 16,8 |
|
|
– |
||
|
Преднизолон 20 мг/кг + этанол 80 % + ГЛФ РУ-64 5 мг/кг |
30,48± |
|
|
6,90*&# |
-78 |
|
|
Преднизолон 20 мг/кг + этанол 80 % + ранитидин 28 мг/кг |
64,13± |
|
|
7,20* |
-54 |
|
|
Преднизолон 20 мг/кг + этанол 80 % + омепразол 3,7 мг/кг |
65,23± |
|
|
10,54* |
-53 |
|
|
Примечание. * – достоверность относительно контроля Р < 0,05, & – достоверность относительно группы получавших ранитидин в эквивалентной дозе Р < 0,05, # – достоверность относительно группы получавших омепразол в том же уровне дозы Р < 0,05. N = 50, так как для исследования использовалось 10 животных в группе, производили по 5 измерений глубины на участках. |
||
Заключение
Исследуемая готовая лекарственная форма на основе динитрата 2-фенил-9-диэтиламиноэтилимидазо[1,2-а]бензимидазола проявляет выраженное антиульцерогенное действие при моделировании преднизолон-этанолового повреждения слизистой желудка по показателям макро- и микроскопического исследования. У экспериментальных животных зафиксировано снижение степени и площади повреждения слизистой оболочки желудка, снижение интенсивности кровоизлияний, деструкции кровеносных сосудов и степени некроза. Полученные эффекты сопоставимы с действием препаратов сравнения ранитидина и омепразола. По показателю глубины повреждения слизистой оболочки желудка ГЛФ РУ-64 достоверно превосходила действие препаратов сравнения. Данные результаты сопоставимы с полученными ранее результатами по гастропротекторной активности фармацевтической субстанции динитрата 2-фенил-9-диэтиламиноэтилимидазо[1,2-а]бензимидазола. Таким образом, разработанная на основе фармацевтической субстанции динитрата 2-фенил-9-диэтиламиноэтилимидазо[1,2-а]бензимидазола ГЛФ РУ-64 обеспечивает гастропротекторное и антиульцерогенное действие при моделировании преднизол-этанолового повреждения, что позволяет считать дальнейшее изучение данной лекарственной формы перспективным с целью пополнения арсенала гастропротекторных средств на фармацевтическом рынке.
Библиографическая ссылка
Черников М.В., Абисалова И.Л., Хромова Н.А. ИЗУЧЕНИЕ ПАТОФИЗИОЛОГИЧЕСКИХ МЕХАНИЗМОВ ПРОТИВОЯЗВЕННОЙ АКТИВНОСТИ ГОТОВОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ ДИНИТРАТА2-ФЕНИЛ-9-ДИЭТИЛАМИНОЭТИЛИМИДАЗО[1,2-А]БЕНЗИМИДАЗОЛА НА МОДЕЛИ ЭТАНОЛ-ПРЕДНИЗОЛОНОВОГО ПОВРЕЖДЕНИЯ СЛИЗИСТОЙ ОБОЛОЧКИ ЖЕЛУДКА // Современные проблемы науки и образования. 2023. № 2. ;URL: https://science-education.ru/ru/article/view?id=32589 (дата обращения: 25.05.2026).
DOI: https://doi.org/10.17513/spno.32589