В современной хирургии одним из основных достижений представляется лечение самых тяжелых патологий живота. Данные исследований обнадеживают лечение данных болезней по применению малотравматичных методов, особенно лапароскопических. Безусловно, такого рода повышенная хирургическая эффективность чаще характерна для госпитальной хирургии. В то же время до сих пор у больных ургентными болезнями живота сохраняется риск формирования осложнений, причем на высоком уровне, которые нуждаются в оперативной коррекции. У подобных больных показания к повторным вмешательствам часто определяются запоздало. Следовательно, вопросу прогнозирования послеоперационных последствий в раннем периоде хирургического лечения должно уделяться особое внимание.
Большинство прогностических методов, используемых в определении течения послеоперационного периода, основываются на клинических и биохимических критериях. В их число входит параметр «лейкоцитарный индекс интоксикации», рассчитывающийся по формуле Я.Я. Кальф-Калифа. Данный показатель учитывает гранулоцитарные и агранулоцитарные особенности лейкоцитарной формулы [1].
В практике имеется метод определения степени воспалительной реакции путем оценки биомаркеров прокальцитонина и С-реактивного белка (СРБ). Значение данных маркеров увеличивается при инфекционных и воспалительных патологиях. Выявлена его высокая точность в определении интоксикации при перитоните и сепсисе [2]. Возрастание СРБ в первые пять суток достоверно связано с высокой вероятностью смертности, а при его уменьшении, напротив, риск неблагоприятного исхода понижается [3].
В определении послеоперационных исходов используются параметры цитокиновой (интерлейкин-1 (ИЛ), ИЛ-4, ИЛ-6, ИЛ-8, ИЛ-12, фактор некроза опухоли-альфа и др.) и иммунной (клеточной и гуморальной) систем. Обнаружено их увлечение при кардиохирургических патологиях [4].
По данным исследователей выявлено наличие у больных с ургентными абдоминальными патологиями ассоциации между развитием послеоперационных последствий и расстройствами системы гемостаза. При этом были успешно применены параметры функционального состояния активности системы свертывания и фибринолиза в прогнозировании развития послеоперационных осложнений [5].
В литературе описан метод прогнозирования исхода лечения острых инфекционных заболеваний при помощи оценки уровня метаболитов фибрина. Выявлено, что даже небольшое увеличение продуктов такого рода отрицательно сказывается на прогнозе [6].
Определение исхода послеоперационного периода у больных острыми хирургическими патологиями возможно по оценке уровня миоглобина в плазме крови при помощи техники гемагглютинации. Показано, что при значении миоглобина 1024–2048 нг/мл прогнозируют развитие осложнений в послеоперационном периоде. В то же время увеличение этого показателя свыше 2048 нг/мл указывает на прогрессирующее течение и риск неблагоприятного исхода (патент RU 2 067 768 C1).
Для диагностики эндогенной интоксикации в ранней стадии острой патологии, особенно при осложненном послеоперационном течении, у пациентов исследуют плазменный уровень средних молекул в предоперационном и послеоперационном периоде. Выявлено, что повышение содержания данного параметра на 34% относительно референсного значения считается риском развития эндотоксикоза и послеоперационных последствий. При этом нормализация уровня средних молекул указывает на благоприятный исход послеоперационного периода [7].
Итак, в литературе встречаются разные методы, позволяющие провести своевременную диагностику инфекционно-воспалительных осложнений. Однако каждый способ имеет свои минусы, некоторые из них характеризуют следствия патологического процесса, но не определяют его состояние, которое является наиболее информативным в оценке течения и исхода заболевания. Решение данной задачи можно осуществлять путем включения продуктов катаболических процессов пораженных тканевых структур в прогностические тесты [8].
Цель исследования: предложить оригинальный метод прогнозирования вероятности осложнений в раннем периоде после хирургического вмешательства, основанный на полной оценке маркеров гнойно-воспалительных процессов и активности триггерных агентов.
Материал и методы исследования
Выполнено исследование 144 пациентов с ургентными патологиями живота. По причине заболевания больные разделены на 3 группы. Первая группа (n=77) – с острым перитонитом, вторая (n=38) – с острой кишечной непроходимостью (ОКН), третья (n=29) – с панкреонекрозом.
Средний возраст составлял примерно 48,3±5,6 года у пациентов первой группы, 52,1±7,3 года – второй и 44,2±6,2 года – третьей.
Длительность патологии составила 23,3±2,6 ч в первой группе, 19,3±1,9 ч – во второй и 27,1±2,5 ч – в третьей.
Вид лечения – хирургический. Объем оперативной коррекции был связан с характером заболевания. Больные ОКН и острым перитонитом были оперированы после поступления в клинику и проведения предоперационной подготовки, а пациенты с панкреонекрозом – при развитии осложнений.
Методы исследования. Наряду со стандартными тестами определены параметры процессов липопереокисления (малоновый (МД) диальдегид (Д.Ю. Егоров, А.В. Козлов, 1988)); эндотоксикоза (молекулы (МСМ) средней массы (О.И. Пикуза, Л.З. Шакирова, 1994)); мембранодестабилизирующих явлений (лизоформы (ЛФ) фосфолипидов по методике хроматографии на силикагелевых пластинах и денситометра Model GS-670 (BIO-RAD, США, (Phosphor Analyst/ PS Sowtware) (Д. Хиггинс,1990)).
На основе вышеуказанных параметров разработан индекс определения исхода раннего периода после операции (патент № 2729730) [9]:
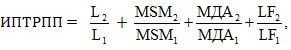
где ИПТРПП – индекс исхода, L1 – лейкоциты в предыдущий момент, L2 – лейкоциты в текущий момент, MSM2 – МСМ в текущий момент, MSM1 – МСМ в предыдущий момент, MDA2 – МДА диальдегида в текущий момент, MDA1 – МДА в предыдущий момент, LF1 – ЛФ в предыдущий момент, LF2 – ЛФ в текущий момент.
Полученные результаты статистически были обработаны с помощью программ Microsoft Excel 2013 и Statistica 6.1 при значимости p<0,05.
Результаты исследования и их обсуждение
Для прогнозирования гнойных и воспалительных процессов определены содержание лейкоцитов в плазме крови, а также степень токсемии, сопутствующей данным процессам. Интенсивность системных нарушений оценивается интегральным определением одного из основных мембранодестабилизирующих маркеров – перекисного окисления мембранных липидов по содержанию МД. При этом выраженность мембранодестабилизирующих процессов выявлена по активности ЛФ – молекулярного метаболита вышеуказанных патологических явлений клеточных биомембран и тканевой деструкции. Параметры определены в плазме крови, что упрощало расчеты.
Обоснование экстраполирования параметров степени мембранодестабилизирующих реакций разных тканей и органов, определенных в крови, представились результаты экспериментальных и клинических исследований. В последних была показана высокая степень корреляционной связи (r=0,87–1,0, р<0,05) между вышеуказанными параметрами в различных объектах.
Клинические значения индекса, определяющего течение раннего периода после операции, оценены достоверными результатами клинических и биохимических тестов более 144 пациентов разной ургентной болезней живота.
Выявлено, что значение индекса до 3,4 указывает на отсутствие риска послеоперационных осложнений, с одной стороны, и на адекватность проводимого лечения – с другой.
При наблюдении показано, что примерно у 76 исследуемых пациентов с острыми абдоминальными патологиями значение индекса равнялось 1,8–3,4 в первые 3 суток после хирургической терапии. Данный период протекал без каких-либо последствий. Необходимо подчеркнуть, что это касалось всех заболеваний.
Приводим пример данной группы. Пациент П. поступил в клинику с диагнозом «острая кишечная непроходимость, осложненная острым перитонитом». С данных анамнеза: срок патологии около 2 дней. Он был оперирован в течение 3 ч после проведения предоперационной подготовки. Интраоперационно хирургического вмешательства у пациента диагностированы внутреннее ущемление грыжи, серозно-фибринозный перитонит. В нижнем илеоцекальном углублении проведено устранение ущемленной части кишки. Кишечная жизнеспособность сохранена, но имеются выраженные воспалительные изменения. Выполнены назоинтестинальная интубация, санирование и дренирование брюшной полости.
Результат лабораторных анализов, сделанных в первые 4 суток после операции, показал, что через 2 дня после хирургической коррекции индекс прогнозирования равнялся 3,6, что свидетельствует о низком риске послеоперационных осложнений. На 3-и и 4-е сутки он составил 2,7 и 1,6 соответственно, что свидетельствовало об отсутствии возможности формирования осложнений. Это также подтверждало то, что клиническое течение протекало в раннем послеоперационном периоде без осложнений. Кишечные шумы возникли спустя 1,5 дня после операционной терапии. Назоинтестинальный зонд извлечен спустя 3 суток. Пациент выписан из клиники с выздоровлением.
Данными исследований показано, что при значении индекса прогнозирования раннего послеоперационного периода примерно 3,5–4,1 возникает настороженность в отношении возникновения риска развития осложнений.
Наши исследования выявили, что у 44 изучаемых пациентов в первые 3 суток хирургической коррекции индекс был в пределах 3,5–4,1. У 37 больных ранний послеоперационный период протекал без каких-либо последствий. Но среди 7 больных регистрированы раневые осложнения. Обратим внимание, что это отмечено среди всех нозологий.
Установлено, что при индексе от 4,2 и выше вероятность развития осложнений становится высокой, что служит основанием кардинального пересмотра терапевтического плана с включением более эфферентных методов или повторных операций.
У 20 исследованных пациентов изучаемый индекс в 1–3-й дни хирургического вмешательства оказался выше 4,2. При этом его значение в динамике наблюдения сохранилось на высоком уровне. У данных больных выявлено формирование разного рода осложнений.
Так, среди 13 больных отмечены раневые последствия гнойного вида. Индекс прогнозирования раннего периода после операции в 1–5-е сутки соответствовал 4,2–4,8. После вскрытия и дренирования гнойной раны значение параметра снижалось до 2,3±0,2.
В раннем послеоперационном периоде у 3 больных регистрирована острая пневмония (поражение тканей легких около 30%). У них индекс был в пределах 4,2–5,2. Пациентам проведена смена антибиотика и включены антиоксиданты. Значение индекса уменьшилось по ходу лечения до 2,4±0,2.
Среди 4 пациентов зарегистрированы третичный перитонит и септическое состояние. У них индекс составлял 4,3–5,5. Им выполнены повторные операции для санации брюшной полости. Далее выявлено, что у 2 больных отмечена положительная динамика с выздоровлением. Индекс данных пациентов уменьшался до 2,6 и 2,8 соответственно. У других 2 больных комбинированное лечение не было успешным. Значение индекса увеличивалось и соответствовало 5,2 и 5,7. Исход этих больных – летальный в результате прогрессирования перитонита и развития флегмоны брюшной стенки.
Приводим пример. Пациент С. госпитализирован в клинику с диагнозом «ОКН, осложненная перитонитом». Длительность патологии примерно 2 суток. Пациент был оперирован после предоперационной подготовки. Во время операции обнаружены опухоль слепой кишки с инфильтратом, ОКН, диффузный фибринозный перитонит. Хирургическая коррекция: резекция терминального отдела тощей кишки, слепой кишки и части восходящего отдела оболочной кишки. Культя ушита наглухо, выполнен илеоасцендоанастомоз, проведены назоинтестинальное зондирование и дренирование абдоминальной полости. В раннем сроке после операции состояние пациента не улучшалось. Результаты клинического, лабораторного и инструментального исследований показали существенные отклонения параметров функционального статуса системы гомеостаза. Со стороны респираторной системы имели место выраженные нарушения в виде двусторонней пневмонии. В то же время последствий со стороны брюшной полости не регистрировано. Спустя 2 дня после хирургического лечения выявлены симптомы перистальтики кишечника, через 5 суток извлечен назоинтестинальный зонд. Раневых осложнений также не было. Проведение послеоперационной терапии не оказалось успешным, состояние пациента не улучшалось. Симптомы респираторной депрессии нарастали. Установлен сепсис. Пациент переведен на искусственную вентиляцию легких. При этом его состояние не восстановилось. Присоединилась острая почечная дисфункция, и наступила смерть.
Данными лабораторных исследований показано, что спустя 2 дня после хирургического вмешательства значение индекса прогнозирования раннего послеоперационного периода составляло 4,7, что указывало на высокую степень возможности развития осложнений. Спустя 3–5–7 суток индекс увеличивался еще больше и составлял 5,2, 5,3, 5,6 соответственно, что также подтверждало высокий риск развития последствий.
Итак, применение индекса прогнозирования раннего срока после хирургического вмешательства у пациентов с ургентными патологиями живота поможет определить риск возможности развития в этом периоде разного рода осложнений.
Результаты применения у больных ургентными болезнями живота данного способа показали высокую точность в оценке течения раннего периода хирургического лечения и адекватности послеоперационной терапии, так как он позволяет определить как явления гнойно-воспалительных процессов, так и степень их выраженности на организменном уровне.
Выводы
1. В предложенном методе определяются вероятность формирования воспалительных и гнойных процессов с применением не только стандартных параметров (содержание лейкоцитов и токсинов в плазме крови), но и показателей эндотоксикоза (уровня молекулы средней массы), липопереокисления (количества малонового диальдегида), а также их степень выраженности по активности мембранодестабилизирующих явлений (активности лизоформ фосфолипидов).
2. Определение исследованных параметров обладает интегральной количественной характеристикой, а не статической, что позволяет динамично оценить ранний послеоперационный период и быстро и достоверно прогнозировать риска развития осложнений.
3. Расчет индекса прогнозирования течения раннего срока после хирургического лечения апеллируют на абсолютными данными, связанными с многими обстоятельствами, как технические нюансы каждой лаборатории, что в целом позволяет исключить возможность ошибочного прогноза.
Библиографическая ссылка
Власов А.П., Муратова Т.А., Власова Т.И., Хозина Е.А., Лещанкина Н.Ю., Рубцов О.Ю., Аль-Кубайси Ш.С., Ларина В.С. ЛИПИДНЫЕ ДЕСТАБИЛИЗАЦИИ – ПАТОГЕНЕТИЧЕСКАЯ ОСНОВА СПОСОБА ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ УРГЕНТНЫХ ЗАБОЛЕВАНИЙ ЖИВОТА // Современные проблемы науки и образования. 2022. № 6-1. ;URL: https://science-education.ru/ru/article/view?id=32269 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/spno.32269



