Свойства мелатонина (МТ), обусловленные биологией гормона эпифиза (мозговой железы), известны с конца прошлого века, вызывают повышенный интерес исследователей в силу его универсальных возможностей в лечении различных патологий [1]. Считается, что мелатонин в глазах участвует в модуляции многих важных функций сетчатки, например, он может модулировать реакцию электроретинограммы. Мелатонин модулирует зрительную функцию и жизнеспособность клеток в сетчатке мыши через рецептор мелатонина MT1. Мелатонин синтезируется в фоторецепторных клетках сетчатки, хрусталике и цилиарном теле [1].
Чувствительные специфические рецепторы к гормону эпифиза мелатонину распространены во многих структурах глазного яблока, что доказывает немаловажную роль мелатонина как в физиологических, так и в биологических процессах глазного яблока [2-4].
Мелатонин также может оказывать защитное действие на фоторецепторы и на другие типы клеток, такие как ганглиозные клетки. Некоторые исследования выявили участие мелатонина в патогенезе возрастной дегенерации желтого пятна. В литературе есть сообщения, что выработка мелатонина снижена у пациентов с ВМД по сравнению с контрольной группой того же возраста, что позволяет предположить, что дефицит мелатонина может играть роль в патогенезе ВМД [1; 5].
Мелатонин, обладающий антиоксидантными и противовоспалительными свойствами, регулирующий циркадный ритм, может представлять мощный инструмент для противодействия возрастным изменениям, в том числе болезням глаз [6].
Агрессивные воздействия солнечного излучения и токсикантов окружающей среды подвергают орган зрения окислительным атакам. В настоящее время накоплено большое количество доказательств участия оксидативного стресса в развитии многих глазных заболеваний, включая катаракту, глаукому, возрастную макулярную дегенерацию и диабетическую ретинопатию.
Концентрация мелатонина в сыворотке значительно различается в зависимости от возраста. Максимальный уровень мелатонина наблюдается у новорожденных, с возрастом его количество уменьшается, и наименьшие значения фиксируются у пожилых людей. Этот факт, возможно, объясняется ухудшением работы супрахиазматического ядра [7].
Мелатонин синтезируется в фоторецепторных клетках сетчатки, хрусталике и цилиарном теле [5; 8]. Кроме того, специфические рецепторы мелатонина расположены в ряде других структур глаза, что еще раз подчеркивает важную роль мелатонина в биохимических и физиологических процессах глаза [9; 10].
В глобальном масштабе число людей всех возрастов с нарушениями зрения оценивается в 285 миллионов. Амблиопия в последние годы является одной из наиболее частых причин значительного снижения максимально корригированной остроты зрения у детей дошкольного и школьного возраста [8].
Задача заключалась в оценке уровня мелатонина в структурах глазного яблока при обскурационной амблиопии у кроликов в условиях эксперимента с целью обоснования участия мелатонина в патогенезе амблиопии.
Материалы и методы исследования
Исследование выполнялось на двенадцати новорожденных кроликах-самцах (24 глаза) породы шиншилла. Подопытные животные были разделены на 2 группы: 1-я (опытная) группа - 12 глаз, 2-я (контрольная) группа - 12 глаз. При рождении, на 3-и сутки, на глаза хирургическим путем был наложен блефарорафический шов нитью викрил 5,0. Таким путём сформирована модель обскурационной амблиопии, или депривационной амблиопии. В возрасте 1, 2, 3 месяцев (30, 60, 90 дней) по четыре особи (2 – из основной группы и 2 – из контрольной группы) были выведены из эксперимента. Далее из энуклеированных глаз при помощи шприца 1 мл путём аспирации была получена влага передней камеры в объёме 0,75 мл, роговица иссечена вдоль лимба корнеосклеральными ножницами, сосудистая оболочка отделена от склеральной шпоры шпателем, радужка и хрусталик были удалены пинцетом, при помощи ложки для эвисцерации комплекс сетчатка / стекловидное тело был извлечен из склеральной полости, а также из периферической вены уха кролика произведен забор 0,75 мл венозной крови шприцем 1 мл. Животные выводились из эксперимента методом воздушной эмболии после введения кролика в наркоз. Все манипуляции с животными проводили в соответствии с требованиями «Европейской конвенции о защите позвоночных животных, используемых для экспериментов или в иных научных целях» (Страсбург, 1986) и «Правил проведения работ с использованием экспериментальных животных» (согласно приказу Минвуза СССР № 742 от 13.11.1984 «Об утверждении правил проведения работ с использованием экспериментальных животных»).
Концентрацию мелатонина в различных биосубстратах глаза (влага передней камеры и комплекс сетчатка / стекловидное тело) и сыворотке венозной крови кроликов оценивали с помощью иммуноферментного анализа на приборе MULTISKAN FC (Thermo Scientific, США) с применением специального набора Enzyme-linked Immunosorbent Assay Kit For Melatonin (Elabscience, США). Согласно инструкции к набору выполнялись все этапы иммуноферментного анализа.
Обработку полученных данных проводили при помощи методов вариационной статистики с применением статистического пакета Statistica 13,0 (StatSoft Inc., США). Хранение результатов исследования и первичную обработку материала осуществляли в оригинальной базе данных Excel 2010 (Microsoft, США). Гипотеза о принадлежности данных нормальному распределению была отклонена во всех случаях с вероятностью 95%, что обосновало применение непараметрического U-критерия Манна-Уитни. Полученные данные представлены в виде медианы (Ме) и 25-75-го квартилей (Q25-Q75). Уровень статистической значимости оценивали во всех процедурах статистического анализа (p), при этом уровнем критической значимости считали р ≤ 0,05.
Результаты исследования и их обсуждение
В таблице представлены результаты иммуноферментного анализа.
Уровень мелатонина (пг/мл) в различных биосубстратах глаза и сыворотке крови, данные представлены в виде Ме (Q25-Q75)
|
Возраст |
Эксперимент (OD) |
Контроль (OS) |
||||
|
ВПК |
ССТ |
СК |
ВПК |
ССТ |
СК |
|
|
1 |
1,53 (1,47-1,61)* |
12,25 (11,95-12,75)* |
295,7 (291,0-298,6) |
1,99 (1,95-2,02) |
41,53 (40,29-42,62) |
282,0 (275,7-288,3) |
|
2 |
1,31 (1,28-1,35)*# |
7,85 (7,61-8,06)*# |
276,8 (262,0-295,4) |
1,82 (1,79-1,85)# |
27,58 (27,15-28,50)# |
297,1 (285,4-308,4) |
|
3 |
0,97 (0,89-1,05)*# |
1,20 (1,13-1,23)*# |
301,3 (297,4-305,8) |
1,46 (1,39-1,53)# |
13,80 (12,34-15,72)# |
300,4 (289,2-303,3) |
Примечание: ВПК – влага передней камеры;
ССТ – комплекс сетчатка / стекловидное тело;
СК – сыворотка крови;
* – p<0,05 при сравнении эксперимента (OD) с контролем (OS);
# – p<0,05 при сравнении первого месяца с последующими.
При изучении содержания мелатонина в различных биосубстратах была отмечена его максимальная концентрация в сыворотке крови, затем в комплексе сетчатка / стекловидное тело и потом во влаге передней камеры глаза.
Как видно из представленных данных, на протяжении всего эксперимента содержание мелатонина в сыворотке крови всех кроликов не претерпевало значительных изменений и было стабильным.
Содержание мелатонина во влаге передней камеры экспериментального глаза (OD) было статистически значимо ниже, чем в контроле (OS), на протяжении всего эксперимента. На первом месяце эксперимента значение медианы OD было ниже на 23,1% (p<0,05); Q75 OD ниже Q25 OS на 17,4% (p<0,05). На втором месяце значение медианы OD было ниже на 28% (p<0,05); Q75 OD ниже Q25 OS на 24,5% (p<0,05). На третьем месяце значение медианы OD было ниже на 33,5% (p<0,05); Q75 OD ниже Q25 OS на 24,4% (p<0,05). Для большей наглядности полученные данные представлены в виде рисунка (рис. 1).
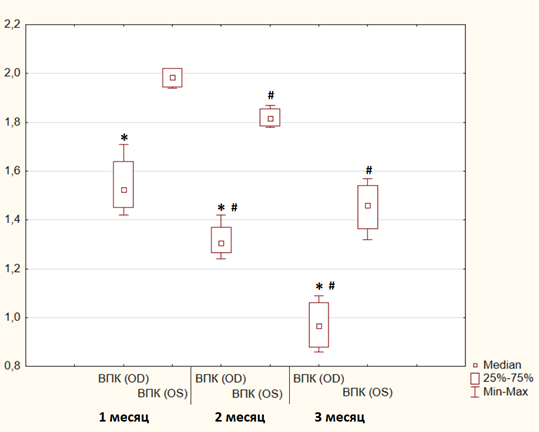
Рис. 1. Динамика уровня мелатонина во влаге передней камеры глаз кроликов, пг/мл
Примечание: ВПК (OD) – влага передней камеры экспериментального глаза (OD); ВПК (OS) – влага передней камеры контрольного глаза (OS); * – p<0,05 при сравнении эксперимента (OD) с контролем (OS); # – p<0,05 при сравнении первого месяца с последующими.
Аналогичная тенденция изменения содержания мелатонина наблюдалась в комплексе сетчатка / стекловидное тело. Концентрация мелатонина была статистически значимо ниже в экспериментальном глазу (OD) относительно контрольного глаза (OS). На первом месяце эксперимента значение медианы OD было ниже на 70,5% (p<0,05); Q75 OD ниже Q25 OS на 68,3% (p<0,05). На втором месяце значение медианы OD было ниже на 71,5% (p<0,05); Q75 OD ниже Q25 OS на 70,3% (p<0,05). На третьем месяце значение медианы OD было ниже на 90,8% (p<0,05); Q75 OD ниже Q25 OS на 90% (p<0,05). Как и в случае с влагой передней камеры глаза, на протяжении всего эксперимента фиксировалась статистическая достоверная тенденция к снижению уровня мелатонина в комплексе сетчатка / стекловидное тело от 1-го месяца исследования к 3-му месяцу исследования в обоих глазах. Для большей наглядности полученные данные представлены в виде рисунка (рис. 2).
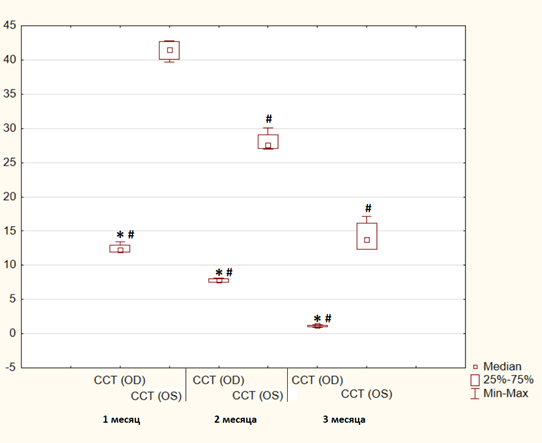
Рис. 2. Динамика уровня мелатонина в комплексе сетчатка / стекловидное тело глаз кроликов, пг/мл
Примечание: ССТ (OD) – комплекс сетчатка / стекловидное тело экспериментального глаза (OD); ССТ (OS) – комплекс сетчатка / стекловидное тело контрольного глаза (OS); * – p<0,05 при сравнении эксперимента (OD) с контролем (OS); # – p<0,05 при сравнении первого месяца с последующими.
Полученные в эксперименте результаты содержания мелатонина во влаге передней камеры и комплексе сетчатка / стекловидное тело статистически значимо ниже в экспериментальных глазах (обскурационная амблиопия), чем в контрольных, на протяжении всего эксперимента, что может свидетельствовать об участии мелатонина в формировании депривационной (обскурационной) амблиопии. Также на протяжении всего эксперимента фиксировалась статистически достоверная тенденция к снижению уровня мелатонина от 1-го месяца исследования к 3-му месяцу исследования в обоих глазах, что соответствует данным литературы о снижении уровня мелатонина в крови детей по мере их роста и взросления. Однако снижение уровня мелатонина в структурах глазного яблока экспериментальных животных с депривационной амблиопией может говорить о вероятном применении мелатонина при лечении пациентов с амблиопией. Фармакотерапевтическое лечение амблиопии широко обсуждается среди офтальмологов, занимающихся лечением амблиопии. Если нейропротекторные препараты, имеющие ноотропный эффект, применяются достаточно часто и их назначение обосновано коллегами из России и из-за рубежа, то применение «естественных метаболитов биохимических процессов» редко встречается в литературе, тогда как мелатонин является регулятором метаболических процессов в организме [11; 12]. В настоящее время ни в российской, ни в зарубежной литературе данных об участии мелатонина как фактора патогенеза нами не найдено, но, судя по полученным в исследовании данным, гипотеза о его участии имеет право на существование и требует дальнейшего изучения данного вопроса.
Вывод. Уровень мелатонина в структурах глазного яблока при обскурационной амблиопии у кроликов ниже, чем в структурах здорового глазного яблока, что свидетельствует об участии мелатонина в патогенезе обскурационной амблиопии.
Библиографическая ссылка
Чупров А.Д., Воронина А.Е. ЭКСПЕРИМЕНТАЛЬНОЕ ОБОСНОВАНИЕ УЧАСТИЯ МЕЛАТОНИНА В ПАТОГЕНЕЗЕ ОБСКУРАЦИОННОЙ АМБЛИОПИИ У КРОЛИКОВ // Современные проблемы науки и образования. 2022. № 6-1. ;URL: https://science-education.ru/ru/article/view?id=32265 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/spno.32265



