Синдром Протея – одна из форм парциального гигантизма, впервые описанная в 1979 г. Cohen&Hayden [1, 2]. Синдром проявляется в мозаичном увеличении отдельных частей тела и связан с аномалией развития эмбриона в постзиготой стадии. Он связан с мутацией гена протеинкиназы AKT1 (164730), располагающегося в 14q32.33 хромосоме, и проявляется клинически в редком мозаичном нарушении роста [3, 4].
В зарубежной литературе его также относят к синдрому опухоли гамартомы (гомологичной фосфатазе и тензину) – the phosphatase and tensin homolog (PTEN) hamartoma tumor syndrome (PHTS). Синдром представляет собой набор заболеваний, возникающих в результате мутаций в гене-супрессоре опухоли PTEN [5, 6]. Он характеризуется вариабельной экспрессией и аномальной пролиферацией во многих системах организма [7, 8]. Клиническими его проявлениями могут быть липомы, разрастания конечностей, дерматологические поражения и злокачественные новообразования [9–11]. Диагностика и лечение различных подтипов PHTS затруднены в связи с редкой встречаемостью заболевания [2]. В мире насчитается около 200 известных случаев данного заболевания (частота встречаемости менее 1 случая на 1 млн населения). В группу заболеваний, объединенных названием «PHTS-синдром», входят синдром Каудена (CS), синдром Баннаяна–Райли–Рувалькабы (BRRS), связанный с PTEN синдром Протея (PS), и связанный с PTEN Протее-подобный синдром [12].
С целью установки диагноза у пациентов проводится клиническое обследование на основании критериев, выделенных D. Nguyen в 2004 г. [13].
В зарубежной и отечественной литературе публикации по данному заболеванию включают в себя преимущественно описание клинических случаев синдрома Протея в детской практике [14, 15].
Цель исследования – продемонстрировать клинический случай проявления синдрома Протея у взрослого пациента с гигантизмом верхней конечности и тактику его лечения в травматолого-ортопедической практике.
Материалы и методы исследования. Во время выездной консультации специалистов ФГБУ НИИТО им Я.Л. Цивьяна в Сахалинскую область в 2017 г. на консультативный прием обратился пациент с пороком развития правой кисти, парциальным гигантизмом правой верхней конечности. Было рекомендовано оперативное лечение после консультации онколога с заключением о возможности выполнения хирургического лечения в условиях травматолого-ортопедического отделения и об отсутствии признаков злокачественного образования, требующего специализированного онкологического медицинского пособия. Из анамнеза: изменения возникли в детском возрасте, длительное время проходил в различных стационарах и клиниках диагностику, определялись с тактикой лечения. На момент обращения удовлетворимого решения лечения не было.
Пациент поступил в травматолого-ортопедическое отделение № 3 Новосибирского НИИТО им. Я.Л. Цивьяна в ноябре 2020 г. На момент госпитализации пациент М., 35 лет, предъявлял жалобы на порок развития правой кисти, радиальную девиацию пятого пальца, увеличение объема пятого пальца, порочное положение V пальца с ограничением функции кисти. Дополнительно выявлены объемные образования по локтевой поверхности кисти, лучезапястного и локтевого суставов, объемные мягкотканные подкожные образования области правого предплечья, эпизоды онемения по ходу локтевого нерва (рис. 1).

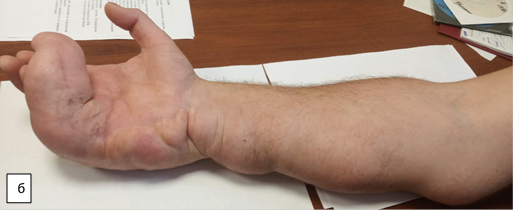
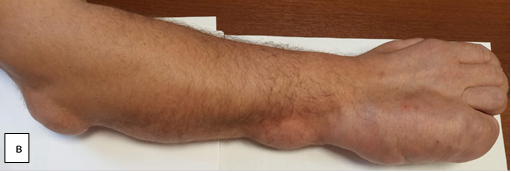
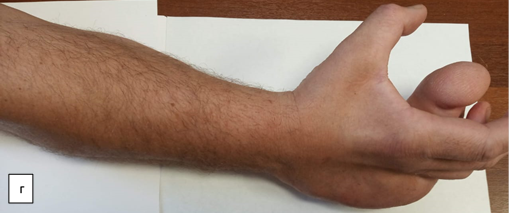
Рис. 1. Фотографии правой верхней конечности пациента до оперативного вмешательства: а – ладонная поверхность; б – локтевая поверхность; в – тыльная поверхность; г – лучевая поверхность (описание в тексте)
При клиническом исследовании был установлен гигантизм пятого луча кисти. Объем движений по Марксу в лучезапястном суставе (ЛЗС), пястно-фаланговых суставах (ПФС) и межфаланговых суставах (МФС) I–III пальцев в полном объеме. Объем движений в ПФС V пальца: разгибание/сгибание 0-0-30, приведение/отведение 4-0-4; в проксимальном МФС V пальца разгибание/сгибание 0-0-10; в дистальном МФС V пальца разгибание/сгибание 0-0-0. Объем движений в ПФС IV пальца: разгибание/сгибание 0-0-60, приведение/отведение 8-0-8, в проксимальном МФС IV пальца: разгибание/сгибание 0-0-80, в дистальном межфаланговом суставе IV пальца: разгибание/сгибание 2-0-70. При этом объем движений в суставах IV пальца был преимущественно уменьшен за счет натяжения кожных покровов и сформированного тяжа по ладонной поверхности от области основания V пальца.
При пальпации отмечались подкожные сдвигаемые мягкотканные образования округлой формы в диаметре до 5–8 см в области дорсальной поверхности локтевого сустава, предплечья и мягкотканное утолщение по локтевой поверхности лучезапястного сустава и кисти за счет подкожно-жировой клетчатки. Мышечная сила в верхней конечности снижена не была. Кровоснабжение и чувствительность на момент осмотра в руке нарушены не были.
Из обязательных общих критериев, выделенных D. Nguyen, у пациента были выявлены мозаичность поражения, прогрессирующее течение, спорадичность случая. Из специфических критериев был выявлен один критерий группы В, а именно диспропорциональная гипертрофия одной конечности. Из специфических критериев группы С была выявлена дисрегуляция жировой ткани в виде липом.
Пациенту выполнялось рентгенологическое исследование правой верхней конечности: области кисти, ЛЗС, локтевого сустава в двух проекциях и оси конечности. Были установлены анкилоз межфаланговых суставов V пальца правой кисти с формированием единого костного блока, сформированного под углом, открытым в лучевую сторону, бугристая деформация и гиперплазия трехгранной, крючковидной и гороховидной костей, пятой пястной кости, фаланг V пальца правой кисти. Проекционная гипертрофия мягких тканей правого предплечья и кисти показана на рисунке 2.
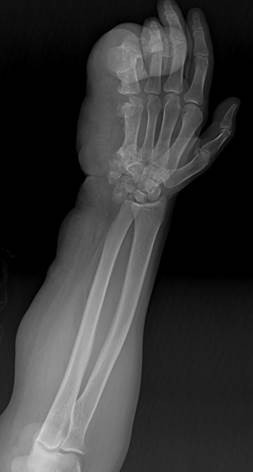
Рис. 2. Рентгенография правой верхней конечности пациента в прямой проекции, предоперационный снимок (описание в тексте)
С учетом сложной многоплоскостной деформации верхней конечности было принято решение о выполнении мультиспиральной компьютерной томографии (МСКТ) с контрастированием основных сосудистых магистралей и ядерной магнитно-резонансной томографии (яМРТ).
На момент исследования нарушений кровоснабжения сосудистого русла локтевой и лучевой артерий правой верхней конечности при МСКТ-ангиографии установлено не было (рис. 3).
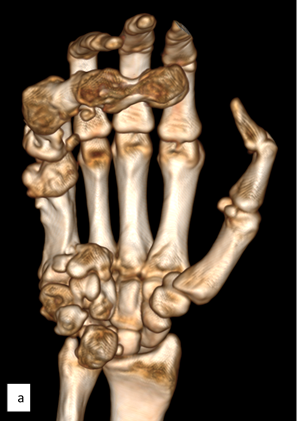

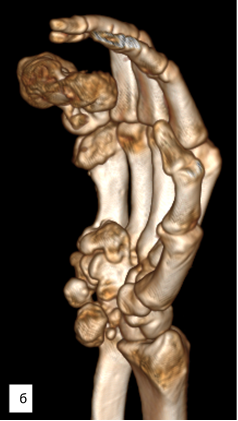
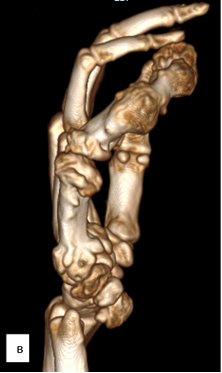
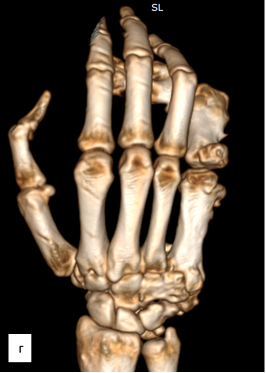
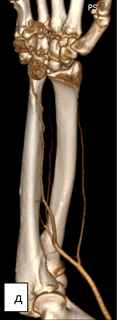
Рис. 3. МСКТ-исследование правой кисти: а – ладонная поверхность; б – лучевая поверхность; в – локтевая поверхность; г – тыльная поверхность; д – артериография магистральных сосудов (описание в тексте)
На яМРТ-исследовании кисти определялись бугристая гипертрофическая деформация локтевых сегментов трехгранной, гороховидной и крючковидной костей правого запястья, пятой пястной кости, фаланг V пальца (регионарный гигантизм пятого луча кисти); анкилоз проксимального и дистального межфаланговых суставов V пальца кисти, угловая деформация костного межфалангового блока V пальца кисти, гипертрофия подкожно-жировой клетчатки локтевого отдела кисти и V пальца; дефект локтевого сегмента головки пятой пястной кости; вторичный артрозо-артрит пятого пястно-фалангового сустава кисти; миозит ладонных и тыльных межкостных мышц правой кисти (рис. 4).
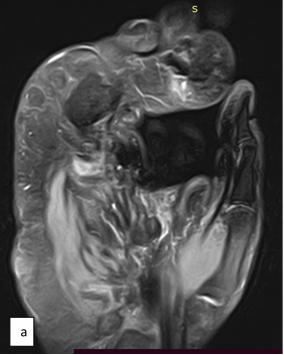
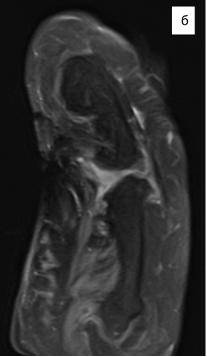
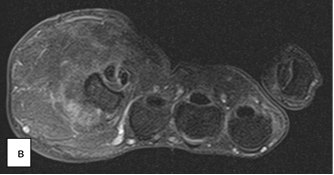
Рис. 4. МРТ-исследование правой кисти: а – фронтальная проекция; б – сагиттальная проекция; в – аксиальная проекция (описание в тексте)
На яМРТ-исследовании предплечья определялась регионарная гипертрофия подкожно-жировой клетчатки дорсо-локтевой областей правого предплечья и правого локтевого сустава (рис. 5).
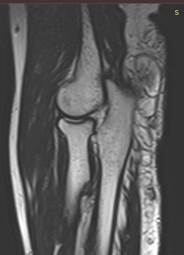
Рис. 5. МРТ-исследование правого локтевого сустава и проксимальной трети предплечья, сагиттальная проекция (описание в тексте)
Для исключения вероятного более проксимального распространения аномалии развития выполнялось яМРТ-исследование плечевой области. Были установлены признаки тендинита сухожилия надостной мышцы правого плечевого сустава, субкоракоидальный, субдельтовидный бурсит, умеренный теносиновит длинной головки бицепса. Признаков гигантизма подкожно-жировой клетчатки, в частности этой области, установлено не было.
Пациенту было предложено реконструктивно-пластическое хирургическое вмешательство:
а) субтотальное иссечение гипертрофированной подкожно-жировой клетчатки в пределах поля зрения на уровне предплечья;
б) мобилизация локтевого сосудисто-нервного пучка вдоль правого предплечья, кисти;
в) освобождение мышц гипотенора, локтевого сосудисто-нервного пучка и пальцевого сосудисто-нервного пучка V пальца от объемных образований;
г) корригирующая остеотомия костного блока на вершине деформации V пальца кисти в проекции проксимального МФС с выведением пальца в физиологическое положение;
д) продольная резекция дистальной и средней фаланг V пальца после релиза мягких тканей с целью уменьшения ширины костной ткани;
е) остеосинтез фрагментов V пальца правой кисти при помощи биодеградируемого пина, проведенного в разных плоскостях.
В конце оперативного вмешательства по ходу операционных разрезов были установлены резиновые выпускники. Выполнялась иммобилизация в условиях гипсовой лонгеты лучезапястного сустава и V пальца правой кисти (рис. 6). Затем пациент в удовлетворительном состоянии был выписан для дальнейшего амбулаторного наблюдения по месту жительства. Через 2 недели пациент повторно был госпитализирован в Новосибирский НИИТО в связи с развившимся инфицированным некрозом кожи и подкожно-жировой клетчатки области хирургического шва V пальца правой кисти. Пациент предъявлял жалобы на онемение и почернение дистальной фаланги V пальца кисти, инфекционное отделяемое, геморрагическое отделяемое по установленному в локтевой сустав дренажу около 20 мл в сутки.
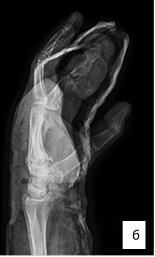
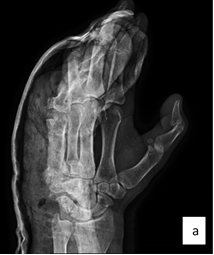
Рис. 6. Рентгенография правой кисти пациента, послеоперационный контроль: а – прямая проекция; б – боковая проекция (описание в тексте)
Клинически был выявлен участок некроза области дистальной фаланги V пальца кисти, шов в области предплечья зажил на всем протяжении первичным натяжением. Принято решение о выполнении некрэктомии области шва V пальца. В послеоперационном периоде потребовались регулярные санационные перевязки на фоне антибиотикотерапии препаратом широкого действия Ципрофлоксацин. Полноценное закрытие раны грануляционными тканями произошло за 9 дней. Пациент в удовлетворительном состоянии был выписан для дальнейшего амбулаторного наблюдения по месту жительства.
В рекомендациях пациенту даны указания: во-первых, о сопутствующем высоком риске развития злокачественных образований других локализаций и потребности в наблюдении онкологом по месту жительства; во-вторых, о возможности выполнения молекулярно-генетического исследования.
Результаты исследования и их обсуждение. Во время оперативного вмешательства было установлено, что на предплечье макроскопически подкожно-жировая клетчатка была не изолирована, а фиброзно припаяна к окружающим мягким тканям, распространялась в дистальном направлении на предплечье до уровня лучезапястного сустава с переходом на лучезапястный сустав, локтевой отдел кисти и на V палец, в проксимальном направлении – до уровня локтевого сустава.
В структуре гипертрофированной подкожно-жировой клетчатки были выявлены более плотные фиброзные перемычки, обусловившие значительные технические трудности при определении границ здоровых и патологических тканей, сосудисто-нервных образований.
Помимо гипертрофии мягкотканных структур, отмечались гипертрофия и деформация костей с образованием анкилозов межфаланговых суставов V пальца правой кисти. В послеоперационном периоде наблюдалось вторичное расхождение швов, потребовавшее повторного вмешательства, удаления гематомы, некрэктомии вдоль V пальца правой кисти, наложения повторных швов.
Субъективная оценка пациентом проведенного лечения: в первые 6 месяцев состояние правой кисти доставляло пациенту неудобство и психологический дискомфорт. Причиной дискомфорта являлся стереотип поведения кисти. Через год пациент стал отмечать большую возможность активного функционирования кисти. По прошествии более года с момента операции пациент отмечает улучшение социально-бытовых навыков, точности выполнения мелкой моторики кистью (рис. 7).
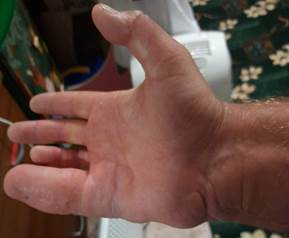
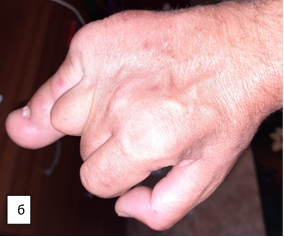
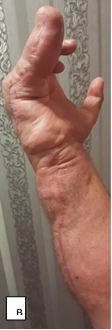
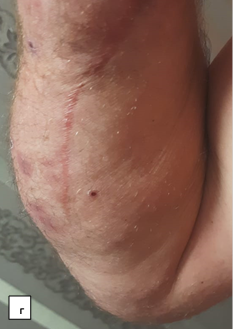
Рис. 7. Фотографии правой верхней конечности пациента после оперативного вмешательства: а – ладонная поверхность; б – тыльная поверхность; в – локтевая поверхность кисти; г – локтевая поверхность предплечья
По данным гистологического исследования, в интраоперационном биопсийном материале, окрашенном гематоксилин-эозином, были выявлены фрагменты зрелой жировой и фиброзной ткани с толстостенными сосудами. Морфологическая картина соответствовала липофиброме.
Следует обратить особое внимание на то, что у пациентов с данным синдромом установлен повышенный риск развития злокачественных новообразований различных локализаций, помимо гипертрофированной конечности. В связи с этим необходимы онкологическая настороженность и соответствующий диспансерный учет.
Дифференциальный диагноз включает в себя множество вариантов патологических изменений жировой ткани: липома, липофиброматоз, липофибросаркома и др. Корректная постановка диагноза требует использования большого числа диагностических процедур, таких как МСКТ, МРТ, гистологическое исследование, молекулярно-генетическое типирование. В связи с грубым разрастанием фиброзно-рубцовых перемычек внутри патологически гипертрофированной жировой ткани обязательным аспектом предоперационного обследования должно стать исследование сосудистого русла.
Заключение. Уникальность и редкость синдрома Протея требуют выполнения широкого спектра диагностических процедур. Для достижения удовлетворительного результата необходимо многоэтапное хирургическое лечение. В послеоперационном периоде важную роль играют реабилитация и психологическая адаптация взрослого человека. С точки зрения динамического наблюдения амбулаторно необходимо следить за органами-мишенями.
Библиографическая ссылка
Александров Т.И., Прохоренко В.М., Чорний С.И., Симонова Е.Н. ЛЕЧЕНИЕ ПАЦИЕНТА С ЛОКАЛЬНЫМ ГИГАНТИЗМОМ ВЕРХНЕЙ КОНЕЧНОСТИ: СИНДРОМ ПРОТЕЯ (СЛУЧАЙ ИЗ ПРАКТИКИ) // Современные проблемы науки и образования. 2022. № 6-1. ;URL: https://science-education.ru/ru/article/view?id=32228 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/spno.32228



