Цветовое зрение – один из типов зрительного ощущения, сенсорное восприятие светового излучения, исходящего от источника света или отраженного от объекта, с чувством восприятия цвета, определяемого длиной волны.
Цель обзора – проанализировать основные теории цветовосприятия с учетом современного понимания строения фоторецепторного аппарата сетчатки глаза для возможной дальнейшей разработки основных принципов лечения офтальмологической патологии, включая повышение эффективности фармакологического действия офтальмологических лекарственных препаратов.
Фундаментальные теории цветовосприятия
Существует большое разнообразие теорий, но применяются четыре основополагающие теории формирования цветового зрения:
1. Теория Томаса Юнга (1802 г.): на сетчатке определяются три независимых механизма цветового зрения (три группы нервных волокон) в зависимости от длины волны. [1–3] (таблица).
Фоторецепторы с соответствующей длиной волны
|
Фоторецептор |
Пигмент |
Диапазон, нм |
Пиковая длина волны, нм |
|
S (фиолетово-синий) |
Цианолаб (не обнаружен) |
400–500 |
420–440 |
|
M (желто-зеленый) |
хлоролаб |
450–630 |
534–545 |
|
L (красно-желтый) |
эритролаб |
500–700 |
564–580 |
2. Теория Гельмгольца (1853 г.): строение сетчатки подразумевает наличие трех видов колбочек с пределом чувствительности на три основных спектра: красный, зелёный и синий. Недоказательным является устройство обработки сигналов, восприятие контрастности изображения и анатомического строения цветовоспринимающей системы глаза. В случае если бы в глазу человека существовало бы три типа колбочек, то всякий тип колбочек обязан находиться на «собственной дистанции» от хрусталика. Данный факт обязан подтверждаться гистологическими исследованиями, кроме того, все колбочки схожи и находятся на внутренней поверхности сферы, образованной оболочками глазного яблока.
3. Теория Эвальда Геринга (1870 г.) — оппонентная гипотеза цветового зрения: определенная пара рецепторов (красно-зеленые, желто-голубые и черно-белые) восприимчива к свету волн разной длины, но в наибольшей степени чувствительна к волнам конкретной длины [3–5].
4. Нелинейная теория С. Ременко (1975 г.): состоит из двух основных постулатов:
- в структуре сетчатки глаза есть два вида световоспринимающих элементов: однотипные палочки и колбочки, которые включают в себя восприятие сразу к нескольким областям спектра;
- нелинейность процессов формирования сигналов цветности [6].
Каждый цвет, воспринимаемый нашим глазом, это разноволновые колебания, отраженные от объекта. Чтобы получить отдельный монохроматический цвет, преломление света осуществляется через призму, происходит отделение каждого цвета с последующим формированием соответствующей длины волны (рис. 1, цит. по W.B. Marks, W.H. Dobelle, E.F. MacNichol).
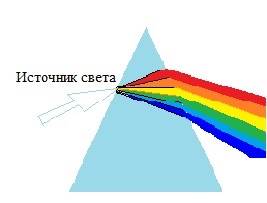
Рис. 1. Преломление света через призму
Хрусталик глаза – анатомическая линза, состоящая из двух призм, расположенных основаниями друг к другу. Можно отметить значимый «недостаток» хрусталика глаза – хроматическую аберрацию. Для формирования резкого изображения на сетчатку должны попасть лучи из середины видимого спектра. При этом красные лучи собираются в точке за фокусной поверхностью, а синие лучи – перед ней. Таким образом, хроматическая аберрация – это процесс фокусировки, обусловленный длиной волны света [7]. С учетом хроматической аберрации оправдано присутствие на сетчатке двух разных групп фоторецепторов (палочки и колбочки). В процессе преломления света при размещении фоторецепторов за хрусталиком (призмой) распределение лучей происходит на определенную зону каждой группы фоторецепторов. В случае продольного расположения приёмника необходимо присутствие пигментов, которые усиливают поглощение. Такими пигментами являются хлоролаб (задерживает зеленые лучи, пропускает красные лучи) и эритролаб (поглощает красные лучи) (рис. 2, цит. по W.B. Marks, W.H. Dobelle, E.F. MacNichol).
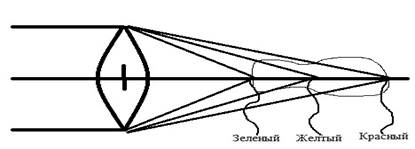
Рис. 2. Светопреломление хрусталика глаза
Для представления модели цветовосприятия, основой которой является нелинейная теория С. Ременко, следует представить следующее: фильтрация света осуществляется оптически прозрачными средами глаза: роговица, хрусталик и стекловидное тело. Основной поток ультрафиолетовых лучей задерживается хрусталиком и роговицей, а инфракрасных лучей – стекловидным телом. Оставшиеся лучи из середины видимого спектра попадают на типовые фоторецепторы сетчатки – палочки и колбочки.
Локализация и строение палочек и колбочек уникальны. Палочки, ввиду своей большей длины и большей площади, способны к восприятию практически всей видимой части спектра. Учитывая «фильтрацию» света глазными средами, интенсивность света и наличие светочувствительного родопсина, максимальная чувствительность палочек приходится на сине-фиолетовый и зеленый. В свою очередь, на колбочки приходится максимальное восприятие желтого спектра, хотя они, как и палочки, воспринимают почти всю область спектра. Усиление поглощения колбочками осуществляется благодаря хлоролабу и эритролабу. Основные функции колбочки – это восприятие информации о яркости и о максимуме освещенности. Сигнал яркости связан с сигналом, получаемым непосредственно от палочки в нейроне. Далее происходит формирование сигнала цветности Y и общего яркостного сигнала Z. Сигнал максимума освещенности колбочки представляет собой второй сигнал цветности X. Благодаря передаче сигналов Y, Z, X по нейронным сетям к головному мозгу и сравнению с памятью происходит формирование ощущения цвета (рис. 3, цит. по W.B. Marks, W.H. Dobelle, E.F. MacNichol).
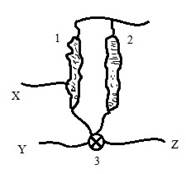
Рис. 3. Схема формирования яркости и цветности
На основе принципов нелинейной теории цветового зрения выстроена простая работающая фотоэлектрическая модель глаза, которая способна идентифицировать всевозможные цвета и оттенки (колориметр).
Двухкомпонентная нелинейная теория С. Ременко на сегодняшний день всецело отражает механизмы строения системы цветовосприятия глаза, но до сих пор не получила всеобщего признания ввиду отсутствия объяснения участия головного мозга в формировании цветового образа у человека.
Фоторецепторы на сетчатке имеют строго определенную пространственную конфигурацию в виде мозаики. В фовеа она состоит из гексагональной (шестигранной) упаковки колбочек. За границами фовеа шестигранная упаковка колбочек нарушается палочками, при этом архитектура системы палочка-колбочка сохранна: восемь или шесть палочек вокруг одной колбочки. Исходя из разных плотностей популяций фоторецепторов в сетчатке человека, становится понятно, что плотность колбочек высочайшая в ямке фовеа и снижается за пределами ямки до относительно ровной плотности в периферической зоне сетчатки глаза. Известно, что самая большая концентрация палочек в кольце вокруг ямки фовеа около 4,5 мм или 18 градусов. В данной области наблюдается шестиугольная симметрия: вокруг каждой колбочки располагается шесть палочек (рис. 4, цит. по C.A.Curcio, K.R Sloan, O. Packer, A.E. Hendrikson, R.E. Kalina). Слепое пятно свободно от фоторецепторов [5–8].
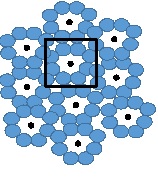
Рис. 4. Схематичное строение палочек и колбочек вокруг фовеа
Существует восьмиугольная симметрия на сетчатке глаза с угловым расстоянием 7‒8°, где одна колбочка окружена восемью палочками. Количество палочек достоверно больше и достаточно для формирования «окружения» каждой колбочки в центре (желтое пятно); при этом число палочек заметно уменьшается к периферии.
Современное представление фоторецепторного аппарата сетчатки глаза
Длительное время единственно достоверным являлся тот факт, что фоторецепторный аппарат глаза состоит из палочек и колбочек. В 2007 г. общепризнанным стало открытие 1991 г. фоторецепторов Intrinsically photosensitive retinal ganglion cells (ipRGC) – внутренних светочувствительных клеток сетчатки (составляют около 1 % светочувствительных клеток сетчатки). Пигмент, содержащийся в ipRGC – меланопсин, поэтому они получили название melanopsin-containing retinal ganglion cells (mRGC) [9]. В самых ранних исследованиях ipRGC были описаны как однородная популяция, участвующая исключительно в передаче световых сигналов, не связанных с формированием изображения. Данные фоторецепторы реагируют на свет при отсутствии реакции палочек и колбочек. В исследованиях доказано, что меланопсин экспрессируется в ганглиозных клетках грызунов и приматов. В сетчатке ipRGS обеспечивают возбуждение дофаминергических амакриновых клеток и связаны с ГАМКергическими амакриновыми клетками посредством щелевидных соединений. Обнаружено влияние ipRGC на работу биологических часов, сон, зрачковый световой рефлекс [10–12]. В отличие от палочек и колбочек, ipRGS реагируют на свет постоянно, но гораздо медленнее, информируя человека об интенсивности светового потока. К основным функциям ipRGC относятся:
1. Синхронизация циркадных ритмов посредством передачи сигнала через ретиногипоталамический тракт RHT (Retinohypothalamic tract). По аксонам ipRGC передача нервного импульса производится к комплексу структур головного мозга: супрахиазматическому ядру гипоталамуса через зрительный нерв и хиазму, оливарному претектальному ядру, дорсальному латеральному коленчатому телу. Супрахиазматическое ядро подаёт сигналы к стимуляции работы эпифиза (шишковидной железы) и выработке мелатонина [13, 14].
2. Регулирование величины «диафрагмы» глаза путем подачи нервного импульса к оливарному ядру предкрышечной области среднего мозга в ответ на изменяющиеся условия окружающего освещения.
3. Световая регуляция при резком ярком освещении (засветках) путем высвобождения мелатонина и затемнения излишнего светового излучения [15].
Возбуждение в клетках ipRGC происходит благодаря меланопсину, реагирующему на синюю часть видимого спектра, воспринимаемые пики которого находятся в пределах ~480 нм [16]. При этом механизм фототрансдукции человека не изучен достаточно, но, вероятно, напоминает механизм фототрансдукции беспозвоночных. Кроме прямой реакции на свет, эти клетки могут получать возбуждающее и тормозящее действие от палочек и колбочек с помощью синаптических связей клеток сетчатки [15, 17, 18].
Клинические исследования группы фоторецепторов ipRGC
В 2007 г. Zaidi с коллегами представили работу [15], в которой анализировали фототрансдукцию пациентов с нарушениями структуры палочек и колбочек, но сохранным ганглиозным слоем клеток сетчатки, и пришли к выводу, что вне зависимости от патологии палочек и колбочек у пациентов сохранялись циркадные поведенческие паттерны, высвобождение мелатонина и реакция зрачка на свет [19–21]. Обнаружено влияние возбуждения ipRGC при головной боли во время приступов мигрени [22–24].
В последнее время доступно всё больше зарубежных исследований, связанных с влиянием различных офтальмологических заболеваний на ipRGC. Одно из таких исследований опубликовал B. Feigl с коллегами. Целью исследования было оценить влияние глаукомы на внутренние светочувствительные клетки сетчатки. Обследован 41 пациент, из этого числа 25 чел. страдали глаукомой и 16 чел. составляли здоровую контрольную группу. Оценку функций проводили с помощью реакции зрачков благодаря инфракрасной пупиллометрии в ответ на воздействие света с разной длиной волны. Выполнены 7- и 10-секундные вспышки коротковолновых (488 нм – синий спектр) и длинноволновых (610 нм – красный спектр) стимулов. Проанализированы исходный диаметр зрачка, амплитуда зрачковой реакции (в процентах от исходного диаметра зрачка) и скорость реакции зрачка на синий и красный спектр у пациентов с начальной, развитой и далеко зашедшей глаукомой в сравнении с контрольной группой пациентов. По результатам исследования на синий спектр показатели инфракрасной пупиллометрии у пациентов с развитой и далеко зашедшей стадиями глаукомы были значительно ниже, чем у контрольной группы. Причем у пациентов с далеко зашедшей глаукомой по сравнению с начальной стадией глаукомы показатели были самыми низкими. Скорость реакции зрачка на красный и синий спектр существенно не отличалась. Параметры контрольной группы и группы с начальной стадией глаукомы существенно не отличались по каким-либо параметрам. Авторы пришли к заключению, что у лиц с развитой и далеко зашедшей стадиями глаукомы имеется дисфункция ipRGC, которую можно контролировать с помощью инфракрасной пупиллометрии и считать клиническим индикатором прогрессии глаукомы [24].
В исследовании A. Martínez-Águila и коллег обнаружено влияние циркадного ритма на разнообразную патологию органа зрения. Основные действующие молекулы меланопсин и мелатонин принимают участие в гомеостазе. В экспериментальных моделях и клинических исследованиях выявили влияние данных молекул на синдром сухого глаза, язвенные процессы роговицы, катаракту, миопию, заболевания сетчатки и глаукому. В частности, одним из последних исследований была оценка влияния циркадного ритма и выработки мелатонина при глаукоме. Мелатонин оказывает влияние на образование внутриглазной жидкости и отток через трабекулярную сеть в зависимости от времени суток. По результатам исследования сделан вывод, что лечение различной глазной патологии, в том числе и глаукомы, можно улучшить при анализе действия лекарственного вещества с учетом циркадного ритма человека. Мелатонин и его аналоги рекомендуется рассматривать как потенциальные препараты для снижения ВГД. Кроме того, при создании новых лекарственных препаратов следует использовать мелатонин как коадъюдант, обладающий антиоксидантными и антиангиогенными свойствами, а также улучшающий циркадный ритм [22, 25].
Заключение
С учетом знания полного и детального анатомического строения структур глаза, а именно сетчатки, возможно повысить эффективность лечения различной офтальмологической патологии. Благодаря изучению влияния циркадного ритма, биохимических реакций мелатонина можно достичь наибольшего фармакологического действия лекарственных препаратов в отношении некоторых заболеваний, например глаукомы.
Библиографическая ссылка
Чупров А.Д., Синькова В.И., Кузнецов И.В. ТЕОРИИ ЦВЕТОВОСПРИЯТИЯ. ФОТОРЕЦЕПТОРНЫЙ АППАРАТ СЕТЧАТКИ ГЛАЗА // Современные проблемы науки и образования. 2021. № 6. ;URL: https://science-education.ru/ru/article/view?id=31287 (дата обращения: 23.05.2026).
DOI: https://doi.org/10.17513/spno.31287



