Рак молочной̆ железы (РМЖ) [1] является основной причиной смертности (более 17%) и онкологической патологии (более 20%) женщин среди злокачественных заболеваний [2]. При этом данные показатели неуклонно растут [3]. В России РМЖ ежегодно ставят 54тысячам женщин. Число новых случаев в 2020 году составило 19,3 млн, и 10 млн – летальных исходов. Уровень заболеваемости РМЖ в России в 2019 году составил 91,2 на 100 тысяч женщин [4]. А в 2018 году показатель был 89,8 – на 100 тысяч женского населения [5]. То есть мы видим небольшой постепенный рост заболеваемости. В Самарской области в 2019 г. заболеваемость злокачественными новообразованиями составила 526,9 на 100 тыс. населения. В структуре общей онкологической заболеваемости преобладают новообразования кожи (17,6%), РМЖ (11,5%) и рак лёгких (8,1%). В показателях заболеваемости женщин превалируют опухоли кожи (21,5%), РМЖ (20,5%) и рак тела матки (7,4%). РМЖ в перечне общей заболеваемости занимает второе место (12,3–13,8%) [6]. Важно отметить, что рост увеличивается только среди женщин, чей возраст свыше 45 лет, среди молодого населения рост не отмечается. Данная статистика подчёркивает важность исследования методов диагностики и лечения РМЖ.
Причина возникновения РМЖ остаётся не до конца изученной, но существуют факторы риска, которые увеличивают риск развития данного заболевания [7]. На данный момент аспекты первичной профилактики являются первоочередными в международной практике борьбы с раком [8].
Лучевая диагностика РМЖ проводится с помощью маммографии, ультразвукового исследования (УЗИ), магнитно-резонансной томографии (МРТ) и позитронно-эмиссионной томографии (ПЭТ). УЗИ молочных желёз – доступный и экономически выгодный скрининговый метод выявления РМЖ, но менее эффективен по сравнению с маммографией. УЗИ рекомендовано в качестве дополнения к маммографии для пациенток с высоким риском РМЖ, беременных женщин и лиц, которым противопоказана маммография. Но при ультразвуковом исследовании акустические признаки нормальной ткани и объёмных образований молочных желёз схожи. Более того, УЗИ операторозависимый метод, поэтому должно выполняться опытным специалистом, что существенно влияет на чувствительность и специфичность исследования. МРТ позволяет получить полипроекционные изображения с возможностью использования контрастного вещества. МРТ молочной железы выполняется пациентам с высоким риском РМЖ, но не рекомендована для популяции в целом из-за значительного уровня ложноположительных результатов, высокой стоимости, длительности процедуры, отсутствия достаточного количества аппаратуры, опытных специалистов и клинической применимости. По сравнению с маммографией и УЗИ, МРТ менее специфичен, но более чувствителен к обнаружению небольших опухолей у женщин с высоким риском РМЖ. ПЭТ - наиболее точный метод визуализации распространения опухолей или их реакции на терапию, позволяет получить полипроекционные исследования, но является длительным дорогостоящим методом исследования. Основным методом ранней диагностики РМЖ остаётся маммография [9; 10].
Цель исследования – изучение особенностей ранней комплексной клинической, маммографической и гистологической диагностики рака молочной железы.
Материал и методы исследования
Проведено ретроспективное исследование 100 пациенток Самарского областного клинического онкологического диспансера (СОКОД) за 2019-2020 годы. Критериями включения являлись проведение маммографии более чем 12 месяцев назад и отсутствие диагностированного рака груди. Предпочтение отдавалось пациенткам, которые проходили процедуру маммографии впервые. Критерии исключения: беременность и период лактации.
Всем женщинам было проведено анкетирование, включающее следующие разделы: общую информацию, вопросы по качеству жизни, по пищевому и акушерско-гинекологическому статусу исследованных. Пациенткам была выполнена скрининговая маммография в двух проекциях на цифровом маммографе Sonographer 2000 D. Результаты исследования оценивались по категориям BI-RADS [11] и гистологическому исследованию.
Результаты исследования и их обсуждение
Возраст обследованных женщин составил 35-60 лет (средний возраст 48,5 ± 5,4 года). В результате исследования наиболее распространённой возрастной группой, которая обратилась за консультацией, являются пациентки в возрасте от 45 до 49 лет, что соответствует мировой статистике [12].
После анализа маммограмм по классификации BIRADS было выявлено 12% и 6% (рис. 1) пациенток с результатами обследования, соответствующими 4 и 5 категориям (соответственно).
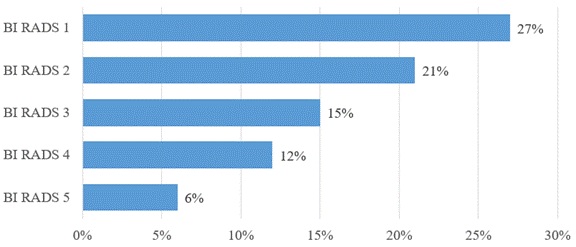
Рис. 1. Распределение исследований пациенток по шкале BI RADS
Выявлены 48% обследуемых c результатами в пределах нормы и 15% пациенток с ранней стадией рака молочной железы (рис. 2). Обследуемым с РМЖ ранней стадии проведена пункция образований под рентгеновским контролем [13]. При цитологическом исследовании полученного материала злокачественных клеток у данных обследуемых не было выявлено. Пациентки были госпитализированы в отделение опухолей наружной локализации СОКОД на оперативное лечение. Результаты гистологического исследования удалённых тканей: фиброзно-кистозная болезнь (2% пациенток, n=2) и инвазивный рак молочной железы ранней стадии (13% пациенток, n=13).
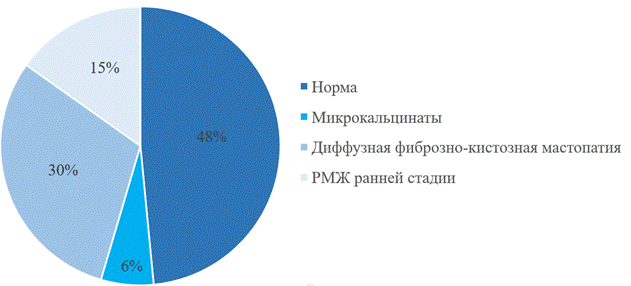
Рис. 2. Распределение исследований пациенток по данным маммографии
Маммограммы пациенток были разделены на три группы. Группу I составили изображения пациенток с нормальной структурой молочной железы, II – с фиброзно-кистозной мастопатией, III – с раком молочной железы. Для определения различий между исследуемыми группами выполнен многомерный дискриминантный анализ на основании результатов гистологического исследования образований молочной железы. Критериями адекватности дискриминантной модели являлись l Уилкса и степень достоверности полученного F-критерия. Полученная дискриминантная модель содержит семь переменных и характеризуется низкой l Уилкса (0,18), высоким уровнем F-критериев при достаточной толерантности (табл. 1), что свидетельствует об оптимальном определении принадлежности пациента.
Данное многомерное пространство признаков позволяет оценить дифференциальную способность полученной математической модели на основе квадратов расстояний Махаланобиса (рис. 3). Расстояние между центроидами групп максимально для классификации пары «ММГ с нормальной структурой» и «рак молочной железы» (12,63) и минимально для пары «ММГ с нормальной структурой» и «ММГ с фиброзно-кистозной мастопатией» (4,52).
Распределение канонических переменных на рисунке 4 свидетельствует о хорошей дискриминации между исследуемыми группами.
Таблица 1
Характеристика дискриминантной модели признаков пациентов
|
Общая lУилкса модели 0,18378 |
||||||
|
Переменные |
lУилкса |
Частная lУилкса |
F-исключения |
p (F) |
Толерантность |
R2 |
|
Толщина кожи |
0,19 |
0,94 |
1,48 |
0,24 |
0,73 |
0,27 |
|
ACR |
0,19 |
0,95 |
1,36 |
0,26 |
0,56 |
0,44 |
|
Размер образования |
0,25 |
0,86 |
4,29 |
0,02 |
0,49 |
0,51 |
|
Локализация образования |
0,22 |
0,90 |
2,57 |
0,09 |
0,51 |
0,49 |
|
Контуры образования |
0,22 |
0,86 |
3,73 |
0,03 |
0,41 |
0,59 |
|
Характер распределения кальцинатов |
0,21 |
0,84 |
5,22 |
0,01 |
0,77 |
0,23 |
|
Размер кальцинатов |
0,23 |
0,78 |
7,58 |
0,01 |
0,49 |
0,51 |
|
Характер распределения кальцинатов |
0,24 |
0,8 |
6,23 |
0,01 |
0,38 |
0,62 |
|
Форма кальцинатов |
0,23 |
0,82 |
5,93 |
0,01 |
0,51 |
0,49 |
|
Лимфоаденопатия |
0,22 |
0,9 |
2,57 |
0,08 |
0,79 |
0,21 |
|
Категория BI RADS |
0,21 |
0,83 |
5,26 |
0,01 |
0,55 |
0,45 |
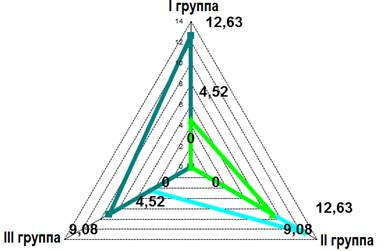
Рис. 3. Квадраты расстояний Махаланобиса между центроидами групп в многомерном пространстве признаков.
Ось абсцисс – пары групп; ось ординат – расстояния Махаланобиса
Прикладное значение разработанной дискриминантной модели отражено в таблице 2, где представлены результаты классификации пациентов на группы. Анализ работы модели показал, что максимальная эффективность классификации получена для групп «ММГ с нормальной структурой», где доля истинно положительных значений составила 87,8%, и «рак молочной железы», при котором дискриминантная модель не имела ложных интерпретаций.
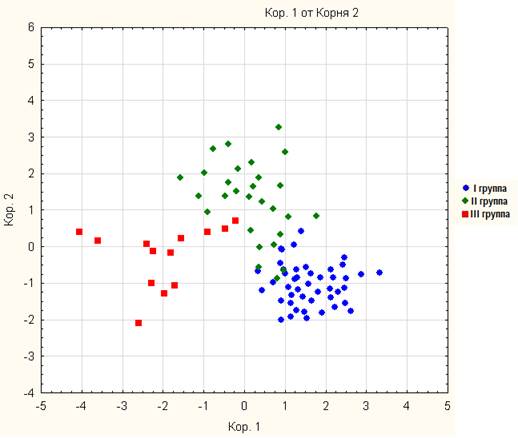
Рис. 4. Диаграмма рассеивания канонических значений в пространстве признаков дискриминантной модели
Таблица 2
Оценка эффективности дискриминантной модели
|
|
Процент - правиль. |
Норма |
РМЖ |
Фиброзно-кистозная мастопатия |
|
Норма |
87,8 |
40 |
0 |
5 |
|
РМЖ |
100 |
0 |
13 |
0 |
|
Фиброзно-кистозная мастопатия |
65,52 |
8 |
2 |
32 |
|
Всего |
84,54 |
48 |
15 |
37 |
Применение дискриминантной модели позволяет с высокой точностью распознать РМЖ с помощью маммографии.
Полученные данные иллюстрируют следующие клинические примеры.
Клинический случай 1 (рис. 5) пациентки Л., 42 лет. На маммограммах левой молочной железы, выполненных в двух проекциях, в верхне-наружном квадранте определяется одиночное неправильной овальной формы образование, размерами 17х21х24 мм, средней интенсивности, с нечёткими неровными контурами. Заключение: фиброаденома левой молочной железы. Фиброзно-кистозная мастопатия. BI RADS слева – 3. Гистологическое заключение: фиброаденома левой молочной железы. Фиброзно-кистозная мастопатия.
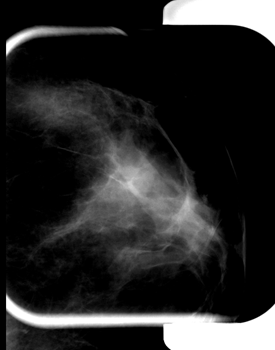
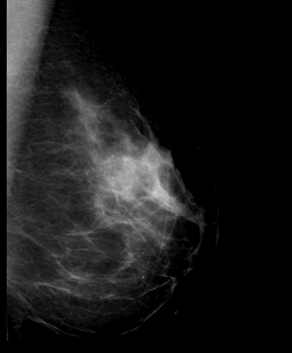
А Б
Рис. 5. Маммограммы левой молочной железы (в двух проекциях) пациентки Л., 42 лет. Фиброаденома левой молочной железы: А – прицельное исследование в краниокаудальной проекции, Б – медиолатеральная проекция
Клинический случай 2 (рис. 6) пациентки М., 41 года, с впервые выявленным раком правой молочной железы. На маммограммах правой молочной железы в двух проекциях в нижне-внутреннем квадранте определяется утолщение кожи, одиночное неправильной округлой формы образование, до 25 мм в диаметре, высокой интенсивности, с нечёткими неровными лучистыми контурами, неоднородной структуры за счёт включения сгруппированных микрокальцинатов. В правой аксиллярной области определяются единичные лимфатические узлы размерами до 20 мм с неизменённой структурой. Заключение: рак правой молочной железы. Фиброзно-кистозная мастопатия с преобладанием фиброзного компонента. BIRADS справа – 4с. Гистологическое заключение: инвазивная карцинома правой молочной железы.
По завершении анализа полученных данных мы получили следующие результаты:
1) наиболее распространённой возрастной группой, которая обратилась за консультацией, являются пациентки в возрасте от 45 до 49 лет (29%);
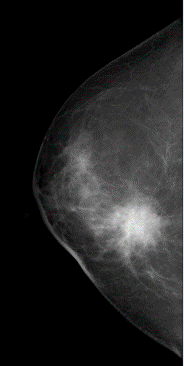
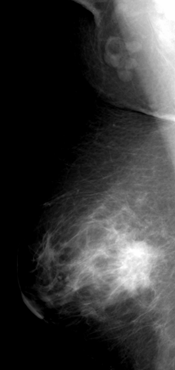
А Б
Рис. 6. Маммограммы левой молочной железы пациентки М., 41 года. Инвазивная карцинома правой молочной железы: А – краниокаудальная проекция, Б – медиолатеральная проекция
2) BIRADS1 при скрининговой маммографии преобладает (27% пациенток), BIRADS4 и BIRADS5 выявлены у 12% и 6% обследованных соответственно;
3) у 13% обследованных пациенток был выявлен рак молочной железы ранней стадии.
Заключение
Таким образом, в результате проведенного многомерного анализа получены данные об эффективности комплексной клинической и маммографической диагностики для раннего выявления рака молочной железы.
Библиографическая ссылка
Цимбалист Е.Д., Пышкина Ю.С. ОЦЕНКА ЭФФЕКТИВНОСТИ ДИАГНОСТИЧЕСКИХ ПРИЗНАКОВ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ // Современные проблемы науки и образования. 2021. № 5. ;URL: https://science-education.ru/ru/article/view?id=31192 (дата обращения: 18.05.2026).
DOI: https://doi.org/10.17513/spno.31192



