До настоящего времени актуальным остается поиск новых методов противоопухолевого лечения, которые были бы более эффективными и более безопасными для пациентов [1, 2]. Есть доказательства того, что соединения селена (Se) могут обладать как химиопрофилактической [3–5], так и противоопухолевой активностью [6, 7].
Считается, что селенорганические соединения менее токсичны, чем неорганические соединения селена [7, 8]. Механизм противоопухолевого действия селенсодержащих соединений в основном основан на индукции ими апоптоза клеток [9], а также на их влиянии на экспрессию генов и различные сигнальные пути клеток, процессы репарации и повреждения ДНК, ангиогенез и метастазирование [10]. Весьма важна также способность соединений селена повышать чувствительность раковых клеток к стандартной химио- и лучевой терапии и тем самым ее эффективность, а также снижать побочные эффекты такой терапии [7, 11]. К сожалению, эти механизмы иногда разнонаправлены и до конца не изучены [12].
Часто эти эффекты связаны с высокой антиоксидантной и, возможно, прооксидантной активностью метаболитов селенсодержащих соединений и образованием активных форм кислорода с окислением тиольных групп белков в клетке, что может приводить к дозозависимому окислительному стрессу [11, 13] и неоднозначному влиянию на динамику онкопроцесса.
Соединения Se могут также запускать неапоптотические механизмы клеточной смерти, вызывая остановку клеточного цикла [3, 11, 12], некроз [3, 12], аутофагию [11, 12], ферроптоз [13], некроптоз [14], энтоз [15], аноикис [16, 17], нетоз [18] или митотическую катастрофу [12].
Важным аспектом в области создания и изучения эффективных фармацевтических субстанций является контроль соотношения активность – токсичность. В связи с этим изучение безопасности селенсодержащих соединений, прежде всего селеноорганических, является актуальной задачей, так же как и дальнейшая оценка их специфической активности.
Цель исследования – изучение острой токсичности химической субстанции ди-[3(5)-метилпиразол-4-ил]селенид при внутрижелудочном введении беспородным мышам.
Материалы и методы исследования
В эксперименте использовали 65 нелинейных мышей весом 18–20 г – 30 самцов и 35 самок (протокол биоэтической комиссии ФГБУ «РНИОИ» МЗ РФ № 19 от 22.09.2015 г.). Все животные для проведения испытания поступили из сертифицированного питомника филиал «Андреевка» ФГБУН НЦБМТ ФМБА России (Московской обл.) и имели ветеринарное свидетельство и паспорт здоровья. Животных содержали в соответствии с действующими правилами (ГОСТ 33044-2014). Все процедуры с животными проводили, руководствуясь правилами Европейской Конвенции.
Объектом исследования острой токсичности явился ди-[3(5)-метилпиразол-4-ил]селенид, химическое строение и молекулярная структура которого были подтверждены методами спектроскопии ЯМР и ИК-спектроскопии.
Животные были рандомизированы в основные (введение ди-[3(5)-метилпиразол-4-ил]селенида) и контрольные (носитель) группы. Субстанцию суспендировали в физиологическом растворе и вводили в объеме 0,5 мл внутрижелудочно через назогастральный зонд. Контрольным группам был введен в аналогичном объеме физиологический раствор.
Все исследование проводилось в 2 этапа согласно общепринятым рекомендациям [19]. На предварительном этапе суспензию субстанции вводили однократно в дозах, начиная с 500 мг/кг, которая выбрана с учетом низкой токсичности селенорганических соединений [7, 8]. Последующие дозы (1000, 1500 и 2000 мг/кг) вводили согласно рекомендациям [19], с интервалом 72 ч (табл. 1). Наблюдение за каждым животным осуществляли в 1-е сутки после введения препарата и затем ежедневно последующие 7 дней.
Таблица 1
Дизайн эксперимента по оценке острой токсичности ди-[3(5)-метилпиразол-4-ил]селенида при внутрижелудочном введении беспородным мышам
|
Этап |
Продолжительность этапа |
Группа |
Доза, мг/кг |
Количество животных |
|
|
самки |
самцы |
||||
|
Предварительный |
72 ч между дозами
|
О |
500 |
1 |
– |
|
О |
1000 |
1 |
– |
||
|
О |
1500 |
1 |
– |
||
|
О |
2000 |
1 |
– |
||
|
К |
Носитель |
1 |
– |
||
|
Основной |
14 дней |
О |
3000 |
6 |
6 |
|
О |
5500 |
6 |
6 |
||
|
О |
8000 |
6 |
6 |
||
|
О |
10500 |
6 |
6 |
||
|
К |
Носитель |
6 |
6 |
||
Условные сокращения: О – основная группа, К – контрольная группа.
На втором этапе (основном) вводили однократно внутрижелудочно исследуемую субстанцию в дозах 3000, 5500, 8000 и 10500 мг/кг и проводили наблюдение за каждым животным в 1-е сутки каждый час после введения и затем ежедневно 14 дней.
В ходе эксперимента оценивали изменение массы тела животных, поведенческие реакции. Оценивали общее состояние животных: шерстный покров, позу, походку, способность сохранять неестественное положение тела, мышечный тонус, издаваемые звуки, раны, кровотечения, количество и консистенцию фекальных масс (диарея), массу тела. Производили подсчет количества погибших в исследовании животных.
Эвтаназия выживших животных была проведена ингаляцией двуокиси углерода на 7-е (для предварительного этапа) и на 15-е (для основного этапа) сутки эксперимента. Патоморфологическое исследование проводили в течение 2 ч после смерти животного. Для установления токсикометрических параметров острой токсичности субстанции использовали метод пробит-анализа по Личфилду–Уилкоксону.
Статистический анализ результатов исследования проводили с помощью программы STATISTICA 12.0 (StatSoft Inc., США). Осуществляли оценку нормальности распределения признаков, используя критерий Шапиро–Уилка и Колмогорова–Смирнова. Для оценки достоверности различий средних величин независимых выборок применяли критерий Стьюдента с установленным уровнем значимости p≤0,05.
Результаты исследования и их обсуждение
На предварительном этапе исследования после введения ди-[3(5)-метилпиразол-4-ил]селенида во всех исследованных дозах на протяжении всего периода не отмечено гибели подопытных животных, а также изменений внешнего вида, поведения, двигательной активности.
Результаты исследований основного этапа острой токсичности изучаемой химической субстанции на белых беспородных мышах показали выраженные токсические признаки отравления веществом, на основании чего была рассчитана токсическая летальная доза при внутрижелудочном введении.
В ходе основного этапа у животных всех опытных групп обнаружилась сходная картина проявления токсических признаков. После внутрижелудочного введения ди-[3(5)-метилпиразол-4-ил]селенида наблюдалось постепенное развитие признаков токсического отравления: снижение двигательной и исследовательской активности, нарушение дыхания (учащение с последующим урежением частоты дыхательных движений), нахохливание и сутулая поза. Гибель мышей регистрировалась в течение 4 дней после введения тестируемой субстанции. В более отдаленные сроки наблюдений смерти животных не наблюдалось. Все контрольные мыши были живы и не имели признаков интоксикации. Характеристика проявления летальных эффектов у животных представлена в таблице 2.
Таблица 2
Летальные эффекты животных при внутрижелудочном введении ди-[3(5)-метилпиразол-4-ил]селенида (основной этап исследования)
|
Доза, мг/кг |
Самки |
Самцы |
||
|
Павшие животные |
Всего животных |
Павшие животные |
Всего животных |
|
|
3000 |
0 |
6 |
1 |
6 |
|
5500 |
3 |
6 |
3 |
6 |
|
8000 |
4 |
6 |
5 |
6 |
|
10500 |
6 |
6 |
6 |
6 |
|
носитель |
0 |
6 |
0 |
6 |
При введении ди-[3(5)-метилпиразол-4-ил]селенида в дозе 3000 мг/кг у всех мышей выявлено снижение двигательной и исследовательской активности через 3 ч в сочетании с нарушением дыхания и нахохливанием. Летальный исход наступил у 1 самца спустя 17 ч после введения. У самок летальных исходов при данной дозировке не наблюдалось. После ухудшения показателей здоровья реабилитация у самцов наступала через 14–15 ч и у самок через 13–15 ч.
После введения дозы 5500 мг/кг в течение первых 30 мин у всех самцов снизилась активность и нарушилось дыхание, а спустя 1 ч появились сутулая поза и нахохливание. У самок снижение активности наступало в среднем через 1 ч после введения. Спустя 30–40 мин возникли нарушение дыхания, сутулая поза и нахохливание. Гибель у самцов наступила спустя 17,5–23 ч и у самок через 19–26 ч. Реабилитация выживших животных наступила в среднем через 15–17 ч. При применении ди-[3(5)-метилпиразол-4-ил]селенида в данной дозе погибли 50% животных обоего пола.
После введения субстанции в дозе 8000 мг/кг у всех самцов в первые 30 мин после введения выявлено нарушение двигательной активности. В течение в среднем 12,5 ч погибли 5 из 6 самцов. Среди самок у одной особи снижение активности проявилось через 30 мин, и она погибла через 16,5 ч. У остальных павших самок (2 из 4 павших самок) токсические признаки появились спустя 1 ч после введения, а гибель наступила через 23–42 ч. Реабилитация выживших животных наступила в среднем спустя 2 суток.
При введении дозы 10500 мг/кг у самцов признаки отравления проявились в течение первых 30 мин, среди самок все симптомы проявились в промежутке 30–60 мин. Гибель самок наступила в промежутке 13–26 ч, а самцы погибли через 10,5–14 ч. При дозировке 10500 мг/кг количество погибших животных составило 100%.
Полученные результаты позволили определить полулетальную дозу ди-[3(5)-метилпиразол-4-ил]селенида при внутрижелудочном введении беспородным мышам, которая составила ЛД50= 5400±77,8 мг/кг. Также были определены дозы ЛД10, ЛД16 и ЛД84, которые составили 3547±54,1, 4703±64,3 и 8869±69,5 соответственно.
Динамика гибели животных при внутрижелудочном введении фармакологической субстанции ди-[3(5)-метилпиразол-4-ил]селенида представлена в таблице 3.
Таблица 3
Временная характеристика проявления летальных эффектов у животных при внутрижелудочном введении ди-[3(5)-метилпиразол-4-ил]селенида
|
Доза, мг/кг |
Пол |
Наблюдаемый эффект (гибель) в динамике (сутки) |
% гибели |
% гибели обоего пола |
|||||||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
||||
|
3000
|
Самки |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
0 |
8,3 |
|
Самцы |
1 |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
16,7 |
||
|
5500 |
Самки |
1 |
2 |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
50 |
50 |
|
Самцы |
2 |
1 |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
50 |
||
|
8000 |
Самки |
1 |
2 |
1 |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
66,7 |
75 |
|
Самцы |
5 |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
83,3 |
||
|
10500 |
Самки |
3 |
2 |
1 |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
100 |
100 |
|
Самцы |
6 |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
100 |
||
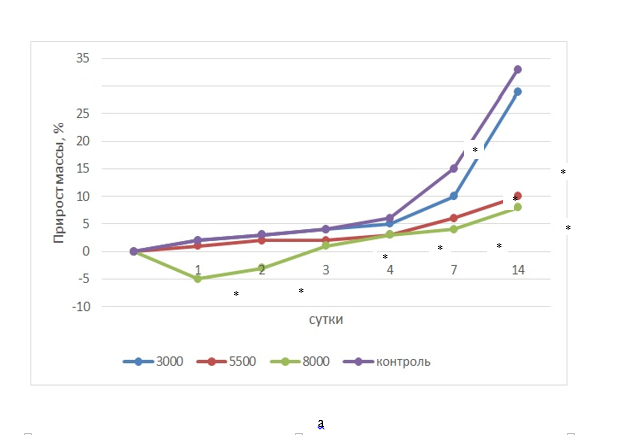
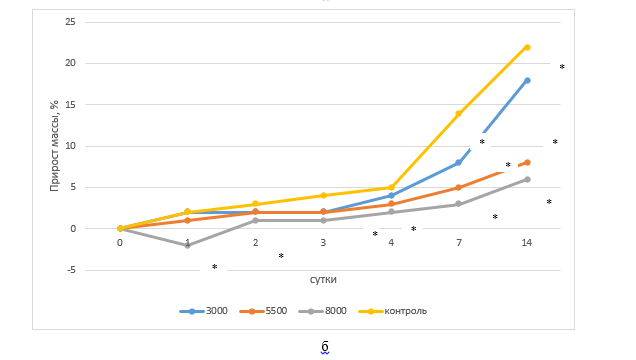
Динамика массы тела (%) при исследовании острой токсичности при внутрижелудочном введении нелинейным мышам ди-[3(5)-метилпиразол-4-ил]
Примечание: а – самцы, б – самки, * – статистически значимые различия с контролем при р<0,05
Результаты основного этапа исследования показали, что у выживших животных после введения ди-[3(5)-метилпиразол-4-ил]селенида отмечается положительный прирост массы тела в динамике наблюдения (рисунок). После исчезновения признаков острого отравления клиническое состояние животных было аналогично состоянию животных в контрольной группе. После введения субстанции в высоких дозах отмечается меньший прирост массы тела. При введении ди-[3(5)-метилпиразол-4-ил]селенида в дозе 8000 мг/кг в течение первых суток показано снижение массы тела ниже исходных значений, а со вторых суток отмечалась положительная динамика прироста. В остальных группах у животных обоего пола масса тела нарастала в течение первых суток после введения. В группе с дозой 8000 мг/кг у всех животных статистически значимо прирост массы тела был ниже контроля на всех этапах основного эксперимента. Наиболее выраженные различия в процентном приросте массы тела для различных групп обнаружены на 7-е и 14-е сутки эксперимента. На 7-е сутки после введения доз субстанции 3000, 5500 и 8000 мг/кг прирост массы в среднем был ниже относительно контроля в 2,4 раза, 4,1 и 5,2 раза соответственно, а на 14-е сутки для этих же доз – в 1,5 раза, 3,7 и 7,1 раза соответственно (для всех случаев при р<0,05).
При патологоанатомическом вскрытии павших животных с внутрижелудочным введением ди-[3(5)-метилпиразол-4-ил]селенида в указанных дозах обнаружена сходная картина морфологических нарушений кровообращения. При этом патологических изменений в других органах не было выявлено. У выживших экспериментальных животных при вскрытии после эвтаназии наблюдаемая морфологическая картина была сходна с контролем.
Заключение
Полученные результаты исследования химической субстанции ди-[3(5)-метилпиразол-4-ил]селенида позволили определить полулетальную дозу ЛД50 при внутрижелудочном введении нелинейным мышам обоего пола, которая дает возможность характеризовать изученное селенорганическое соединение как малотоксичное соединение. Химическая субстанция ди-[3(5)-метилпиразол-4-ил]селенид относится к 4-му классу опасности согласно нормативным документам [20]. Определение показателя ЛД50 для ди-[3(5)-метилпиразол-4-ил]селенида может быть использовано при выборе доз для оценки его специфической противоопухолевой активности.
Работа по синтезу субстанции проведена в Южном федеральном университете при финансовой поддержке Министерства науки и высшего образования Российской Федерации [государственное задание в области научной активности, Южный федеральный университет, проект FENW-2020-0031 (0852-2020-0031)].
Библиографическая ссылка
Кит О.И., Златник Е.Ю., Комарова Е.Ф., Максимов А.Ю., Морковник А.С., Дорофеенко А.И., Лукбанова Е.А., Непомнящая Е.М., Диваева Л.Н., Жуковская О.Н., Шапошников А.В., Позднякова В.В., Лысенко И.Б., Касьяненко В.Н. ОЦЕНКА ОСТРОЙ ТОКСИЧНОСТИ СЕЛЕНОРГАНИЧЕСКОГО СОЕДИНЕНИЯ С ПОТЕНЦИАЛЬНЫМ ПРОТИВООПУХОЛЕВЫМ ДЕЙСТВИЕМ // Современные проблемы науки и образования. 2021. № 4. ;URL: https://science-education.ru/ru/article/view?id=31048 (дата обращения: 09.04.2026).
DOI: https://doi.org/10.17513/spno.31048



