В литературе наиболее часто встречается описание эмфизематозного и бронхитического фенотипов ХОБЛ, которые протекают как с частыми, так и с редкими обострениями [1, 2]. Установлено, что каждый эпизод обострения ХОБЛ приводит к ухудшению показателей функции дыхания и газообмена, более быстрому прогрессированию заболевания, к декомпенсации сопутствующих хронических заболеваний и к значимому снижению качества жизни [3]. Наиболее частыми причинами, вызывающими обострение ХОБЛ, считают пневмотропные вирусы, бактерии, табакокурение и другие внешние загрязняющие факторы, усиливающие как местную, так и системную воспалительную реакцию [4], что проявляется либо повышением в крови циркулирующих цитокинов, хемокинов и белков острой фазы, либо аномалиями в циркулирующих клетках [5]. Среди биомаркеров риска и тяжести обострения ХОБЛ наиболее информативными признаны С-реактивный белок (СРБ), фибриноген, прокальцитонин, интерлейкин-6 (IL-6), фактор некроза опухоли альфа (TNF-α) [6]. В статье, посвященной метаанализу данных 14 научных работ [7], сообщается о повышении концентрации СРБ, фибриногена, TNF-α и о более высоком количестве лейкоцитов в крови больных ХОБЛ по сравнению с контрольными пациентами. В анализах крови изменяется не только общее количество лейкоцитов, но и формула крови. Например, относительная и абсолютная лимфопения свидетельствует об угнетении иммунных механизмов защиты, что необходимо учитывать при выборе терапии [8]. Одним из наглядных показателей соотношения факторов неспецифической защиты организма и иммунологического статуса является нейтрофильно-лимфоцитарный индекс (НЛИ). Показано, что оценка изменения отношения нейтрофильных лейкоцитов к лимфоцитам является простым и быстрым способом определения уровня воспалительных реакций [9]. Изучена связь между НЛИ и развитием патологии верхних дыхательных путей, острым коронарным синдромом, летальным исходом у пациентов с сердечной и почечной недостаточностью, с декомпенсированным циррозом печени, с онкологическими заболеваниями, включая метастатическое поражение, доказана прогностическая ценность НЛИ в определении как краткосрочного, так и долгосрочного прогноза, получены данные о положительной корреляции между значением НЛИ и уровнем провоспалительных цитокинов IL-6 и IL-8 [10, 11]. В реальной клинической практике не всегда представляется возможным определение многочисленных маркеров системного воспаления, поэтому необходимо продолжить поиск новых методов диагностики для прогноза обострений ХОБЛ. Таким маркером может стать НЛИ, который является информативным и легкодоступным показателем, требующим только дифференцированного подсчета формулы крови.
Цель работы: изучение клинико-функциональных показателей ХОБЛ с частыми обострениями и связи между уровнем НЛИ и маркерами системного воспалительного ответа (CРБ, IL-6, TNF-α) в периоды ремиссии и обострения.
Материал и методы исследования
Исследование проводилось на базе больницы Пущинского научного центра РАН (Б ПНЦ РАН) и Института фундаментальных проблем биологии РАН (ИФПБ РАН) по государственному заданию, программа № 0576-2020-0006. Одобрено локальным этическим комитетом БПНЦ РАН (протокол № 14 от 04.09.2018 г.). Все пациенты подписывали информированное согласие и проходили полное клинико-лабораторное и инструментальное обследование. Диагноз ХОБЛ установлен в соответствии с рекомендациями Global Initiative for Chronic Obstructive Lung Disease, GOLD-2020 [1]. По результатам спирометрических нарушений и по частоте обострений в исследование были включены 56 пациентов с верифицированным диагнозом ХОБЛ средней степени тяжести, которые были распределены на 3 группы:
1-я группа (n=22) – пациенты с ХОБЛ 2-й ст., с частыми обострениями, в стадии ремиссии;
2-я группа (n=34) – пациенты с ХОБЛ 2-й ст., без частых обострений, в стадии ремиссии;
3-я группа – группа контроля (n=16) – условно здоровые пациенты, которые не имели документального, анамнестического, клинико-лабораторного и инструментального подтверждения заболеваний респираторного тракта и сердечно-сосудистой системы.
Критериями включения в исследование для пациентов 1-й и 2-й групп наблюдения служили: возраст от 40 до 80 лет, период ремиссии в течение последних 4 недель, отсутствие базисной терапии на момент включения в исследование, индекс курения >10 пачко/лет, ОФВ1/ФЖЕЛ ≤0,70. Для пациентов группы контроля – возраст от 40 до 80 лет, отсутствие задокументированных хронических заболеваний легких, верхних дыхательных путей и сердечно-сосудистой системы и указания на них в анамнезе.
Критерии исключения из исследования для всех групп:
– острые инфекционные заболевания и туберкулез легких;
– онкологические заболевания любой локализации и болезни крови;
– обострение хронических заболеваний, требующих стационарного лечения;
– наличие диагностированной ишемической болезни сердца в виде стенокардии напряжения, перенесенных инфарктов миокарда, нарушений ритма, хронической сердечной недостаточности, гипертонической болезни 3-й ст., сахарного диабета 1-го и 2-го типов;
– хирургические вмешательства на легких в анамнезе и другой локализации в течение последних 6 месяцев;
– злоупотребления алкоголем и наркотическими веществами, наличие в анамнезе и в настоящее время психических расстройств;
– беременность и период лактации;
– добровольный отказ от дальнейшего обследования и лечения.
Обострения (до 3–4 раз в году) чаще всего возникали в осенне-зимний период, протекали с температурой, гнойной мокротой, одышкой и по результатам анализа амбулаторных карт диагностировались как обострение хронического бронхита и/или ОРВИ и лечились только антибактериальными препаратами. При включении в исследование проводилась спирометрия на спирометре Spiro USB Micro Medical spuds 5 с использованием компьютерного приложения фирмы «Валента», Санкт-Петербург. Значения ОФВ1 и ОФВ1/ФЖЕЛ после использования бронхолитика (Вентолина 400 мкг) были решающими для постановки диагноза ХОБЛ и оценки степени спирометрических нарушений. Для оценки выраженности клинических проявлений использовался опросник САТ. Степень выраженности одышки оценивали по шкале mMRC. Сопутствующие заболевания имели все пациенты 1-й и 2-й групп наблюдения: заболевания сердечно-сосудистой системы имели 33 пациента (28 мужчин и 5 женщин); хронический риносинусит неаллергической этиологии – 12 мужчин и 2 женщин; заболевания желудочно-кишечного тракта – 15 мужчин и 5 женщин, заболевания мочеполовой системы – 5 мужчин и 3 женщины. Согласно комплексной оценке всех симптомов, данных КТ (на аппарате марки SIMENS Somatom Emotion Германия, 16-срезовый) и функционального обследования, по делению на категории АВСD пациенты с ХОБЛ были распределены в группы: «А» – симптомов меньше, низкий риск – 13 мужчин и 2 женщины; «В» – симптомов больше, низкий риск – 15 мужчин и 4 женщины; «С» – симптомов меньше, высокий риск – 14 мужчин и 5 женщин; «D» – симптомов больше, высокий риск – 3 мужчин. Все пациенты до включения их в исследование не пользовались бронхолитиками короткого или длительного действия. Больные с ХОБЛ после включения в группы наблюдения стали получать базисную терапию длительно действующими бронходилататорами (М-холиноблокаторами и бета-адреномиметиками).
При обострении ХОБЛ у пациентов групп C и D к бронходилататорам добавляли ингаляционные глюкокортикостероиды (ИГКС) и по показаниям – антибиотики [1].
Активность воспалительного процесса изучали в динамике, в стадии ремиссии и при обострении по биомаркерам: С-реактивный белок (СРБ) определяли иммунотурбодиметрическим методом с использованием набора реагентов «ДДС», Россия, на биохимическом автоматическом анализаторе Dirui CS400 КНР. Референсные значения – 0–0,5 мг/дл. Провоспалительные цитокины: интерлейкин-6 (IL-6) и фактор некроза опухоли-альфа (TNF-α) – определяли методом иммуноферментного анализа с использованием наборов фирмы «ВекторБест» (Новосибирск). Референсные значения для IL-6 были от 0 пг/мл до 7 пг/мл и для TNF-α – от 0 пг/мл до 8 пг/мл. Проводился подсчет формулы крови и рассчитывался индекс соотношения нейтрофилов и лимфоцитов (НЛИ), который отражал соотношение клеток неспецифической и специфической защиты. В норме НЛИ соответствует значению 1,74+0,98 [10]. Статистическая обработка данных проводилась с использованием компьютерной программы Statistica 8.0, непараметрическими методами (сравнение групп с помощью критериев Манна–Уитни, Фридмана, определение наличия связи между группами при помощи методов корреляции Спирмена). Различия показателей считались достоверными при р<0,05.
Результаты исследования и их обсуждение
В клинической картине ХОБЛ ведущей жалобой больных как в 1-й, так и во 2-й группах наблюдения была одышка. В 1-й группе она присутствовала у 18 из 22 пациентов (81,8%); во 2-й группе – у 21 из 34 пациентов (61,7%), кашель беспокоил чаще при обострении после ОРВИ, физическая активность была снижена у всех пациентов 1-й и 2-й групп наблюдения, прежде всего за счет утренних симптомов. Длительность кашля до включения в исследование составила в 1-й группе 20,07±0,71 года, во 2-й группе – 18,44±1,42 года; длительность одышки в 1-й группе – 8,54±0,42 года и во 2-й группе – 7,76±0,72 года, что отражало недооценку пациентами своего состояния и привычку к колебаниям выраженности симптомов по мере прогрессирования заболевания [3]. В таблице приведена клинико-функциональная характеристика пациентов, включенных в группы наблюдения.
Таблица
Клинико-функциональные характеристики больных ХОБЛ
|
Показатели |
Группа 1
|
Группа 2
|
Группа контроля |
|
ХОБЛ 2-й ст., с частыми обострениями n=22 |
ХОБЛ 2-й ст., без частых обострений n=34 |
Условно здоровые пациенты, n=16 |
|
|
Возраст, лет |
67,5±7,8 |
63,4±6,7 |
61,5±6,4 |
|
Пол: |
|||
|
Мужской |
18 |
29 |
9 |
|
Женский |
4 |
5 |
3 |
|
Индекс пачко/лет |
32,6±4,1 |
30,2±6,5 |
28,4±5,6 |
|
ОФВ1, % |
49,6±6,7 |
62,5±5,9 * |
96,2±2;9** |
|
Индекс Тиффно |
57,1±9,7 |
64,5±6,7 * |
98±8,9** |
|
SpO2, % |
93,6±3,9 |
94,8±9,1 |
98,4±9,6** |
|
Сатурация 02 после теста с 6-минутной ходьбой, % |
91,5±5,8 |
93,6±6,7 * |
97,3±6,6** |
|
Тест с 6-минутной ходьбой, м |
340,8 ±18,9 |
390,5±7,8 * |
580,9±9,6** |
|
САТ ≥10 баллов; число пациентов |
22 |
29 |
1 |
|
mMRC ≥2 балла, число пациентов |
18 |
21 |
0 |
|
Сопутствующие сердечно-сосудистые заболевания, число пациентов |
18 |
15 |
0 |
Примечание: *– p<0,05 между 1-й и 2-й группами наблюдения; **– p<0,05 между 1-й группой и группой контроля.
Повышенную массу тела имели все обследованные пациенты групп наблюдения, индекс массы тела составил 24,27±0,49. Толерантность к физической нагрузке оценивали по тесту с 6-минутной ходьбой. Из представленных данных видно, что у пациентов 1-й группы наблюдения этот показатель был значительно снижен по сравнению с пациентами 2-й группы и группы контроля (p1–3<0,05). Через 12 и 24 месяца на фоне базисной терапии длительно действующими бронхолитиками при комплексной клинико-лабораторной и инструментальной оценке течения ХОБЛ была отмечена положительная динамика у пациентов всех групп наблюдения. Однако показатели ФВД оставались на низких значениях. В 1-й группе наблюдения через 3 года ОФВ1% составил 51,5±5,9, во 2-й группе – 64,3±7,1 (р<0,001). Такую же тенденцию имели данные теста с 6-минутной ходьбой – 360,7± 12,7 м и 420,9±29,4 м (р<0,05) соответственно. В группе пациентов с ХОБЛ, имеющих редкие обострения на фоне длительно действующих бронхолитиков, отмечена более благоприятная динамика и, следовательно, меньший риск последующих обострений.
Известно, что активный воспалительный процесс в дыхательных путях является одним из основных звеньев патогенеза развития ХОБЛ, а биомаркеры воспаления могут играть ключевую роль как для ранней диагностики, так и при оценке риска последующего обострения. В исследованиях [12] было показано, что средние уровни СРБ у пациентов с ХОБЛ 4 степени в сравнении с 1 ( р <0,004), 2 (р<0,03) и 3 (р<0,03) степенью тяжести болезни были статистически значимо выше. Следовательно, увеличение тяжести ХОБЛ ассоциировалось с большим увеличением уровня СРБ. Повышенные значения СРБ имелись у пациентов с более низкими значениями объема форсированного выдоха за 1-ю секунду (ОФВ1). Dentener et al. при сравнении сывороточных маркеров воспаления у больных ХОБЛ и группы контроля отметили повышение уровней СРБ (11,8 против 4,1 мг/л) и лейкоцитов крови (7,2 х 109/л против 4,8 х 109/л) у больных ХОБЛ, которые снижались на фоне терапии [13]. Общеизвестно, что ответом на острое воспаление/обострение хронического воспаления в организме при любой локализации является, прежде всего, реакция системы крови. Изучение уровня лейкоцитов, нейтрофилов и лимфоцитов периферической крови у пациентов групп наблюдения показало, что в 1-й группе наблюдения в период ремиссии уровень лейкоцитов составил (9,9±5,5)×109/л, нейтрофилов – (8,05±1,8)×109/л, уровень лимфоцитов – (1,2±0,4)×109/л. Во 2-й группе уровень лейкоцитов составил (7,78±4,9)×109/л, уровень нейтрофилов – (5,0 ± 1,4)×109/л и лимфоцитов – (2,09 ± 0,3)×109/л. Количество лимфоцитов у пациентов в 1-й группе было в 1,74 раза ниже, чем у пациентов в группе с ХОБЛ без обострений, p<0,05. При обострении ХОБЛ в 1-й группе уровень лейкоцитов составил (12,3±6,2)×109/л, уровень нейтрофилов – (9,7±1,8)×109/л и лимфоцитов – (1,1±0,4)×109/л, во 2-й группе наблюдения – соответственно (8,72±4,6)×109/л; (6,12±1,4)×109/л и (2,4±0,6)×109/л. В группе контроля уровень лейкоцитов составил (5,26±2,43)×109/л, нейтрофилов – (3,31±0,78)×109/л и лимфоцитов – (1,86±0,67)×109/л. Между группами наблюдения различия отмечены по показателям абсолютного количества лейкоцитов, нейтрофилов и лимфоцитов (р<0,05).
Индекс соотношения нейтрофилов и лимфоцитов (НЛИ), отражающий соотношение клеток неспецифической и специфической защиты, в 1-й группе наблюдения в период ремиссии был выше, чем в группе контроля, на 4,93±0,45 у.е. и повышался в период обострения на 2,11±0,9 у.е. Через 8 недель НЛИ в период ремиссии оставался повышенным и превышал показатели контроля на 1,18±0,43 у.е. У пациентов с фенотипом ХОБЛ без частых обострений также было отмечено повышение уровня НЛИ на 0,62±0,35, 0,78±0,47 и 0,49±0,29 у.е. соответственно. В период обострения НЛИ у пациентов с фенотипом ХОБЛ с частыми обострениями был в 3,4 раза выше, чем у пациентов с ХОБЛ без обострений, что подтверждает более выраженные воспалительные проявления у пациентов 1-й группы наблюдения. Из литературных данных известно, что перенесенное обострение у пациентов с ХОБЛ повышает риск последующего обострения, и наиболее опасным временем для развития повторного нового обострения (или рецидива) принято считать первые 8 недель после очередного обострения [14]. В наших исследованиях показано, что у пациентов 1-й группы наблюдения в период ремиссии при значениях НЛИ 6,53–7,09 у.е. следующее обострение наступало через 3–4 недели и протекало тяжелее, чем у пациентов с этим индексом в пределах 3,45–4,63 у.е. Уровень СРБ у них в период ремиссии был 4,73±3,09 мг/дл, т.е. на 4,62 мг/дл превышал референсные значения; во 2-й группе наблюдения – 3,67±2,17 мг/дл, что также превышало референсные значения и указывало на сохранение активности воспалительного процесса даже в период ремиссии. Через 8 недель на фоне базисной терапии длительно действующими бронхолитиками уровень СРБ у пациентов 1-й группы снизился до 3,28±2,44 мг/дл, но оставался повышенным, что создавало риск нового обострения. Во 2-й группе наблюдения уровень СРБ снизился с 3,67±2,17 мг/дл до 2,86±1,48 мг/дл. Исследования N. Mehrotra с соавторами показали, что при ХОБЛ ведущая роль в формировании хронического системного воспалительного процесса принадлежит IL-6, который выступает в качестве предиктора смерти у больных ХОБЛ с частыми обострениями [14]. В наших исследованиях установлено, что у пациентов с ХОБЛ с частыми обострениями наблюдалось значимое повышение как спонтанной, так и индуцированной продукции IL-6 (p<0,05), что в первую очередь связано с формированием нейтрофильного типа воспаления, проявляющегося в активации гранулоцитов в ответ на токсические факторы (в частности, курение) и вирусно-бактериальные патогены. Сохранение высоких значений спонтанной и индуцированной продукции IL-6 указывало на персистенцию воспаления, несмотря на клиническое купирование обострения. Именно с IL-6 связывают выработку белков острой фазы воспаления и влияние IL-6 на ремоделирование бронхов по механизму повреждения эпителия дыхательных путей. В свою очередь, нейтрофилы являются основными мишенями IL-6 в легких, что подтверждает ключевую роль этого цитокина в патогенезе нейтрофильного воспаления респираторного тракта. В наших исследованиях средние значения маркеров системного воспаления IL-6 и TNF-α были выше у пациентов 1-й группы наблюдения, чем у пациентов 2-й группы наблюдения, и составили соответственно: 12,76±3,82 пг/мл – 25,0±1,82 пг/мл и 7,99±1,67 пг/мл – 18,84±3,82 пг/мл (референсные значения до 7,0 пг/мл для IL-6 и до 8,0 пг/мл для TNF-α). При анализе данных тяжести обострения и показателей НЛИ и IL-6 было установлено, что, чем тяжелее протекало обострение, тем выше были значения НЛИ и IL-6, как спонтанного, так и индуцированного ФГА, что отражало в большей степени возможности иммунокомпетентных клеток реагировать на действие патогенного фактора.
Корреляционный анализ показателей НЛИ и IL-6 выявил, что коэффициент корреляции (r) у пациентов 1-й группы в период обострения был в 3 раза выше, чем у пациентов 2-й группы наблюдения (для 1-й группы r=0,194870 и для 2-й группы r=0,06337). Это подтверждало диагностическую и прогностическую значимость НЛИ при фенотипе ХОБЛ с частыми обострениями.
Корреляционная зависимость между НЛИ и IL-6 у пациентов 1-й группы в период обострения представлена на рисунке 1.
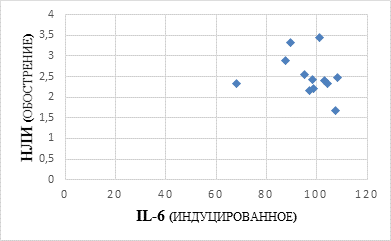
Рис. 1. Корреляционная зависимость между НЛИ и IL-6 у пациентов 1-й группы в период обострения. Коэффициент корреляции – 0,194870 при p<0,05
Такая же зависимость была показана ранее в исследованиях R. Zahorec (2001), согласно которым индекс соотношения нейтрофилов и лимфоцитов, названный автором «нейтрофильно-лимфоцитарный стрессовый фактор», имел хорошую прогностическую значимость при оценке тяжести состояния у больных, перенесших плановое и экстренное оперативное вмешательство, политравму, инфаркт миокарда, у больных с сепсисом и острым панкреатитом [15]. Нами были также выявлены достоверные корреляционные связи между НЛИ и ОФВ1, НЛИ и TNF-α, уровнем СРБ мг/дл и НЛИ у.е. Так, коэффициент корреляции (r) между НЛИ и СРБ был равен 0,0725893 у пациентов 1-й группы и 0,04806 у пациентов 2-й группы при p<0,05, что в 1,5 раза выше при фенотипе ХОБЛ с частыми обострениями.
Корреляционная зависимость между СРБ и НЛИ у пациентов 1-й группы в период обострения представлена на рисунке 2.
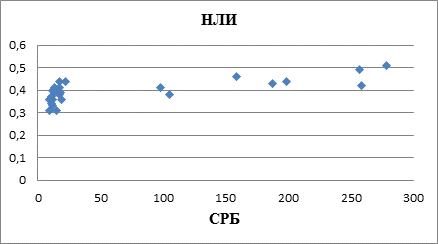
Рис. 2. Корреляционная зависимость между СРБ и НЛИ у пациентов 1-й группы в период обострения, r=0,0725893 при p<0,05
Заключение
Полученные нами результаты позволили сделать вывод, что клинический анализ крови и лейкоцитарные индексы интоксикации, в частности НЛИ, могут служить маркером риска очередного обострения. Уровни С-реактивного белка (СРБ), интерлейкина-6 (IL-6) и нейтрофильно-лимфоцитарный индекс (НЛИ) являются значимыми биомаркерами воспаления и положительно коррелируют между собой. Оценка НЛИ как показателя напряжения иммунитета позволит прогнозировать возникновение очередного обострения при фенотипе ХОБЛ с частыми обострениями. При мониторинге клинического анализа крови повышение НЛИ у пациентов с ХОБЛ с частыми обострениями в период ремиссии может рассматриваться как неблагоприятный прогностический фактор очередного обострения и его тяжести, что актуально для своевременного внесения изменений в тактику лечения. Таким образом, индекс соотношения нейтрофилов и лимфоцитов (НЛИ) может быть использован в качестве дополнительного диагностического метода в прогнозе очередного обострения при фенотипе ХОБЛ с частыми обострениями.
Библиографическая ссылка
Косякова Н.И., Грачев С.В., Прохоренко И.Р. КЛИНИКО-ФУНКЦИОНАЛЬНЫЕ ОСОБЕННОСТИ И МАРКЕРЫ СИСТЕМНОГО ВОСПАЛЕНИЯ ПРИ ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНИ ЛЕГКИХ С ЧАСТЫМИ ОБОСТРЕНИЯМИ // Современные проблемы науки и образования. 2021. № 2. ;URL: https://science-education.ru/ru/article/view?id=30725 (дата обращения: 29.04.2026).
DOI: https://doi.org/10.17513/spno.30725



