Ксерогель, в отличие от гидрогеля, состоит из сшитых полимеров, из которых удалена жидкая среда, благодаря этому уменьшается пористость, давление внутри геля, вязкость, а коэффициент диффузии при этом имеет очень высокое значение, благодаря этому ксерогели представляют большой интерес для биомедицинских исследований [1]. Ксерогелевые материалы можно адаптировать под конкретные задачи раневой повязки, пористость, весовое соотношение и желаемую кинетику лекарственного средства [2]. На сегодняшний день нами обнаружено только одно средство против шрамов и рубцов на ксерогелевой основе XERAGEL (КСЕРОГЕЛЬ) BIODERMIS XSO-797, регистрационное удостоверение: РЗН 2013/1085 от 05.09.2013. Производитель: Biodermis, 1820 Whitney Mesa Drive, Henderson, Nevada 89014, USA (США). Отечественных аналогов нет.
Цель исследования - оценить фармакокинетику ксерогеля на основе нейтрального гидрозоля диоксида титана при внутривенном введении, для последующего применения в качестве противоожогового средства.
Материал и методы исследования
Синтез ксерогеля на основе нейтрального гидрозоля диоксида титана был осуществлен в лаборатории SCAMT Университета ITMO.
Распределение ксерогеля при его однократном внутривенном введении было изучено на самцах крыс Wistar, массой 180–200 граммов, содержащихся в стандартных условиях вивария. Было сформировано 3 группы крыс по 16 животных, в каждой из групп ксерогель вводили в дозах 0,2, 0,1 и 0,05 мл/кг соответственно. Взятие образцов крови проводилось до начала введения ксерогеля (фон) и далее спустя 10 минут, 20 минут, 40 минут, 1 час, 10 часов и 24 часа после введения. Взятие образцов органов (кожи, селезенки, печени, почки) проводили у животных, подвергнутых эвтаназии до начала введения ксерогеля (фон) и далее спустя 1, 24, 72, 120 часов после введения ксерогеля. В каждую временную точку все образцы забирали не менее чем от 4 животных. Все манипуляции с использованием животных проводились в соответствии с этическими принципами, установленными Европейской конвенцией по защите позвоночных животных, используемых для экспериментальных и других научных целей (принятой в Страсбурге 18.03.1986 и подтвержденной в Страсбурге 15.06.2006). Стандартные образцы анализируемого элемента для калибровочных растворов были приготовлены из монокомпонентного стандарта Ti MERСK в 0,1 N HNO3. Диапазон калибровочных растворов: 0,001-10 мг/л. По результатам экспериментов, на основании полученных первичных данных и общей биэкспоненциальной модели: С = A*exp(-αt) + B*exp(-βt) [3] (1), были построены фармакокинетические модели выведения ксерогеля из организма экспериментальных животных. В этой модели α – константа, характеризующая скорость нарастания концентрации вещества, β – константа, описывающая скорость элиминации изучаемого соединения, t – время, прошедшее после введения ксерогеля, в минутах, А и В – константы, описывающие амплитуду изменения исследуемого вещества. C – концентрация исследуемого соединения в исследуемом образце. Для каждой из моделей рассчитывались следующие параметры: константа всасывания ксерогеля (Ка), константа элиминации ксерогеля (Кel), объем распределения ксерогеля в мл (Vd), клиренс ксерогеля, мл/мин. (Kl), площадь под фармакокинетической кривой, мкг/мл/мин. (AUC). Между расчетными, модельными показателями и экспериментальными значениями рассчитывался коэффициент линейной корреляции Пирсона. Проверказначимостимодели регрессии проводилась с использованием F-критерия Фишера, при заданном уровне значимости (р) p <0,01.
Результаты исследования и их обсуждение
Количественные данные по концентрации ксерогеля в крови были получены только для максимальной дозы 2000 мкг/крысу, поскольку при введении меньших доз концентрация ксерогеля в крови, вследствие его адсорбции в органах, была недостаточна для количественной оценки, анализ проб показал значения ниже пределов чувствительности метода (табл. 1). При этом используемая математическая модель приняла вид:
|
С = 1,196×exp(-0,13562t) + 0,283×exp(-0,00044t). |
(2) |
Результаты расчетов на основании выражения (2) представлены в таблице 1.
Таблица 1
Значения концентрации оксида титана в крови животных при однократном в/в введении в дозе 2000 мкг
|
Время, t, мин. |
Cэ, мкг/мл |
См, мкг/мл |
Δ, См–Сэ, мкг/мл |
|
10 |
0,59 |
0,59 |
0,00 |
|
20 |
0,36 |
0,36 |
0,00 |
|
40 |
0,34 |
0,28 |
-0,06 |
|
60 |
0,20 |
0,28 |
0,08 |
|
600 |
0,21 |
0,22 |
0,01 |
|
1440 |
0,15 |
0,15 |
0,00 |
Примечания. Экспериментальные (Сэ) и модельные (См), Δ – разность между значениями (См-Сэ); коэффициент корреляции (r) между значениями (См) и (Сэ); коэффициент корреляции r = 0,961, уровень значимости (р) p = 0,002 (<0,01).
Таблица 2
Фармакокинетические параметры динамики нейтрального гидрозоля диоксида титана
|
Исследуемый объект |
Кровь |
Гомогенат печени |
Гомогенат селезенки |
||||
|
Номер модели |
(2) |
(6) |
(7) |
(8) |
(12) |
(13) |
(14) |
|
Ка |
0,13562 |
0,00030 |
0,00011 |
0,00065 |
0,00007 |
0,00041 |
0,00108. |
|
Кel |
0,00044 |
0,00009 |
0,00004 |
0,00029 |
0,00002 |
0,00013 |
0,00039 |
|
Vd, мл |
6761,325 |
113,298 |
47,887 |
51,228 |
47,807 |
50,472 |
51,001 |
|
Kl, мл/мин. |
15.372 |
0.011 |
0.002 |
0.015 |
0.001 |
0.007 |
0.020 |
|
AUC, мкг/мл/мин. |
650.5 |
189811,9 |
550078,8 |
33540,9 |
1901577,4 |
147859,0 |
25202,4 |
На основании приведенных данных (табл. 2) можно заключить, что имеет место быстрая динамика всасывания ксерогеля и достаточно медленная динамика его выведения, т.к. значения Ка>>Кеl, 0,13562>>0,00044 соответственно. Коэффициенты корреляции (r = 0,961) между экспериментальными и модельными значениями концентраций ксерогеля, а также уровень значимости p = 0,002 (<0,01) демонстрируют адекватность используемой фармакокинетической модели для описания зависимости величины (С) от (t) [4]. Динамика выведения ксерогеля из крови крыс указывает на возможность его поступления и накопления во внутренних органах животных, например в селезенке и печени.
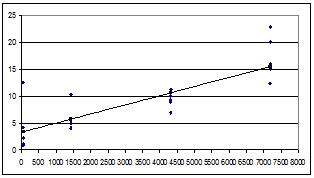
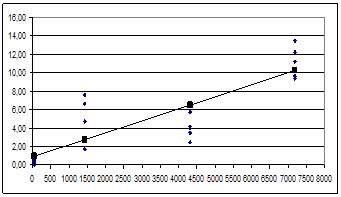
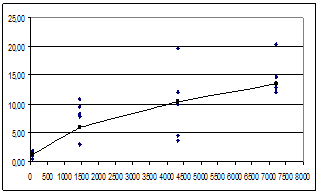
Количественные данные по концентрации ксерогеля в печени крыс были получены для всех использованных доз ксерогеля, которые составили 2000, 1000 и 500 мкг на крысу. В течение эксперимента наблюдалось увеличение концентрации ксерогеля в печени животных, данные в виде тренда приведены на (рис. 1 А-В).
|
А |
Б |
|
В |
|
Рис. 1. Изменение концентрации диоксида титана в печени крыс после внутривенного введения ксерогеля: А) доза ксерогеля 2000 мкг, Б) доза ксерогеля 1000 мкг, В) доза ксерогеля 500 мкг
Примечания. Ось абсцисс - время после введения ксерогеля, минут. Ось ординат - концентрация ксерогеля, С, мкг/гр. Сплошная линия – трендовые значения концентрации ксерогеля. Точки – экспериментальные значения концентрации ксерогеля.
Трендовая (не камерная) зависимость изменения параметра (С) от (t) для внутривенного введения 2000 мкг представлена в виде выражения (3):
|
С=3,3112+0,0017t, |
(3) |
где t – время, прошедшее после введения ксерогеля, минут;для внутривенного введения 1000 мкг – в виде выражения (4):
|
С=0,4529×t0,3438, |
(4) |
для внутривенного введения 500 мкг – в виде выражения (5):
|
С=0,8661+0,0013t. |
(5) |
Коэффициенты корреляции для выражений (3), (4) и (5) составили: r = 0,812; r =0,800 и r =0,845 соответственно. Критерий Фишера (F) для выражений (3), (4) и (5) составил: 32,83; 30,6 и 45,07 соответственно, при р <0,001.
Указанные статистические параметры для выражений (3), (4) и (5) демонстрируют достаточную информативность значимость полученных трендов на фоне трех исследованных доз, что позволяет сделать заключение о наличии эффекта накопления ксерогеля в печени экспериментальных животных. Однако отмечается высокая вариабельность концентраций ксерогеля в интервале доз от 500 до 2000 мкг/кг, что приводит к приближенным оценкам его фармакокинетических характеристик.
Параметры фармакокинетической модели для тренда (3) имеют следующий вид (6):
|
С = 25,433×(exp(-0,00009t)-exp(-0,00030t)). |
(6) |
Параметры фармакокинетической модели для тренда (4) имеют следующий вид (7):
|
С = 31,308×(exp(-0,00004t)-exp(-0,00011t)). |
(7) |
Параметры фармакокинетической модели для тренда (5) имеют следующий вид (8):
|
С = 17,716×(exp(-0,00029t)-exp(-0,00065t)). |
(8) |
На основании приведенных данных (табл. 2) можно заключить, что при внутривенном введении ксерогеля в интервале доз от 500 до 2000 мкг наблюдаются сопоставимые фармакокинетические параметры. Анализ фармакокинетических параметров показывает, что на фоне внутривенного введения диоксида титана в печени крыс происходит накопление ксерогеля, так как параметры Ка> Кel и значения клиренса минимальны [5]. Это подтверждает трендовые зависимости величины (С) от времени (t), представленные на (рис. 2 А-В). При увеличении дозы диоксида титана эффект его накопления в печени становится более выраженным.
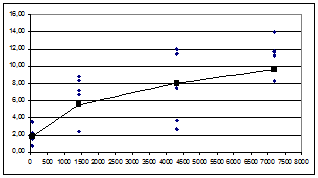
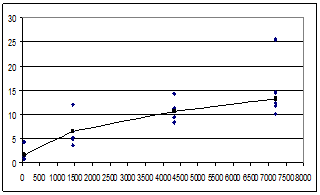
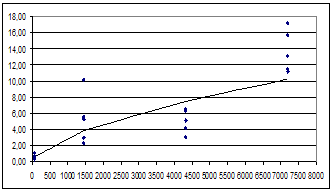
Количественные данные по концентрации ксерогеля в селезенке крыс были получены для всех использованных доз ксерогеля, которые составили 2000, 1000 и 500 мкг на крысу. В течение эксперимента наблюдалось увеличение концентрации ксерогеля в селезенке животных, данные в виде тренда приведены на (рис. 2 А-В).
|
А |
Б |
|
В |
|
Рис. 2. Изменение концентрации диоксида титана в селезенке крыс после внутривенного введения ксерогеля: А) доза ксерогеля 2000 мкг, Б) доза ксерогеля 1000 мкг,
В) доза ксерогеля 500 мкг
Примечания. Ось абсцисс - время после введения ксерогеля, минут. Ось ординат - концентрация ксерогеля, С, мкг/гр. Сплошная линия – трендовые значения концентрации ксерогеля. Точки – экспериментальные значения концентрации ксерогеля.
Трендовая (не камерная) зависимость изменения параметра (С) от (t) для внутривенного введения ксерогеля в дозе 2000 мкг представлена в виде выражения (9):
|
С=0,2535×t0,4453 |
(9) |
для внутривенного введения в дозе 1000 мкг – в виде выражения (10):
|
С=0,1478×t0,508 |
(10) |
для внутривенного введения в дозе 500 мкг – в виде выражения (11):
|
С=0,0479×t0,6038 |
(11) |
Коэффициенты корреляции для выражения (9), (10) и (11) составили: r = 0,903; r =0,881 и r =0,925 соответственно. Критерий Фишера (F) для выражения (9), (10) и (11) составил: 79,48; 62,64 и 106,97 соответственно, при р <0,001.
Полученные статистические параметры для выражений (9), (10) и (11) показывают достаточную информативность и значимость трендов на (рис. 3 А-В). Направленность изменений концентраций диоксида титана демонстрирует наличие эффекта накопления ксерогеля в селезенке в интервале доз от 500 до 2000 мкг.
Параметры фармакокинетической модели для тренда (9) составили (12):
|
С = 59,534×(exp(-0,00002t)-exp(-0,00007t)). |
(12) |
Параметры фармакокинетической модели для тренда (10) составили (13):
|
С = 29,610×(exp(-0,00013t)-exp(-0,00041t)). |
(13) |
Параметры фармакокинетической модели для тренда (11) составили: (14):
|
С = 15,291×(exp(-0,00039t)-exp(-0,00108t)). |
(14) |
На основании приведенных данных можно заключить, что при внутривенном введении ксерогеля в интервале доз от 500 до 2000 мкг наблюдаются сопоставимые фармакокинетические параметры. В селезенке крыс отмечается накопление ксерогеля, так как параметры Ка > Кel и значения клиренса минимальны. Это подтверждает трендовые зависимости величины (С) от времени (t), представленные на (рис. 3 А-В). При увеличении дозы диоксида титана эффект его накопления в селезенке становится более выраженным.
Количественные данные по концентрации диоксида титана в коже крыс были получены для всех изученных доз ксерогеля, которые составили 2000, 1000 и 500 мкг на крысу. Спустя 60 минут после введения ксерогеля средняя концентрация диоксида титана в коже для 3 вышеуказанных доз составила 17,21; 7,49 и 3,91 мкг/грамм соответственно. Спустя 24 часа и далее в процессе эксперимента ксерогель в коже не определялся, что может быть связано со спецификой проницаемости кожных покровов для мезопористых гелей [6].
Оценка концентрации диоксида титана в почках крыс была проведена для всех изученных доз ксерогеля, которые составили 2000, 1000 и 500 мкг на крысу. Ни на одном из изученных сроков забора органа диоксид титана в почках крыс не определялся. На основании этих данных можно заключить, что при внутривенном введении ксерогель в почках крыс не накапливается и в его выведении из организма почки участия не принимают.
Исследования токсичности различных форм диоксида титана многочисленны, особое внимание исследователей обращают на себя наноматериалы на основе диоксида титана [7; 8], однако, несмотря на их обилие, данных о трансдермальном пути поступления недостаточно. Вместе с тем в органах-мишенях возможен рост генерации реактивных форм кислорода, перекисного окисления липидов, также возможно внутриклеточное депонирование вследствие прикрепления наночастиц к внутриклеточным органеллам и биологическим макромолекулам после повреждения клеточных мембран [9]. В наших исследованиях на модели термического ожога IIIБ степени, при ежедневном нанесении ксерогеля на раневой дефект, продемонстрировано более полноценное ремоделирование кровеносного русла раневого дефекта, с большей активацией популяций базальных кератиноцитов области раневого дефекта, по отношению к морфологической картине в группе препарата сравнения – аргосульфана [10]. В основе такого рода эффектов могут лежать эпидермально-мезенхимальные эффекты [11], аналогично эффектам силиконовых гелей [12].
Заключение
Изучение фармакокинетики ксерогеля при его однократном внутривенном введении крысам показало, что динамика выведения ксерогеля диоксида титана из крови была достаточно медленной. В коже накопления ксерогеля не наблюдалось, спустя 24 часа после внутривенного введения его концентрация в этом органе была нулевой, в почках концентрация диоксида титана была нулевой в течение всего периода эксперимента. Полученные результаты характеризуют безопасность использования полученного ксерогеля оксида титана в качестве потенциального противоожогового средства.
Библиографическая ссылка
Дуданов И.П., Виноградов В.В., Криштоп В.В., Никонорова В.Г. ФАРМАКОКИНЕТИКА ПЕРСПЕКТИВНОГО КСЕРОГЕЛЯ НА ОСНОВЕ НЕЙТРАЛЬНОГО ГИДРОЗОЛЯ ДИОКСИДА ТИТАНА ДЛЯ ТЕРАПИИ ОЖОГОВЫХ РАН // Современные проблемы науки и образования. 2021. № 2. ;URL: https://science-education.ru/ru/article/view?id=30714 (дата обращения: 01.04.2026).
DOI: https://doi.org/10.17513/spno.30714