Медикаментозная терапия является одной из основных составных частей лечения и профилактики заболеваний, в том числе сердечно-сосудистых и других хронических неинфекционных, основные из которых служат причиной практически 75% смертей в РФ и других развитых странах [1]. Помимо оценки эффективности лечения, первоочередное значение имеет анализ безопасности применяемых медицинских препаратов, поскольку комплексная терапия у пациентов с этими заболеваниями продолжается в течение многих лет, часто десятилетий [2], и небольшие по интенсивности токсического воздействия побочные эффекты могут кумулироваться, оказывать негативное воздействие сразу на несколько систем организма, усугубляя течение основного заболевания(-ий). При этом наиболее распространенные статистические методы анализа безопасности лекарств основаны на регистрации отдельных побочных эффектов [3, 4] (поражения отдельных систем организма), без учета их взаимного влияния, по крайней мере, без использования математически формализованных методов системного анализа. Также применение традиционных статистических методов не позволяет дать единую численно выраженную оценку безопасности препаратов сразу по нескольким системам организма или показателям, характеризующим функционирование этих систем [4].
Оценка безопасности препаратов проводится, как правило, на анализе большого количества наблюдений, особенно в клинических исследованиях третьей фазы и постмаркетинговых. Так, безопасность липиднормализующих препаратов (ЛНП) была исследована в сотнях исследований, отвечающих критериям доказательной медицины, с вовлечением десятков тысяч пациентов [3, 5]. Такой подход не всегда удается реализовать, например при разработке новых препаратов, особенно в первую и вторую фазу испытания лекарственных средств [4, с. 201]. Особенно актуальна проблема анализа безопасности лекарств на небольших выборках в настоящее время. Например, в условиях пандемии новой коронавирусной инфекции COVID-19 ученые, врачи должны экстренно разрабатывать и внедрять в клиническую практику новые методы лечения и профилактики при ограниченном количестве наблюдений на национальном [6], глобальном уровнях, делая сложный выбор по принципу «риск/польза».
Необходима разработка новых методов оценки безопасности лекарственных препаратов на основе одновременного анализа по нескольким показателям с учетом их взаимного влияния на небольшом количестве наблюдений с использованием анализа рисков неблагоприятных последствий. Для решения этих задач перспективным является энтропийно-вероятностное моделирование, представляющее собой синтез энтропийного и риск-анализа многомерных стохастических систем.
Цель исследования – разработать метод энтропийно-вероятностного анализа безопасности лекарственных средств и апробировать его на примере терапии липиднормализующими препаратами.
Материал и методы исследования
Энтропийно-вероятностное моделирование объединяет системно-энтропийный и риск-анализ многомерных стохастических систем. Основные этапы метода в упрощенном виде можно представить следующим образом.
Первый этап (системный анализ) – представление популяции как сложной, многомерной, вероятностной (стохастической), открытой и самоорганизующейся системы, представленной в виде случайного вектора (многомерной случайной величины) 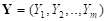 , где каждый элемент Yi – это показатель функционирования одной из подсистем организма. Для анализа выбираются наиболее важные подсистемы, характеризующиеся объективно измеримыми, желательно выраженными численно, показателями.
, где каждый элемент Yi – это показатель функционирования одной из подсистем организма. Для анализа выбираются наиболее важные подсистемы, характеризующиеся объективно измеримыми, желательно выраженными численно, показателями.
Второй этап (энтропийный анализ) – анализ поведения системы на основе определения ее энтропии. Энтропия является фундаментальным свойством любых открытых систем с неоднозначным, вероятностным поведением и представляет собой комплексную величину, характеризующую меру неупорядоченности (разброса, колеблемости составных элементов) и организованности (взаимной зависимости всех элементов) системы [7]. В упрощенном виде расчет энтропии можно представить следующим образом: Общая энтропия системы = сумма энтропий хаотичности подсистем + сумма энтропий самоорганизации подсистем, или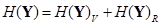 .
.
Подробно математическое обоснование формулы расчета дифференциальной энтропии H(Y) случайного вектора Y представлено в [7]. Формула расчета энтропии в кратком виде:
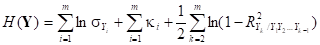 ,
,
где 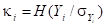 – энтропийный показатель типа закона распределения случайной величины Yi;
– энтропийный показатель типа закона распределения случайной величины Yi; 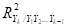 - индексы детерминации регрессионных зависимостей;
- индексы детерминации регрессионных зависимостей; 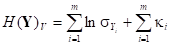 - энтропия хаотичности, а
- энтропия хаотичности, а 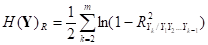 - энтропия самоорганизации. В целом, энтропия обладает триализмом и «существуют три причины изменения энтропии многомерной случайной величины Y: изменение степени рассеяния ее компонент, изменение форм распределений ее компонент и изменение тесноты корреляционных связей между ее компонентами» [7, с. 94]. Анализ энтропии по значимым подсистемам дает общее предварительное представление о системе, ее поведении без введения каких-то «искусственных» классифицирующих/ограничивающих параметров или характеристик. Первый и второй этапы являются частью системно-энтропийного анализа (СЭА). Пример использования СЭА в клинической медицине для оценки эффективности лекарственных средств представлен в [8].
- энтропия самоорганизации. В целом, энтропия обладает триализмом и «существуют три причины изменения энтропии многомерной случайной величины Y: изменение степени рассеяния ее компонент, изменение форм распределений ее компонент и изменение тесноты корреляционных связей между ее компонентами» [7, с. 94]. Анализ энтропии по значимым подсистемам дает общее предварительное представление о системе, ее поведении без введения каких-то «искусственных» классифицирующих/ограничивающих параметров или характеристик. Первый и второй этапы являются частью системно-энтропийного анализа (СЭА). Пример использования СЭА в клинической медицине для оценки эффективности лекарственных средств представлен в [8].
Третий этап – анализ системной энтропийной взаимосвязи. Системно-энтропийный подход позволяет на более глубоком уровне изучать взаимозависимости систем через вычисление энтропийной многомерной перекрестной корреляционной взаимосвязи между всеми элементами подсистем, например до и после лечения (или между разными системами), т.е. через расчет энтропийных коэффициентов системной взаимосвязи. Пусть X и Y – непрерывные случайные векторы (многомерные случайные величины), тогда энтропия взаимосвязи H(X ÇY) между X и Y равна [9]:
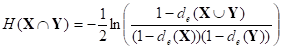 ,
,
где de(X), de(Y), de(XÈY) – коэффициенты тесноты совместной корреляционной связи X, Y, XÈY.
Если X° и Y° – гауссовские случайные векторы, то 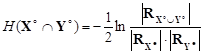 .
.
Четвертый этап. Риск-анализ (моделирование на основе анализа риска многомерной стохастической системы) основан на представлении медико-биосоциальной системы в виде случайного вектора с взаимозависимыми компонентами, характеризующимися определенными числовыми характеристиками. Применение этого метода позволяет дать на популяционном уровне, а также при обследовании небольшой по объему выборки количественную оценку риска здоровью через определение вероятности неблагоприятных исходов, абсолютных (количественно выраженных) значений риска. Данные характеристики определяются относительно оптимальных, пороговых и критических уровней каждой компоненты (например, показателей, характеризующих основные факторы риска). Вероятность неблагоприятного исхода P(D), т.е. перехода пациентов в «риск-зону» относительно пороговых, критических уровней показателей отдельных подсистем при учете их взаимной зависимости, определяется следующим образом: 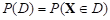 ,
, 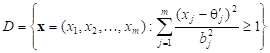 .
.
Более подробно методика и применение риск-анализа в профилактической медицине представлены в [10].
Риск-анализ имеет определенное сходство с СЭА, поскольку при его использовании также оцениваются рассеяние и взаимная коррелированность компонент. Однако, в отличие от СЭА, риск-анализ дает более точную, прикладную характеристику системы, поскольку она анализируется относительно исходно уже определенных характеристик (точек отсчета) – оптимальных, пороговых и критических в плане негативных последствий для системы значений. Эти значения могут задаваться на основе экспертных оценок, литературных данных (национальных клинических рекомендаций), данных предварительного обследования, относительно математического ожидания и др. Метод риск-анализа позволяет также оценить конкретный вклад компонент в негативные изменения системы.
Пятый этап – комплексная оценка системы на основе данных СЭА и риск-анализа. Анализируются показатели: общая энтропия с детализацией на энтропию хаотичности и самоорганизации, различные коэффициенты системной энтропийной взаимосвязи, вероятности неблагоприятного исхода и абсолютные значения риска.
Пример использования энтропийно-вероятностного (ЭВ) моделирования в клинической практике. Для практического применения ЭВ-анализа нами была взята клиническая группа пациентов, принимавших участие в открытом исследовании по сравнительной эффективности, безопасности различных ЛНП у пациентов с ишемической болезнью сердца. Исследование проводилось в 1997–2001 гг. Подробно характеристика групп клинического наблюдения представлена в [8]. Пациенты принимали препараты из группы статинов (аторвастатин, симвастатин, ловастатин, флувастатин), а также фибратов (ципрофибрат). Далее в статье группы пациентов обозначены по названию: «Аторвастатин», «Симвастатин», «Ловастатин», «Флувастатин», «Ципрофибрат». Средние дозы препаратов составили для групп: «Аторвастатин» – 8,6 мг, «Симвастатин» – 10,5 мг, «Ловастатин» – 17,0 мг, «Флувастатин» – 33,0 мг, «Ципрофибрат» – 100 мг. Ловастатин назначался в форме дженерика, остальные – в виде оригинальных лекарственных препаратов.
Гепатобилиарная система была выбрана для оценки безопасности липиднормализующих препаратов, поскольку одним из основных распространенных и клинически значимых побочных эффектов этих средств является гепатотоксичность [1, 3]. Подсистемы гепатобилиарной системы для оценки безопасности гиполипидемических препаратов представлены следующим образом: общий билирубин (значения приведены по Иендрашеку), ферменты аспартатаминотрансфераза (АСТ) и аланинаминотрансфераза (АЛТ) (значения приведены по методу Райтмана–Френкеля в ммоль/(ч·л.)). Эти показатели определялись до начала лечения ЛНП и через 1,5 месяца. Для анализа по этим показателям группы клинического наблюдения были случайным образом сокращены (в сравнении с данными, представленными в [8]), в том числе с целью анализа применения ЭВ-модели при малых выборках, до следующих значений: Аторвастатин – 14 человек, Симвастатин – 41 человек, Ловастатин – 30 человек, Флувастатин – 23 человека, Ципрофибрат – 18 человек. Эта выборка не отличалась по своим основным характеристикам (возрасту, средним уровням липидов и др.) от исходной группы. Термины «система», «подсистема» употребляются в статье, главным образом, в терминологии системного анализа.
Статистическая обработка результатов клинической части исследования проводилась с помощью пакета прикладных статистических программ Statistica 7. Сопоставимость исходных сформированных групп оценивали с помощью критерия множественных сравнений Краскелла–Уоллиса с последующим уточнением характера межгрупповых различий по U-критерию Манна–Уитни. Статистическую значимость различий оценивали с помощью t-критерия, построения доверительных интервалов, а также с использованием непараметрических методов – с помощью критерия Вилкоксона (для связанных групп), Манна–Уитни (для несвязанных групп). Различия считались достоверными при уровне значимости p<0,05. Форму распределения выборки проверяли на основе комплексной оценки с учетом ГОСТ Р ИСО 5479–2002.
Результаты исследования и их обсуждение
Для апробирования методики мы анализировали действие различных ЛНП (разные группы (статины, фибрат), оригинальные/неоригинальные препараты, статины разных поколений и др.), хорошо исследованных в плане безопасности применения в масштабных контролируемых исследованиях и в многолетней клинической практике, чтобы иметь возможность сопоставить результаты применения на малых выборках нового метода ЭВ-анализа с надежными литературными данными.
Изучение частоты побочных эффектов, сравнение по относительным показателям (например, доля лиц с повышением АСТ, АЛТ выше нормы) на столь малой выборке некорректны и малоинформативны, поскольку имеет место низкая вероятность обнаружения нечасто встречающихся событий. Так, незначительное повышение АЛТ при применении статинов возникает у 0,5–2,0% пациентов, причем чаще при применении более мощных статинов или высоких доз [3, с. 154]. Чтобы выявить такое отклонение (например, повышение уровня АЛТ у 1% пациентов), в соответствии с распространенным эмпирическим правилом необходимо было бы обследовать 300 пациентов («чтобы иметь высокую вероятность выявления события, встречающегося с частотой 1/n, необходимо обследовать 3×n пациентов» [4, с. 247]).
Статистически достоверное изменение средних значений показателей, характеризующих «безопасность гепатобилиарной системы» (общий билирубин, АСТ, АЛТ) при лечении липиднормализующими препаратами, также можно зафиксировать только при большом количестве наблюдений при использовании одномерного (по одной подсистеме) анализа. Мы провели предварительное сравнение средних показателей уровней АСТ, АЛТ, общего билирубина до и после лечения. По исходным уровням показателей исследуемые группы не отличались. Изменения уровней АСТ, АЛТ, общего билирубина не приняли статистически достоверного характера при использовании нами стандартных статистических методов (см. выше статистическую обработку результатов исследования) из-за малого числа наблюдений.
Таким образом, обычные статистические методы одномерного (по одной подсистеме) анализа не позволяют сделать на столь малой выборке какие-то, пусть даже предварительные, на уровне трендов, выводы об отличиях в гепатотоксичности ЛНП.
Применим ЭВ-анализ гепатобилиарной системы (здесь и далее гепатобилиарная система анализируется в плане гепатотоксичности ЛНП). Полагаем, что если препарат обладает гепатотоксичностью, пусть даже небольшой, то при терапии будет изменение соответствующих показателей гепатобилиарной системы. После применения ЭВ-анализа сравним полученные данные с литературными.
Первый этап. Для оценки безопасности ЛНП нами были выделены следующие подсистемы гепатобилиарной системы:
– общий билирубин (показатель пигментного обмена – маркер нарушения метаболизма желчных пигментов, повышается главным образом при паренхиматозной желтухе, при механической желтухе (за счет прямой фракции) [11]);
– ферменты АСТ и АЛТ – маркеры цитолиза гепатоцитов. Являются «прямыми» маркерами поражения печеночных клеток. В клинической практике широкое распространение получило совместное определение этих двух ферментов для диагностики заболеваний печени [11].
Определение этих показателей рекомендуется для контроля безопасности применения ЛНП в клинической практике [1, 3].
Второй этап (энтропийный анализ). При СЭА одновременно анализируются колеблемости всех вариантов подсистем (энтропия хаотичности) при их взаимной перекрестной зависимости (энтропия самоорганизации), в результате получается единая численно выраженная оценка системы на основе нового математического метода анализа. Результаты СЭА представлены в таблице 1.
Таблица 1
Результаты системно-энтропийного анализа гепатобилиарной системы по показателям «Общий билирубин», «АСТ», «АЛТ» до и после терапии липиднормализующими препаратами
|
Препарат |
Данные СЭА |
HV |
HR |
H |
DH |
d H |
|
Аторвастатин |
До лечения |
2,121 |
–0,333 |
1,787 |
–1,636 |
–91,6% |
|
После лечения |
0,372 |
–0,221 |
0,152 |
|||
|
Симвастатин
|
До лечения |
2,902 |
–0,086 |
2,817 |
0,413 |
14,7% |
|
После лечения |
3,406 |
–0,175 |
3,230 |
|||
|
Ловастатин |
До лечения |
2,496 |
–0,226 |
2,270 |
0,030 |
1,3% |
|
После лечения |
2,400 |
–0,101 |
2,299 |
|||
|
Флувастатин
|
До лечения |
2,567 |
–0,051 |
2,516 |
0,127 |
5,0% |
|
После лечения |
2,859 |
–0,216 |
2,643 |
|||
|
Ципрофибрат
|
До лечения |
1,561 |
–1,077 |
0,484 |
0,988 |
204,1% |
|
После лечения |
1,538 |
–0,066 |
1,472 |
Примечание: H(V) – энтропия хаотичности; H(R) – энтропия самоорганизации; H(Y) – общая энтропия системы; DH – изменение общей энтропии (в абсолютных значениях); d H – изменение общей энтропии (в %).
Анализ результатов, представленных в таблице 1, показал, что по «гипоэнтропийному» эффекту ЛНП распределились следующим образом (снижение энтропии от большего к меньшему в %): Аторвастатин – Ловастатин – Флувастатин – Симвастатин – Ципрофибрат. Разница между Ловастатином, Флувастатином, Симвастатином небольшая. Наиболее выраженное снижение энтропии среди статинов наблюдалось у Аторвастатина (снижение главным образом за счет энтропии хаотичности, система стала более стабильной), у остальных препаратов этой группы изменения были незначительными. Энтропия самоорганизации у статинов была в абсолютных значениях небольшой. Существенное увеличение энтропии в группе Ципрофибрата произошло за счет резкого увеличения энтропии самоорганизации (взаимосвязи между подсистемами стали слабее) при неизменных значениях энтропии хаотичности.
Третий этап (анализ системной энтропийной взаимосвязи (СЭВ)). В таблице 2 представлены значения коэффициентов системной энтропийной взаимосвязи (H(Y0ÇY1)) гепатобилиарной системы, которые показывают, есть ли какая-то взаимосвязь (корреляция) между гепатобилиарной системой (Y) до (Y0) и после (Y1) лечения на основе многомерного (по всем подсистемам одновременно) энтропийного корреляционного анализа. Преимущества использования системной энтропийной взаимосвязи перед одномерным корреляционным анализом (Спирмена или Пирсона): одновременный перекрестный анализ взаимосвязи между двумя множествами факторов (парный корреляционный анализ позволяет определить корреляцию только между двумя факторами; регрессионный анализ – только между одним фактором и множеством факторов); единая численно выраженная оценка взаимосвязи между системами; отсутствие необходимости учитывать характер распределения в каждой подсистеме; нет эффекта множественных сравнений. В таблице 2 также представлены результаты анализа многомерной энтропийной системной взаимосвязи между элементами липидной системы (X) (включает уровни общего холестерина, триглицеридов, холестерина липопротеинов высокой плотности) и гепатобилиарной системы (Y), изменяющимися при проявлении гепатотоксичного действия при терапии ЛНП. Возможность такого подхода к анализу безопасности ЛНП требует дополнительного изучения, здесь приводится для демонстрации возможностей метода.
Таблица 2
Показатели энтропийных коэффициентов системной взаимосвязи
|
Препарат |
H(X0ÇY0) |
H(X1ÇY1) |
dH(XÇY) |
DH(XÇY) |
H(Y0ÇY1) |
|
Аторвастатин |
0,403 |
0,135 |
–66,6% |
–0,269 |
0,244 |
|
Симвастатин |
0,287 |
0,157 |
–45,3% |
–0,130 |
0,218 |
|
Ловастатин |
0,443 |
0,644 |
45,6% |
0,202 |
0,203 |
|
Флувастатин |
0,358 |
0,196 |
–45,2% |
–0,162 |
0,275 |
|
Ципрофибрат |
0,369 |
0,393 |
6,5% |
0,024 |
0,540 |
Примечание: H(X0ÇY0) – энтропийный коэффициент системной взаимосвязи липидной и гепатобилиарной систем до начала лечения; H(X1ÇY1) – после лечения; DH(XÇY) = H(X1ÇY1) – H(X0ÇY0); dH(XÇY) = (H(X1ÇY1) – H(X0ÇY0)) / H(X0ÇY0) × 100 %; H(Y0ÇY1) – коэффициент системной энтропийной взаимосвязи гепатобилиарной системы до (Y0) и после (Y1) терапии липиднормализующими препаратами.
Анализ данных таблицы 2. В группе статинов после лечения взаимосвязи между липидной и гепатобилиарной системой существенно выросли в группе Ловастатина (+45,6%) в сравнении со снижением в других группах, что, возможно, отчасти обусловлено меньшим липиднормализующим эффектом Ловастатина [8] и/или потенциально большей гепатотоксичностью. В группе Ципрофибрата незначительно вырос показатель dH(XÇY). Если бы ЛНП не оказывали какого-либо действия на показатели АСТ, АЛТ, общего билирубина, то не было бы никакой корреляции (взаимосвязи) между этими показателями до и после лечения. Данные анализа СЭВ показывают существенно более высокий показатель H(Y0ÇY1) для Ципрофибрата (0,540) – этот коэффициент в 2–2,5 раза выше, чем в группе статинов. Характер этой взаимосвязи (изменение в лучшую или худшую сторону) будет определен после этапа риск-анализа. Определение достоверности различий требует дополнительного математического обоснования, тем не менее, столь высокая разница не может быть случайной исходя из формулы (см. выше по тексту) определения СЭВ.
Четвертый этап. Риск-анализ безопасности гиполипидемических препаратов. В таблице 3 представлены оптимальные, пороговые, критические уровни АСТ, АЛТ, общего билирубина. Принципы определения уровней для риск-анализа изложены в [10] и выше по тексту.
Таблица 3
Оптимальные, пороговые, критические уровни АСТ, АЛТ, общего билирубина для проведения риск-анализа гепатобилиарной системы
|
Показатель |
Нижний критический уровень |
Нижний пороговый уровень |
Оптимальный уровень |
Верхний пороговый уровень |
Верхний критический уровень |
|
Общий билирубин (мкмоль/л) |
1,0 |
3,4 |
11,95 |
20,5 |
32,5 |
|
АСТ (ммоль/ч·л) |
0,01 |
0,1 |
0,275 |
0,45 |
1,35 |
|
АЛТ (ммоль/ч·л) |
0,01 |
0,1 |
0,39 |
0,68 |
2,04 |
Для общего билирубина верхний и нижний пороговые уровни определены как границы нормы [12]. Верхний критический уровень общего билирубина определен в 32,5 мкмоль/л, поскольку с этих значений внешне (сначала на склерах, затем на кожных покровах) становится заметным желтушное окрашивание [11]. Оптимальный уровень – среднее между границами нормы. Для ферментов АСТ и АЛТ верхний критический уровень определен как трехкратное превышение нормы, поскольку этот уровень обозначен как показание для отмены статинов [1, 3]. Верхний и нижний пороговые уровни определены как границы нормы [12]. Оптимальный уровень – среднее между границами нормы.
Определив оптимальные, пороговые и критические уровни параметров гепатобилиарной системы, мы по методике риск-анализа многомерных стохастических систем [10] рассчитываем до и после лечения вероятности неблагоприятных (в плане гепатотоксичности) исходов (P(D)) и абсолютные значения риска (r(Y)) (показывают, насколько «далеко заходит» в зону риска система). Данные представлены в таблице 4.
Таблица 4
Результаты риск-анализа гепатобилиарной системы по показателям «Общий билирубин», «АСТ», «АЛТ» до и после терапии липиднормализующими препаратами
|
Препарат |
P(D) |
DP(D) |
dP(D), % |
r(Y) |
Dr(Y) |
dr(Y), % |
||
|
Исходный уровень |
После лечения |
Исходный уровень |
После лечения |
|||||
|
Аторвастатин |
0,899 |
0,915 |
0,016 |
1,8 |
3,33 |
3,46 |
0,13 |
3,9 |
|
Симвастатин |
0,884 |
0,797 |
–0,087 |
–9,8 |
3,08 |
2,60 |
0,48 |
–15,6 |
|
Ловастатин |
0,874 |
0,960 |
0,086 |
9,8 |
3,05 |
3,27 |
0,22 |
7,2 |
|
Флувастатин |
0,940 |
0,862 |
–0,078 |
–8,3 |
3,33 |
2,80 |
0,53 |
–16,1 |
|
Ципрофибрат |
0,753 |
0,883 |
0,130 |
17,3 |
2,85 |
2,96 |
0,11 |
3,9 |
Примечание: P(D) – вероятность неблагоприятного (в плане гепатотоксичности) исхода (значения от 0 до 1; при умножении на 100 вероятность P(D) будет выражена в %); DP(D) – разница P(D) до и после лечения; dP(D) – разница абсолютных значений P(D) до и после лечения относительно исходного уровня в %; r(Y) – абсолютные значения риска; D r(Y) – разница абсолютных значений риска до и после лечения; d r(Y) – разница абсолютных значений риска до и после лечения относительно исходного уровня в %.
Высокие уровни P(D) и абсолютного риска обусловлены тем, что мы изначально выбрали низкие (более жесткие) пороговые и критические уровни. Но при анализе важно изменение – главное, чтобы после терапии показатели существенно не увеличились.
Анализ результатов, представленных в таблице 4, показал, что в группе статинов по материалам риск-анализа неблагоприятные показатели гепатотоксичности выявлены в группе Ловастатин – рост вероятности неблагоприятного (в плане гепатотоксичности) исхода на 9,8% при увеличении абсолютного риска на 7,2%. Из исследованных препаратов наихудший показатель безопасности в плане гепатотоксичности установлен в группе Ципрофибрат – рост P(D) 17,3% при незначительном росте абсолютного риска.
Пятый этап (комплексная оценка системы на основе данных СЭА и риск-анализа) – результаты представлены в разделе «Выводы» (см. ниже по тексту).
В целом полученные данные энтропийно-вероятностного анализа о худших показателях гепатотоксичности Ловастатина и Ципрофибрата совпадают с литературными. Риск нарушения функции печени при лечении статинами в невысоких дозировках остается низким [3, 5], «все изученные ингибиторы редуктазы имели сходную переносимость. Не было никаких случаев стойкого повышения уровня сывороточных трансаминаз…» [13]. Выявленные нами различия среди статинов по потенциальной гепатотоксичности обусловлены, видимо, тем, что Ловастатин был единственным неоригинальным препаратом, а дженерики могут отличаться по эффективности и безопасности от оригинального препарата [14, с. 140]. Наихудшие показатели по гепатотоксичности обнаружены у Ципрофибрата как по результатам СЭА (наибольший прирост общей энтропии, коэффициента системной энтропийной взаимосвязи), так и по результатам риск-анализа. В целом фибраты в сравнении со статинами обладают худшей переносимостью – отказ от лечения из-за побочных эффектов достигает 5% [15]. Повышение уровня печеночных ферментов, холелитиаз являются наиболее известными нежелательными явлениями, связанными с действием фибратов [2, 3]. «Усиление литогенности желчи, видимо, общегрупповое свойство фибратов» [15, с. 228], вследствие чего наиболее реальными осложнениями являются образование камней в желчном пузыре и иные нарушения гепатобилиарной системы, хотя это в меньшей степени характерно для Ципрофибрата [14].
Сделать сравнение проведенного нами исследования с данными других зарубежных и российских исследователей не представляется возможным, поскольку метод энтропийно-вероятностного анализа новый и в литературе такой подход для анализа медико-биосоциальных систем не описан. Данные наших исследований по применению системно-энтропийного и риск-анализа в профилактической медицине представлены в [8, 9, 10].
При анализе гепатотоксичности для демонстрации возможностей ЭВ-анализа были использованы показатели, характеризующие пигментный обмен (общий билирубин), клеточный цитолиз (АСТ, АЛТ). Определение этих параметров используется в соответствии с национальными и иными рекомендациями для контроля терапии ЛНП [1, 3]. В комплексный анализ гепатотоксичности препаратов можно включить и иные показатели, например характеризующие холестаз (щелочная фосфатаза и др.). В рамках данной работы мы на малом числе наблюдений рассмотрели только один сегмент анализа такого широкого понятия, как безопасность лекарственных средств. В целом, в комплексную оценку безопасности терапии ЛНП можно включить другие параметры, характеризующие рабдомиолиз (креатинфосфокиназа), показатели побочных эффектов, которые не определяются количественно, т.е. жалобы (диспепсические явления и др.), – метод ЭВ-моделирования позволяет это сделать после квантификации (сведения качественных характеристик к количественным).
Использование энтропийно-вероятностного анализа позволяет выявить неблагоприятные побочные эффекты лекарственной терапии при небольших изменениях изучаемых параметров с учетом их взаимной коррелированности (в том числе на малых выборках пациентов) и получить единую численно выраженную характеристику безопасности лекарственных средств. Мы полагаем, что использованный нами метод энтропийно-вероятностного анализа имеет универсальное значение и может быть использован в целом для оценки безопасности лекарственных средств.
Выводы
Выводы по результатам энтропийно-вероятностного анализа терапии липиднормализующими препаратами по параметрам, характеризующим гепатобилиарную систему (общий билирубин, АСТ, АЛТ):
1. Изменение общей энтропии (в %) составило: для Аторвастатина –91,6, для Симвастатина +14,7, для Ловастатина +1,3, для Флувастатина +5,0, для Ципрофибрата +204,1. На изменение общей энтропии в группе статинов повлияла в основном энтропия хаотичности, в группе ципрофибрата – главным образом энтропия самоорганизации.
2. Коэффициенты системной энтропийной взаимосвязи составили: для Аторвастатина – 0,244, для Симвастатина – 0,218, для Ловастатина – 0,203, для Флувастатина – 0,275, для Ципрофибрата – 0,540.
3. Изменение вероятности неблагоприятного исхода (в %) и абсолютного риска (приведены в скобках в %) составило: для Аторвастатина +1,6 (+3,9), для Симвастатина –9,8 (–15,6), для Ловастатина +9,8 (+7,2), для Флувастатина –8,3 (–16,1), для Ципрофибрата – +17,3 (+3,9).
4. Неблагоприятные изменения гепатобилиарной системы после терапии липиднормализующими препаратами (рост общей энтропии, увеличение вероятности неблагоприятного исхода при росте абсолютного риска, высокие коэффициенты системной энтропийной взаимосвязи) выявлены для Ципрофибрата и Ловастатина.
5. Разработан метод энтропийно-вероятностного анализа безопасности лекарственных средств, который объединяет системно-энтропийный и риск-анализ многомерных стохастических систем. На этапе предварительной оценки этот метод можно использовать даже при небольшом числе наблюдений.
Работа выполнена при поддержке РФФИ (грант № 20-51-00001).
Библиографическая ссылка
Яшин Д.А., Тырсин А.Н. ЭНТРОПИЙНО-ВЕРОЯТНОСТНЫЙ АНАЛИЗ БЕЗОПАСНОСТИ ЛЕКАРСТВЕННЫХ СРЕДСТВ НА ПРИМЕРЕ ТЕРАПИИ ЛИПИДНОРМАЛИЗУЮЩИМИ ПРЕПАРАТАМИ // Современные проблемы науки и образования. 2021. № 2. ;URL: https://science-education.ru/ru/article/view?id=30614 (дата обращения: 08.04.2026).
DOI: https://doi.org/10.17513/spno.30614



