Ожоговая септикотоксемия, развитие которой связано с инфекционными осложнениями при ожоговой болезни, продолжает оставаться одной из основных проблем, возникающих при лечении ожоговой травмы [1]. Это связано с тем, что при ожоговой септикотоксемии разворачивается целый каскад реакций, связанных с выраженной интоксикацией в сочетании с иммунодепрессией, при которых подавлены клеточные механизмы иммунитета, что способствует развитию системного воспалительного ответа, гемодинамических и микроциркуляторных расстройств [2].
Несмотря на совершенствование современных методов оказания специализированной комбустиологической помощи пострадавшим с тяжелой термической травмой, именно инфекционные осложнения в период развития ожоговой септикотоксемии являются ведущей причиной летальности этой категории пациентов [1, 2].
Следует отметить, что трудности в оказании эффективной медицинской помощи вызваны сложностями проведения антибактериальной терапии при устойчивости патогенной флоры к используемым лекарственным препаратам, что часто связано с госпитальными штаммами микрооранизмов, таких как протей, синегнойная палочка, стафилококк, кишечная палочка, а также их комбинации. При инфицировании обширных глубоких ожоговых ран бактериальной флорой, устойчивой к антибиотикам, возникает не поддающееся антибактериальной терапии гнойное воспаление с развитием тяжелой ожоговой септикотоксемии, которая может протекать по типу гнойно-резорбтивной лихорадки.
Тяжелое течение ожоговой септикотоксемии вызывает развитие дистрофических и некробиотических изменений органов с формированием полиорганной недостаточности. При этом одним из органов-мишеней при септикотоксемии является сердце.
Настоящее исследование было проведено с целью выявления механизмов, лежащих в основе микроциркуляторных расстройств миокарда при септикотоксемии и приводящих к снижению сократительной способности миокарда левого желудочка. Для этого необходимо было провести оценку ультраструктуры и анализ транспортных функций эндотелиальных клеток кровеносных капилляров миокарда различных отделов левого желудочка сердца у пациентов с ожоговой септикотоксемией.
Цель исследования – провести оценку патоморфологических изменений миокарда и ультраструктуры эндотелиоцитов кровеносных капилляров мышцы сердца различных отделов левого желудочка сердца при ожоговой септикотоксемии.
Материалы и методы исследования. Исследуемые наблюдения включали 32 случая смерти от ожоговой септикотоксемии, средний возраст составил 39±4,5 года. В качестве контрольной группы был использован материал от пяти трупов лиц, умерших от «острой коронарной смерти», средний возраст которых 41±5,5 года. Выбор материала контроля был связан с тем, что у скоропостижно умерших были выявлены минимальные поражения венечных артерий атеросклерозом в стадии липоидоза и липосклероза, а при судебно-гистологическом исследовании атеросклеротический кардиосклероз проявлялся незначительно.
Полученный материал фиксировали в 10%-ном забуференном формалине (Biovitrum, Россия) в течение 24 ч, затем производили стандартную проводку материала в гистопроцессоре (STP200, Leica, Германия). На ротационном микротоме из образцов, заключенных в парафин, получали срезы толщиной около 5 мкм, которые окрашивали гематоксилином и эозином. Поляризационно-микроскопическое исследование проводили на универсальном микроскопе Leica DM 4000B, который был оснащен встраиваемыми анализатором и поляризатором. Для фотографирования использованы цифровая фотокамера Leica DFC 320 и компьютерная программа Leica QWin. Для поляризационной микроскопии использовали окрашенные гематоксилином и эозином и неокрашенные срезы.
Материал для электронно-микроскопического исследования был получен от 5 трупов лиц, умерших от ожоговой септикотоксемии (4 мужчин, 1 женщина), и 3 трупов – при скоропостижной смерти от острой коронарной недостаточности в процессе ранней аутопсии через 2 ч после наступления биологической смерти в танатологическом отделе ГБУЗ НСО «Новосибирское областное клиническое бюро судебно-медицинской экспертизы». Забор кусочков миокарда производился из области передней, задней и боковой стенок левого желудочка сердца.
Таким образом, в ходе проведения работы была выполнена качественная и количественная оценка патоморфологических изменений миокарда левого желудочка и ультраструктуры эндотелиоцитов мышцы сердца. Для электронно-микроскопического исследования фрагменты миокарда размером до 1 мм3 фиксировали в 4%-ном растворе параформальдегида, приготовленном на среде Хенкса, с последующей дополнительной дофиксацией в течение 1 ч в 1%-ном растворе ОsO4 на фосфатном буфере (pH=7,4). После этого исследуемый материал дегидратировали в растворах этилового спирта возрастающей концентрации, начиная с 30%-ного до 100%-ного раствора, заливали эпоксидной смолой «Epon» (Serva, Германия). Из блоков готовили полутонкие срезы толщиной около 1 мкм на ультратоме Leica UC7/FC7 (Германия/Швейцария), окрашивали толуидиновым синим. Затем проводили выборку определенных участков сердечной мышцы для ультраструктурного исследования под световым микроскопом Leica DME. Следующим этапом полученные ультратонкие срезы толщиной 70–100 нм контрастировали насыщенным водным раствором уранилацетата и цитратом свинца. В электронном микроскопе JEM 1400 (Япония) получали цифровые микрофотографии фрагментов цитоплазмы эндотелиоцитов кровеносных капилляров миокарда при увеличении х30000. Электронограммы морфометрировали с помощью компьютерной программы Image J. Определяли объемные плотности везикулярных структур, мультивезикулярных телец, митохондрий, цистерн гранулярной эндоплазматической сети, аутофагосом, аутолизосом, липидов при использовании открытой тестовой системы с шагом 60 нм. Полученные результаты были обработаны с использованием пакета программ STATISTICA v. 6 (StatSoftInc., США). Различия независимых выборок оценивали с помощью U-критерия Манна–Уитни, считали достоверными при p<0,05.
Результаты исследования и их обсуждение. При микроскопическом исследовании во всех случаях ожоговой септикотоксемии были обнаружены острые расстройства кровообращения в виде сладжа эритроцитов и выраженного отека стромы. Наблюдалось чередование участков волнообразной деформации мышечных волокон и выраженной фрагментации кардиомиоцитов. Наряду с описанными изменениями были выявлены очаги кровоизлияний и в ряде полей зрения – фибриновые микротромбы. Кроме того, местами просматривалась лейкоцитарная инфильтрация миокарда, встречались участки мононуклеарной инфильтрации сердечной мышцы. Исследование срезов в поляризованном свете позволяло выявить острые очаговые повреждения кардиомиоцитов в виде множественных контрактур I, II и III степени. Кроме того, в некоторых полях зрения в кардиомиоцитах отсутствовала анизотропия, связанная с миоцитолизисом. Описанные патоморфологические изменения были более выражены в субэндокардиальных отделах левого желудочка сердца.
Электронно-микроскопическое исследование эндотелиоцитов при ожоговой септикотоксемии позволило выявить ультраструктурные изменения эндотелия кровеносных капилляров. В передней и задней стенках левого желудочка отмечали более выраженный отек цитоплазмы и органелл, чем в боковой стенке (рис. 1). Набухание митохондрий и гранулярной эндоплазматической сети было обнаружено во всех трех отделах миокарда левого желудочка, которые достоверно не отличались от величин контрольной группы.
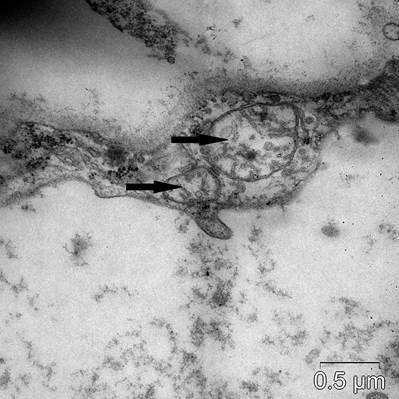
Рис. 1. Набухание митохондрий в зоне передней стенки левого желудочка при ожоговой септикотоксемии (стрелки)
При ультраструктурном стереологическом анализе сердечной мышцы умерших от ожоговой септикотоксемии было выявлено снижение суммарной объемной плотности везикулярных структур, которая складывалась из объемных плотностей люминальных, аблюминальных кавеол и транспортных везикул, отвечающих за транспортные и обменные процессы в клетке. В эндотелиоцитах передней стенки левого желудочка наблюдалось уменьшение объемной плотности этих органелл на 70,8%, в задней стенке – на 42,4%, в боковой стенке – на 30,6% по сравнению с контрольной группой.
При морфометрии объемной плотности мультивезикулярных телец при ожоговой септикотоксемии обращало на себя внимание их значительное увеличение. Наибольшая объемная плотность мультивезикулярных телец отмечалась в эндотелиальных клетках кровеносных капилляров миокарда задней стенки левого желудочка (рис. 2). В передней стенке объемная плотность мультивезикулярных телец была на 27,7% меньше, чем в задней стенке, а в боковой – на 64,8%.
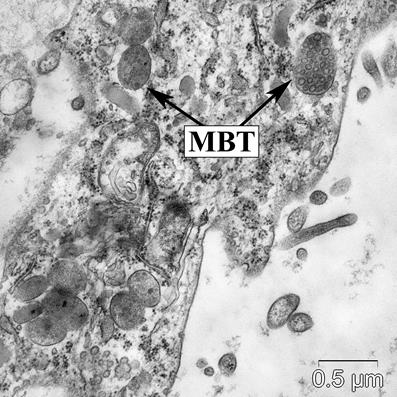
Рис. 2. Везикулярный транспорт в эндотелиальных клетках кровеносных капилляров миокарда задней стенки левого желудочка ожоговых пациентов. Примечание: МВТ – мультивезикулярное тельце
В эндотелиоцитах кровеносных капилляров миокарда левого желудочка у пациентов с ожоговой септикотоксемией было обнаружено накопление липидных включений в цитоплазме. Объемная плотность липидов была максимальной в боковой стенке левого желудочка, в задней на 31,1% меньше, в передней на 56,5% относительно боковой стенки. В эндотелиальных клетках наблюдали признаки выраженной активации аутофагии. Так, показатель объемной плотности аутофагосом в боковой стенке левого желудочка сердца умерших от ожоговой септикотоксемии был в 13 раз больше, чем в контрольной группе (рис. 3). При сравнении с боковой стенкой объемная плотность аутофагосом в задней стенке была меньше на 43,8%, а в передней стенке – на 51,2%. В аутофагосомах можно было идентифицировать фрагменты цитоплазмы, митохондрий, везикулярных структур и липидов. При ультраструктурном анализе миокарда наибольшее содержание аутолизосом было обнаружено в эндотелиоцитах кровеносных капилляров передней стенки левого желудочка, в области боковой стенки на 30,3% меньше, чем в передней, а в капиллярах задней стенки – на 37,8% меньше.
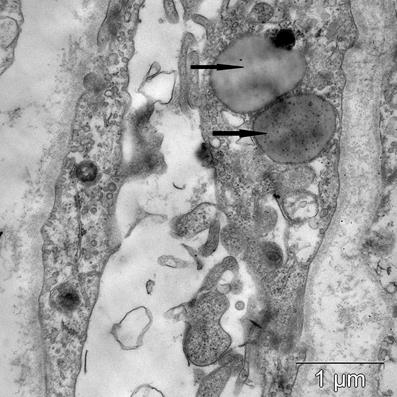
Рис. 3. Липофагия в боковой стенке левого желудочка (стрелки)
Таким образом, выявленные ультраструктурные изменения эндотелиоцитов кровеносных капилляров миокарда левого желудочка умерших от ожоговой болезни в период септикотоксемии в виде набухания цитоплазмы и органелл, а также снижения объемной плотности везикулярных структур, возможно, обусловлены интоксикацией и воспалительным ответом, наблюдаемыми при ожоговой септикотоксемии.
По нашему мнению, выявленные изменения были связаны с тем, что, являясь механизмом внутриклеточной системы деградации органелл, цитоплазмы, белков и макромолекул, базальная аутофагия необходима для поддержания клеточного гомеостаза и нормального функционирования клетки [3, 4]. Аутофагия может развиваться в ответ на гипоксическое или токсическое влияние, а также при повреждениях ДНК. При этом процесс удаления поврежденных органелл, метаболитов белков, патогенных микроорганизмов является компенсаторным внутриклеточным механизмом, позволяющим избежать гибели клетки [5]. На современном этапе появились данные, согласно которым нарушение процесса аутофагии играет важную роль в патогенезе ряда заболеваний, в том числе при патологии органов системы кровообращения [6].
Известно, что развитие воспаления или заболеваний органов системы кровообращения сопровождается клеточным и плазменным окислительным стрессом, которое приводит к накоплению липидов в субэндотелиальном пространстве [7, 8]. Располагаясь на границе внеклеточного матрикса и крови, эндотелиоциты способны поглощать липиды при рецептор-опосредованном эндоцитозе [9, 10], поэтому выявленная липофагия в эндотелиальных клетках кровеносных капилляров миокарда пострадавших с ожоговой септикотоксемией следует рассматривать как реакцию организма на развитие эндотелиальной дисфункции при ожоговой болезни, так же как резорбцию липидов в лизосомах.
С учетом вышеизложенного можно заключить, что активное развитие аутофагии в эндотелиоцитах кровеносных микрососудов миокарда левого желудочка человека при ожоговой септикотоксемии является важным компенсаторным внутриклеточным механизмом реагирования эндотелия на гипоксическое и токсическое воздействие при ожоговой септикотоксемии.
При оценке выявленных изменений следует отметить, что более выраженные патоморфологические изменения кардиомиоцитов и эндотелиоцитов капилляров наблюдались в передней стенке миокарда левого желудочка, что, вероятно, может быть связано с особенностями кровоснабжения данной области сердца.
Таким образом, в результате проведенного морфологического исследования посредством световой микроскопии в случаях ожоговой септикотоксемии были обнаружены острые расстройства кровообращения миокарда в виде сладжа эритроцитов, выраженного отека стромы, очагов кровоизлияний и образования фибриновых микротромбов. Патоморфологические изменения миокарда были связаны с образованием участков чередования волнообразной деформации мышечных волокон и выраженной фрагментации кардиомиоцитов, острыми очаговыми повреждения кардиомиоцитов в виде множественных контрактур I, II и III степени и миоцитолизиса, которые были более выраженными в субэндокардиальных отделах левого желудочка сердца. Кроме того, местами просматривалась лейкоцитарная инфильтрация миокарда, встречались участки мононуклеарной инфильтрации сердечной мышцы.
При ультраструктурном стереологическом анализе были выявлены изменения эндотелиоцитов кровеносных капилляров миокарда левого желудочка в виде набухания цитоплазмы и органелл, а также снижение объемной плотности везикулярных структур, развитие которых при ожоговой септикотоксемии было обусловлено интоксикацией и воспалительным ответом. Выявленные структурные изменения были более выражены в передней и задней стенках левого желудочка сердца. Кроме того, в эндотелиальных клетках была отмечена значительная активация аутофагии, которую следует рассматривать как компенсаторный внутриклеточный механизм при гипоксическом и токсическом воздействии в случаях развития ожоговой септикотоксемии.
Заключение. Морфологическое исследование мышцы сердца миокарда при ожоговой септикотоксемии на тканевом уровне позволило выявить острые расстройства кровообращения и очаговые повреждения миокарда в области передней боковой и задней стенок левого желудочка сердца, более выраженные в субэндокардиальных отделах. При этом не было выявлено превалирования статистически значимых патоморфологических изменений в каком-то определенном из изучаемых отделов сердца. Выявленные при ультраструктурном исследовании эндотелиальных клеток кровеносных капилляров миокарда морфологические признаки снижения транспортных функций эндотелия и активации внутриклеточной деградации были более выраженными в передней и боковой стенках левого желудочка. Полученные данные позволяют расширить понимание механизмов альтерации эндотелия и развития сократительной недостаточности миокарда левого желудочка для последующей разработки кардиопротекции при лечении пациентов с ожоговой септикотоксемией.
Библиографическая ссылка
Савченко С.В., Гребенщикова А.С., Бгатова Н.П., Таскаева Ю.С., Летягин А.Ю., Новоселов В.П. ПАТОМОРФОЛОГИЯ МИОКАРДА И УЛЬТРАСТРУКТУРА ЭНДОТЕЛИОЦИТОВ КРОВЕНОСНЫХ КАПИЛЯРОВ МЫШЦЫ СЕРДЦА ПРИ ОЖОГОВОЙ СЕПТИКОТОКСЕМИИ // Современные проблемы науки и образования. 2021. № 1. ;URL: https://science-education.ru/ru/article/view?id=30497 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/spno.30497



