Для раскрытия невыясненных механизмов возникновения и развития пародонтита, распространенность которого достигает 98% [1], широко используется его моделирование на лабораторных животных. Этот метод, в отличие от клинических исследований, позволяет получить детализированные объективные данные о патогенезе данного процесса и оценить защитные эффекты разнообразных способов профилактики и лечения пародонтита, в том числе и c помощью фармакологических препаратов. Следует подчеркнуть, что экспериментальное моделирование заболевания является необходимым и обязательным этапом внедрения новых лекарственных средств и способов лечения в клиническую практику [2].
В предшествующих исследованиях [3, 4] был выяснено, что такие иммуномодуляторы, как трекрезан (оксиэтиламмония метилфеноксиацетат), полиоксидоний (азоксимера бромид) и метапрот (моногидрат этилтиобензимидазол гидробромид), при воспроизведении у животных экспериментального пародонтита (ЭП) оказывают выраженное протективное действие и способны предупреждать структурно-функциональные изменения в тканях пародонта.
Среди механизмов, которые становятся ведущими в патогенезе пародонтита, отмечены нарушения энергетического баланса, повреждения тканей за счет избыточной пероксидации и развития вторичного иммунодефицита. Иммунный ответ в больном организме определяется пока недостаточно изученной кооперацией различных систем организма, в которой наблюдаются процессы дизрегуляции [5]. Взаимосвязь между этими системами осуществляют различные виды цитокинов [6]. При развитии воспаления отмечается формирование воспалительных цитокинов: интерлейкина-1β (ИЛ-1β), фактора некроза опухоли-α (ФНОα), интерлейкина-6 (ИЛ-6). Однако выраженность цитокиновой секреции и ее презентация зависят от вида патогенетического фактора и тоже изучены не в полной мере. Несмотря на ограниченный жизненный цикл, провоспалительные цитокины обладают высокой агрессивностью в отношении клеток хозяина. Окончание их продукции происходит во многом за счет действия антивоспалительных цитокинов, осуществляющих торможение синтеза или инактивацию провоспалительных факторов. В основном это интерлейкин-4 (ИЛ-4), интерлейкин-10 (ИЛ-10), интерлейкин-13 (ИЛ-13) и некоторые другие. Баланс между про- и антивоспалительными цитокинами является важным компонентом патогенеза, определяющим выраженность патологических реакций, и прогностически значим для определения исхода воспаления.
Целью проведенного исследования явилось изучение закономерностей изменений соотношения про- и противовоспалительных цитокинов в сыворотке крови крыс при моделировании пародонтита и корригирующем воздействии иммуномодулирующих препаратов.
Материал и методы исследования. Данное исследование проведено в Военно-медицинской академии им. С.М. Кирова (лаборатория кафедры фармакологии) с соблюдением этических норм согласно Европейской конвенции по защите позвоночных животных, используемых в экспериментальных и научных целях (Страсбург, 1986), и одобрено этическим комитетом Военно-медицинской академии им. С.М. Кирова МО РФ.
Эксперименты проведены на 82 крысах-самцах (линия Вистар) массой 200–250 г сопоставимого возраста. Все крысы были разделены на 5 групп: 1-я группа (n=18) – контроль; 2-я группа (n=16) – моделирование ЭП; 3-я группа (n=15) – ЭП + полиоксидоний 0,75 мг/кг; 4-я группа (n=17) – ЭП + трекрезан 25 мг/кг; 5-я группа (n=16) – ЭП + метапрот 25 мг/кг. Экспериментальный асептический пародонтит воспроизводили животным путем инъекции по 0,15 мл 2%-ного водного раствора формальдегида (однократно) на уровне нижних коренных зубов в наружную часть десны с обеих сторон [7]. Введение формальдегида осуществлялось под эфирным наркозом. Контрольные животные получали инъекции физиологического раствора (0,9% NaCl) такого же объема, как и животные других групп.
На месте введения формальдегида через сутки развивалось выраженное воспаление тканей пародонта. Воспалительные изменения сохранялись до 2 недель. На 3-й день от начала эксперимента животным внутрибрюшинно в течение 5 дней ежедневно вводили один из иммуномодуляторов (полиоксидоний 0,75 мг/кг, трекрезан или метапрот по 25 мг/кг) или физиологический раствор (контроль). На 7-й день от начала эксперимента, соответствующий острому периоду ЭП [8], животных умерщвляли декапитацией, производили забор крови с центрифугированием (2500 об/мин, температура +4ºC, 20 мин) и выделением сыворотки. Замороженную сыворотку до тестирования хранили при отрицательной температуре (–20ºC). Концентрацию цитокинов определяли методом протонного мультиплексного анализа с использованием проточной иммунофлюориметрии [6] на анализаторе Bio-рlex Protein Assau System, Bio-Rad Laboratories (США). Использовали, согласно инструкции изготовителя, коммерческие наборы Milliplex Map Rat Citokine/Chemokine (Merk Millipore). Основой метода являются специфическая связь цитокинов с твердой фазой в виде суспензии гранул с флуоресцентной меткой и конъюгирование с сопоставимыми моноклональными антицитокиновыми антителами. С помощью проточного флуориметра производили оценивание результатов путем автоматического разделения гранул по специфическому свечению меток. Используя компьютерную программу «Bio-plex Manager», автоматически высчитывали в тестируемых образцах с помощью стандартных калибровочных разведений концентрацию исследуемых цитокинов. Результат выражали в пикограммах/мл (пг/мл).
Статистическая обработка полученных данных была произведена с помощью пакета STATISTICA 6, США. Для определения близости к нормальному закону распределения использовали критерии согласия Колмогорова–Смирнова с поправкой Шапиро–Уилка. При статистической обработке результатов применены критерии U-Манна–Уитни и t-Стьюдента. Достоверным считали различие при уровне значимости 95% (p<0,05) в сравниваемых группах. Данные представлены в виде среднего арифметического (М) и среднеквадратичной ошибки среднего арифметического (m).
Результаты исследования и их обсуждение. Развитие острой стадии (фазы) экспериментального пародонтита, вызванного введением формалина в ткань десны, привело к значительным трансформациям уровня цитокинов в крови крыс (табл. 1). Это отражает как местную, так и системную реакцию организма на воспаление [9].
Таблица 1
Изменения содержания цитокинов при экспериментальном пародонтите и введении иммуномодуляторов в сыворотке крови крыс (M±m)
|
Цитокины пг/мл |
Контроль |
ЭП |
ЭП + полиоксидоний |
ЭП + трекрезан |
ЭП + метапрот |
|
Группы крыс |
1-я группа |
2-я группа |
3-я группа |
4-я группа |
5-группа |
|
ИЛ-1β |
0,12±0,03 |
0,61±0,07* |
0,21±0,03** |
0,26±0,04*/** |
0,30±0,015*/** |
|
ФНОα |
3,1±0,5 |
14,2±1,4* |
4,8±0,6** |
5,2±0,5*/** |
5,8±0,6*/** |
|
ИЛ-2 |
0,39±0,06 |
0,28±0,04 |
0,51±0,06** |
0,48±0,05*/** |
0,34±0,03 |
|
ИНФγ |
0,2±0,04 |
0,39±0,05* |
0,6±0,05*/** |
0,48±0,05* |
0,41±0,05* |
|
ИЛ-4 |
0,16±0,03 |
0,20±0,03 |
0,72±0,08*/** |
0,59±0,06*/** |
0,51±0,05*/** |
|
МСР-1 |
2,4±0,5 |
3,9±0,4* |
2,9±0,3 |
2,85±0,3** |
3,2±0,07 |
|
ИЛ-6 |
0,31±0,05 |
1,06±0,14* |
0,49±0,06*/** |
0,61±0,06*/** |
0,7±0,08*/** |
|
ИЛ-10 |
0,12±0,03 |
0,25±0,02* |
0,98±0,1 */** |
0,41±0,05*/** |
0,61±0,05*/** |
|
ИЛ-12 (р70) |
0,34±0,07 |
0,31±0,04 |
0,56±0,06*/** |
0,85±0,08** |
0,41±0,04 |
|
ИЛ-13 |
0,09±0,002 |
0,24±0,03* |
0,42±0,01*/** |
0,48±0,04*/** |
0,38±0,02*/** |
|
ИЛ-17А |
1,8±0,4 |
2,1±0,3 |
1,9±0,2 |
1,8±0,2 |
2,0±0,3 |
Примечание. * – различия значимы (p<0,05) при сравнении с соответствующими показателями в группе контроля (1-я группа); ** – различия значимы (p<0,05) при сравнении с соответствующими показателями в 3-й, 4-й, 5-й группах крыс по отношению к группе крыс с экспериментальным пародонтитом (ЭП) (2-я группа); МСР – моноцитарный хемотаксический белок; ФНО – фактор некроза опухоли; ИЛ – интерлейкин;
ИНФ – интерферон.
Согласно полученным данным, отмечена достоверная разница (p<0,05) между уровнем практически всех цитокинов в контроле (1-я группа крыс) и при моделировании экспериментального пародонтита (2-я группа крыс). Найдено, что в сыворотке крови значительно и достоверно (в 4–5 раз) увеличилась концентрация провоспалительных цитокинов ИЛ-1β (р<0,001), ФНОα (р<0,001) и ИЛ-6 (р<0,001); примерно на 60% вырос уровень моноцитарного хемотаксического белка (хемокина МСР-1) (р<0,05). Отмечено отсутствие достоверного подъема антивоспалительного цитокина ИЛ-4 (р>0,05). Несмотря на достоверное возрастание в крови других противовоспалительных цитокинов (ИЛ-10 (р<0,01) и ИЛ-13 (р<0,001), их уровень повышения не соответствует уровню увеличения провоспалительных факторов и явно недостаточен для ограничения воспалительной реакции. Эти данные свидетельствуют о дисбалансе продукции про- и противовоспалительных цитокинов при экспериментальном пародонтите (преобладает секреция провоспалительных цитокинов при относительной недостаточности выработки противовоспалительных цитокинов) (рис. 1).
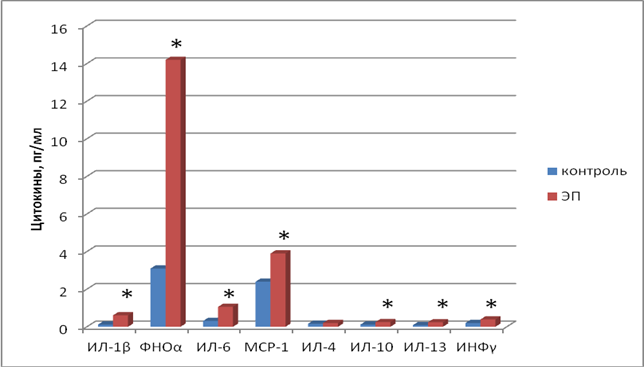
Рис. 1. Соотношение важнейших провоспалительных и антивоспалительных цитокинов у крыс контрольной группы (1-я группа) и крыс с экспериментальным пародонтитом
(2-я группа); ФНО – фактор некроза опухоли; МСР – моноцитарный хемотаксический белок; ИЛ – интерлейкин; ИНФ – интерферон; ЭП – группа крыс с экспериментальным пародонтитом; контроль – группа крыс контрольной группы; * – различия значимы (p<0,05) при сравнении с соответствующими показателями в группе контроля
Данное патологическое состояние, характеризующееся нарушением регуляции иммунных процессов, способствует генерализации воспаления и усиливает вероятность и выраженность развития его деструктивных форм. Известно, что провоспалительные цитокины, оказывая воздействие на клетки эндотелия, увеличивают синтез молекул адгезии для моноцитарно-гранулоцитарных лейкоцитов, обеспечивая в тканях пародонта их мобилизацию и усиление продукции коллагеназы, разрушающей зубодесневое прикрепление (периодонт), и стимулируя активность остеокластов костной ткани челюстей [10, 11]. Кроме того, повышение ФНОα и особенно ИЛ-6 способствует увеличению в тканях пародонта плазматических клеток, продуцирующих IgG. IgG активирует комплемент, так как имеет рецептор для С1-комплемента, что предрасполагает к пролонгированию и персистированию воспаления.
В нашем исследовании получено почти 2-кратное достоверное увеличение интерферона γ (ИНФγ) (р<0,01), который является лимфокином, обладающим про- и антивоспалительными свойствами. Он оказывает влияние на дифференцировку и рост миелоидных клеток, которые, становясь зрелыми моноцитами, увеличивают хелперный ответ Th1-типа и стимулируют экспрессию антигенов главного комплекса гистосовместимости [6].
Значительную роль в развитии деструктивных форм воспаления играет недостаточность продукции антивоспалительных цитокинов, тормозящих развитие вторичной альтерации тканей путем ограничения воспалительной реакции. Противовоспалительные цитокины ингибируют активные формы кислорода, способствуют предупреждению микроциркуляторных расстройств [10, 12], уменьшают выработку провоспалительных цитокинов [13].
Таким образом, представленные результаты констатируют тот факт, что у животных с экспериментальным пародонтитом наблюдается дизрегуляция продукции различных форм цитокинов. Дисбаланс соотношения провоспалительных и антивоспалительных факторов обусловливает деструктивный характер воспаления и его тяжесть.
При введении иммуномодуляторов: полиоксидония, трекрезана или метапрота – на фоне ЭП отмечено достоверное (p<0,05) и значительное увеличение антивоспалительных цитокинов ИЛ-4, ИЛ-10 и ИЛ-13. Так, по сравнению с контролем уровень ИЛ-4 вырос в 4,5 раза на фоне введения полиоксидония (р<0,001); в 3,7 раза на фоне введения трекрезана (р<0,01) и в 3,2 раза при введении метапрота (р<0,001). По сравнению со 2-й группой крыс (моделирование экспериментального пародонтита без введения иммуномодуляторов) на фоне интраперитонеального введения полиоксидония, трекрезана или метапрота уровень ИЛ-4 достоверно возрос в 3,6 (р<0,001); 3,0 (р<0,01) и 2,6 (р<0,001) раза соответственно. Уровень ИЛ-10 в контрольной группе животных по сравнению с уровнем ИЛ-10 также достоверно увеличился в 8,2 раза (полиоксидоний) (р<0,001), в 3,4 раза (трекзан) (р<0,001) и в 5,1 раза (метапрот) (р<0,001). По сравнению с группой животных с ЭП введение иммуномодуляторов на фоне воспаления повышало уровень ИЛ-10 от 1,6 раза (метапрот) (р<0,001) до 3,9 раза (полиоксидоний) (р<0,001). Аналогичные достоверные изменения уровня ИЛ-13 по сравнению с контролем отмечены на фоне введения полиоксидония (р<0,001), трекрезана (р<0,05) и метапрота (р<0,01) – 4,7; 5,3 и 4,2 раза соответственно (рис. 2).
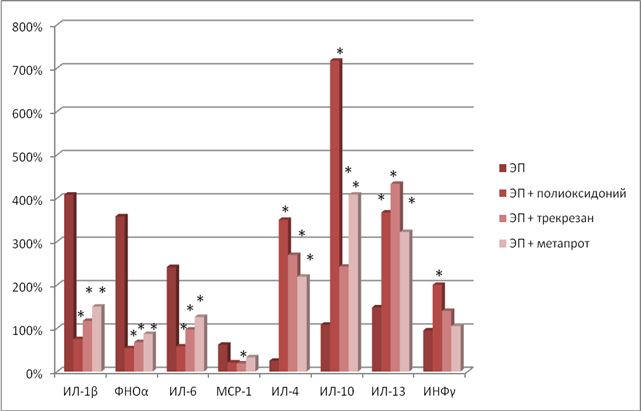
Рис. 2. Изменения уровней провоспалительных и антивоспалительных цитокинов у крыс с экспериментальным пародонтитом (ЭП) (2-я группа) и крыс с экспериментальным пародонтитом на фоне лечения полиоксидонием (ЭП + полиоксидоний – 3-я группа крыс), трекрезаном (ЭП + трекрезан – 4-я группа крыс) и метапротом (ЭП + метапрот –
5-я группа крыс); ФНО – фактор некроза опухоли; МСР – моноцитарный хемотаксический белок; ИЛ – интерлейкин; ИНФ – интерферон; * – различия значимы (p<0,05) при сравнении с соответствующими показателями в группе крыс с экспериментальным пародонтитом. Уровень соответствующих цитокинов у интактных животных (контроль – 1-я группа крыс) принят за 0%
Из представленных данных видно, что указанные препараты, стимулируя выработку антивоспалительных интерлейкинов ИЛ-4, ИЛ-10 и ИЛ-13, уровень которых в сыворотке крови многократно увеличивался, одновременно достоверно уменьшают (р<0,001) и производство у подопытных животных провоспалительных цитокинов ИЛ-1β, ФНОα и ИЛ-6. При этом в 2–3 раза по сравнению с контролем повысилась концентрация ИНФγ (р<0,001), а также ИЛ-2 (р<0,05 – ЭП + трекзан) и ИЛ-12(р70) (р<0,05 – ЭП + полиоксидоний) – цитокинов, обладающих мощной способностью к адаптивному иммунному ответу. Следовательно, введение исследуемых иммуномодуляторов в целом довольно успешно предупреждало резкое угнетение иммунорегулирующих функций, обусловленных как повреждающим действием формалина, так и комплексом патогенных факторов, индуцирующих вторичную альтерацию.
Заключение. Таким образом, восстановление иммунорегулирующей функции цитокинов является одним из важных механизмов защитного эффекта используемых химических препаратов при экспериментальном пародонтите. Их эффективность можно представить следующим образом: полиоксидоний > трекрезан > метапрот.
Библиографическая ссылка
Мокренко Е.В., Вязьмин А.Я., Шабанов П.Д., Сусликова М.И., Мокренко М.Е., Губина М.И. ЦИТОКИНОВЫЙ ПРОФИЛЬ КРОВИ КРЫС ПРИ ЭКСПЕРИМЕНТАЛЬНОМ ПАРОДОНТИТЕ И ДЕЙСТВИИ ИММУНОМОДУЛЯТОРОВ // Современные проблемы науки и образования. 2020. № 6. ;URL: https://science-education.ru/ru/article/view?id=30432 (дата обращения: 17.05.2026).
DOI: https://doi.org/10.17513/spno.30432



