При изучении адгезиогенеза важную роль играет синтетическая активность фибробластов, которые участвуют в синтезе компонентов межклеточного матрикса и формировании грануляционной ткани при разрешении воспалительного процесса [1]. При хронической эмпиеме плевры стадия фиброзной организации напрямую зависит от фибробластов, которые пролиферируют и проникают в плевральную жидкость как из висцеральной, так и париетальной плевры, образуя соединительную ткань [2]. За счет формирования грануляционной ткани листки плевры утолщаются, делая их менее подвижными. При длительном воспалении происходит усиление фиброза с ограничением дыхательной экскурсии легкого [3; 4]. Поэтому разрешение воспалительного процесса в плевральной полости зависит не только от подавления воспалительного ответа, но и ингибирования пролиферации фибробластов и синтеза коллагена [5; 6].
Известно, что пролиферативная, миграционная способность и синтетическая активность фибробластов напрямую зависит от клеточного микроокружения. На функциональную активность фибробластов могут влиять другие клетки, в особенности при воспалительном процессе [7; 8]. В то время как за клеточную пролиферацию и регуляцию апоптотических процессов отвечает ядерный транскрипционный фактор NF-kB. После его активации происходит блокирование апоптоза, что продлевает жизнь в клетках-эффекторах в очаге воспаления. Следовательно, период воспалительной реакции увеличивается, что может стать причиной формирования фиброза и устойчивости фибробластов к апоптозу [9]. Таким образом, для оценки выраженности адгезиогенеза в плевральной полости и определения эффективности использования различных биологических субстратов при хронической эмпиеме плевры могут быть использованы иммуногистохимические маркеры, такие как NF-kB и FGF-1.
Цель исследования – оценить выраженность адгезиогенеза в плевральной полости при биологическом потенцировании адгезиогенеза с помощью иммуногистохимических маркеров (NF-kB p65, FGF-1).
Материал и методы исследования. Исследование проведено на 450 нелинейных половозрелых крысах-самцах. Все животные содержались в стандартных условиях вивария Пятигорского медико-фармацевтического института – филиала ФГБОУ ВО «ВолгГМУ» Минздрава России согласно с «Правилами проведения работ с использованием экспериментальных животных». Эксперимент составлен в соответствии с приказами МЗ РФ № 267 от 19.06.2003 г. «Об утверждении правил лабораторной практики» и МЗ СССР № 755 от 12.08.1977 г. и «Международными рекомендациями по проведению медико-биологических исследований с использованием животных» (1985), придерживаясь принципов биоэтики и правил лабораторной практики (GLP). Использование экспериментальных животных признано необходимым, допускается и регламентируется ст. 25 и 26 «Европейской конвенции о защите позвоночных животных».
Эксперимент проводили в два этапа. Для начала всем животным внутриплеврально в V межреберье по подмышечной линии вводили 1 млрд взвеси E. coli в течение 28 дней для моделирования хронической эмпиемы плевры и образования ригидной плевральной полости [10]. Затем все животные были разделены по 90 особей на пять экспериментальных групп, две из которых были группами контроля и три опытные группы с использованием методов биологического стимулирования адгезиогенеза. Животным I группы (негативный контроль, НК) лечение не проводилось – внутриплеврально вводили 1,0 мл физиологического раствора, а животным II группы (позитивный контроль, ПК) - 1,0 мл 1% раствора доксициклина. Использование плазмы, обогащенной тромбоцитами (PRP), в качестве адгезива применяли в III опытной группе (набор для забора крови Plasmolifting™, ООО «Плазмолифтинг», г. Казань, Россия. ТУ 9437-002-27837594-2015, регистрационное удостоверение № РЗН 2016/3980 от 19.04.2016). В IV опытной группе с той же целью использовали аутологичную жировую взвесь (липофилинг), а в V опытной группе применяли метод сочетанного потенцирования адгезиогенеза с использованием обоих биологических субстратов. На 10, 20 и 30-е сут. от начала второго этапа животные выводились из эксперимента по 30 особей из каждой группы.
Для иммуногистохимического исследования, которое проводили непрямым пероксидазным методом, использовали поликлональные кроличьи антитела - Anti-NF-kB p65 antibody (Abcam, Англия), Anti-FGF-1 antibody (Abcam, Англия). Микрофотографии полученных микропрепаратов были сделаны с использованием микроскопа LeicaDM 100 с цифровой фотокамерой. Морфометрическое исследование с дальнейшей оценкой экспрессии иммунопозитивного материала проводили с помощью программы LAS Version 4.2.7. Для статистической обработки полученных данных использовали программные пакеты Exсel 7.0 (Microsoft, USA). Для анализа вида распределения полученных результатов использовали критерий Колмогорова-Смирнова. Достоверность данных с нормальным распределением оценивали с помощью параметрического t-критерия Стьюдента. Различия считали достоверными при p<0,05.
Результаты исследования и их обсуждение
При иммуногистохимическом исследовании образцов животных I группы установлено, что на 10-е сут. эксперимента происходит утолщение плевры, преимущественно висцеральной, за счет миграции фибробластов и формирования тонких волокон соединительной ткани. При этом объемная доля (ОД) иммунопозитивных клеток к ядерному фактору NF-kB составила 26,86±0,5% (p<0,05). Однако при оценке экспрессии фактора роста фибробластов (FGF-1) были выявлены единичные иммунопозитивные клетки, ОД которых составила 8,16±0,5% (p<0,05).
При анализе иммунореактивности тканей плевральной полости к NF-kB и FGF-1 во II группе достоверных отличий от группы НК выявлено не было. В процентном соотношении ОД иммунопозитивных клеток составила 25,15±1,2% и 9,28±1,2% соответственно (p<0,05).
В III опытной группе, где для стимуляции адгезиогенеза использовалась плазма, обогащенная тромбоцитами, на данном сроке наблюдалось увеличение миграции фибробластов с образованием сосудов незрелой соединительной ткани. ОД иммунопозитивных клеток к NF-kB составила 28,72±0,8% (p<0,05). Неоангиогенез и синтез внеклеточного матрикса формирующихся спаек плевральной полости сопровождался наличием иммунопозитивных клеток к FGF-1 (10,92±1,5%, p<0,05), которые были представлены макрофагами, отдельными фибробластами, а также клетками сосудистой стенки. В свою очередь это приводило к стимуляции фибробластов и увеличению их синтетической функции.
В то же время в IV опытной группе высокая экспрессия ядерного фактора NF-kB свидетельствовала о сохранении клеточного инфильтрата и формировании каркаса спайки. Процентное соотношение транскрипционного фактора составило 33,01±1,4% (p<0,05), что в 1,2 раза было больше, чем в группе НК. В данной группе адгезиогенез сопровождался экспрессией FGF-1, где иммунопозитивные клетки составляли значительную часть структурных элементов спайки и располагались не только со стороны париетальной и висцеральной плевры, но и собственно незрелой соединительной ткани. ОД позитивно окрашенных клеток составила 12,83±1,2% (p<0,05), что было достоверно больше, чем в группах контроля.
Диффузное расположение позитивно окрашенных клеток к NF-kB определялось в V опытной группе, что составило 35,22±0,8% (p<0,05). На данном сроке эксперимента клеточный состав спайки свидетельствовал об активации синтетической функции фибробластов, что подтверждается экспрессией FGF-1. Так, иммунопозитивное окрашивание клеток к FGF-1 наблюдалось как в месте формирования коллагеновых волокон, так и вокруг разнокалиберных сосудов, что подтверждает фазу раннего созревания соединительной ткани. Со стороны ОД позитивных клеток (16,31±0,8%) были выявлены достоверные отличия от показателей группы НК и ПК (p<0,05), рис. 1.
На 20-е сут. эксперимента в группе НК экспрессия NF-kB была повышена, где позитивное окрашивание имело значительное число клеточных элементов, формирующих сращения в плевральной полости, что связано, по-видимому, с выраженной воспалительной реакцией. В данном случае ОД иммунопозитивных клеток составила 27,13±1,3% (p<0,05). На данном сроке эксперимента среди волокон незрелой соединительной ткани определялись иммунопозитивные клетки к FGF-1, ОД которых составила 11,52±0,4% (p<0,05).
При этом в группе ПК с использованием доксициклина экспрессия транскрипционного фактора сопровождалась сохранением признаков воспаления и формированием волокон соединительной ткани, что составило 23,38±0,3% (p<0,05). При этом иммунопозитивные клетки большей частью определялись вокруг сосудов соединительной ткани. Экспрессия FGF-1 в клетках соединительной ткани распределялась неравномерно с преобладанием иммунопозитивных клеток вокруг сосудов, а также среди волокон соединительной ткани собственно спайки. Определение ОД иммунопозитивных клеток к FGF-1 выявило, что она была достоверно выше (18,21±0,8%) по сравнению с группой НК (p<0,05).
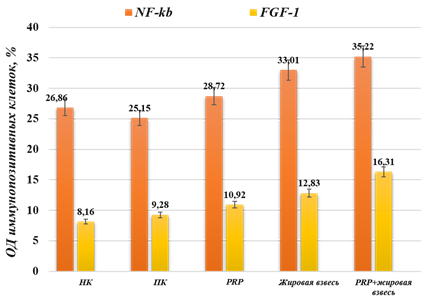
Рис. 1. Хроническая эмпиема плевры. 10-е сутки эксперимента.
Показатели экспрессии NF-kb и FGF-1, p<0,05
В III опытной группе ОД позитивно окрашенные клеток против NF-kB, расположенных непосредственно в самой спайке, составила 24,09±1,6% (p<0,05). Наряду с этим в данной группе наблюдалось увеличение числа иммунопозитивных клеток к FGF-1, что сопровождалось формированием волокон соединительной ткани и новообразованием сосудов различного диаметра. Однако процентное содержание позитивно окрашенных клеток было незначительно выше, чем в ПК на этом сроке, что составило 19,85±0,5% (p<0,05).
В то же время в IV опытной группе на этом сроке наблюдалось достоверное снижение ОД иммунопозитивного материала к NF-kB (12,76±1,1%). При оценке экспрессии FGF-1 в соединительной ткани было установлено, что возрастала ОД позитивно окрашенных клеток, которая составила 32,12±0,8%, что в 3,9 раза больше показателей группы НК и ПК (p<0,05).
Аналогичное снижение экспрессии NF-kB наблюдалось и в группе с сочетанным потенцированием адгезиогенеза (11,37±1,5%, p<0,05). При этом позитивно окрашенные клетки располагались среди волокон соединительной ткани, что свидетельствовало о сохранении воспалительной реакции наряду с пролиферацией фибробластов и созреванием спайки. Установлено, что количество иммунопозитивных клеток к FGF-1 было максимальным по сравнению с другими сроками эксперимента (37,02±1,5%, p<0,05), что свидетельствовало об активном адгезиогенезе и формировании сращений в плевральной полости. На рисунке 2 представлена сравнительная характеристика процентного содержания иммунопозитивных клеток к NF-kB и FGF-1 на 20-е сут. хронической эмпиемы плевры.
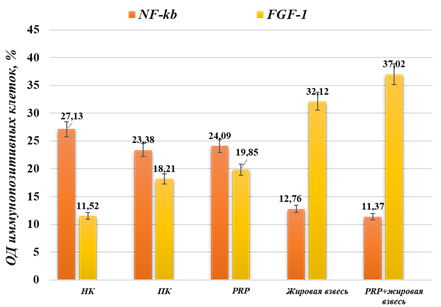
Рис. 2. Хроническая эмпиема плевры. 20-е сутки эксперимента.
Показатели экспрессии NF-kb и FGF-1, p<0,05
К концу эксперимента в группе НК ОД иммунопозитивных клеток к ядерному фактору NF-kB составила 16,24±1,6% (p<0,05), что свидетельствовало о сохранении воспаления. При этом определялись единичные позитивно окрашенные клетки к FGF-1 (21,76±3,4%, p<0,05), хаотично расположенные среди соединительнотканных волокон. В поле зрения преобладали сосуды, что свидетельствовало о нарушении процессов адгезиогенеза по отношению к срокам созревания спаек.
Снижение ОД иммунопозитивных клеток к NF-kB на 30-е сут. отмечалось и в группе ПК, что значительно отличалось от показателей на более ранних сроках - 15,02±1,4% (p<0,05). Иммунопозитивные клетки к NF-kB распределялись равномерно среди волокон соединительной ткани спаек, характеризующиеся наличием небольшого количества сосудов и единичных клеток воспалительного ряда. В соединительной ткани спаек определялось большое количество фибробластов, однако иммунопозитивными к FGF-1 были некоторые клетки, ОД которых составила 26,51±1,5% (p<0,05).
В III опытной группе низкие показатели ОД позитивно окрашенных клеток к NF-kB (14,37±1,5%, p<0,05) также отличались по сравнению с 10-ми и 20-ми сутками эксперимента. Однако в процентном отношении на 30-е сутки данный показатель оставался достаточно высоким с большим числом иммунопозитивных клеток к NF-kB. Созревание соединительной ткани сопровождалось изменением экспрессии FGF-1, где определялось множество иммунопозитивных клеток, что свидетельствовало о прогрессирующем адгезиогенезе с формированием обилия соединительнотканных волокон. При этом ОД позитивных клеток была выше, чем в ПК (28,33±0,4%, p<0,05), рис. 3.
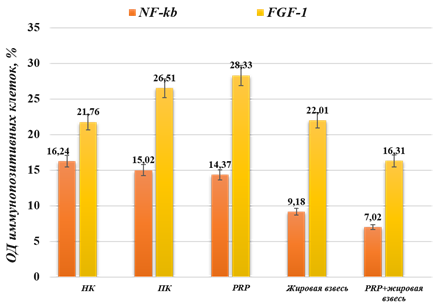
Рис. 3. Хроническая эмпиема плевры. 30-е сутки эксперимента.
Показатели экспрессии NF-kb и FGF-1, p<0,05
В IV и V опытных группах на 30-е сут. наблюдалось незначительное число иммунопозитивных клеток к NF-kB, где ОД составила 9,18±0,8% и 7,02±1,2% соответственно (p<0,05), что подтверждает отсутствие воспалительного инфильтрата и наличие зрелой соединительной ткани с преобладанием коллагеновых волокон. Иммунопозитивные клетки к FGF-1 в соединительной ткани особей IV опытной группы составляли 22,01±2,3% (p<0,05), что незначительно отличалось от показателей группы НК и ПК на этом сроке. В то же время в V группе выявлены единичные иммунопозитивные клетки (11,49±3,2%, p<0,05), что свидетельствует о высокой степени зрелости соединительной ткани.
Выводы. Таким образом, в результате иммуногистохимического исследования было установлено, что на 20-е сут. эксперимента максимальные значения иммунопозитивных клеток к FGF-1 и NF-kВ были зафиксированы в группе сочетанного потенцирования адгезиогенеза, что свидетельствовало о высокой пролиферативной активности фибробластов и усилении их синтетической функции с заполнением соединительной тканью остаточной плевральной полости. Однако к 30-м сут. в этой группе наблюдается резкое снижение ОД иммунопозитивных клеток к обоим маркерам, что указывает на формирование зрелой спайки и снижению продукции внеклеточного матрикса, что в свою очередь свидетельствует о безопасности применения данного способа при хронической эмпиеме плевры. В то же время в группах контроля и при изолированном применении плазмы, обогащенной тромбоцитами, на этом сроке экспрессия FGF-1 сохраняется, что в сочетании с увеличением процента иммунопозитивных клеток к NF-kВ фактору свидетельствует о неконтролируемом спайкообразовании и может привести к тотальному заращению плевральной полости.
Библиографическая ссылка
Калашникова С.А., Айдаева С.Ш., Полякова Л.В., Калашникова Е.А., Филиппова В.П. ИСПОЛЬЗОВАНИЕ ИММУНОГИСТОХИМИЧЕСКИХ МАРКЕРОВ В ОЦЕНКЕ ВЫРАЖЕННОСТИ АДГЕЗИОГЕНЕЗА В ПЛЕВРАЛЬНОЙ ПОЛОСТИ ПРИ БИОЛОГИЧЕСКОМ ПОТЕНЦИРОВАНИИ // Современные проблемы науки и образования. 2020. № 5. ;URL: https://science-education.ru/ru/article/view?id=30170 (дата обращения: 10.06.2026).
DOI: https://doi.org/10.17513/spno.30170



