Глиальные опухоли представляют собой первичные новообразования центральной нервной системы, составляющие 81% злокачественных опухолей головного мозга [1]. Согласно классификации Всемирной организации здравоохранения глиальные опухоли подразделяют на подтипы на основании морфологических, иммуногистохимических и генетических маркеров, а именно на высокодифференцированные глиомы – диффузные астроцитомы (IDHmut, IDHwt и NOS) и олигодендроглиомы (IDHmut, 1p/19q коделеция) и низкодифференцированные глиомы – анапластические астроцитомы (IDHmut, IDHwt, NOS), анапластические олигодендроглиомы (IDHmut, 1p/19q коделеция) и глиобластомы (IDHmut, IDHwt, NOS) [2]. Особенностью глиальных опухолей является инвазивный рост с отсутствием четкой границы между опухолью и неизмененной тканью мозга, что ограничивает возможность хирургического лечения. Глиобластомы составляют подавляющее большинство глиом, являются интенсивно пролиферирующими опухолями, характеризуются высокой цитологической гетерогенностью и слабым ответом на существующее лечение, заключающееся в циторедуктивной резекции с последующей комбинированной радио- и химиотерапией [3]. Медиана общей выживаемости пациентов с глиомами высокой степени злокачественности составляет 14,6 месяца, а 5-летняя выживаемость равна 9,8% [4].
У 10–15% пациентов со злокачественными глиомами наблюдается феноменальная послеоперационная продолжительность жизни более 3 лет. Высокий уровень 3-летней выживаемости больных с первичной глиобластомой в первую очередь объясняется индивидуальным подходом к лечению. Такая группа пациентов характеризуется молодым возрастом и низким уровнем экспрессии гена MGMT, что позволяет им перенести интенсивную многокурсовую химиотерапию [5]. Мутации в гене IDH1 (особенно R132H) также ассоциированы с лучшей выживаемостью пациентов со злокачественными глиомами [3]. Однако различия между отдельными пациентами диктуют необходимость поиска новых прогностических биомаркеров.
Нейроонкогенез может быть вызван целым рядом генетических и эпигенетических изменений, к основным из которых можно отнести нарушения, связанные с p53, HIF-1α, EGFR, PI3K, PTEN, mTOR, RAS, RAF, MEK [3, 6]. Однако эти изменения отражают, какие сигнальные пути нарушены в глиомах, но не дают понимания реальных молекулярных механизмов, которые контролируют клеточные процессы, приводящие к образованию и прогрессии опухоли. Идентификация молекулярных механизмов, лежащих в основе развития заболевания, может значительно расширить арсенал терапевтических подходов. На данный момент ведется множество клинических исследований, но их результаты в большинстве случаев не соответствуют научным ожиданиям [7].
Ряд исследований демонстрируют, что профиль экспрессии микроРНК в глиальных опухолях значительно изменяется по сравнению с гистологически не измененной нервной тканью, определяет возможность дальнейшего прогрессирования опухоли и итоговый успех терапии [8, 9]. МикроРНК представляют собой тип коротких некодирующих РНК, которые играют важную роль в регуляции экспрессии генов. Идентификация аберрантно экспрессируемых микроРНК имеет большое значение для прогноза течения заболевания пациентов с глиомами. Как участники посттранскрипционной и транскрипционной регуляции экспрессии генов микроРНК оцениваются в качестве потенциальных терапевтических агентов при лечении глиальных опухолей головного мозга [9].
В связи с этим целью настоящей работы стало исследование дифференциальной экспрессии микроРНК и возможности их применения в качестве предикторов выживания пациентов с глиомами высокой степени злокачественности.
Материалы и методы исследования
Исследование было одобрено этическим комитетом ФГБУ «Национальный медицинский исследовательский центр онкологии» Минздрава России. В выборку вошли 30 пациентов (14 мужчин и 16 женщин) с первично диагностированной глиальной опухолью головного мозга (26 случаев GIV и 4 случая GIII). Средний возраст составил 59,2±9,1 года. В каждом случае было получено добровольное информированное согласие пациента на включение в исследование. Диагноз был подтвержден гистологически в соответствии с классификацией ВОЗ опухолей ЦНС (2016). Точки забора биологического материала определяли с применением Medtronic S7 (Medtronic, Ирландия). Образцы глиом были отобраны интраоперационно. Контрольная точка располагалась на расстоянии 15 мм от границы опухоли по траектории доступа к новообразованию, не затрагивая функционально значимые зоны головного мозга (по данным МРТ). За 2 часа до проведения операционного вмешательства пациенты принимали 5-аминолевулиновую кислоту. Для визуализации границы опухолевой ткани производили оценку флуоресценции модулем Blue 400 микроскопа CarlZeiss OPMI PENTERO (Zeiss AG, Германия). Контрольный биоптат флуоресценции не имел. Фрагменты тканей замораживали в жидком азоте и хранили при –80°С.
Выделение РНК. Фрагменты ткани помещали в TRIzol (Thermo Fisher, США) и гомогенезировали с помощью MagNALyser (Roshe, Швейцария). Нуклеиновые кислоты выделяли согласно рекомендациям производителя TRIzol (ThermoFisher, США). Очистку РНК проводили с использованием набора miRNA miniKit (Qiagen, Германия). Для удаления геномной ДНК полученные образцы РНК обрабатывали препаратами ДНК-азы 1 (ThermoFisher, США). Концентрацию нуклеиновых кислот оценивали на флуориметре Qubit (Thermo Fisher, США) согласно инструкции производителя. Синтез кДНК осуществляли с использованием MMLV Reverta («Синтол», Россия).
Исследование экспрессии 13 микроРНК (miR-215-5p, miR-22-3p, miR-122-5p, miR-107, miR-324-5p, miR-34a-5p, miR-155-5p, miR-21-5p, miR-497-5p, miR-330-3p, miR-146a-5p, miR-92a-1-5p, miR-326) проводили методом RT-qPCR. В качестве референсных использовали последовательности микроРНК miR-191-5p, miR-103a-1-5p и малой ядерной РНК RNU49. Дизайн праймеров для исследуемых микроРНК осуществляли с применением miRBase v.22. ПЦР в реальном времени проводили на термоциклере Bio-Rad CFX96 (Bio-Rad, США). Анализ данных количественной ПЦР осуществляли методом 2-ΔΔСt
Анализ данных. Статистическую обработку данных проводили с помощью пакета программ STATISTICA 10 (Statsoft inc., США). Различия экспрессии между опухолевой тканью и условно нормальной тканью рассчитывали с помощью W-критерия Вилкоксона. Анализ влияния экспрессии микроРНК на выживаемость пациентов проводили в программной среде вычислений R 3.6.2. (пакеты «survival» и «survminer»). Для экспрессии микроРНК рассчитывали точку отсечения с использованием стандартизированного лог-рангового критерия. Для визуализации данных выживаемости пациентов применяли метод Каплана–Майера. Значение p<0,05 указывает на статистическую значимость.
Результаты исследования и их обсуждение
МикроРНК играют критически важную роль в регуляции онкогенов и генов супрессоров опухолей. Таким образом, транскрипционный профиль микроРНК может быть использован как высокоточный диагностический и прогностический параметр. Методом RT-qPCR нами была произведена оценка уровня относительной экспрессии микроРНК miR-215-5p, miR-22-3p, miR-122-5p, miR-107, miR-324-5p, miR-34a-5p, miR-155-5p, miR-21-5p, miR-497-5p, miR-330-3p, miR-146a-5p, miR-92a-1-5p, miR-326 в 30 парных образцах тканей глиом высокой степени злокачественности и условно нормальных тканей мозга. В результате было выявлено статистически значимое (p<0,05) увеличение относительной экспрессии в 2,9 раза для miR-155-5p (73% пациентов). Как тенденция отмечено увеличение экспрессии в 3,8 раза (р=0,0581) для miR-21-5p (67% пациентов). Снижение экспрессии (p<0,05) в 1,9, 1,6, 1,8, 2,2, 11,7, 1,4 и 1,1 раза соответственно было показано для miR-215-5p (73% пациентов), miR-22-3p (63% пациентов), miR-107 (80% пациентов), miR-324-5p (100% пациентов), miR-330-3p (100% пациентов), miR-326 (70% пациентов) и miR-122-5p (83% пациентов) (рис. 1).
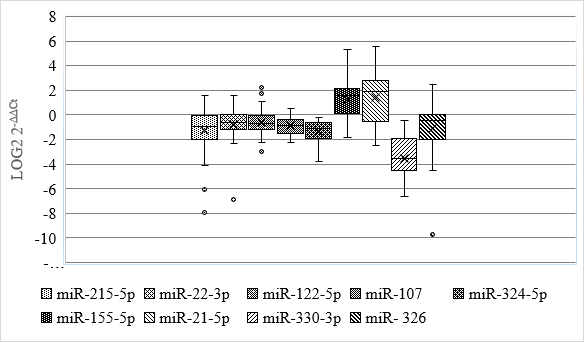
Рис. 1. Изменение относительной экспрессии исследуемых микроРНК в образцах злокачественных глиом по отношению к неизмененной ткани мозга
В результате в глиомах высокой степени злокачественности было идентифицировано две группы микроРНК с возросшим (miR-155-5p, miR-21-5p) и, наоборот, снизившимся уровнем экспрессии (miR-215-5p, miR-22-3p, miR-107, miR-324-5p, miR-122-5p, miR-330-3p, miR-326) по сравнению с неизмененной тканью мозга.
В представленной работе мы предприняли попытку определить прогностическую значимость микроРНК в качестве возможных предикторов выживания пациентов с глиомами высокой степени злокачественности на основании клинических данных и паттерна экспрессии 13 микроРНК. Анализ транскрипционной активности микроРНК выявил, что изменение экспрессии miR-22-3P, miR-107 и miR-330-3P в глиомах головного мозга тесно связано со снижением выживаемости пациентов и свидетельствует о негативном прогнозе течения онкологического заболевания. Снижение экспрессии miR-22-3p, miR-107 или miR-330-3p приводило к повышению медианы общей выживаемости приблизительно в 6 (p=0,038), 4 (p=0,048) и 4 (p=0,0088) раза соответственно (рис. 2).
Изменение экспрессии miR-330 может оказывать влияние на злокачественный процесс. В исследовании Qu S., Yao Y., Shang C., et al. были выявлены онкогенная роль miR-330 в клетках глиобластомы человека и ее связь с геном SH3GL2. Было показано, что сверхэкспрессия miR-330 может активировать пролиферацию, способствовать миграции и инвазии, а также ингибировать апоптоз клеток U87 и U251 [10].
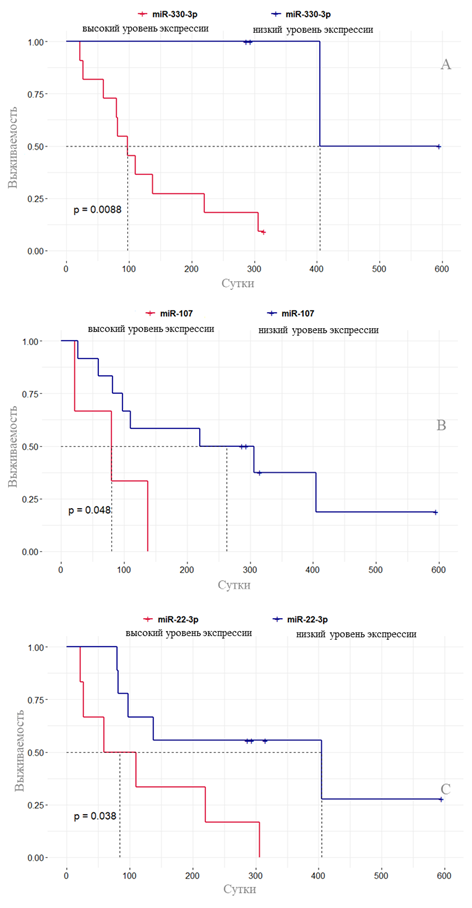
Рис. 2. Изменение выживаемости пациентов со злокачественными глиомами в зависимости от экспрессии микроРНК miR-330-3p (А), miR-107 (B), miR-22-3p (С)
MiR-22-3p играет существенную роль в инициации и прогрессировании различных типов опухолей. MiR-22-3p идентифицирована как мощная онкогенная микроРНК, способствующая пролиферации и инвазии клеток рака простаты [11]. Недавно было обнаружено, что miR-22-3p активируется в спинальной диффузной астроцитоме, где она способствует клеточной инвазии путем подавления TIMP2 (Tissue inhibitor of metalloproteinases 2) [12]. В исследовании Han M., Wang S., Fritah S., et al. было показано, что miR-22-3p активно транскрибируется в клетках глиобластомы, где изменение ее экспрессии было связано с негативными для пациента клиническими исходами [13].
МикроРНК miR-107 участвует в регуляции жизненно важных процессов, таких как клеточное деление, миграция и ангиогенез. Изменение экспрессии miR-107 вызывает развитие множества новообразований. miR-107 действует как опухолевый супрессор, вызывая остановку клеточного цикла при раке легкого и глиоме путем подавления экспрессии CDK6 [14]. Однако miR-107 может выступать в качестве онкогена, способствующего инвазии и метастазированию при раке груди и желудка посредством регуляции экспрессии DICER1 [15].
На многие важные вопросы, касающиеся функций микроРНК в реализации противоопухолевого эффекта, еще предстоит ответить. Однако возможность использования микроРНК в качестве прогностических маркеров и в будущих терапевтических подходах представляет перспективное направление. Возможное участие miR-330-3p, miR-22-3p, miR-107 в нейроонкогенезе делает их привлекательными инструментами таргетной терапии.
Заключение
Уровень экспрессии микроРНК miR-22-3p, miR-107 и miR-330-3p может быть использован как предиктор в оценке выживания пациентов с глиомами высокой степени злокачественности. Обнаруженное изменение общей выживаемости пациентов в зависимости от уровня экспрессии микроРНК miR-22-3p, miR-107 и miR-330-3p делает их привлекательными инструментами генной терапии онкопатологии, не имеющей в настоящее время эффективных методов лечения. Однако наличие возможных побочных эффектов, а также нестрогая специфичность действия микроРНК требуют дальнейшего изучения.
Исследование выполнено в рамках госзадания «Молекулярно-генетические маркеры глиом».
Библиографическая ссылка
Аллилуев И.А., Пушкин А.А., Росторгуев Э.Е., Кузнецова Н.С. ПРОГНОСТИЧЕСКАЯ ЗНАЧИМОСТЬ МИКРОРНК MIR-22-3P, MIR-107 И MIR-330-3P В ОЦЕНКЕ ВЫЖИВАЕМОСТИ ПАЦИЕНТОВ С ГЛИОМАМИ ВЫСОКОЙ СТЕПЕНИ ЗЛОКАЧЕСТВЕННОСТИ // Современные проблемы науки и образования. 2020. № 5. ;URL: https://science-education.ru/ru/article/view?id=30122 (дата обращения: 10.06.2026).
DOI: https://doi.org/10.17513/spno.30122



