По данным Bray F. и др. (2018), во всем мире в 2018 году было зарегистрировано около 1 миллиона новых случаев КЖ, что сделало рак желудка третьей ведущей причиной смертности от рака во всем мире и побуждает Всемирную организацию здравоохранения объявить его проблемой общественного здравоохранения [1]. Хотя некоторые формы злокачественных опухолей желудка, например кардиального отдела желудка, уменьшаются благодаря лучшему наблюдению, выявлению и лечению, есть и другие формы КЖ, которые увеличиваются в частоте, например кардиальной части желудка. Так, в США наблюдается 70%-ный рост заболеваемости некардиальным раком желудка в некоторых возрастных группах (25-39 лет). Это свидетельствует, что, несмотря на прогресс лечения во многих областях онкологии, все еще многое предстоит выяснить, почему идет рост заболеваемости опухолями некардиального отдела желудка [2].
Несмотря на прогресс в комбинированном лечении злокачественных опухолей желудка, до сих пор как непосредственные, так и отдаленные результаты лечения, а также показатели выживаемости остаются не совсем удовлетворительными [3]. Основным стандартом лечения КЖ является хирургический метод, при котором проводится гастрэктомия или полное удаление органа. В большинстве случаев проводится удаление желудка с иссечением регионарных лимфоузлов, а также удаление селезенки. При ранних стадиях КЖ можно проводить сохранные операции в виде частичных резекций желудка. Однако, учитывая, что в Кыргызстане имеется высокий процент запущенности (70-80% больных КЖ поступают в специализированное отделение с III-IV стадиями опухолевого процесса), сохранные операции практически не проводятся.
Во многих странах мира широко внедряется лапароскопическая или роботизированная методика гастрэктомии при ранних формах рака желудка. Так, многие ретроспективные и несколько проспективных рандомизированных исследований в разных странах показали, что лапароскопическая методика также имеет право на существование, так как при этом уменьшается число послеоперационных осложнений и сокращается время для заживления швов. Лапароскопическая резекция желудка доказала свою эффективность даже при некоторых местнораспространенных опухолях [4; 5].
Полная резекция опухоли и диссекция лимфатических узлов в комбинации с неоадъювантной и послеоперационной химиотерапией/радиотерапией показывает значительное улучшение выживаемости при распространенной КЖ [6; 7].
Основным патологическим синдромом, возникающим после гастрэктомии, является рефлюкс-эзофагит, возникающий вследствие заброса желчи в пищевод по приводящей петле и встречающийся в 37-90% случаев [8; 9].
Цель исследования: совершенствование хирургических методов лечения с целью профилактики основных постгастрэктомических осложнений на основе анализа различных видов тонкокишечной пластики.
Материалы и методы исследования. Материалом для исследования явились пациенты с раком желудка. Место проведения операций и исследований – отделение абдоминальной онкологии Национального центра онкологии и гематологии Министерства здравоохранения Киргизской Республики. За период с мая 2015 по ноябрь 2019 г. было обследовано 130 пациентов, больных раком желудка. Согласно протоколу лечения после соответствующего обследования больным раком желудка проводилась гастрэктомия. С целью контроля аностомоза и изучения состояния слизистой пищевода и кишечника проводилась гастродуоденоскопия.
Были изучены результаты эндоскопического исследования больных раком желудка (Т1-4 N0-2 МО), оперированных в объеме гастрэктомия с разными вариантами тонкокишечной пластики. При Национальном центре онкологии и гематологии исследовано 130 больных КЖ, которые были разделены на 3 группы в зависимости от примененного метода видоизменения проходимости кишечника. В первой группе было 54 больных КЖ c формированием эзофагоэнтероанастомоза по Давыдову и Шалимову. Во вторую группу вошли 53 пациента, которым выполнена гастрэктомия с формированием тонкокишечной пластики по Ру. Третью группу составили 23 больных, которым выполнена гастрэктомия с образованием резервуара из тонкой кишки на специальной петле, так называемая непересеченная петля. Основной целью таких пластических операций являлась профилактика осложнений в виде рефлюкс-эзофагита, наиболее распространенного после таких операций.
Визуализация желудка, а именно оставшегося ложа, проводилась гастроскопом по стандартной технологии. При этом проводилось обследование и осмотр слизистой, а подозрительные участки отправлялись на морфологическое исследование. Важным этапом при гастроскопическом исследовании являлась оценка состояния анастомоза, выявление воспалительных процессов или рубцовых стриктур после операции гастрэктомии. В послеоперационном периоде каждые три месяца после хирургического лечения проводили контрольное обследование больных с помощью эзофагоеюноскопии, задачей которого являлось исследование на наличие рефлюкс-эзофагита и анастомозита.
Использованы статистические методы исследования, используемые в биомедицине, в частности программа SPSS-16. Для изучения достоверности использован критерий согласия Пирсона или критерий согласия χ 2 {\displaystyle \chi ^{2}} (хи-квадрат) – непараметрический метод, который позволяет оценить значимость различий между фактическим (выявленным в результате исследования) количеством исходов или качественных характеристик выборки, попадающих в каждую категорию, и теоретическим количеством, которое можно ожидать в изучаемых группах при справедливости нулевой гипотезы. Также проводилась коррекция на непрерывность (Continuity Correction). Для выборок маленьких размеров использован точный тест Фишера.
Результаты исследования. Гистологически наиболее часто встречалась аденокарцинома у 112 (75,2%) больных, в том числе низкодифференцированная – в 82 (58,2%), умеренно дифференцированная – в 21 (14,9%) и высокодифференцированная – в 3 (2,1%) случаях. Недифференцированный вариант аденокарциномы встречался у 6 (4,6%), перстневидно-клеточный рак – у 11 (8,5%) и слизистый рак – у 6 (4,6%) больных. Самой редкой гистологической формой злокачественного образования желудка в нашем исследовании явилась лейомиосаркома, которая установлена у 1 (0,7%) больного.
Во всех группах больных среди аденокарцином преобладал низкодифференцированный вариант опухоли: в первой группе было 36 (66,7%), во второй – 28 (52,8%) и 11 (40,7%) соответственно.
Распределение по стадиям было следующим: во всех трех группах имело место преобладание III-а стадии: 35 (64,8%) в первой группе, 40 (75,5%) – во второй и 18 (66,7%) – в третьей группе. Пациентов со II стадией было 10 (18,5%) в первой группе, 7 (13,2%) – во второй и 6 (22,2%) – в третьей. Больных с первой стадией рака желудка было всего четверо, из них в первой группе данную стадию имел всего 1 пациент (1,8%), во второй группе – 2 (3,8%) и в третьей – 1 больной (3,7%).
С III-b стадией пациентов было несколько больше в первой группе – 8 (14,8%), чем во второй – 4 (7,5%) или третьей группах – 2 (7,4%).
По локализации чаще всего выявлялся рак тела желудка (65 больных, или 50%), затем рак кардиального отдела (28 пациентов, или 21,5%) и рак антрального отдела (22 больных, или 16,9%). Остальные 15 больных (11,5%) имели локализации в других отделах желудка.
Большинство пациентов во всех трех группах были оперированы лапаротомным или чрезбрюшинным доступом: 49 (91,8%) – в первой группе, 48 (90,1%) – во второй и 26 (96,30%) – в третьей.
Некоторым пациентам (n=25) из-за проникновения или прорастания опухоли в соседние органы (печень, поджелудочная железа, большой сальник) объем оперативного вмешательства расширялся. Проводились расширенные и комбинированные хирургические резекции. Резекция поджелудочной железы выполнена у 4 (2,8%), резекция левой доли печени проведена у 6 (4,3%), резекция поперечной ободочной кишки у 8 (5,7%) больных. Операция сопровождалась спленэктомией у 1 (1%) больного. Также у одного пациента произведена резекция поперечной ободочной кишки с субтотальной резекцией поджелудочной железы.
После удаления желудка восстановительный этап был завершен формированием терминолатерального эзофагоэнтероанастомоза по Давыдову.
Перед операцией всем больным для диагностики РЖ проводился стандартный комплекс диагностических мероприятий, включающий общеклинические исследования крови и мочи, биохимические исследования функции печени, почек, эндоскопию пищевода, желудка и двенадцатиперстной кишки. В план обследования также входило рентгенологическое исследование пищевода и желудка с помощью контрастных веществ. Неотъемлемой частью обследования являлось также ультразвуковое исследование органов брюшной полости. Всем пациентам проводилась оценка сердечно-сосудистой и дыхательной систем (ЭКГ, функция внешнего дыхания).
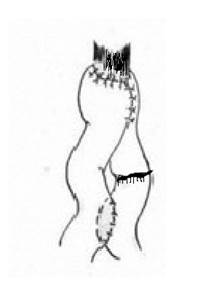
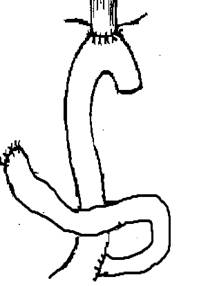
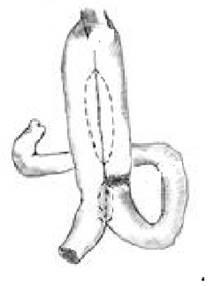
Восстановление проходимости пищеварительного тракта по группам выглядело следующим образом (рисунок).
|
|
|
|
|
Формирование пищеводно-кишечного анастомоза с перевязкой приводящей петли |
Формирование пищеводно-кишечного анастомоза по Ру |
Сформированный резервуар после гастрэктомии с перевязкой приводящей петли (uncut-Py) |
Реконструкции пищеварительного тракта после гастрэктомии по группам больных
Воспалительные и рубцовые изменения в нижнегрудном отделе пищевода классифицированы по Savary-Miller (1978) (табл. 1) [7].
Таблица 1
Классификация рефлюкс-эзофагита по Savary-Miller
|
Градация/степень изменений |
Характеристика изменений слизистой пищевода |
|
1 |
Не сливающиеся (не конфлюэнтные) эритематозные эрозии, одна или более |
|
2 |
Множественные конфлюэнтные, сливные, не окружающие просвет эрозии |
|
3 |
Сливные конфлюэнтные эрозии, окружающие просвет пищевода эрозивные повреждения слизистой оболочки |
|
4 |
Осложнения: язва, стеноз, пищевод Барретта |
Первое контрольное исследование (эндоскопическое) было выполнено через три месяца после оперативного вмешательства. При этом в первой группе больных эзофагит первой степени был выявлен у 2 (3,7%) пациентов, эзофагит 2-й и 3-й степени имели по 1 (1,9%) пациенту. Во второй и третьей группах через 3 месяца после операции во время контрольного осмотра не было выявлено признаков эзофагита. При сравнении между группами разница была статистически не достоверной (p>0,05). В таблице 2 представлены данные эндоскопии через 6 месяцев после гастрэктомии.
Таблица 2
Данные эндоскопического исследования через 6 месяцев после операции
|
Градация эзофагита |
Группа I (n=54) |
Группа II (n=53) |
Группа III (n=23) |
|
Эзофагит 1-й степени |
14 (25,9%)* |
2 (3,8%) |
- |
|
Эзофагит 2-й степени |
7 (13%) |
- |
- |
|
Эзофагит 3-й степени |
1 (1,9%) |
- |
- |
* - P < 0,001 (хи-квадрат Пирсона).
Через 6 месяцев наблюдения показатели эзофагитов значительно изменились; так, в первой группе из 54 больных эзофагит первой степени выявлен у 14 (25,9%). Согласно методике сравнения значений хи-квадрат Пирсона (Pearson Chi-Square) р=0,001, а с коррекцией на непрерывность (Continuity Correction) р=0,003, что достоверно чаще встречалось по сравнению со второй группой, где эзофагит был выявлен у 2 (3,8%) больных. В третьей группе эзофагит какой-либо степени не наблюдался ни у одного больного (табл. 3).
Множественные конфлюэнтные, сливные, не окружающие просвет эрозии (2-я степень по градации Savary) были выявлены у 7 (13%) больных в первой группе. Во второй и третьей группах через 6 месяцев наблюдения признаки эзофагита 2-й степени не были выявлены ни у одного больного. У 1 (1,9%) больного в первой группе пациентов выявлена клиника эзофагита 3-й степени (сливные конфлюэнтные эрозии, окружающие просвет пищевода эрозивные повреждения слизистой оболочки).
Таблица 3
Достоверность хи-квадрат Пирсона при сравнении групп пациентов с эзофагитами
(Chi-Square Tests)
|
|
Value |
df |
Asymp. Sig. (2-sided) |
Exact Sig. (2-sided) |
Exact Sig. (1-sided) |
|
Pearson Chi-Square |
10,321 |
1 |
,001 |
|
|
|
Continuity Correction |
8,653 |
1 |
,003 |
|
|
|
Likelihood Ratio |
11,448 |
1 |
,001 |
|
|
|
Fisher's Exact Test |
|
|
|
,002 |
,001 |
|
Linear-by-Linear Association |
10,225 |
1 |
,001 |
|
|
|
N of Valid Cases |
107 |
|
|
|
|
В таблице 4 представлены данные эндоскопического исследования через 9 месяцев после операции гастрэктомии с реконструкцией кишечника.
Таблица 4
Данные эндоскопического исследования через 9 месяцев после операции
|
Градация эзофагита |
Группа I (n=54) |
Группа II (n=53) |
Группа III (n=23) |
|
Эзофагит 1-й степени |
14 (25,9%)* |
4 (7,5%) |
- |
|
Эзофагит 2-й степени |
25 (46,3%)** |
2 (3,8%) |
- |
|
Эзофагит 3-й степени |
2 (3,7%) |
- |
- |
*- P <0,011, ** - P = 0,000.
По результатам эндоскопического исследования через 9 месяцев установлено, что эзофагит I степени в первой группе выявлен у 14 (25,9%) больных и 4 (7,5%) пациентов во второй группе. При подсчете по хи-квадрат минимальное значение ожидаемых значений было равно 8,92 (> 5). Следовательно, значимость Р по Пирсону составила 0,011, т.е. различие статистически значимое, а с коррекцией на непрерывность (Continuity Correction) р=0,022. Эзофагит II степени достоверно чаще встречался (p<0,005) в группе больных с петлевой пластикой с перевязкой приводящей петли (uncut Roux), где выявлен у 25 (46,3%) больных по сравнению с группой больных, оперированных по Ру, где установлен эзофагит II степени у 2 (3,8%) больных. Минимальное ожидаемое значение составило 13,37, что > 5, берем хи-квадрат Пирсона (Pearson Chi-Square) – р = 0,000, следовательно, различие статистически значимо. Эзофагит III степени констатирован у 2 (3,7%) пациентов в первой группе, во второй и третьей группах рефлюкс-эзофагит не был выявлен ни у одного пациента. При расчете в двух клетках ожидаемое значение меньше 5. Поэтому берем точный тест Фишера, при котором р = 0,495. Следовательно, различий нет. Также не было различий по методике Pearson Chi-Square (р=0,157) и Continuity Correction (р=0,484).
Спустя год в динамическом наблюдении, по данным таблицы 5, мы видим, что эзофагит I степени встречался во всех трех группах: 6 (11,1%) в 1-й, 5 (9,4%) – во 2-й и 3 (13%) – в 3-й соответственно. С поправкой на непрерывность разница между группами не достоверна (p=1,000).
Таблица 5
Данные эндоскопического исследования через 12 месяцев после операции
|
Градация эзофагита |
Группа I (n=54) |
Группа II (n=53) |
Группа III (n=23) |
|
Эзофагит I степени |
6 (11,1%) |
5 (9,4%) |
3 (13%) |
|
Эзофагит II степени |
34 (63%)* |
3 (5,7%) |
- |
|
Эзофагит III степени |
5 (9,3%) |
- |
- |
|
Эзофагит IV степени |
1 (1,9%) |
- |
- |
*- Р=0,000.
Эзофагит II степени чаще наблюдался у пациентов с петлевой пластикой и перевязкой приводящей петли, выявленный у 34 (63%) больных, по сравнению с пациентами, оперированными по способу Ру (n=3, 5,7%): разность достоверна, p=0,000. Эзофагит III встречался у 5 (9,3%) и при сравнении со второй группой (n=0) разность была статистически не достоверной (тест Фишера, р=0,057), и у 1 (1,9%) больного первой группы.
Выводы. Таким образом, после радикальной гастрэктомии у пациентов с раком желудка развивался постгастрэктомический рефлюкс-эзофагит. Во всех трех группах больных в различные периоды времени наблюдались явления эзофагита определенной степени выраженности. В целом эзофагиты были не выраженными, в основном I, II степени. В третьей группе пациентов, оперированных с формированием тонкокишечного резервуара на непересеченной петле, статистически достоверно реже наблюдались явления эзофагита, по сравнению с другими группами.
Библиографическая ссылка
Тойгонбеков А.К., Уметов М.З., Рамалданов Р.А., Омурбаев Э.Э., Сафаров М.А., Макимбетов Э.К. РЕЗУЛЬТАТЫ ЭНДОСКОПИЧЕСКОГО ИССЛЕДОВАНИЯ БОЛЬНЫХ РАКОМ ЖЕЛУДКА ПОСЛЕ ГАСТРЭКТОМИИ С РАЗНЫМИ ВАРИАНТАМИ ТОНКОКИШЕЧНОЙ ПЛАСТИКИ // Современные проблемы науки и образования. 2020. № 2. ;URL: https://science-education.ru/ru/article/view?id=29734 (дата обращения: 19.05.2026).
DOI: https://doi.org/10.17513/spno.29734