Общепринятым фактом в мировой медицине на сегодняшний день является то, что операции на открытом сердце имеют, пожалуй, наиболее высокий оперативный риск операционных осложнений, в том числе и летальных. Это связано, прежде всего, с особой важностью оперируемого органа для жизнедеятельности как отдельных органов и систем, так и для всего организма в целом [1]. Нарушение какой-либо из функций сердца непременно ведет к развитию целой цепочки событий, появлению патологических симптомов, которые, объединяясь в синдромы, при отсутствии своевременного лечения могут привести к летальному исходу. Во многом возникновение послеоперационных осложнений в кардиохирургической практике связано с исходным состоянием больного [2].
Согласно представленным в литературе данным, частота встречаемости сочетания умеренной или выраженной митральной недостаточности, хирургически значимого атеросклероза коронарных артерий и сниженной фракции выброса левого желудочка варьируется от 12 до 38%. В связи с неуклонным ростом числа больных с сочетанием всех вышеперечисленных патологий проблема выбора хирургической тактики лечения в подобных ситуациях чрезвычайно актуальна [3; 4]. Несмотря на технический прогресс, совершенствование оборудования, развитие торакоскопической хирургии и накопленный хирургами опыт, частые летальные исходы лечения данных пациентов продолжают оставаться важным фактором в отказе от оперативного лечения [5; 6].
Традиционной методикой лечения данной категории больных является коронарное шунтирование, протезирование митрального клапана, резекция аневризмы левого желудочка (при ее наличии) в условиях искусственного кровообращения. Наиболее опасным жизнеугрожающим осложнением данных операций является длительная сердечная слабость, вплоть до невозможности остановки аппарата искусственного кровообращения. Высокая продолжительность таких операций в сочетании с высокой продолжительностью искусственного кровообращения значительно усугубляет состояние больного и удлиняет сроки госпитализации, а также часто приводит к летальному исходу [7]. Стентирование является безопасным и полезным методом, позволяющим быстро скорректировать значимые стенозы коронарных артерий, предотвратив необходимость последующего коронарного шунтирования в большом комплексе хирургического лечения данных пациентов. В мировой литературе представлены единичные случаи стентирования данной категории больных с такой комбинацией патологий, так как обычно применяются методики традиционной кардиохирургии с искусственным кровообращением. Без какого-либо хирургического лечения летальность пациентов в течение года достигает 45-65% из-за высокой скорости прогрессирования сердечной недостаточности [8].
Особенно актуальным это является в лечении пациентов, перенесших крупноочаговый инфаркт миокарда, осложнившийся митральной недостаточностью в раннем периоде [9; 10]. Невозможность применения традиционных методик хирургического лечения у данной категории больных делает особенно актуальной разработку новых алгоритмов и подходов в лечении этих больных [11; 12].
Цель исследования: изучить механизм ремоделирования левого желудочка, с последующим изменением степени митральной недостаточности, в результате хирургической реваскуляризации миокарда.
Материал и методы исследования. Настоящее исследование основано на анализе материалов обследования и лечения 97 больных с выраженной недостаточностью митрального клапана, низкой фракцией выброса левого желудочка и сопутствующими хирургически значимыми стенозами коронарных артерий (КА) (рис. 1). Средний возраст больных составил 65,4±4,7 года. Наибольшее количество больных вошло в группу 60-70 лет – 51 (52,6%), 50-60 лет – 38 (39,2%), 40-50 – 8 (8,2%). Количество мужчин примерно в 2,4 раза превысило количество женщин (69 и 28 соответственно). У 43 (44,3%) пациентов было 3-сосудистое поражение КА. У 22 (22,7%) пациентов было 2-сосудистое поражение КА. У 32 (33%) пациентов было монопоражение коронарных артерий. Всем пациентам была выполнена полная реваскуляризация миокарда. Из них 39 (40,2%) пациентам выполнялось стентирование коронарных артерий, 58 (59,8%) больным было выполнено коронарное шунтирование. Стентирование проводилось пациентам с фракцией выброса левого желудочка (ЛЖ) менее 30% и 3-й степенью митральной недостаточности (v.c. от 6 до 8 мм). Коронарное шунтирование проводилось пациентам с фракцией выброса левого желудочка (ФВЛЖ) более 40% и умеренной митральной недостаточностью (v.c. от 3,5 до 5 мм). Пациентам в группе коронарного шунтирования делалась чреспищеводная эхокардиография (ЧПЭхоКГ) интраоперационно для подтверждения отсутствия необходимости коррекции клапанного порока. Больные, которым хирургическая коррекция порока проводилась, не были включены в данное исследование.
Все больные были обследованы стандартными клиническими, рентгенологическими, инструментальными и лабораторными методами обследования. Проводился анализ первичных диагнозов, данных ультразвуковой диагностики, коронарографий, историй болезни оперированных больных. Результаты консервативного и оперативного лечения прослежены в сроки до 1 года.
Анализировались динамика митральной недостаточности до и после стентирования коронарных артерий, динамика фракции выброса левого желудочка, конечный диастолический объем (КДО), конечный систолический объем (КСО), размеры левого желудочка. Эффективностью лечения считалось рецидив жалоб, снижение КДО более чем на 15%, КСО на 15%, снижение митральной недостаточности на 1 степень (или уменьшение v.c. более чем на 1,5 мм).
Статистическая обработка результатов исследований проводилась с помощью пакета прикладных программ Microsoft Excel 2000 и Statistica 5.5 фирмы StatSoft Inc. (США). Результаты представлены в виде среднеарифметической и ее стандартной ошибки (М±m). Межгрупповое сопоставление показателей проводилось с помощью t-критерия Стьюдента для независимых выборок. Межгрупповые различия считались достоверными при р<0,05.
Результаты исследования и их обсуждение. Жалобы на одышку после физической нагрузки предъявляли 83 (85,6%) больных, а также на боль в области сердца – 71 (73,2%), на приступы сердцебиения или перебои в работе сердца – 19 (19,6%), повышенную утомляемость, слабость – 54 (55,7%) человека. Клинические признаки сердечной недостаточности на уровне IIа – 43 (44,3%) больных, IIб-- – 29 (30%), и III степени – 25 (25,7%).
Таблица 1
Динамика ЭхоКГ у пациентов до и после стентирования
|
|
До лечения |
Через 5 суток |
Через 30 суток |
Через 12 мес. |
|
КДР, см |
6,91±0,37 |
5,79±0,26* |
5,61±0,28 |
5,62±0,18 |
|
КСР, см |
5,12±0,32 |
4,29±0,14* |
4,32±0,14 |
4,39±0,11 |
|
КСО, мл |
153±14 |
95±17* |
92±15 |
95±17 |
|
КДО, мл |
217±23 |
163±21* |
159±22 |
161±19 |
|
ФВ, % |
25,7±3,2 |
43,2±2,9* |
44,1±2,6 |
43,5±2,2 |
* - разница между изучаемым и предыдущим показателем достоверна (р≤0,05).
Исходные параметры пациентов в группе стентирования составили: конечный диастолический размер (КДР) 6,91±0,37 см, конечный систолический размер (КСР) 5,12±0,32 см, КСО 153±14 мл, КДО 217±23 см, фракция выброса (ФВ) 25,7±3,2% (таблица 1). В результате хирургического лечения методом стентирования через 5 дней наблюдалась положительная динамика эхокардиографических показателей: КДР 5,79±0,26 см, КСР 4,29±0,14 см, КСО 95±17 мл, КДО 163±21 мл, ФВ 43,2±2,9%. Через 30 дней КДР 5,61±0,28 см, КСР 4,32±0,14 см, КСО 92±15 мл, КДО 159±22 мл, ФВ 44,1±2,6%. Через 12 месяцев КДР 5,62±0,18 см, КСР 4,39±0,11 см, КСО 95±17 мл, КДО 161±19 мл, ФВ 43,5±2,2%. Отмечено достоверное уменьшение показателей размеров и объемов ЛЖ: КДР (на 18,7%), КСР (на 15,6%), КДО (на 26,7%), КСО (на 39,8%), что приводило к достоверному увеличению ФВ левого желудочка на 37,6% (р <0,05). Отмечено достоверное снижение степени митральной недостаточности на 30,7% (изменения средней v.c. с 6,5 до 4,5 мм).
Таблица 2
Динамика ЭхоКГ у пациентов до и после коронарного шунтирования
|
|
До лечения |
Через 5 суток |
Через 30 суток |
Через 12 мес. |
|
КДР, см |
6,85±0,34 |
6,05±0,18* |
5,95±0,23 |
5,96±0,28 |
|
КСР, см |
5,37±0,21 |
4,72±0,14* |
4,61±0,17 |
4,64±0,13 |
|
КСО, мл |
111±14 |
89±17 мл* |
91±16 |
89±16 |
|
КДО, мл |
192±22 |
163±21* |
169±21 |
167±19 |
|
ФВ, % |
42,4±4,5 |
45,4±2,9* |
46,2±3,2 |
46,4±2,7 |
* - разница между изучаемым и предыдущим показателем достоверна (р≤0,05).
Исходные параметры пациентов в группе коронарного шунтирования составили (таблица 2): КДР 6,85±0,34 см, КСР 5,37±0,21 см, КСО 111±14 мл, КДО 192±22 см, ФВ 42,4±4,5%. В результате хирургического лечения методом коронарного шунтирования через 5 дней наблюдалась положительная динамика эхокардиографических показателей: КДР 6,05±0,18 см, КСР 4,72±0,14 см, КСО 89±17 мл, КДО 163±21 мл, ФВ 45,4±2,9%. Через 30 дней КДР 5,95±0,23 см, КСР 4,61±0,17 см, КСО 91±16 мл, КДО 169±21 мл, ФВ 46,2±3,2%. Через 12 месяцев КДР 5,96±0,28 см, КСР 4,64±0,13 см, КСО 89±16 мл, КДО 167±19 мл, ФВ 46,4±2,7%. Отмечено достоверное уменьшение показателей размеров и объемов ЛЖ: КДР (на 12,4%), КСР (на 13,4%), КДО (на 16,3%), КСО (на 13,5%), что приводило к достоверному увеличению ФВ левого желудочка на 8,6% (р <0,05). Отмечено достоверное снижение степени митральной недостаточности на 25% (изменения v.c. с 4,4 до 3,3 мм).
Клинически отмечалось уменьшение проявления сердечной недостаточности, снижение функционального класса достигнуто у 33 (84,6%) больных после стентирования и 41 (70,7%) больного после коронарного шунтирования. Достичь желаемого эффекта удалось у – 74 (76,3%) больных.
Несмотря на то что больные из группы стентирования имели исходно более низкие показатели на ЭхоКГ, результаты в данной группе лечения оказались лучше, чем в группе пациентов, перенесших коронарное шунтирование (рис. 2, 3). Это может быть связано с повреждением миокарда вследствие искусственного кровообращения, неадекватной реваскуляризацией. Смертность одногодичная в группе больных, перенесших стентирование, составила 1 пациент (2,56%), а в группе пациентов, перенесших шунтирование, составила 3 пациента (5,17%).
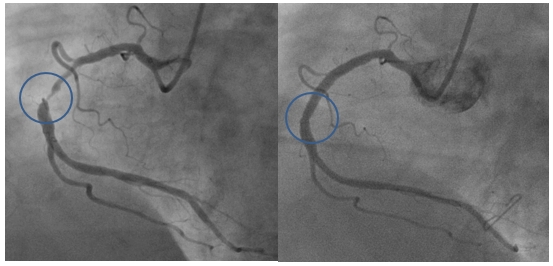
Рис. 1. Стеноз коронарной артерии до и после стентирования у пациента с митральной недостаточностью
Таким образом, мы видим, что, несмотря на широкий спектр оперативных вмешательств как малоинвазивных, так и торакотомических, существует ряд не решенных вопросов, связанных с адекватностью реваскуляризации миокарда. На данный момент существует большое количество международных и национальных рекомендаций по выбору того или иного способа реваскуляризации, тем не менее не учитываются такие моменты, как восстановление функции митрального клапана, играющего большую роль в гемодинамическом ремоделировании левого желудочка сердца.
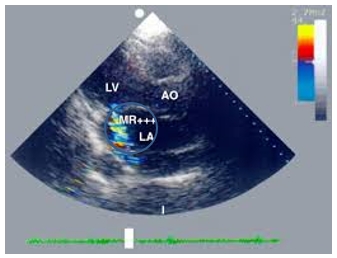
Рис. 2. Митральная недостаточность у пациента с ИБС до стентирования
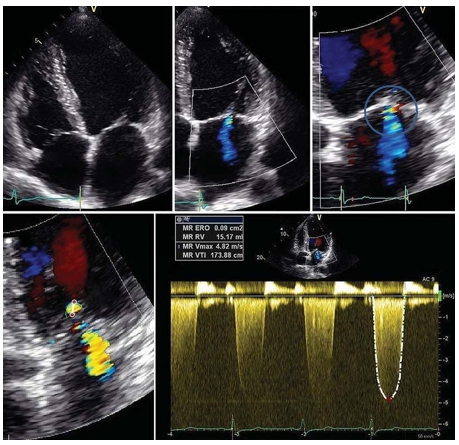
Рис. 3. Митральная недостаточность у пациента с ИБС после стентирования
По нашему мнению, недостаточность митрального клапана возникает в результате ишемии кардиомиоцитов и нарушения каркасной прочности кольца, при восстановлении адекватного кровоснабжения возобновляются функциональные способности сердечной мышцы, что приводит в ряде случаев к ликвидации клапанной недостаточности. В результате ишемии происходит смещение папиллярных мышц и апикальное натяжение митральных створок, что лежит в патогенезе митральной недостаточности. Первоочередное использование стентирования оправдано у больных с выраженной сердечной недостаточностью, как подготовительный этап для открытого аортокоронарного шунтирования, позволяющий улучшить кровоснабжение миокарда и повысить фракцию выброса левого желудочка. На данный момент дискутируется методика «the bridge» перед аортокоронарным шунтированием, для этого используют стентирование, лазерную реваскуляризацию миокарда, постановку контр-пульсатора, трансэндокардиальную трансплантацию мезенхимальных стволовых клеток, введение различных ангиогенных факторов роста и др.
Выводы
1. У больных с митральной недостаточностью ишемического генеза на фоне атеросклеротического поражения коронарных артерий хирургическое лечение коронарной патологии значимо (р<0,05) снижает степень митральной недостаточности в результате ремоделирования ЛЖ.
2. Реваскуляризация миокарда методом стентирования, как первый и основной этап лечения, позволяет уменьшить время последующего оперативного лечения (протезирования или пластики митрального клапана, в случае если в этом останется необходимость), увеличить фракцию выброса левого желудочка, снизить выраженность митральной недостаточности.
3. Применение мини-инвазивных технологий позволяет увеличить 1- и 6-месячную выживаемость пациентов с данной патологией.
4. Реваскуляризация миокарда приводит к улучшению гемодинамических показателей функционирования сердца и улучшению общего состояния пациентов (исчезновение многих жалоб, увеличение переносимости физической нагрузки и др.).
Библиографическая ссылка
Михайличенко В.Ю., Костямин Ю.Д., Самарин С.А., Бутырский А.Г., Баснаев У.И. АНАЛИЗ РЕЗУЛЬТАТОВ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПАЦИЕНТОВ С МИТРАЛЬНОЙ НЕДОСТАТОЧНОСТЬЮ КАК РЕЗУЛЬТАТА ДЛИТЕЛЬНО ПРОГРЕССИРУЮЩЕЙ КОРОНАРНОЙ ПАТОЛОГИИ В СОЧЕТАНИИ СО СНИЖЕННОЙ ФРАКЦИЕЙ ВЫБРОСА ЛЕВОГО ЖЕЛУДОЧКА // Современные проблемы науки и образования. 2019. № 6. ;URL: https://science-education.ru/ru/article/view?id=29412 (дата обращения: 19.05.2026).



