В последние десятилетия наблюдается тенденция увеличения распространенности ожирения в детском, подростковом и юношеском возрасте [1–3]. Исследования показывают, что у подростков и юношей с ожирением данная патология сохраняется и во взрослом периоде жизни [4]. Известно, что гипоталамус управляет сложными физиологическими реакциями, такими как контроль пищевого поведения; энергетический обмен; циркадный ритм продукции гормонов; реактивность на стрессовые ситуации; фертильность [5]. С одной стороны, ожирение может способствовать нарушению регуляторной функции гипоталамуса [6]. С другой стороны, изменение циркадного ритма продукции гормонов, неадекватная реакция на стресс и нарушение фертильности еще в большей степени усугубляют дисметаболические эффекты ожирения [7]. Так, ожирение, вызванное чрезмерным питанием, может на клеточном уровне провоцировать воспаление гипоталамуса, инициируя повреждение его структур и ослабление регуляторной функции [8]. Вместе с тем воспаление гипоталамуса, особенно в области дугообразного ядра и перивентрикулярной области, также ассоциировано с ожирением и диабетом [9]. Эти патологические изменения могут протекать одновременно, поэтому достаточно сложно определить, являются ли воспалительные процессы в гипоталамусе основной причиной метаболического синдрома или же источником некоторых из этих проблем является резистентность к гипоталамическим гормонам [10]. Исследований, посвященных изучению маркеров метаболического синдрома у юношей и лиц молодого возраста с разной стадией половозрелости и этиологией ожирения, ранее нее проводилось. Имеются единичные работы по изучению данной проблемы в детском возрасте [11]. Понимание механизмов, лежащих в основе патофизиологии гипоталамического ожирения, имеет решающее значение для выработки лечебно-профилактической стратегии, которая сможет предотвратить или ослабить неблагоприятные последствия ожирения.
Цель исследования - изучить предикторы и частоту развития метаболического синдрома у юношей и лиц молодого возраста в зависимости от степени их половозрелости и этиологии ожирения.
Материал и методы исследования. Обследованы 100 лиц мужского пола в возрасте от 18 лет до 26 лет (средний возраст 20,5±2,2 года), поступивших по направлению райвоенкоматов в эндокринологическое отделение Санкт-Петербургского городского бюджетного учреждения здравоохранения «Городская Мариинская больница». Все юноши были разделены на 4 группы: I группа - пациенты позднего пубертатного периода с ожирением, ассоциированным с гипоталамическим синдромом (n=31); II группа - пациенты позднего пубертатного периода с конституционально-экзогенным неосложненным ожирением (n=10); III группа - половозрелые пациенты с ожирением, ассоциированным с гипоталамическим синдромом (n=36); IV группа – половозрелые пациенты с конституционально-экзогенным неосложненным ожирением (n=23).
Половое развитие оценивалось по шкале Tanner. Гипоталамический синдром верифицировался при наличии симптомокомплекса, включающего ожирение и розовые стрии. Метаболический синдром диагностировался в соответствии с рекомендациями Российского медицинского общества по артериальной гипертонии (2013). Степень артериальной гипертензии определялась в соответствии с рекомендациями Европейского общества кардиологов и Европейского общества по артериальной гипертензии (2018). Артериальная гипертензия 1-й степени диагностировалась при уровне АД 140-159 и/или 90-99 мм рт. ст.; артериальная гипертензия 2-й степени определялась при уровне АД 160-179 и/или 100-109 мм рт. ст.; артериальная гипертензия 3-й степени диагностировалась при уровне АД ≥180/ ≥110 мм рт. ст. Дизайн исследования представлен на рисунке 1.
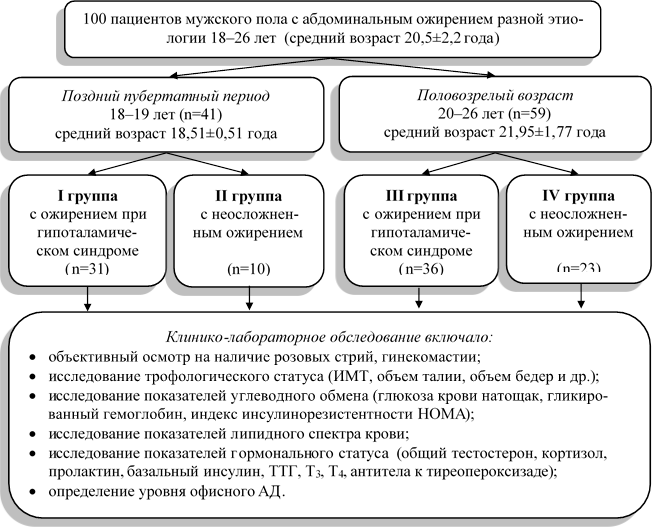
Рис. 1. Дизайн исследования
Лабораторные исследования проводились в утренние часы натощак. Кортизол исследовался дважды – утром натощак в 7.00 и вечером в 21.00.
Количественные переменные представлены в виде среднего арифметического значения ± стандартного отклонения (М±σ). Категориальные переменные представлены в виде долей в процентах. Проверка гипотез о равенстве двух средних для параметрических данных производилась с помощью t-критерия Стьюдента. Статистически значимыми считали различия при р<0,05.
Результаты исследования и их обсуждение. Согласно результатам однофакторного дисперсионного анализа достоверных различий по индексу массы тела (ИТМ) и объему бедер между группами пациентов не установлено (р>0,05), но установлены различия по показателям объема талии и соотношению объем талии / объем бедер (табл.). Так, у пациентов I и III групп, имевших признаки гипоталамического синдрома, объем талии оказался больше, чем у пациентов II и IV групп, имевших признаки конституционально-экзогенного ожирения (р<0,01). Это свидетельствует о том, что при гипоталамическом синдроме признаки абдоминального ожирения более выражены, чем при конституционально-экзогенном ожирении, независимо от степени половозрелости.
Особенности трофологического статуса в зависимости от степени половозрелости и этиологии ожирения
|
Показатели |
Поздний пубертат |
Половозрелый возраст |
F |
p |
||
|
I группа (M±σ) n=31 |
II группа (M±σ) n=10 |
III группа (M±σ) n=36 |
IV группа (M±σ) n=23 |
|||
|
Индекс массы тела (кг/м2) |
42,09±1,18 |
38,56±2,08 |
40,59±1,08 |
38,40±1,43 |
1,6 |
>0,05 |
|
Объем талии (см) |
151,52±3,01 |
135,20±5,31 |
152,11±2,76 |
137,05±3,66 |
6,1 |
<0,01 |
|
Объем бедер (см) |
109,29±2,13 |
109,60±3,75 |
106,92±1,95 |
109,52±2,59 |
0,34 |
>0,05 |
|
Соотношение объем талии / объем бедер |
1,39±0,03 |
1,24±0,05 |
1,43±0,03 |
1,26±0,04 |
3,7 |
<0,01 |
На рисунке 2 представлены среднее количество компонентов метаболического синдрома и индекс HOMA в обследованных группах пациентов. Установлено, что наибольшее количество компонентов метаболического синдрома определялось в группах пациентов, имевших признаки гипоталамического синдрома (в I группе 2,19±0,08; в III группе 2,22±0,07), в то время как в группах пациентов, имевших конституционально-экзогенное ожирение, количество компонентов метаболического синдрома было несколько ниже (во II группе 1,70±0,14; в IV группе 1,82±0,09). Это касалось и индекса HOMA, свидетельствующего о степени инсулинорезистентности. Таким образом, получены данные о том, что при гипоталамическом синдроме наблюдаются более неблагоприятный профиль кардиометаболических факторов риска и более высокая степень инсулинорезистентности, чем при конституционально-экзогенном ожирении, независимо от степени половозрелости организма.
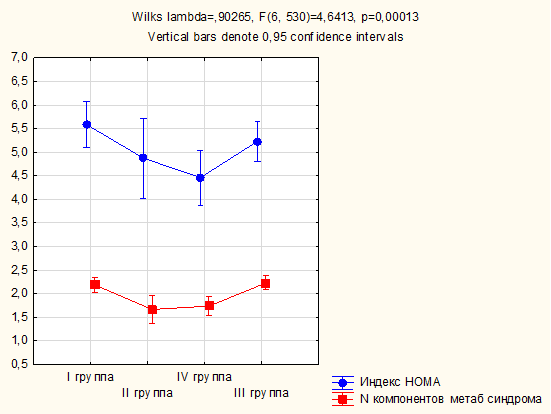
Рис. 2. Количество компонентов метаболического синдрома и уровень инсулинорезистентности в зависимости от степени половозрелости пациентов и этиологии ожирения
Ожирение как изолированный кардиометаболический фактор риска встречалось только у 24,0% обследованных пациентов, а в 76% случаев оно сочеталось с другими компонентами метаболического синдрома. Среди наиболее распространенных комбинаций следует отметить сочетание артериальной гипертензии с ожирением (35,0%), сочетание артериальной гипертензии, дислипидемии и ожирения (24%). Метаболический синдром в виде сочетания абдоминального ожирения, артериальной гипертензии, гипергликемии натощак, дислипидемии определялся только у 2,0% обследованных пациентов. Исследование показало, что дополнительный критерий метаболического синдрома присутствовал у большинства пациентов, как с осложненным (в I группе – 77,4%; в III группе - 83,8%), так и с неосложненным ожирением (во II группе – 70,0%; в IV группе – 63,6%). Таким образом, наиболее высокий риск развития метаболического синдрома определяется в III группе пациентов.
Во всех группах пациентов наиболее часто встречающейся комбинацией являлось сочетание артериальной гипертензии с ожирением (рис. 3). Так, в I группе эта комбинация встречалась в 35,5%, во II группе – в 40,0%, в III группе – в 35,1% и в IV группе – в 31,8% случаев. В группах пациентов с гипоталамическим синдромом чаще, чем при конституционально-экзогенном ожирении, отмечалось сочетание артериальной гипертензии, дислипидемии и ожирения. Все компоненты метаболического синдрома присутствовали только у 6,5% пациентов I группы. В группах половозрелых пациентов (III и IV группы) встречались более разнообразные комбинации компонентов метаболического синдрома, чем в группах пациентов пубертатного периода (I и II группы). Количество компонентов метаболического синдрома находилось в прямой связи с базальным уровнем инсулина (r=0,54; р<0,05), индексом инсулинорезистентности HOMA (r=0,36; р<0,05), объемом талии (r=0,43; р<0,05) и уровнем кортизола в вечернее время суток (r=0,29; р<0,05).
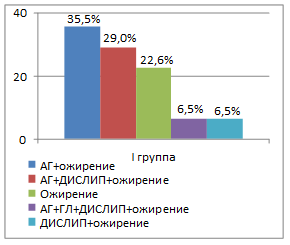
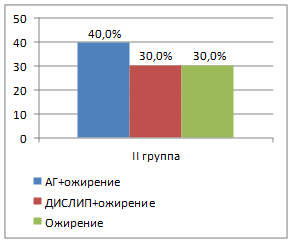
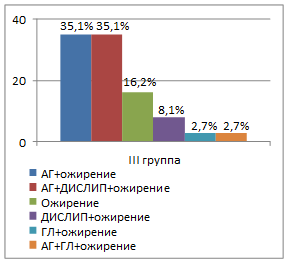
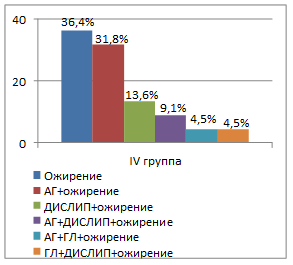
Рис. 3. Варианты компонентов метаболического синдрома в зависимости от степени половозрелости пациентов и этиологии ожирения (АГ – артериальная гипертензия; ДИСЛИП – дислипидемия; ГЛ – гипергликемия натощак)
Получены данные о том, что на степень артериальной гипертензии непосредственное влияние оказывают суточный профиль кортизола и уровень пролактина (рис. 4). Так, в подгруппе пациентов с артериальной гипертензией 3-й степени уровень утреннего кортизола оказался достоверно выше, чем в подгруппах пациентов с артериальной гипертензией 2-й степени и 1-й степени (422,75±40,54; 380,86±19,11; 312,57±15,60 нмоль/л; р<0,01). Это касалось и уровня вечернего кортизола (219,68±35,72; 191,86±16,84; 99,74±13,75 нмоль/л; р<0,01), пролактина (224,07±50,20; 209,18±23,66; 142,61±19,32 мМЕ/л; р<0,01) и общего тестостерона (16,45±1,39; 14,56±0,82; 12,62±0,69 нмоль/л; р<0,01).
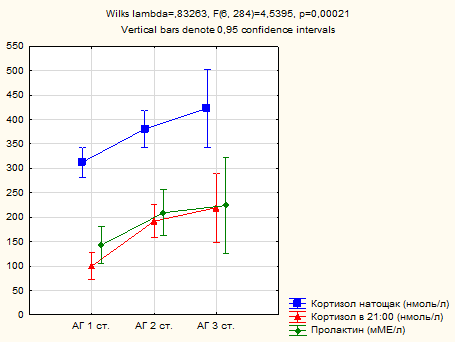
Рис. 4. Связь артериальной гипертензии с гормональным профилем (АГ – артериальная гипертензия)
Заключение. Гипоталамический синдром ассоциируется с более неблагоприятным профилем кардиометаболических факторов риска и более высокой степенью инсулинорезистентности, чем конституционально-экзогенное ожирение, независимо от степени половозрелости организма. Количество компонентов метаболического синдрома находится в прямой зависимости от базального уровня инсулина, степени инсулинорезистентности, выраженности абдоминального ожирения и суточного профиля кортизола. Наиболее часто встречающимся компонентом метаболического синдрома, как при осложненном, так и при неосложненном ожирении, является комбинация ожирения с артериальной гипертензией. Тяжесть артериальной гипертензии зависит от степени повышения кортизола, пролактина и тестостерона. Все компоненты метаболического синдрома в виде сочетания абдоминального ожирения, артериальной гипертензии, гипергликемии натощак, дислипидемии присутствовали у 6,5% юношей пубертатного возраста с гипоталамическим ожирением. Большинству пациентов с гипоталамическим синдромом присущи те же факторы риска развития хронических неинфекционных заболеваний, что и при метаболическом синдроме. Наиболее высокий риск развития метаболического синдрома определялся в III группе пациентов (83,8%). Пациенты с гипоталамическим синдромом нуждаются в диспансерном наблюдении, профилактическом консультировании и модификации имеющихся факторов риска развития хронических неинфекционных заболеваний.
Библиографическая ссылка
Церцвадзе Л.К., Авдеева М.В., Щеглова Л.В., Ерина М.Ю. ПРЕДИКТОРЫ МЕТАБОЛИЧЕСКОГО СИНДРОМА У ЮНОШЕЙ И ЛИЦ МОЛОДОГО ВОЗРАСТА В ЗАВИСИМОСТИ ОТ СТЕПЕНИ ИХ ПОЛОВОЗРЕЛОСТИ И ПРИЧИНЫ ОЖИРЕНИЯ // Современные проблемы науки и образования. 2019. № 5. ;URL: https://science-education.ru/ru/article/view?id=29094 (дата обращения: 15.05.2026).
DOI: https://doi.org/10.17513/spno.29094



