Гемолитико-уремический синдром (ГУС) относится к группе первичных тромботических микроангиопатий (ТМА), характеризуется одновременным развитием микроангиопатической гемолитической анемии, тромбоцитопении и острой почечной недостаточности.
Тромботическая микроангиопатия морфологически характеризуется повреждением сосудов микроциркуляторного русла, отеком и отслойкой эндотелиальных клеток от базальной мембраны, образованием тромбов, что вызывает окклюзию просвета сосуда и приводит к развитию ишемии различных органов. Клинически ТМА проявляется тромбоцитопенией потребления, гемолитической анемией, признаками ишемического повреждения органов и тканей, главным образом почек и центральной нервной системы [1].
Наиболее часто (90-95% случаев) наблюдается типичный или постдиарейный ГУС (Д+ ГУС), возникающий после кишечной инфекции, вызванной шигатоксин-продуцирующей E.coli О157:Н7 (STEC-HUS) [2-4]. В 5-10% всех случаев диагностируется атипичный ГУС (аГУС, комплемент-опосредованная ТМА), причиной которого является генетическая аномалия белков, регулирующих процесс альтернативного пути активации системы комплемента [2; 3; 5; 6].
Показатели заболеваемости STEC-HUS значительно варьируют в разных регионах, составляя 2-5 случаев на 100 000 детского населения до 5 лет [2; 7]. Основным источником STEC-инфекции является крупный рогатый скот. Заражение обычно происходит при употреблении термически недостаточно обработанных молока и говядины, немытых овощей и фруктов, инфицированной воды. При попадании в организм с пищей или водой шигатоксин-продуцирующие штаммы Е. coli связываются со специфическими рецепторами на слизистой оболочке толстой кишки, продуцируют экзо- и эндотоксины, размножаются и вызывают повреждение, гибель клеток, что приводит к развитию колита, нередко геморрагического [7]. Ведущая роль в патогенезе при типичном ГУС принадлежит микроангиопатии, возникающей под воздействием шигатоксина, имеющего рецепторы на мембранах эндотелиальных клеток сосудов многих органов, но особенно их много в эндотелии почечных клубочков, мезангиальных клетках у детей первых трёх лет жизни. С возрастом их количество снижается, с этим связывается наиболее частое развитие STEC-HUS у детей до 3 лет. Тромботическая микроангиопатия наблюдается в головном мозге, легких, сердце, кишечнике, печени. Поэтому при гемолитико-уремическом синдроме часто наблюдается полиорганная недостаточность [8]. Летальность от STEC-HUS при своевременной и адекватной терапии составляет 1-5% [7; 9], у 5% детей через 5-7 лет отмечается развитие хронической почечной недостаточности (ХПН), полностью восстанавливают почечную функцию 70-85% пациентов, перенесших STEC-HUS [3; 7; 8].
Эпидемиология атипичного гемолитико-уремического синдрома изучена недостаточно. Согласно литературным данным, распространенность его составляет 1-3 случая на 1 000 000 населения [5; 6]. Летальность при аГУС варьирует в пределах 5-10% случаев, у половины больных наблюдается исход в ХПН [7]. Заболевание чаще манифестирует до 18 лет, но достаточно часто (40% случаев) диагностируется во взрослом возрасте [1; 5]. Клинико-морфологические проявления тромботической микроангиопатии при аГУС являются результатом генетически обусловленной хронической неконтролируемой активации системы комплемента [5; 6]. Преимущественное поражение почек при аГУС, возможно, связано с повышенной чувствительностью эндотелия капилляров почечных клубочков к повреждению, индуцированному нарушенной регуляцией комплемента. К основным плазменным протеинам, регулирующим альтернативный путь активации комплемента, относятся факторы I (CFI) и Н (CFH), мембраносвязанным – тромбомодулин (THBD) и мембранный кофакторный протеин (MCP). У 30% детей с аГУС наблюдаются мутации гена CFH, в 12% случаев диагностируются сочетанные мутации [1]. Атипичный гемолитико-уремический синдром, обусловленный мутациями CFH и CFI, манифестирует, как правило, в возрасте 6 месяцев и 2 месяцев - соответственно. При мутации MCP заболевание чаще всего проявляется после первого года жизни. Возраст дебюта аГУС у взрослых пациентов от характера мутаций не зависит. Манифестацию аГУС обуславливает взаимодействие генетических аномалий в системе комплемента и факторов внешней среды, что провоцирует дополнительную активацию комплемента у предрасположенных лиц. Большинство эпизодов аГУС связаны с инфекцией верхних дыхательных путей и желудочно-кишечного тракта. Диарея провоцирует аГУС у 1/3 пациентов, что может затруднять дифференциальную диагностику с STEC-HUS [5]. Понимание роли системы комплемента при аГУС привело к появлению перспективного направления в терапии заболевания – использованию моноклональных антител – ингибиторов системы комплемента [1; 6].
Для дифференциальной диагностики между основными формами первичной ТМА (STEC-HUS, аГУС и тромботическая тромбоцитопеническая пурпура) рекомендуется определение активности протеазы ADAMTS-13. Снижение её до 5% и менее характерно для тромботической тромбоцитопенической пурпуры (ТТП). У пациентов с аГУС и STEC-HUS активность ADAMTS-13, как правило, превышает 5% и имеет прямую корреляционную связь с тяжестью течения патологического процесса. Атипичный гемолитико-уремический синдром диагностируется у больного, имеющего характерные признаками ТМА, при исключении STEC-ГУС и ТТП. Идентификация мутаций факторов комплемента для верификации диагноза и определения тактики лечения при аГУС не требуется. Но для определения прогноза, особенно у пациентов, которым планируется трансплантация почки, генетическое исследование необходимо [1; 7].
Цель исследования: провести анализ показателей заболеваемости и клинико-лабораторных признаков гемолитико-уремического синдрома у детей Республики Мордовия.
Материалы и методы исследования. Ретроспективно проанализированы истории болезни детей (n = 23), госпитализированных в Детскую республиканскую клиническую больницу по поводу гемолитико-уремического синдрома, за период с 2000 по 2018 г. У всех больных был диагностирован типичный ГУС. Возраст пациентов составил от 5 месяцев до 5 лет, девочек было 10, мальчиков - 13. Оценены клинические проявления заболевания, данные лабораторных (клинический анализ крови; общий анализ мочи; показатели белковых фракций, креатинина, мочевины, билирубина, амилазы, лактатдегидрогеназы в сыворотке крови) и инструментальных (УЗИ почек, печени, поджелудочной железы; ЭКГ; ЭХОКГ) методов обследования. Для оценки скорости клубочковой фильтрации использовали формулу Schwarts [10]. Стадию острого почечного повреждения (ОПП) определяли согласно педиатрической классификации p-RIFLE критериев ОПП [11]. Статистическая обработка включала анализ частоты встречаемости признака и средних величин. Для определения значимости различий использован t-критерий Стьюдента.
Результаты исследования и их обсуждение. Ретроспективный анализ историй болезни показал, что в большинстве случаев (91,3%) гемолитико-уремический синдром был диагностирован у детей первых 3 лет жизни (в том числе в 26,1% случаев у пациентов до 1 года), несколько чаще у мальчиков (соотношение 1.3:1). Заболеваемость ГУС за анализируемый период варьировала в пределах 0,67–5,19 на 100 000 детского населения до 15 лет (рисунок 1).
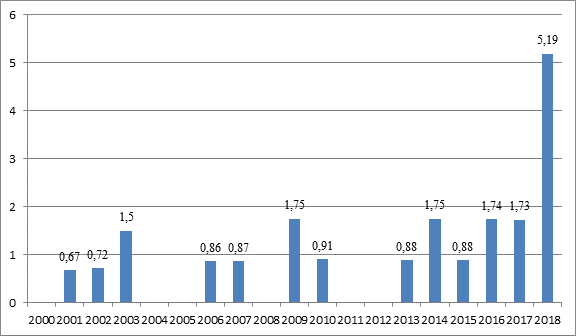
Рис. 1. Заболеваемость ГУС у детей Республики Мордовия
С 2000 по 2010 г. было зарегистрировано 9 случаев ГУС (заболеваемость составила 0,67–1,75 на 100 000 детского населения до 15 лет), тогда как за период с 2011 по 2018 г. – 14 случаев (заболеваемость составила 0,88-5,19 на 100 000 детского населения до 15 лет). Необходимо отметить, что 26,1% (n = 6) случаев заболевания отмечались в 2018 году. Несколько чаще (60,8%; n = 15) ГУС регистрировался в летне-осенний период по сравнению с зимне-весенним сезоном (39,1%; n = 8) (рисунок 2).
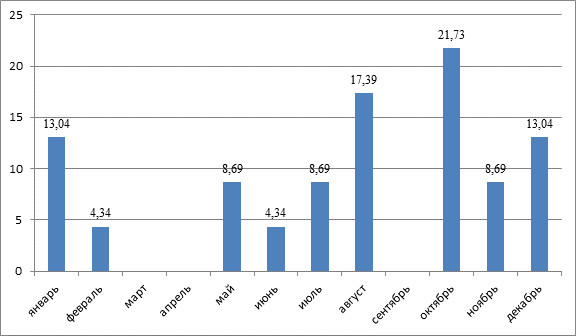
Рис. 2. Частота диагностирования ГУС у детей Республики Мордовия в зависимости от времени года
Продромальная фаза характеризовалась наличием диареи (78,3%), рвоты (69,6%), повышением температуры тела (65,2%), болями в животе (30,4%). Наличие крови в стуле отмечалось только у 6 (26,1%) пациентов в среднем через 3,8 ± 0,8 (2-5) дней от появления диареи. Клинико-лабораторные проявления ГУС диагностированы в среднем через 4,7 ± 1,9 (2–8) дней от момента возникновения патологических симптомов и через 4,1 ± 1,8 (2–5) дней после появления признаков гемоколита. Причем длительность продромального периода у детей первого года жизни была несколько меньше (3,1 ± 0,8; 2–4 дня) по сравнению с больными старше 1 года (5,4 ± 1,8; 2–8 дней). В первые трое суток от начала острой кишечной инфекции развитие ГУС отмечалось у половины детей (50% случаев) первого года жизни и в 29,4% случаев – у пациентов старше 1 года.
У всех детей при госпитализации отмечалась анемия с уровнем гемоглобина у большинства пациентов (69,6%) ниже 80 г/л (74,1 ± 17,8 г/л). Анемия тяжелой степени отмечалась несколько чаще (45,4%) по сравнению со средней (36,3%) и легкой (18,3%) степенью. Необходимо отметить, что повышение содержания непрямого билирубина в крови выявлено у 53,9% больных (49,5 ± 15,8 ммоль/л). Тромбоцитопения отмечалась в 100% случаев, варьировала в пределах 49000–150000 × 109/л (80000,3 ± 25000,8 × 109/л). Показатели тромбоцитов несколько ниже были у детей, имеющих при поступлении стадию недостаточности (70000,2 ± 19150,1 × 109/л), по сравнению с больными, у которых при манифестации ГУС диагностирована стадия повреждения (79380,4 ± 21840,1 × 109/л) и стадия риска (110000,6 ± 36060,2 × 109/л). Лейкоцитоз выявлен у 78,3% пациентов, в том числе у 13,1% - выше 20000 × 109/л. Гематурия наблюдалась в 88,9% случаев, в том числе 50% – макрогематурия. Причем у детей с макрогематурией в 88,9% случаев была диагностирована стадия повреждения ОПП. Протеинурия была выявлена у 77,8% пациентов. При этом слабо выраженная протеинурия отмечалась в 22,2% случаев (в том числе 11,1% - у больных в стадии риска, 11,1% - стадии повреждения ОПП), умеренно выраженная – 44,5% случаев (в том числе 11,1% - у детей в стадии риска, 27,8% - стадии повреждения и 5,6% - стадии недостаточности ОПП), выраженная протеинурия (11,1% случаев) наблюдалась только у больных в стадии недостаточности ОПП.
У трети (30,4%) детей при поступлении отмечалась анурия, более чем в половине случаев (65,2%) наблюдались признаки гипергидратации (отеки, артериальная гипертензия). Несколько чаще (43,5%) была диагностирована II стадия ОПП по сравнению с III (39,1%) и I (17,4%) стадиями. Концентрация мочевины в среднем составила 22,66 ± 6,3 ммоль/л, креатинина - 279,64 ± 89,1 мкмоль/л. В зависимости от стадии ОПП показатели мочевины и креатинина представлены в таблице.
Показатели биохимического анализа крови у детей с ГУС
|
Показатели биохимического анализа крови |
Стадии ОПП |
||
|
I |
II |
III |
|
|
Мочевина (ммоль/л) |
12,2 ± 3,3 |
24,2 ± 7,4 |
25,7 ± 6,5 |
|
Креатинин (мкмоль/л) |
114,8 ± 12,1* |
207,6 ± 67,1 |
360,6 ± 63,7* |
|
Лактатдегидрогеназа (Ед/л) |
1929,8 ± 448,5 |
3355,5 ± 980,8 |
3820,1± 961,1 |
|
Альбумин (г/л) |
31,4 ± 1,9 |
32,1 ± 3,8 |
29,2 ± 4,9 |
*p < 0,001.
У всех больных выявлено повышение уровня лактатдегидрогеназы (ЛДГ) до 3349,1 ± 1107,3 Ед/л. Несколько выше концентрация ЛДГ отмечалась у пациентов с III стадией ОПП по сравнению с I и II стадиями (таблица 1). У большинства пациентов диагностировано снижение альбумина в крови (92,9% случаев) с тенденцией к увеличению степени выраженности в зависимости от стадии ОПП (таблица 1). По данным ультразвукового исследования, у всех детей выявлено увеличение объема почек с уплотнением почечной паренхимы.
Клиника поражения центральной нервной системы в виде генерализованных судорог отмечалась у 5 пациентов (21,7% случаев). При этом 2 из 5 больных были в возрасте до 1 года (5 месяцев, 11 месяцев), 3 – от 1 года до 2 лет. Кроме того, необходимо отметить, что у 4 из 5 детей была диагностирована III стадия ОПП.
Отек поджелудочной железы при ультразвуковом исследовании был выявлен у 47,8% больных, в том числе в 26,1% случаев - у детей с III стадией, 13,1% - II стадией, 8,6% - I стадией ОПП. Повышение уровня амилазы в крови выявлено только у пациентов в стадии недостаточности ОПП до 177 ± 49,6 Ед/л.
Поражение печени проявлялось гепатомегалией в 82,6% случаев, диффузными изменениями паренхимы печени по данным ультразвукового исследования - 30,4%, повышением уровня трансаминаз в 52,2% случаев. Причем повышение содержания АЛТ, АСТ отмечалось у всех пациентов в стадии недостаточности ОПП, у трети (33,3%) - в стадии повреждения, и не отмечалось отклонения от нормы в стадии риска ОПП.
В 21,7% (n = 6) случаев была диагностирована вторичная кардиопатия, проявляющаяся в том числе обменными нарушениями в миокарде (8,6%; n=2), нарушением функциональной способности миокарда (4,3%; n=1), нарушением внутрижелудочковой проводимости (4,3%; n=1), дилатацией обоих предсердий (4,3%; n=1).
Заместительную почечную терапию (перитонеальный диализ) получали 9 (39,1%) детей, в том числе 2 (8,7%) больных первого года жизни и 7 (30,4%) – в возрасте 1–3 лет. Длительность анурии до 7 дней наблюдалась у 4 детей, от 8 до 12 дней – у 4 пациентов, и у 1 ребенка анурия длилась более 1 месяца, с последующим исходом в хроническую почечную недостаточность. Летальность среди детей, находившихся на заместительной почечной терапии, составила 11,1% (n = 1), среди всех пациентов с ГУС – 4,3% (n = 1).
Заключение. Таким образом, заболеваемость ГУС в Республике Мордовия за период с 2000 по 2018 г. варьировала в пределах 0,67–5,19 на 100 000 детского населения до 15 лет с максимальным подъемом (5,19 на 100 000 детского населения до 15 лет) в 2018 году. В большинстве случаев (91,3%) гемолитико-уремический синдром диагностировался у детей первых 3 лет жизни (в том числе в 26,1% случаев у пациентов до 1 года), несколько чаще у мальчиков (соотношение 1.3:1). Манифестации гемолитико-уремического синдрома предшествовали: диарея (78,3%), рвота (69,6%), повышение температуры тела (65,2%), боли в животе (30,4%), появление крови в стуле (26,1% случаев). В период разгара ГУС у трети (30,4%) детей отмечалась анурия, более чем в половине случаев (65,2%) наблюдались признаки гипергидратации, в 21,7% случаев - поражение центральной нервной системы. Проведение заместительной почечной терапии потребовалось в 39,1% случаев. Летальность среди больных, находившихся на заместительной почечной терапии, составила 11,1%, среди всех пациентов с ГУС – 4,3%.
Библиографическая ссылка
Раздолькина Т.И., Московская Е.Ф., Вешкина Т.И., Яушева Е.А., Верещагина В.С. АНАЛИЗ КЛИНИЧЕСКИХ ПРОЯВЛЕНИЙ ГЕМОЛИТИКО-УРЕМИЧЕСКОГО СИНДРОМА У ДЕТЕЙ РЕСПУБЛИКИ МОРДОВИЯ // Современные проблемы науки и образования. 2019. № 2. ;URL: https://science-education.ru/ru/article/view?id=28746 (дата обращения: 07.06.2026).



