В современной хирургической практике широко распространено использование различных эндопротезов. Они представляют собой инородные субстанции, вживляемые в организм пациента, для компенсации утраченных или ослабленных структур, тканей, органов и их функций. Поэтому в связи с появлением новых имплантов все больше происходит расширение сфер их применения и медицинских показаний к использованию таких средств медицинского назначения, что в свою очередь требует всестороннего изучения в условиях многопрофильных лабораторий. Выбор адекватного и эффективного протеза в каждой клинической ситуации – важная задача для врача-хирурга, и для ее решения необходимо знание фундаментальных закономерностей реакции макроорганизма на них [1]. Исследования кафедры оперативной хирургии и топографической анатомии имени профессора А.Д. Мясникова Федерального государственного бюджетного образовательного учреждения высшего образования «Курский государственный медицинский университет» Министерства здравоохранения Российской Федерации (ФГБОУ ВО «КГМУ» Минздрава России), в первую очередь, направлены на изучение безопасности и эффективности применения имплантов.
Главными объектами для разработки и изучения стали: сетчатые протезы, применяемые для герниопластики, пластики трахеи, матки, а также сосудистые импланты, противоспаечные мембраны и гели, губчатые аппликационные гемостатические средства.
Цель исследования: обобщить и изложить в одной работе многолетний опыт кафедры оперативной хирургии и топографической анатомии имени профессора А.Д. Мясникова Курского государственного медицинского университета в изучении имплантов.
Работа в сфере имплантологии на кафедре начиналась с изучения проблемы лечения наружных грыж живота. Классический принцип пластики грыжевых ворот с натяжением тканей является травматичным, сопровождается частыми рецидивами (до 10-30%), в постоперационном периоде выраженной болевой симптоматикой, иногда требующей введения наркотических анальгетиков. Предложенный сотрудниками кафедры метод пластики грыжевых ворот «без натяжения» имеет определенные преимущества перед традиционными методиками: уменьшение операционной травмы, что в свою очередь снижает интенсивность болевой симптоматики в послеоперационном периоде, позволяя в некоторых случаях отказаться от введения наркотических анальгетиков, сокращает время пребывания пациентов в стационаре и лимитирует процент рецидивов до 0,1-1% [2-5]. Однако любой эндопротез воспринимается организмом как инородное тело, что вызывает ассоциированные с протезированием осложнения, такие как скопление серозной жидкости вблизи полотна импланта, образование гематом и нагноение операционной раны. В отдаленном послеоперационном периоде одним из негативных последствий использования эндопротезов может стать и нарушение функции брюшного пресса, парестезии и болезненные ощущения в месте стояния инородного тела, что значительно снижает качество жизни пациентов [6-10].
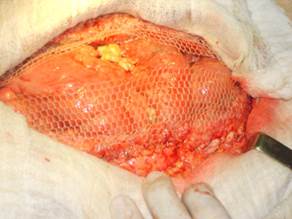
Многие годы на базе кафедры оперативной хирургии и топографической анатомии КГМУ совместно с предприятием ООО «Линтекс» (г. Санкт-Петербург) изучались различные сетчатые импланты с целью обнаружения оптимального варианта, который в меньшей степени вызовет у пациентов различные осложнения. В эксперименте были доказаны преимущества отечественного протеза «Эсфил» в сравнении с имплантами западного производства, что позволило рекомендовать его для использования в клинических условиях. В дальнейшем совместно с кафедрой общей хирургии КГМУ протез «Эсфил» был использован в хирургическом лечении пациентов с послеоперационными вентральными грыжами, ущемленными вентральными грыжами в инфицированных условиях. В эксперименте были доказаны преимущества отечественного протеза «Эсфил» в сравнении с имплантами западного производства, что позволило рекомендовать его для использования в условиях хирургических стационаров. В дальнейшем совместно с кафедрой общей хирургии КГМУ протез «Эсфил» был использован в лечении пациентов с послеоперационными вентральными грыжами, ущемленными вентральными грыжами в инфицированных условиях. Сотрудниками кафедр оперативной хирургии и топографической анатомии и общей хирургии разработан способ эндопротезирования брюшной стенки при операциях на органах брюшной полости и забрюшинного пространства для профилактики образования послеоперационных грыж и коррекции анатомо-функциональной недостаточности брюшной стенки. Также, изучив в эксперименте и клинике возможности использования сетчатых протезов для герниопластики, был апробирован способ лапаростомии крупноячеистым протезом (рисунок 1) в лечении синдрома интраабдоминальной гипертензии у больных с распространенным перитонитом [11].
На базе КГМУ выполнен ряд работ по оценке и исследованию протезов, отличающихся техническими характеристиками (способ плетения и количество волокон в каждой «нити» и пр.), которые разделяли на стандартные и легкие. По результатам исследований установлено, что использование легких протезов типа «Унифлекс легкий» приводит к быстрому, по сравнению со стандартными протезами, инкапсулированию полотна импланта и купированию воспалительных изменений. Стабилизация тканевой реакции на имплант отмечается уже на 30-е сутки, а к 180-м суткам капсула представлена оформленной соединительной тканью, т.е. в течении раневого процесса преобладают репаративные тенденции [12; 13].
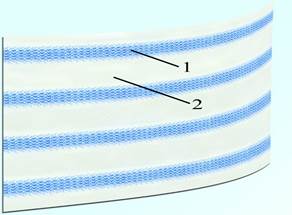
Одним из перспективных направлений кафедры является разработка и экспериментальное изучение материалов с антибактериальными свойствами. Для этого были предложены сетчатые эндопротезы с покрытием наночастицами серебра [14-16]. Показано, что данные материалы наряду с антибактериальной активностью стимулируют репаративные процессы в соединительной ткани, что делает перспективным их использование в клинике. В настоящее время на кафедре в этом направлении проводится разработка методик протезирующей герниопластики, поиск возможностей оптимизации интеграции протеза в биомеханическую систему брюшной стенки. В этой связи создан и экспериментально апробирован новый легкий усиленный эндопротез (рисунок 2) [17]. Предполагается, что протез позволит предотвратить прогрессирование анатомо-функциональной недостаточности брюшной стенки, сохранить ее подвижность при движениях туловища и улучшить качество жизни пациентов.
|
|
|
Рис. 1. Этап лапаростомии крупноячеистым полипропиленовым эндопротезом
|
Рис. 2. Легкий усиленный эндопротез: 1 – усиленная зона, 2 – основная зона |
В настоящее время отмечается тенденция к росту числа случаев длительной ИВЛ, количества трахеостомий, злокачественных новообразований органов дыхания. Все это ведет к увеличению числа пациентов со стриктурами трахеи и формированию ее обширных дефектов [18-21]. Для восстановления анатомической целостности и формы дыхательной трубки прибегают к длительным и, к сожалению, высокотравматичным реконструктивно-пластическим операциям, которые важно выполнять таким образом, чтобы не был нарушен просвет органа. Доля этих операций достаточно мала по причине сложности их выполнения. На данный момент отсутствует универсальная общепринятая методика и протезы для замещения обширных дефектов трахеи [22-24]. На протяжении ряда лет коллектив кафедры оперативной хирургии и топографической анатомии имени профессора А.Д. Мясникова КГМУ в содружестве с уже ранее упомянутой фирмой ООО «Линтекс» занимается решением данной проблемы. По итогам исследований в этой области доказано, что для замещения дефектов трахеи возможно использование сетчатых протезов после их дополнительной экспозиции в претрахеальном пространстве, с целью формирования плотной волокнистой соединительной ткани вокруг протеза. Данная ткань в следующем этапе служит матрицей, некой «подложкой» для роста рыхлой волокнистой соединительной ткани, образование которой в свою очередь обеспечивает герметичность протезу, повышает его эластичность и каркасность. Вышеперечисленные свойства создают необходимые условия для эпителизации внутренней поверхности протеза, образования слизистой оболочки (так называемое двухэтапное замещение – проращивание). На этапе морфологической оценки результатов было установлено, что время экспозиции сетчатого протеза влияет на качество формирующейся перикапсулярной ткани. Для соблюдения всех требуемых свойств подготовленного указанным способом («пророщенного») импланта определена оптимальная экспозиция протеза в претрахеальном пространстве, которая составляет 8 недель [25-27].
Использование «непророщенного» протеза невозможно, замещение участка трахеи неподготовленным сетчатым материалом приводит к множеству осложнений, таких как деформация протеза и нарушение процесса эпителизации, которые в конечном итоге приводят к развитию легочных осложнений [28; 29].
В ходе изучения биомеханических и физико-механических свойств трахеи сделан вывод о прямой зависимости между эластическими свойствами трахеи и импланта, несоответствие которых ведет к осложнениям. Свойства импланта должны быть максимально приближены к свойствам трахеи. Нами была произведена модификация стандартного сетчатого импланта из полипропилена меандровой нитью, которая повысила жесткость протеза, не влияя на его биосовместимость, тем самым приближая имплант к соответствующим нормальной трахее физико-механическим свойствам. Этот проект уже многие годы развивается на базе нашей кафедры. Многие вопросы уже изучены, но еще многие задачи предстоит решить, для того чтобы внедрить эту технологию в практическую хирургию для лечения дефектов трахеи, а в перспективе и для замещения обширных ее участков.
Разработка и тестирование сосудистых имплантов - одно из развивающихся направлений, изучаемых на кафедре. Рост показателей смертности вследствие заболеваний, вызывающих поражение сосудистой стенки, таких как атеросклероз, а также травматические повреждения магистральных артерий ведут к увеличению числа реконструктивных операций, в ходе которых используются пластические материалы для восстановления поврежденных участков артерий. На данный момент не существует имплантов, которые соответствуют всем требованиям так называемого идеального протеза. Многие годы кафедра занимается изучением этой проблемы. Для ее решения были проведены серии экспериментов, нацеленные на исследования:
1) физико-механических свойств сосудистых заплат и их влияние на формирование перикапсулярной оболочки;
2) течения воспаления при использовании различных имплантов;
3) реакции сосудистой стенки на имплантацию протеза.
При изучении физико-механических свойств различных образцов сосудистых заплат разных производителей интересовали такие факторы, как химический состав, толщина заплаты, способ плетения полотна, состав нитей, пористость стенки, прочность образцов и их жесткость. Результатом данных исследований является выявление конкурентных преимуществ вязаных лавсановых имплантов фирмы ООО «Линтекс», таких как минимальная поверхностная плотность, достаточная жесткость, высокая прочность, низкая хирургическая и высокая биологическая пористость. Рассматривалась связь между физико-механическими свойствами протезов и процессом образования перипротезной капсулы. В ходе исследований определено, что доля макрофагов и моноцитов в клеточном слое капсулы прямо коррелирует с поверхностной плотностью и массой образца, а доля клеток фибробластического ряда находится в прямой корреляционной зависимости от толщины имплантов [30].
Также были проведены серии экспериментов, направленных на изучение реакции тканей организма на имплант, в ходе которых рассматривали разные фирмы-производители, сравнивая их по характеристикам скорости протекания воспалительных реакций, выраженности воспалительной реакции и клеточному индексу. Был сделан вывод о том, что реакция тканей лабораторных животных менее выражена при использовании основовязаного лавсанового импланта. Экспериментальным путем была изучена послойная реакция сосудистой стенки на имплантацию протеза в разные сроки экспозиции. Оценивалось выбухание протеза внутрь артерии, а также возможное прободение интимы выпячивающим центром импланта. Доказано, что имплант фирмы «Линтекс» является более стабильным, его волокна реже подвергаются дезорганизации, тем самым его использование в редких случаях ведет к прободению интимы, выпячиванию сосудистого импланта внутрь артерии. По данным электронного микроскопирования, применение лавсановых имплантов отличается большей сохранностью эндотелиальной выстилки [31; 32].
Одной из нерешенных задач абдоминальной хирургии является лечение и профилактика спаечной болезни брюшины. В основе патогенеза избыточного спайкообразования после оперативных вмешательств на органах брюшной полости лежит разрастание соединительнотканных волокон благодаря выпавшему из перитонеального выпота фибрина, который таким образом «склеивает» поверхности органов, а впоследствии такие волокна прорастают сосудами и нервами. Предотвратить развитие описанной ситуации позволит разобщение десерозированных поверхностей на время, необходимое для их ремезотелизации. Для этого применяют вязкие биологически инертные рассасывающиеся барьерные средства [33; 34].
Таким веществом является «Мезогель» (4%-ный водный раствор натриевой соли карбоксиметилцеллюлозы). Он является первым в России сертифицированным барьерным средством. Эффективность данного средства исследовалась нашей кафедрой многие годы. Были проведены серии экспериментов, направленные на изучение барьерной функции препарата на лабораторных животных. В эксперименте на лабораторных животных при использовании средства «Мезогель» отмечалось снижение выраженности спаечного процесса брюшной полости в 7,3 раза по сравнению с животными без применения профилактических средств спайкообразования. Также при оценке влияния указанного средства на патогенную флору выяснили, что оно не вызывает усиления роста и размножения микроорганизмов. Клинические испытания «Мезогеля» проводили совместно с кафедрой общей хирургии КГМУ на базе ОБУЗ КГКБСМП (г. Курск), определили, что введение «Мезогеля» во время операции по поводу острой спаечной кишечной непроходимости позволяет добиться следующих позитивных эффектов: в 2,1 раза снижается системный эндотоксикоз, в 3,3 раза выраженность болевого синдрома, в 2,4 раза улучшается моторно-эвакуаторная функция кишечника в ближайшем послеоперационном периоде, а в отдаленном периоде в 1,3 раза повышается физический компонент качества жизни, что позволяет избежать рецидивов заболевания [35].
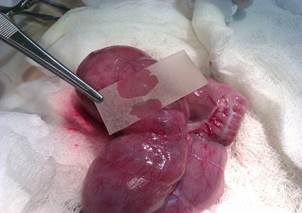
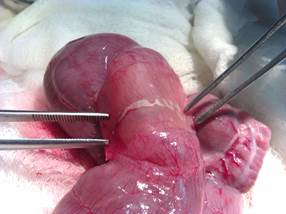
В настоящее время известны различные виды кишечных швов и анастомозов, внедренные в клиническую практику. Однако проблема герметичности и состоятельности швов в послеоперационном периоде остается нерешенной. В ходе изучения солей карбоксиметилцеллюлозы, которая является основой «Мезогеля», была предложена новая функциональная форма в виде рассасывающегося полимерного пленчатого импланта, перспективой использования которого является укрепление швов при операциях на различных отделах желудочно-кишечного тракта и изоляция десерозированных поверхностей. Влияние получившегося импланта на герметичность однорядного кишечного шва изучали в эксперименте in vivo на кроликах породы Советская шиншилла. По итогам исследований были получены следующие результаты: наложение однорядного кишечного шва, герметизированного полимерной мембраной, занимает меньше времени в сравнении с формированием второго ряда узловых швов поверх первого, это значительно уменьшает риск инфицирования брюшной полости [36]. При изучении биологической герметичности и механической прочности толстокишечных анастомозов непосредственно после наложения швов требовалось оказать большое максимальное давление (109,2. ± 1,28 мм рт. ст.) в сравнении с группами исследования, в которых выполнялось наложение однорядного кишечного шва без использования импланта – 64,3 ± 2,18 мм рт. ст. и двурядного кишечного шва – 82,7 ± 1,75 мм рт. ст. соответственно) [37]. В ходе исследования установлено, что изучаемый образец полимерного пленочного импланта обладает такими свойствами, как эластичность, прочность, моделируемость (после имплантации повторяет контуры участка кишки), не требует дополнительной фиксации шовным материалом (рисунок 3 А, Б).
|
А |
Б |
Рис. 3. Макрофотографии (А, Б) этапов герметизации межкишечного анастомоза полимерным пленочным имплантом: А - наложение полимерной мембраны на линию кишечного шва (агрегатное состояние образца - нативное); Б - этап загибания краев полимерной мембраны вокруг участка кишки по ходу линии шва (за счет эластичности, появившейся после контакта мембраны с тканями кишки)
Применение «Мезогеля» в лечении спаечной болезни не единственная его функция. Была проведена работа по исследованию его гемостатической активности при травмах паренхиматозных органов, в ходе чего выяснили, что «Мезогель» обладает сорбционными свойствами и уменьшает величину кровопотери. Используя две конфигурации геля, отличающиеся температурой, мы получили статистически достоверно различающиеся данные. В группе с использованием «Мезогеля» комнатной температуры масса кровопотери при травмах печени и селезенки снизилась и составила 17% и 13% соответственно. Однако в группе с использованием «Мезогеля», подогретого до 36 °С, показатели составили 28% и 40%. Полученные результаты позволяют нам утверждать о гемостатическом свойстве геля, которое основано на формировании матрицы, задерживающей форменные элементы крови, тем самым образуя своеобразную сетку для тромбоцитарного сгустка [38-40].
В рамках исследования способов хирургического гемостаза на кафедре постоянно ведется поиск эффективного губчатого аппликационного кровоостанавливающего средства для использования при травматических повреждениях паренхиматозных органов живота. Нами были разработаны методики моделирования травм и оценки эффективности применения гемостатических средств методиками in vitro и in vivo (время остановки кровотечения и величина кровопотери на моделях стандартных травм печени и селезенки, а также качественные и интегральные показатели), позволяющие в эксперименте всесторонне изучать кровоостанавливающие средства. Результаты исследования позволяют сделать вывод о том, что все использующиеся в эксперименте образцы обладают достоверными кровоостанавливающими свойствами, выраженными в разной степени. Активность последних связана с входящими в состав губок кровоостанавливающими агентами. Более эффективными оказались губки: с транексамовой кислотой 9% и с криопреципитатом 10%, а также гемостатические губки «Биатравм», «Ресорб», «Серджисел Нью Нит» [41; 42].
На начальной стадии изучения сейчас находятся проекты в гинекологии, офтальмологии, урологии.
В экспериментальных условиях нами была доказана возможность укрепления шва матки при помощи сетчатых эндопротезов. Проведена серия экспериментов с использованием протезов фирмы «Линтекс» типа «Унифлекс» и «Эсфил легкий», закрепляя их над швом матки узловыми швами, с целью изучения в динамике характера морфологических изменений миометрия. Оценивая степень разобщенности гладких миоцитов, степень дезорганизации миометрия, интенсивность и распространение гидропической дистрофии, пришли к выводу, что эти материалы обладают недостаточной биосовместимостью и вызывают такие отрицательные эффекты, как формирование кист с воспалительным экссудатом. Также гистологически отмечалась выраженная дезорганизация гладких миоцитов миометрия [43]. Таким образом, на данный момент мы не можем рекомендовать эти материалы для использования в практическом акушерстве и гинекологии, но, безусловно, эта тематика является перспективной и требует дальнейшего экспериментального изучения.
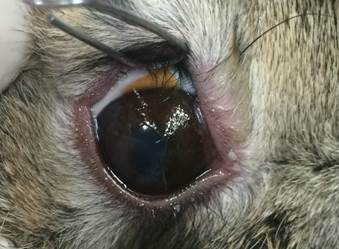
В рамках изучения проблемы инфекционных заболеваний переднего отрезка глаза, совместно с кафедрой офтальмологии КГМУ, было выдвинуто предложение по разработке, изучению и возможному применению полимерных мембран на основе целлюлозы, обладающих пролонгированным антимикробным действием. Выбор данного материала объясняется его высокой степенью адгезии к конъюнктиве и возможностью длительное время аккумулировать активное вещество. Таким образом, использование данного импланта будет способствовать, в короткие сроки, излечиванию инфекционно-воспалительных заболеваний глаз, но успешность данного проекта требует экспериментальных испытаний и дальнейшего изучения тематики (рисунок 4 А, Б) [44].
|
А |
Б |
Рис. 4. Макрофотографии экспериментальной группы с использованием мембран, обладающих антибактериальной активностью. А - дефект эпителия роговицы после нанесения травмы и инфицирования. Б - дефект эпителия роговицы, окрашенный натриевой солью флуоресцеина после нанесения травмы и инфицирования
Одновременная потребность в импланте, обладающем гемостатическим эффектом и структурностью, привело к разработке гемостатических губок, армированных сетчатым протезом. Спектр использования данных комбинированных имплантов велик. Нами была проведена экспериментальная серия клиновидных резекций полюсов почки у кроликов с последующей имплантацией комбинированных имплантов. Целью экспериментов являлось обоснование метода и дальнейшее его применение при органосохраняющих операциях на почках [45; 46].
Заключение
На протяжении многих лет кафедра оперативной хирургии и топографической анатомии им. профессора А.Д. Мясникова КГМУ совместно с ООО «Линтекс» г. Санкт-Петербург успешно проводит исследования, направленные на разработку и изучение отечественных эндопротезов для лечения и профилактики: наружных грыж живота, патологий сосудистой стенки, травматических стриктур трахеи, состоятельности швов кишечника. Мы также ведем разработки новых перспективных передовых направлений использования имплантов в офтальмологии, урологии, гинекологии и трансплантологии и других областях хирургической направленности.
Библиографическая ссылка
Бежин А.И., Липатов В.А., Майстренко А.Н., Нетяга А.А., Рыжов А.С., Северинов Д.А. РАЗРАБОТКА И АПРОБАЦИЯ В ЭКСПЕРИМЕНТЕ ХИРУРГИЧЕСКИХ ИМПЛАНТОВ: ОДНО ИЗ НАПРАВЛЕНИЙ НАУЧНЫХ ИССЛЕДОВАНИЙ КАФЕДРЫ ОПЕРАТИВНОЙ ХИРУРГИИ И ТОПОГРАФИЧЕСКОЙ АНАТОМИИ ИМЕНИ ПРОФЕССОРА А.Д. МЯСНИКОВА КУРСКОГО ГОСУДАРСТВЕННОГО МЕДИЦИНСКОГО УНИВЕРСИТЕТА // Современные проблемы науки и образования. 2019. № 2. ;URL: https://science-education.ru/ru/article/view?id=28680 (дата обращения: 07.06.2026).
DOI: https://doi.org/10.17513/spno.28680