Актуальность проблемы
Острый панкреатит (ОП) остается главной проблем ургентной хирургии, что обусловлено возрастанием уровня заболеваемости и низкими результатами лечения инфекционно-септических осложнений панкреонекроза [1, 2].
Инфицирование ткани поджелудочной железы (ПЖ) и окружающей жировой клетчатки происходит в 40–70% случаев. Это провоцирует массивный по тяжести эндотоксикоз с клинической формой сепсиса с прогрессирующей декомпенсацией всех органов и систем [3, 4].
Прогнозирование течения острого панкреатита способствует своевременному назначению патогенетически направленного консервативного и малоинвазивного лечения, что в ряде случаев может «оборвать» развитие некроза и тем самым предотвратить развитие поздних осложнений.
Проблемы хирургического лечения также окончательно не решены до настоящего времени. Не выработаны четкие показания к малоинвазивным и лапаратомным широким доступам [5].
Общепринятый вариант лечения пациентов с острым панкреатитом в первые 2 недели – консервативно-выжидательная тактика [6]. Но при наличии симптомов раздражения брюшины и УЗИ-признаков свободной жидкости, как правило, применяется лапароскопия для исключения иной патологии, а также с целью санации и дренирования брюшной полости [7]. При увеличении площади некроза в 40–70% случаев может присоединяться бактериальная инфекция с распространением по всей забрюшинной клетчатке забрюшинного пространства [8].
Патогенез ОП к настоящему времени достаточно изучен. Гибель панкреатоцитов происходит достаточно стремительно, и к 3-м суткам ферментативной фазы отмечается их формирование. Реактивная фаза сопровождается сильной воспалительной реакцией организма с выбросом медиаторов воспаления, являющихся дополнительными факторами агрессии. На макроуровне данный процесс выглядит как формирование инфильтрата брюшной полости. Калликреин-кининовая система способствует повреждению сосудистой стенки, выходу жидкой части плазмы в интерстициальное пространство, в котором происходит сдавление гемомикроциркуляторного русла, – возникает так называемый перфузионный блок. Отмечается усиление гипоксии в жизнеспособных тканях. Переход на анаэробный путь окисления приводит к ацидозу и эндотелиальной дисфункции, микротромбообразованию и, как следствие, расширению зоны некрозов. Имеют место образование панкреатических свищей и выход ферментов за пределы поджелудочной железы в свободную брюшную полость. Болевой синдром распространяется над всей поверхностью живота. Снижается барьерная функция кишечника и формированию гнойно-септических очагов. В свою очередь увеличение внутрибрюшного давления за счет пареза кишечника ведет к синдрому интраабдоминальной гипертензии, тем самым дополнительно усугубляет микроциркуляцию в ишемизированных тканях [9, 10].
При введении лекарственных препаратов в венозное русло отмечается их низкая биодоступность в ткани поджелудочной железы и как следствие неэффективность [11]. Прогрессирует интоксикация, инфицируются очаги некрозов, применяются многоэтапные оперативные вмешательства, в результате которых летальность достигает 85% [12]. Все это указывает на необходимость начала ранней адекватной профилактики инфицирования панкреонекроза [13].
Цель исследования
Совершенствование тактики лечения пациентов с острым деструктивным панкреатитом в реактивную фазу путем дополнения комплекса лечения продленной внутриартериальной терапией и дифференцированного хирургического и малоинвазивного лечения для профилактики развития ранних и поздних осложнений.
Материалы и методы исследования
Проведен ретроспективный анализ историй болезни 965 больных с ОП (530 мужчин и 435 женщин) в возрасте от 21 до 80 лет, находившихся на лечении в ГБУЗ КБ № 10 г. Ярославля за период с 2009 по 2016 гг. Отечная форма острого панкреатита диагностирована у 820 (84,9%) больных, деструктивные формы – у 145 (15,1%), инфицированный панкреатит – у 60 (42%): из них очаговый – у 13 (23%); тотальный, субтотальный и крупноочаговый – у 47 (77 %). Стерильный панкреатит – у 85 (57%); из них очаговый – у 62 (73%), тотальный, субтотальный и крупноочаговый – у 23 (27%). Средний койко-день у пациентов с панкреонекрозом (ПН) составил 42,3±7,4 суток. Оценка тяжести состояния больных при поступлении проводилась по шкале APACHE II [14]. Неудовлетворительные результаты вынуждают искать новые подходы к лечению.
Основное число пациентов поступало позднее 24 часов, общая длительность заболевания на момент поступления не превышала 7 суток, что соответствовало реактивной фазе острого панкреатита.
В нашей клинике с целью адресной доставки лекарственных средств (гепарин, пентоксифиллин, верапамил, сандостатин, тиенам, дротаверин, гордокс, контрикал и др.) применяется продленная внутриартериальная регионарная терапия (ПВРТ): производится катетеризация аорты, чревного ствола, желудочно-двенадцатиперстной или селезеночной артерии по методу Сельдингера–Эдмана. Эта методика успешно применяется в мире уже более 50 лет. Однако использование и этого метода в ферментативную фазу было ограничено ввиду позднего обращения пациентов, когда первичные факторы альтерации (липаза, эластаза, трипсин, фосфолипаза А2) активируют каскад вторичных (серотонин, гистамин, брадикинин) и третичных (оксид азота, фактор некроза опухоли, тромбоксан, фактор активации тромбоцитов, простагландины, лейкотриены, интерлейкин 1, 6 и 8). В позднюю фазу – расплавления и секвестрации – также уже нет убедительных данных в пользу эффективности метода продленной внутриартериальной регионарной лекарственной терапии [15].
Критерии включения пациентов в исследование:
– реактивная фаза ОП, формирование инфильтрата в брюшной полости;
– отсутствие положительной динамики клинической картины по интегральной шкале APACHE II (9 и более баллов) в течение 24 часов проводимой консервативной терапии;
– синдром системной воспалительной реакции (СВР) – резорбтивная гипертермия, ЧСС более 90 уд. в минуту, ЧДД более 20 в минуту, число лейкоцитов более 12 х 109;
– подтверждение диагноза по данным УЗИ, МРТ, КТ.
Критерии исключения пациентов из исследования:
– поздняя фаза расплавления, секвестрации и гнойно-септических осложнений;
– положительная динамика по клинической картине и интегральной шкале APACHE II (8 и менее баллов) на фоне проводимой консервативной терапии;
– отсутствие синдрома СВР организма.
Все пациенты (n=66) были разделены на 2 группы.
I группа (n=35) получала консервативное лечение, II группа (n=31) имела то же лечение, но с дополнением ПВРТ.
С целью улучшения перфузии в ПЖ катетер устанавливался чаще всего в гастродуоденальную артерию на 3–5 суток. Мы остановились на следующем комплексе внутриартериальных препаратов: Sol. Drotaverini 4,0; Sol. Pentoxifyllini 5,0; Sol. Verapamili 2,0; Sol. Octridi 0,1 на Sol. NaCl 0,9% – 100,0. Скорость введения указанных препаратов инфузоматом должна быть не более 10 мл в час.
Оценка клинической картины, интегральной шкалы APACHE II, синдрома СВР, определение ферментов в плазме крови и моче, функции внутренних органов проводились на 1-е, 3-и, 5-е, 7-е, 10-е сутки в отделении реанимации. Деструкцию ПЖ подтверждали ультразвуковым исследованием, методом магниторезонансной томографии определяли зону и объем поражения. Признаки перфузионной недостаточности в железе определяли по ангиограммам ПЖ до и после адресной инфузионной терапии. Обработка материала выполнена с использованием программного пакета «BIOSTAT» [16].
Результаты исследования и их обсуждение
Если количество баллов не достигало 8 по шкале APACHE II (отечная форма), пациентам назначали консервативное лечение, которое включало инфузионную, дезинтоксикационную, антисекреторную, антиферментную, спазмолитическую, противовоспалительную терапию. Антибактериальная терапия и энтеральное зондовое питание, как правило, этой категории пациентов не проводились.
Если показатели APACHE II > 9 баллов, с подтвержденным ПН по МРТ или КТ, –назначались карбапенемы. Хирургическое пособие было оказано 89 (61,3%) из 145 пациентов с деструктивными формами острого панкреатита. Лапаротомные операции проведены у 52 (58,4%), летальность достигла 37,5%, лапароскопическая санация и дренирование брюшной полости – у 37 (41,5%) с летальностью 17,2%.
В исследуемой группе (n=31) на ангиографическом исследовании обращало на себя внимание отсутствие артериальной и венозной фазы контрастирования паренхимы в проекции всей поджелудочной железы – «перфузионный блок» (рис. 6). На контрольном рентгенэндоваскулярном исследовании после проведения ПВРТ через 3–5 дней отмечалось значительное усиление контрастирования ангиоархитектоники поджелудочной железы (рис. 2). Летальность в исследуемой группе отсутствовала. Продолжительность госпитализации 30±2,4 суток, что на 12,3 (р<0,005) койко-дней меньше, чем в основной группе. Жалобы на болевой синдром в брюшной полости проходили к 3,2±1,8 суткам, это на 7,2 дня (р<0,05) раньше, чем в основной группе; признаки СВР купировались на 6,4±3,8 сутки, что на 5,6 дня (р<0,05) короче, чем в группе сравнения.
Таким образом, общая летальность у больных с диагнозом «острый панкреатит» в обеих группах составила 4,7%, послеоперационная – 37,5 %; средний койко-день – 42,3±7,4 суток.
У пациентов во II группе с ПВРТ инфицирования панкреонекроза и летальных исходов не было, а средний койко-день составил 30±2,4 суток. Болевой синдром купировался на 7,2 дня раньше, чем в I группе. Признаки синдром СВР также устранялись на 5,6 дня быстрее.
Во II группе отмечается достоверное снижение температуры тела к 3-м суткам и ее нормализация к 10-м суткам. Динамика отражена на рисунке 1. Нормализация показателей лейкоцитарного индекса интоксикации достоверно происходит на 5-е сутки ПВРТ (рис. 2) с одновременным повышением концентрации альфа-амилазы в плазме крови пациентов на 3-и сутки (рис. 3). Показатели билирубина на 7-е сутки достоверно снижались и достигали нормальных величин (рис. 4). На рисунке 5 приведена динамика состояния больных по APACHE II.
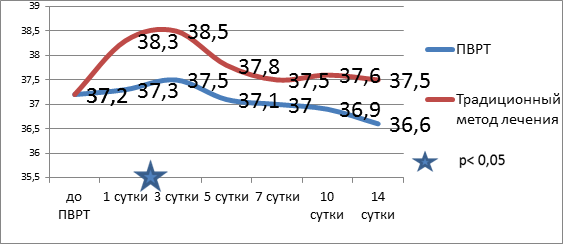
Рис. 1. Динамика показателей температуры у больных в реактивную фазу панкреонекроза при традиционном методе лечения и в комплексе с ПВРТ
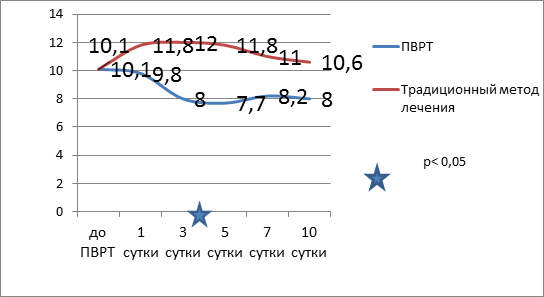
Рис. 2. Динамика показателей лейкоцитарного индекса интоксикации у больных в реактивную фазу панкреонекроза при традиционном методе лечения и в комплексе с ПВРТ
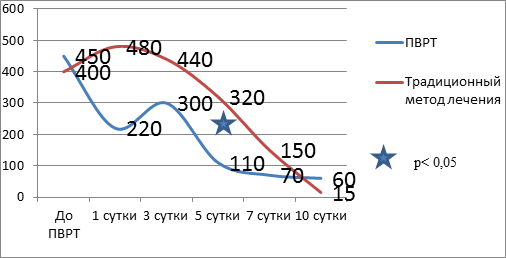
Рис. 3. Динамика альфа-амилазы
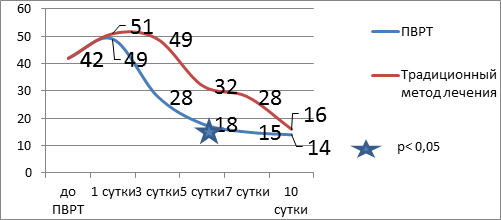
Рис. 4. Динамика билирубина
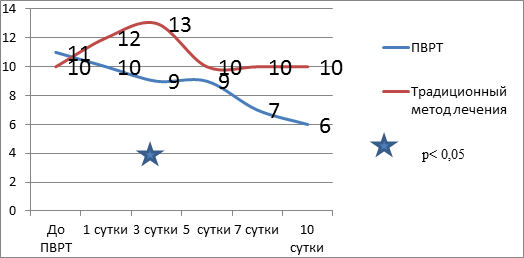
Рис. 5. Динамика состояния больных по APACHE II в реактивную фазу панкреонекроза при традиционном методе лечения и в комплексе ПВРТ
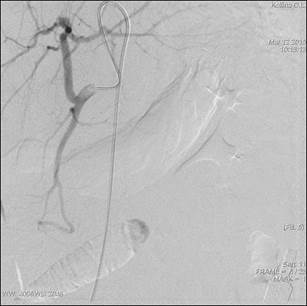
Рис. 6. Диагностическая ангиография перед проведением ПВРТ через 3 суток от начала заболевания
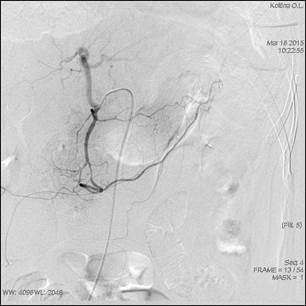
Рис. 7. Контрольная ангиография через 6 суток после ПВРТ
На рисунках 6 и 7 представлен пример успешного лечения пациента К., 1963 г.р., в реактивную фазу панкреонекроза, с инфильтратом брюшной полости (APACHE II 10 баллов), поступавшего по экстренным показаниям с клиникой острого панкреатита спустя 24 часа с момента заболевания. При проведении консервативной терапии у пациента не было существенной положительной динамики. Нарастали явления интоксикации (лейкоцитоз до 25 х 109, сохранялась субфебрильная температура, нарастали явления печеночно-почечной недостаточности, по УЗИ отмечались выпот в сальниковой сумке, брюшной полости, увеличение поджелудочной железы, отек парапанкреатической клетчатки). Пациенту были поставлены показания к селективной катетеризации панкреатодуоденальной артерии с целью диагностики сосудистых нарушений и продленной инфузии лекарственных препаратов для остановки патологического процесса. На первичной ангиографии выявлено скудное контрастирование сосудистого русла поджелудочной железы. Для ПВРТ были выбраны препараты: Sol. Drotaverini 4,0; Sol. Pentoxifyllini 5,0; Sol. Verapamili 2,0; Sol. Octridi 0,1. На 6-е сутки на контрольной селективной ангиографии выявлены артериальная и венозная фазы органного кровотока. Положительная клиническая картина.
Выводы
Включение ПВРТ в комплекс лечения панкреонекроза в реактивную фазу способствует «обрыву» деструктивного процесса, снижению вероятности инфицирования и летальных исходов. Таким образом, разрабатываемая в клинике тактика индивидуального подхода к выбору метода лечения больных острым деструктивным панкреатитом в зависимости от стадии течения и наличия осложнений, а также применение малоинвазивных хирургических технологий и современных методов адресной инфузионной терапии позволяют снизить общую и послеоперационную летальность, сократить пребывание пациентов в стационаре и конечную стоимость лечения.
Библиографическая ссылка
Ширяев Н.П., Хорев А.Н., Благов Д.А., Плюта А.В., Абляев Э.В., Красавин Г.В., Бабич А.А., Клоков В.А. ЗНАЧИМОСТЬ ПРОДЛЕННОЙ ВНУТРИАРТЕРИАЛЬНОЙ ЛЕКАРСТВЕННОЙ ТЕРАПИИ В КОМПЛЕКСНОМ ЛЕЧЕНИИ ПАНКРЕОНЕКРОЗА // Современные проблемы науки и образования. 2019. № 2. ;URL: https://science-education.ru/ru/article/view?id=28662 (дата обращения: 07.06.2026).
DOI: https://doi.org/10.17513/spno.28662



