Согласно данным ежегодных статистических отчетов смертность от последствий дорожно-транспортных происшествий составляет более 1,3 млн случаев и к 2020 г. достигнет пятой позиции среди основных причин смертности и инвалидности [1]. На долю переломов бедренной кости приходится более 10% от всех дорожных травм, ежегодный риск таких переломов составляет от 1 до 3 млн человек в год [2]. Травматические переломы бедренной кости имеют место более чем в 10% повреждений опорно-двигательного аппарата и преимущественно встречаются у молодых людей трудоспособного возраста [3]. Тяжелые повреждения опорно-двигательного аппарата, к которым относятся переломы бедренной кости, сопровождаются системным ответом организма на травму и включают комплекс нейроэндокринных, гемостазиологических и иммунных изменений уже через несколько минут после травмы. Ведущие позиции в реализации ранних системных реакций организма на обширное повреждение тканей занимают факторы врожденного иммунитета. В то же время недостаточное понимание функциональной интеграции комплексного ответа на травматическое повреждение тканей при переломах длинных трубчатых костей, включая факторы как врожденного, так и адаптивного иммунитета, является основным препятствием для создания инновационных методов лечения и совершенствования эффективной терапевтической стратегии при переломах бедра.
Цель работы – провести критический анализ научной литературы в базах данных, индексированных в рецензируемых источниках Рubmed и Российского индекса научного цитирования за период 2010–2018 гг., о механизмах включения системного воспалительного ответа и врожденного компартмента иммунной системы в ответ на травматическое повреждение бедренной кости.
Система комплемента, а также другие плазменные протеолитические системы (фибринообразования, фибринолиза, калликреин-кининовая) активируются в первые минуты после травмы и имеют значение в координации иммунного ответа [4]. Интегративная роль активации системы комплемента в иммунном ответе после травмы представлена на рисунке 1. Активация системы комплемента и концентрация ее компонентов в плазме, прежде всего анафилотоксинов С3а, С4а, связаны с тяжестью травмы и инфекционными осложнениями; отношение С3а/С3 рассматривается как маркер развития острого респираторного дистресс-синдрома, сепсиса, полиорганной недостаточности. После переломов уровень sC5b-9 и Bb коррелирует с тяжестью травмы, гипоперфузией тканей (за счет перекрестной активации тромбина), плохим клиническим прогнозом.
Концентрация C5а в сыворотке возрастает через несколько минут после травмы и коррелирует с показателями смертности, в том числе в связи с ограничением апоптоза и накоплением нейтрофилов в очаге повреждения, вызывающих увеличение площади вторичной альтерации [5]. Избыточная активация системы комплемента чревата развитием комплементопатии со снижением гемолитической активности комплемента и формированием иммунодефицита после переломов бедренных костей. Имеются данные о роли С3а и С5а в развитии респираторного дистресс-синдрома взрослых и полиорганной недостаточности после травматического повреждения тканей, а повышение концентрации С3а и С5а в сыворотке в течение часа после травмы рассматривается как предиктор респираторного синдрома взрослого типа и полиорганной недостаточности [6]. Ряд исследователей не подтверждают связь между уровнем С3а и С5а в сыворотке и клиническими проявлениями. В целом большинство авторов констатируют развитие посттравматической «комплементопатии» (по аналогии с посттравматической «коагулопатией») при тяжелых механических травмах, включающее не только последствия активации системы комплемента, но также истощение ее компонентов, а также дисфункцию в связи с нарушением работы ингибиторов комплемента [7, 4].
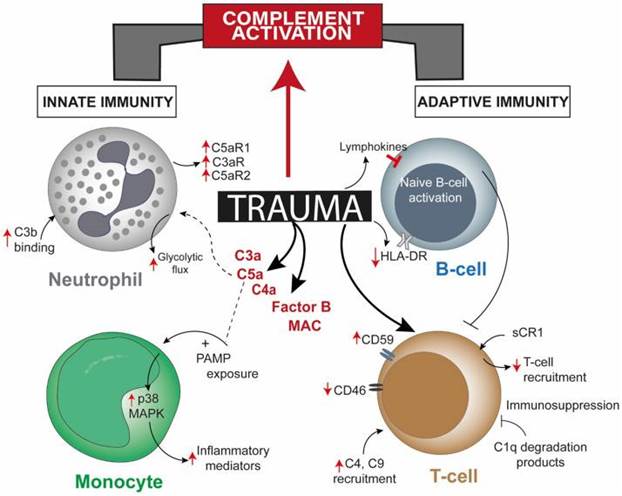
Рис. 1. Роль активации комплемента в реализации врожденного и адаптивного иммунитета после травмы (цит. по [4])
С5а в условиях травмы не только активирует функции нейтрофилов и формирование ВНЛ, изменение метаболизма ПЯЛ за счет усиления гликолиза, но также повышает экспрессию адгезивных молекул на эндотелии, активирует моноциты через р38-МАРК-зависимые пути. Эффекты С5а опосредованы через два рецептора – C5aR1, C5aR2 [8]. Установлено, что блокада рецепторов C5aR1, C5aR2 и C3aR на нейтрофилах коррелирует с инфекционными осложнениями и полиорганной недостаточностью после травмы, а интегрированный клинико-транскриптомный анализ РНК лейкоцитов установил, что низкая экспрессия С5 на 1-й день после травмы сопряжена с развитием нозокомиальных инфекций [9].
В последние годы накоплено большое количество сведений о роли системы комплемента в посттравматическом изменении активности адаптивного иммунитета. Так, продемонстрирована роль повышения концентрации С3 в сыворотке и Т-клеточной инфильтрации очага повреждения [10]. Полагают, что анафилотоксины С3а, С4а, С5а участвуют в регуляции Th17-зависимых реакций. Так, С5а через индукцию миграции дендритных клеток из брюшной полости в кровь приводит к экспансии Th17. Показана роль С5а в регуляции активности T-клеток после травматического повреждения тканей, ассоциированного с DAMP- и PAMP-зависимыми механизмами через стимуляцию или ингибицию продукции макрофагами ИЛ-17, ИЛ-23 [11]. Кроме этого, С5а стимулирует высвобождение гистонов из нейтрофилов, которые в свою очередь индуцируют апоптоз лимфоцитов [12]. Приводят данные о роли системы комплемента в изменении количества и функциональной активности В-клеток после травматического повреждения тканей, инициирующим фактором выступает синдром ишемии-реперфузии при травме [13]. Продемонстрирована роль классического пути активации комплемента и связанной с ним продукции IgM, IgG в формировании вторичной альтерации в ходе ишемии-реперфузии. Изменение синтеза Ig различных классов, а также другие функции В-клеток регулируются С3, комплексом CD19-CR2 и иными факторами [4].
У трансгенных мышей C5aR1-/- и C5aR2-/- по сравнению с контрольной группой диких мышей увеличивается костная масса: у C5aR1-/- за счет снижения количества остеокластов, их гибели путем апоптоза, а у C5aR2-/- за счет увеличения количества остеобластов; после изолированного перелома бедренных костей воспалительный ответ был более выражен у мышей C5aR2-/-, а образование каллюса ускорялось у обоих типов трансгенных мышей [14]. Показано, что избыточная экспрессия C5aR1 в остеобластах значительно ухудшает репарацию костной ткани после травматического перелома [15].
Как видно, роль системы комплемента не ограничивается участием в осуществлении воспалительных реакций, активации клеток врожденного и адаптивного иммунитета, ее компоненты необходимы для опсонизации и удаления не только патогенов, но и погибших клеток, а также репарации костной ткани после повреждения. Компоненты комплемента выступают в роли хемоаттрактантов для стволовых клеток, включая остеобласты и хондробласты при переломах костей, необходимы для поддержания жизнеспособности и получения трофических факторов клетками в области перелома. Рецепторы C3aR и C5aR представлены на остеобластах, хондроцитах, мезенхимальных стволовых и иных клетках, участвующих в заживлении костей после механического повреждения [16]. В экспериментах in vitro и in vivo показана роль C5aR на остеобластах и остеокластах в заживлении костной ткани после поперечного перелома большеберцовой кости за счет активации хемотаксиса остеобластов, остеогенной дифференцировки мезенхимальных стволовых клеток [17].
К ранним реакциям в ответ на массивное повреждение тканей (перелом бедренной кости, сопутствующие повреждения мягких тканей, кровопотеря) относят также формирование синдрома системного воспалительного ответа (SIRS) в результате высвобождения эндогенных факторов DAMPs (damage-associated molecular patterns), к которым в том числе относят митохондриальную ДНК, формиловые пептиды, белок хроматина HMGB1 (High-mobility group box protein) [18, 5]. Именно с DAMPs связывают раннюю активацию систему комплемента, нейтрофилов, моноцитов.
Многие клеточные продукты, синтезируемые в ответ на активацию PRR (паттерн-распознающих рецепторов), таких как TLR, NLR, CLR, MBL, RAGE и иные, рассматривают в качестве диагностических маркеров локальных и системных изменений иммунного статуса, контроля течения посттравматического периода, эффективности проводимой терапии, прогноза инфекционных осложнений, репаративных процессов: ИЛ-1β, ИЛ-33, HMGB1, S100B, белки теплового шока HSP27, HSP60, HSP70, HSP72 и др. Кроме этого, они являются потенциальными терапевтическими мишенями модуляции посттравматических расстройств гомеостаза [18].
Нейтрофилы первыми мигрируют в очаг травматического повреждения и активируются в том числе в ответ на высвобождение PAMPs, DAMPs (такие как АТФ, гистоны, митохондриальная ДНК и др.), активацию комплемента, кининовой системы и коагуляционного каскада, повышение концентрации провоспалительных цитокинов и иные факторы [19]. Активация нейтрофилов опосредована паттерн-распознающими рецепторами, такими как TLRs, NLRs, RAGE, пуринергические рецепторы и др. [20]. Комплекс внутриклеточных событий в нейтрофилах после травмы описывают как «генетический шторм» [21]. Про- и противовоспалительные эффекты нейтрофилов включают хемотаксис, секрецию цитокинов (ИЛ-6, ИЛ-8, ИЛ-1ra, ИЛ-10 и др.), АФК, фагоцитоз, образование НВЛ [22]. Нейтрофилы после травмы участвуют в деградации гема, относящегося к DAMPs, за счет повышения экспрессии гаптоглобина и гемоксигеназы-1 [9]. Неоспорима роль нейтрофилов в инициации репаративных процессов в поврежденных тканях.
Следует учитывать значительную роль нейтрофилов в повреждении интактных клеток и тканей, окружающих зону травмы за счет высвобождения протеаз (эластаза и др.), АФК, провоспалительных микрочастиц, формирования внеклеточных нейтрофильных ловушек, накопления лактата в тканях [23]. Гистоны и ДНК нейтрофилов сами выступают в роли DAMPS и инициируют дальнейшее воспаление, замыкая circulus vitiosus. Кроме этого, первоначальная активация нейтрофилов может смениться угнетением их функции, прежде всего бактерицидной, что в том числе обусловлено высвобождением незрелых нейтрофилов из костного мозга [24].
Выраженность участия нейтрофилов в иммунных реакциях после травматического повреждения определяется многими факторами (рис. 2). Прежде всего это тяжесть первичного механического повреждения тканей, объем хирургического вмешательства, наличие геморрагического шока, внутрибольничные инфекции, коморбидная патология с иммунодефицитом, факторы микробиома, эпигенетический статус.
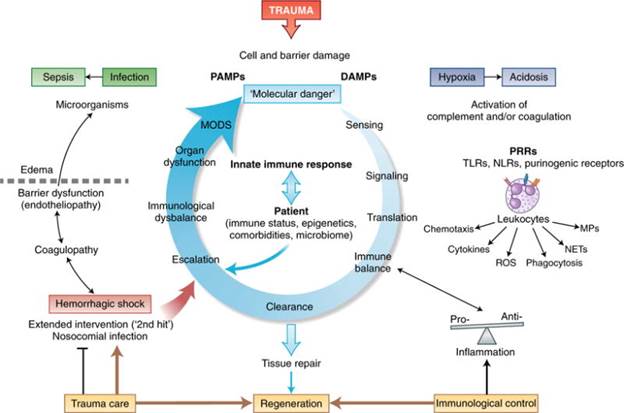
Рис. 2. Роль факторов врожденного иммунитета в посттравматических изменениях гомеостаза (цит. по [19])
Следует отметить, что избыточные реакции врожденного иммунитета (синтез провоспалительных цитокинов, АФК, активация комплемента) могут привести к повреждению и дисфункции эндотелия, что облегчает выход в ткани PAMPs и DAMPs, активирует иммунные реакции и замыкает порочный круг повреждения тканей на ранних этапах после травмы, приводит к возникновению инфекционных осложнений, сепсиса, синдрома полиорганной дисфункции (MODS) [25]. Позднее (14 дней и более после травмы) в связи со стойким катаболизмом белка, супрессией врожденного и адаптивного иммунитета может развиваться синдром стойкого воспаления – иммуносупрессии и катаболизма (PICS), который коррелирует с нарушением репарации тканей, инфекциями, высоким уровнем смертности [26]. Одним из серьезных последствий избыточной активации факторов врожденного иммунитета является повреждение эпителия кишечника и легочной ткани.
В свою очередь избыточная продукция нейтрофилами и моноцитами/макрофагами матриксных металлопротеиназ, протеаз, АФК, лактата, провоспалительных микрочастиц, а также одновременная активация вегетативной нервной системы (как ответ на стресс при травме, генерализованная вазоконстрикция и снижение секреции NO) в совокупности приводят к глобальной дисфункции и повреждению эндотелия [27]. Нарушение микроциркуляции после вазоконстрикции приводит к активации коагуляционного гемостаза, комплемента и тромбоцитов [28]. Компоненты комплемента вызывают повреждение и нарушение деформабильности эритроцитов, усугубляя нарушения микроциркуляции [29]. Тканевой фактор из поврежденных тканей и активированных лейкоцитов запускает образование тромбина, который вместе с АФК, ферментами, компонентами DAMPs (митохондриальная ДНК) и иными факторами повышают экспрессию адгезивных молекул на эндотелиоцитах, проницаемость за счет нарушения плотных контактов, разрушения ГАГ, гликокаликса эндотелиоцитов и вызывают повреждение эндотелия [30]. В целом посттравматические изменения эндотелия, обусловленные факторами врожденного иммунитета, включают изменение фенотипа эндотелиоцитов с антиадгезивного на проадгезивный, с антикоагулянтного на прокоагулянтный, эпигенетические изменения активности генов ферментов (Rittirsch D,2016).
Выводы
1. Массивная травма, включающая повреждение костной и мягких тканей бедра, сопровождается включением ранних реакций врожденного компартмента иммунной системы с последующим развитием «комплементопатии» и формированием вторичного иммунодефицита.
2. На роль диагностических маркеров локальных и системных изменений иммунного статуса, а также перспективных мишеней модуляции посттравматических расстройств гомеостаза, инфекционных осложнений, репаративных процессов могут претендовать следующие клеточные продукты: TLR, NLR, CLR, MBL, RAGE, IL-1β, IL-33, HMGB1, S100B, белки теплового шока и др.
3. Избыточные реакции врожденного иммунитета приводят к дисфункции эндотелия и замыкают порочный круг повреждения тканей на ранних этапах после травмы, что приводит к возникновению инфекционных осложнений, сепсиса, синдрома полиорганной дисфункции.
Библиографическая ссылка
Осиков М.В., Давыдова Е.В., Абрамов К.С. ВРОЖДЕННЫЙ ИММУНИТЕТ ПРИ ИЗОЛИРОВАННЫХ ПЕРЕЛОМАХ БЕДРЕННОЙ КОСТИ // Современные проблемы науки и образования. 2019. № 1. ;URL: https://science-education.ru/ru/article/view?id=28540 (дата обращения: 16.05.2026).



