В современных исследованиях ускорительная масс-спектрометрия (УМС) находит широкое применение в таких науках, как экология, биоорганическая химия, молекулярная биология, иммунология, фармакология, токсикология, а также позволяет осуществлять генетический анализ. Почти во всех этих приложениях используется уникальная чувствительность УМС, которая более чем в 1000 раз выше чувствительности альтернативных методов. С помощью УМС определяются механизмы связывания канцерогенов с ДНК, возраст и время обновления клеток, проводится количественный? анализ состава протеом [1, 2]. Это определяет возможности применения УМС для углубленного изучения отдельных вирусных белков, нахождения первичнои? структуры, возможность секвенирования de novo и определения посттрансляционных модификации? [1].
На сегодняшний день наиболее широко масс-спектрометрический анализ применяется для изучения биологически значимых молекул в пептидах, он позволяет не только устанавливать форму и функции белков, но и проводить полный скрининг. Данный факт объясняется колоссальным разнообразием белков в живых организмах и их исключительнои? функциональной важностью. От установления структуры и функции отдельных белков молекулярная биология перешла к их сплошному скринингу. Современный масс-спектрометрический метод анализа позволяет определять сложные белковые смеси, такие как белки – мишени лекарств или биомаркеры, даже при очень низких концентрациях. В настоящее время нанобиотехнология открывает возможности поиска новых подходов к решению актуальных проблем диагностики в вирусологии.
Среди острых респираторных вирусных инфекций наиболее значимые социально-экономические проблемы вызывает грипп. Вирус гриппа А может вызывать стохастические эпизоотии, ежегодные эпидемии и случайные пандемии. Не так давно, в 2009 г., из-за вируса гриппа A(H1N1)pdm09 возникла первая пандемия в XXI в. Данному патогену было уделено пристальное внимание в связи с опасением повторения катастрофической гриппозной пандемии, аналогичной «Испанке», вызванной вирусом H1N1 в 1918 г. и унесшей по разным оценкам от 50 млн до 100 млн жизней по всему миру. Молекулярные механизмы, за счет которых пандемический вирус гриппа A(H1N1)pdm09 преодолел межвидовой барьер и приобрел высококонтагиозные свойства, легко передаваясь от человека к человеку, до сих пор до конца не изучены. На примере именно пандемического вируса гриппа A(H1N1)pdm09 доказана способность патогена за короткий пассажный период достигать 100%-ной адаптации к млекопитающим и вызывать высоколетальное заболевание среди инфицированных [3]. Данные результаты позволяют предсказать развитие событий в случае создания благоприятных условий для циркулирующего пандемического вируса гриппа к той популяции млекопитающий, иммунный ответ которых он может элиминировать.
Разработка нового метода диагностики с использованием ускорительной масс-спектрометрии позволит изучить вирус-клеточное взаимодействие на примере вируса гриппа с введеннои? меткои? радиоуглерода. Обогащение изотопом 14С вируссодержащей жидкости (ВСЖ) позволит провести сверхточный (с поштучным подсчетом) анализ количества проникших вирусных частиц в легкие экспериментально инфицированных млекопитающих. Благодаря данному методу станет возможным углубленное изучение вирус-клеточного взаимодействия и механизма развития высоколетальнои? инфекции.
Ввиду постоянной эволюции вируса гриппа А крайне важно изучать его вирусологические и химико-физические свойства, поскольку новые данные принесут как фундаментальные, так и важные прикладные знания о вирус-клеточном взаимодействии на примере вируса гриппа в такие области исследований, как ветеринария и медицина.
Цель исследования: разработка метода диагностики вирус-клеточного взаимодействия с помощью ускорительной масс-спектрометрии.
В связи с целью были поставлены следующие задачи:
1) вычисление количества вирусных частиц в ВСЖ и требуемой радиоактивной дозы;
2) разработка методики внесения радиоуглеродной метки в белки вирусной частицы.
Материалы и методы исследования
Для разработки метода диагностики вирус-клеточного взаимодеи?ствия с помощью ускорительной масс-спектрометрии были выбраны нижеследующие реактивы:
– меченая мочевина в виде препарата «Уреакапс» (37 кБк, АО НИФХИ им. Л.Я. Карпова);
– метиловый спирт с радиоуглеродной меткой (радиохимическая чистота 98%, В/О «Изотоп»);
– крос-линкер 1-этил-3-(3-диметиламинопропил)карбодиимид (EDC) (AppliChem, Германия),
– пандемический вирус гриппа А штамм A/Tomsk/273-MA3/2010(H1N1pdm09), адаптированный к аутбредным мышам CD1 (MA-CD1).
Зауглероживание биологических образцов для дальнейшего УМС-анализа будет проводиться на абсорбционно-каталитической установке в ФГБУН Институте катализа им. Г.К. Борескова СО РАН [4], определение содержания радиоуглерода − на уникальной научной установке «Ускорительный масс-спектрометр Института ядерной физики СО РАН» (УНУ «УМС ИЯФ СО РАН») [5].
Результаты исследования и их обсуждение
В связи с ужесточением таможенных требований Российской Федерации на перевозку радиоактивных веществ методика внесения метки в любые материалы, в том числе вирусы, определяется прежде всего доступностью соединений, меченных радиоуглеродом. С этой точки зрения в качестве исходных меченых веществ можно использовать радиоактивные метанол и мочевину. Последний реагент выпускается АО НИФХИ им. Л.Я. Карпова и реализуется для медицинских целей, препарат имеет активность 37 кБк. Оба вещества – и метанол, и мочевина – могут быть ковалентно пришиты к карбоксильным группам белковых молекул, находящимся в оболочке вирусных частиц. Для связывания с вирусным белком первичного амина (мочевины) или спирта (метанола) с образованием амидной или простой эфирной связи соответственно необходима активация карбоксильной группы белка, для чего используют так называемые кросс-линкеры – карбодиимиды. Наиболее распространенным из них является дициклогексил карбодиимид (англ. DCC), использование которого подразумевает проведение реакций в органических растворителях, таких как ацетонитрил, метанол, ДМСО и других, что делает DCC непригодным для внесения метки в биологические объекты, в том числе вирусы. Связывание веществ, имеющих аминогруппу (в нашем случае это мочевина), с карбоксильными группами белков (в нашем случае – вирусных) в водной среде проводят с помощью водорастворимых карбодиимидов, чаще всего 1-этил-3-(3-диметиламинопропил)карбодиимида (англ. 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide, EDC, EDAC или EDCI) по механизму, представленному на рисунке.
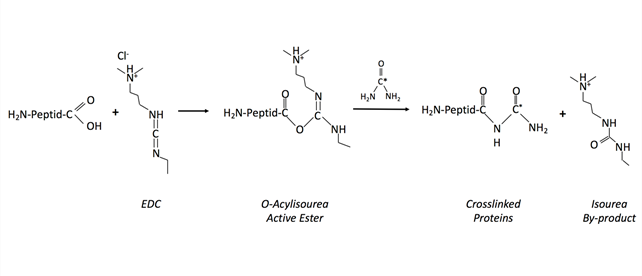
Схема механизма связывания карбоксильной группы, расположенной на поверхностном белке вируса гриппа, с первичным амином (на примере мочевины, меченной 14С)
через активацию карбоксильной группы белка кросс-линкером EDC
(1-ethyl-3-(3-dimethylaminopropyl)carbodiimide).
Результатом реакции белковых групп и мочевины в присутствии EDC являются амидная связь между белком и мочевиной и образование побочного продукта из EDC в виде изомочевины.
Если требуется провести связывание карбоксильной группы со спиртовой группой (например, в случае меченого метанола), можно использовать тот же водорастворимый карбодиимид EDC, однако необходимо присутствие катализатора, в качестве которого обычно применяется 4-диметиламинопиридин (4-dimethylaminopyridine, DMAP).
Очевидно, что для внесения метки необходимо определить количество присутствующих на поверхности вируса гриппа карбоксильных групп и концентрацию вирусных частиц в пробе.
Морфология вирусных частиц (вирионов) чаще представлена в виде сферической формы диаметром 80–120 нм, их оболочка образована липидным бислоем, сформированным из плазматическои? мембраны клетки-хозяина [6, 7]. На поверхности вирусной оболочки находятся гликопротеины – гемагглютинин (hemagglutinin, НА), нейраминидаза (neuraminidase, NA) и интегральный мембранный белок (membrane protein, М2). Первые два гликопротеина представлены в форме шипов и имеют в своей структуре рецептор-связывающие домены (антигенные сайты, эпитопы), при помощи которых вирус взаимодействует с антителами. Для расчета количества карбоксильных групп, содержащихся на поверхности вириона вируса гриппа А, нами был выбран пандемический вирус гриппа A(H1N1)pdm09 в связи с тем, что циркуляция данного патогена до сих пор сохраняется среди сезонных вирусов гриппа.
В условиях BSL3 (biosafety level 3) нами ранее был получен адаптированный вариант вируса гриппа А(H1N1)pdm09 (штамм A/Tomsk/273MA3/2010(H1N1pdm09) (MA-CD1) путем пассирования через аутбредных мышей CD1, вызывающий высоколетальное заболевание среди инфицированных животных и в результате инфекции приводящий к 100%-ной летальности [3]. Расчет количества карбоксильных групп, содержащихся на всех вирусных частицах в объеме 1 мл штамма MA-CD1, выполнили на основании общепринятых данных из литературы [6] и вычисления значения гемагглютинирующей единицы (ГАЕ):
1) согласно литературным данным на поверхности одного гемагглютинина вируса гриппа А субтипа Н1 может быть расположено до 103 аминокислотных остатков, содержащих карбоксильные группы, в антигенных сайтах (наиболее вариабельные эпитопы, взаимодействующие с антителами) [8-10];
2) согласно литературным данным на поверхности одной неи?раминидазы вируса гриппа А субтипа Н1 имеется до 25 эпитопов [11-13];
3) согласно литературным данным на вирионах сферической? структуры располагается примерно 500 шипов HA и 100 шипов NA [7, 14, 15];
4) известно, что 1000 ГАЕ/мл обеспечивается (2–4) x 1010 шт/мл вирусных частиц [6];
5) для штамма MA-CD1 это значение составляет 640 ГАЕ/мл, значит, физический титр вируса гриппа равен
640 ГАЕ/мл x (2-4)x1010
--------------------------
1000 ГАЕ/мл
и дает значение в диапазоне (128–256) x 108 шт/мл;
6) из расчета 128 х 108 шт/мл активных вирусных частиц определяем число карбоксильных групп по нижней границе:
128 х 108 шт/мл х (500 гемагглютининов на поверхности 1 шт вирусной частицы х 103 аминокислоты на поверхности 1 шт НА + 100 нейраминидаз на поверхности 1 шт вирусной частицы х 25 аминокислот на поверхности 1 шт NA) = 6912 x 1011 ед.;
7) из расчета 256 х 108 шт/мл активных вирусных частиц определяем число карбоксильных групп по верхней границе:
256 х 108 шт/мл х (500 гемагглютининов на поверхности 1 шт вирусной частицы х 103 аминокислоты на поверхности 1шт НА + 100 нейраминидаз на поверхности 1 шт вирусной частицы х 25 аминокислот на поверхности 1 шт NA) = 13824 x 1011 ед.
Если в одной пробе объемом 1 мл около (128–256) x 108 шт вирусных частиц, а на их поверхности находится 1014–1015 карбоксильных групп, то для внесения радиоуглеродной метки в пробу потребуется 1014–1015 молекул мочевины. В одной капсуле Уреакапс содержится около 1016 молекул мочевины с радиоуглеродом, значит, потребуется 10–100?кратное разбавление препарата для проведения реакции связывания метки с вирусным белком одной пробы, можно ожидать активность 1 мл пробы в диапазоне от 3700 до 370 Бк. При работе с метанолом с активностью 40 МБк потребуется 10000–100000-кратное разбавление с получением активности пробы того же порядка. Если в организм лабораторного животного масcой около 20 г будет введено 5 мкл пробы, меченной ВСЖ, то оценка удельной активности биологической пробы в среднем по нижней границе дает 0,9 Бк/г, что в 3 раза превышает фоновую активность радиоуглерода живых объектов. Таким образом, можно ожидать достоверного УМС-анализа получаемых проб на содержание радиоуглерода, а значит, и на содержание вирусных частиц.
Для получения контрольного раствора-аналога без радиоактивной метки планируется проведение реакции взаимодействия вирусных частиц с немеченой мочевиной в присутствии EDC в тех же условиях.
Таким образом, предлагается технология, основанная на связывании меченных радиоуглеродом веществ (мочевины и/или метанола) и карбоксильных групп белков вируса гриппа. Связывание затрагивает только углерод в свободных карбоксильных группах и не сопровождается существенным изменением структуры молекулы. Реакция протекает в водной среде в присутствии EDC (1-этил-3-(3-диметиламинопропил)карбодиимид), используемого для связывания с карбоксильной группой. Условия реакции предотвращают гидролиз пептидных связеи?.
Данная работа рассматривает частный случай применения технологии для получения изотопно меченных стандартов вирусных пептидов, белков.
Краткий протокол
1. Определение количества вирусных частиц в ВСЖ.
2. Получение меченого стандарта в реакции образования амидной связи между меченой мочевиной и вирусным белком в присутствии EDC в водной среде.
3. Интраназальное инфицирование экспериментальных животных полученным меченым стандартом.
4. Интраназальное введение экспериментальным животным раствора-аналога без радиоактивной метки.
5. Определение содержания радиоуглерода в различных органах лабораторных животных с помощью УМС-анализа биологических проб.
6. Обработка и обобщение результатов.
Заключение
Предлагаемый нами новый метод диагностики вирус-клеточного взаимодействия подходит для количественного и качественного анализов не только вирусов, но и практически любых пептидов и белков, содержащих хотя бы одну COOH-группу. Предполагается, что данный метод может стать широко востребованным и применим для любых белковых соединений, содержащих в своем составе -COOH группы.
Возможность в лабораторных условиях связывать карбоксильные группы пептидов и белков с меченными радиоуглеродом веществами сделает полученные соединения пригодными для использования в качестве стандартов для количественного УМС-анализа.
Библиографическая ссылка
Прокопьева Е.А., Пархомчук Е.В., Соболев И.А., Шестопалов А.М. РАЗРАБОТКА НОВОГО МЕТОДА ДИАГНОСТИКИ ВИРУС-КЛЕТОЧНОГО ВЗАИМОДЕЙСТВИЯ С ПОМОЩЬЮ УСКОРИТЕЛЬНОЙ МАСС-СПЕКТРОМЕТРИИ // Современные проблемы науки и образования. 2019. № 1. ;URL: https://science-education.ru/ru/article/view?id=28463 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/spno.28463



