Тромбоциты представляют собой уникальные постклеточные структуры, принимающие участие не только в механизмах гемостаза, регуляции реологических свойств крови, но и в обмене биоактивных веществ. При активации тромбоциты выделяют нейротрансмиттеры, серотонин, допамин, гистамин и глутамат и могут влиять на работу нейронов при патологиях нервной системы [1]. С другой стороны, ряд работ убедительно демонстрирует способности тромбоцитов захватывать и депонировать в грануломере приведенные выше соединения [2]. Выше перечисленные структурно-функциональные особенности обеспечивают ту регуляторную функцию в обмене глютамата в микроокружении гемокапилляров, находящихся в различном функциональном состоянии, которую выполняют тромбоциты в нервной ткани в норме и в условиях сосудистых катастроф [3-5]. Вместе с тем, несмотря на наличие многочисленных работ, указывающих на гетерогенность тромбоцитов в структурном и функциональном отношении [6], данные об участии тромбоцитарных субпопуляций в регуляции обмена глютамата отсутствуют. Эксперимент in vitro с участием тромбоцитарной плазмы хорошо зарекомендовал себя в качестве модели для изучения тромбоцитарного отклика при действии тестовых соединений [7-9].
Цель исследования - изучить структурно-функциональные изменения субпопуляций тромбоцитов, выделенных по морфологическим критериям, при высоких концентрациях глютамата in vitro и in vivo.
Материал и методы исследования
Исследование проведено на самцах аутбредного стока Wistar (n=20) массой 190-200 г, содержащихся в стандартных условиях вивария. До взятия под наблюдение в текущем исследовании животные в экспериментах не участвовали. Все крысы получали полнорационный комбикорм для лабораторных животных, вода всегда имелась в свободном доступе.
Все манипуляции с использованием животных проводились в соответствии с этическими принципами, установленными Европейской конвенцией по защите позвоночных животных, используемых для экспериментальных и других научных целей (принятой в Страсбурге 18.03.1986 и подтвержденной в Страсбурге 15.06.2006).
Обогащенную тромбоцитами плазму получали из крови, взятой с использованием 3,8% раствора цитрата натрия в качестве антикоагулянта в пропорции кровь : антикоагулянт – 9 : 1.
Для исследований in vitro у животных под общей анестезией забиралась кровь непосредственно из полости левого желудочка сердца в объеме 5 мл. Кровь центрифугировали при 1300 g в течение 10 мин. С поверхностных слоев пробирки забирали 2,5 мл супернатанта (верхнего слоя). В последующем кровь делили на 2 пробирки – контрольную и экспериментальную для эксперимента in vitro. В экспериментальную пробирку вносили глутамат натрия, до получения конечной концентрации 85 ммоль, что соответствует пиковой концентрации глутамата в центре ишемического ядра при тяжелой церебральной ишемии, при которой развиваются явления эксайтотоксичности [10]. После этого пробирки инкубировали при температуре 37 °С в термостате на протяжении 15 минут. Тромбоцитарный концентрат помещали на предметные стекла.
Для исследования in vivo, предварительно, на аналитических весах готовилась навеска 2,5 г глютамата натрия, которая в дальнейшем разводилась в 10 мл 0,9% раствора хлорида натрия. Полученное количество вещества соответствует 83% LD50 для крыс [11] и 85 ммоль в пересчете на объем тела животного. Полученный раствор вводился животным внутрибрюшинно. Через два часа после введения раствора у животных под общей анестезией забиралась кровь непосредственно из полости левого желудочка сердца в объеме 5 мл. Для получения обогащенной тромбоцитами плазмы цитратную кровь центрифугировали в течение 10 минут при 1300 g. Тромбоцитный концентрат также помещали на предметные стекла. В последующем все мазки окрашивались по Романовскому и Гимзе.
В нашей работе оценивались следующие основные морфометрические характеристики тромбоцитов: большой и перпендикулярный ему диаметр, а также доля синей и красной компоненты фотографии тромбоцитов, предварительно сбалансированной по белому цвету. В последующем рассчитывался фактор формы как отношение большого диаметра к малому, с его ростом степень округлости тромбоцита снижается. Средний диаметр использовали как показатель, пропорциональный площади тромбоцита. Также рассчитывался индекс омоложения тромбоцитов (ИОТР), который отражает насыщенность тромбоцита гранулами, так как при использованном методе окраски последние имеют фиолетово-красный цвет. Для получения статистически достоверных данных морфометрии на одном микропрепарате исследовалось не менее 500 клеток [12].
Анализ первичных данных проводили с помощью специального программного обеспечения ImageJ. Статистический анализ первичных данных проводили методами дисперсионного анализа с помощью программ StatSoft Statistica for Windows 6.0. и Microsoft Excel 2003. Статистическую значимость оценивали с помощью Т-критерия Стьюдента. Данные считали достоверными при р< 0,05.
Результаты исследования и их обсуждение
В результате статистического анализа первичных данных, полученных в экспериментах in vivo и in vitro, отмечено изменение морфометрических характеристик тромбоцитов, а именно количества тромбоцитов с разной степенью вытянутости (рис. 1). В области значений фактора формы более 1,6 она носит разнонаправленный характер относительно показателей контроля. В эксперименте с внесением глутамата in vivo отмечалось достоверное снижение количества вытянутых форм относительно показателей группы контроля (количество тромбоцитов с фактором формы более 1,6 достоверно снизилось с 18±2% до 6±2%), в то время как эксперименте in vitro достоверно выросло до 26±3% от общего количества морфометрированных тромбоцитов. Динамика числа тромбоцитов в области значений фактора формы менее 1,6 в обоих случаях характеризуется однонаправленными изменениями: снижением количества тромбоцитов относительно контрольных показателей в диапазоне фактора формы от 1 до 1,2 и ростом числа тромбоцитов в диапазоне фактора формы от 1,2 до 1,6.
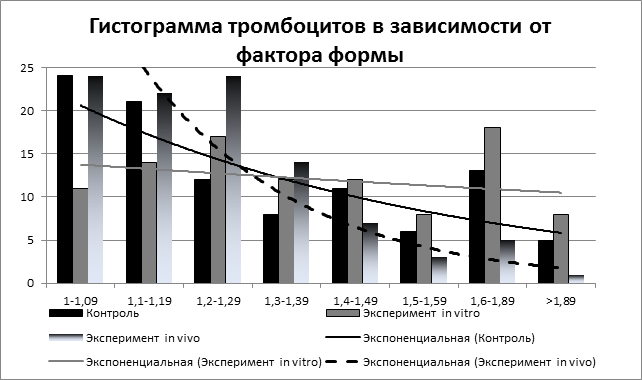
Рис. 1. Диаграмма частот тромбоцитов (процент тромбоцитов от общей выборки) – ось y, в зависимости от степени их вытянутости (отношения длинного диаметра к короткому) – по оси х. Распределение тромбоцитов сглажено при помощи экспоненциальной аппроксимации уравнениями вида y=a*ebx, где a и b – константы, e - основание натурального логарифма
Однако в экспериментальной группе in vitro более выражено снижение – на 20% (с 55±3% до 35±2%) и меньше рост – 12% (с 27±2% до 29±2%). В экспериментальной группе in vivo более выражен рост числа тромбоцитов средней степени вытянутости (фактор формы 1,2-1,6) – на 36% (с 27±2% до 48±2%) и в меньшей степени снижение числа округлых тромбоцитов (фактор формы до 1,2) – 9% (с 55±3% до 46±2%).
Таким образом, можно констатировать, что рост числа вытянутых форм in vitro взаимосвязан со значительным снижением округлых форм и слабо касается форм со средней степенью вытянутости, в то время как в эксперименте in vivo снижение палочковидных форм тромбоцитов ассоциировано со значительным ростом тромбоцитов средней степени вытянутости. Тромбоциты с фактором формы более 1,6 рассматриваются нами как протромбоциты, которые не участвуют в формировании агрегатов и адгезии. Также их число повышается при длительном хранении тромбоцитарной массы [13]. Рост их числа ассоциирован с ростом ИОТР с 1,06 до 1,19, что свидетельствует об увеличении количества «молодых» форм. Вышеописанные процессы могут свидетельствовать об активной дегрануляции тромбоцитов в эксперименте in vitro с потерей способности к тромбобразованию под воздействием высоких концентраций глютамата.
Как известно, тромбоциты способны не только выбрасывать, но и накапливать биоактивные соединения. В связи с этим мы рассмотрели зависимость среднего диаметра – показателя, с которым тесно связана площадь тромбоцитов, от фактора формы тромбоцитов. Достоверная динамика была выявлена только для исследований in vivo, что очевидно, ввиду наличия в организме тромбоцитарных депо, которые, вероятно, были задействованы в реакции на парентеральное введение глутамата. Это характеризовалось значительным и равномерным снижением среднего диаметра для всех степеней вытянутости, в среднем на 0,5 мкм (рис. 2), что согласуется с данными ряда авторов о выбросе в кровоток незрелых форм тромбоцитов при активации тромбоцитопоэа, анемии, или в патогенезе гестоза [14]. В нашем исследовании это сопровождается еще большим ростом ИОТР в экспериментальной группе in vivo, чем в группе in vitro (до 1,36). Изменения среднего диаметра тромбоцитов в экспериментальной группе in vitro не достоверны.
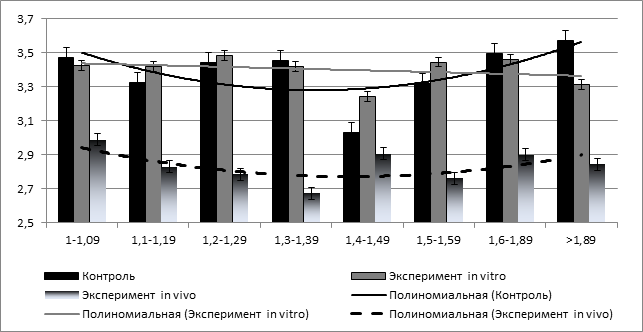
Рис. 2. Диаграмма зависимости среднего диаметра тромбоцитов (мкм) – ось х, от степени их фактора формы (отношения длинного диаметра к короткому) – ось y. Распределение тромбоцитов сглажено при помощи полиномиальной аппроксимации уравнениями вида y=a*х2+bx+c, где a, b и с – константы
Следует отметить, что в крови у крыс выделяется 4 типа тромбоцитов [13]: дисковидные (2-4 мкм), сферические (1-2 мкм), с гладкой поверхностью или различным числом псевдоподий, большие сферические (4-5 мкм), и удлиненные биполярные протромбоциты длиной 2-20 мкм и диаметром 0,5-0,7 мкм, одинаковые по всей длине или сужающиеся к концам наподобие веретена (рис. 3).
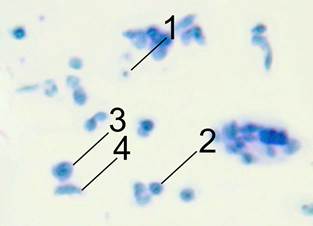
Рис. 3. Мазок обогащенной тромбоцитами плазмы крови крыс. Объектив 40. Фрагмент фотографии: 1 – сферический тромбоцит, 2 – дисковидный тромбоцит, 3 - большой сферический тромбоцит, 4 – протромбоцит
Поскольку последние у человека отсутствуют, то в следующих исследованиях мы исключили тромбоциты с фактором формы больше 1,6 из исследования (рис. 4).
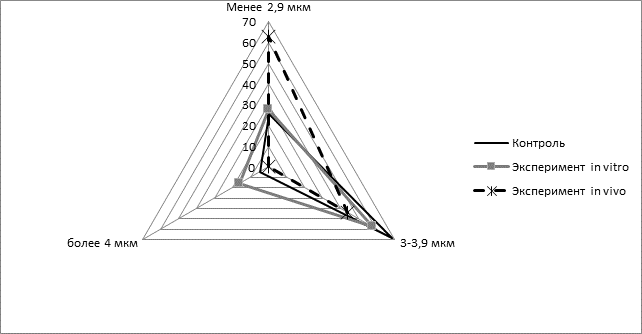
Рис. 4. Диаграмма количества субпопуляций тромбоцитов (процент от общей выборки), выделенных на основании расчета среднего диаметра (средний диаметр 2,9 мкм и менее, средний диаметр 3-3,9 мкм, средний диаметр 4 мкм и более), среди тромбоцитов с фактором формы менее 1,6
На диаграмме в экспериментальной группе in vitro можно наблюдать значительное увеличение доли тромбоцитов со средним диаметром более 4 мкм, которые можно рассматривать как большие сферические по классификации Бурячковской Л.И. [13], возникновение которых связывается автором с активацией более мелких по диаметру дисковидных тромбоцитов. Также на диаграмме визуализируется рост доли сферических тромбоцитов в эксперименте, проведённом in vivo, что связывается нами с выбросом тромбоцитов из депо. Поскольку исследование тромбоцитарного отклика на высокие концентрации глутамата in vitro может рассматриваться как модель ядра ишемии в ткани головного мозга при нарушении церебральной гемоперфузии, то мы можем экстраполировать выявленные в нашем исследовании изменения на локальные процессы, протекающие в нервной ткани при инсульте.
Таким образом, результаты проведенного исследования показали, что высокие концентрации глутамата натрия in vitro приводят к росту активированных форм тромбоцитов и протромбоцитов, по всей вероятности, возникающих из дисковидных тромбоцитов. In vivo эти явления нивелируются за счет увеличения доли сфероцитов, по всей видимости, выброшенных из депо. Полученные результаты позволяют рассматривать изучаемые параметры в качестве прогностических критериев при изучении эксайтотоксичности и требуют дальнейшего изучения.
Исследование выполнено в рамках выполнения государственного задания ФГБОУ ВО «ИвГМА» Минздрава России на 2018 год и плановый период 2019 и 2020 годов «Исследование биомедицинских эффектов макрогетероциклических соединений с противоопухолевой активностью для разработки новых лекарственных средств».
Библиографическая ссылка
Криштоп В.В., Ленчер О.С. ДИНАМИКА ИЗМЕНЕНИЯ МОРФОМЕТРИЧЕСКИХ ПОКАЗАТЕЛЕЙ ТРОМБОЦИТОВ ПРИ ВЫСОКИХ КОНЦЕНТРАЦИЯХ ГЛУТАМАТА В ЭКСПЕРИМЕНТЕ IN VIVO И IN VITRO // Современные проблемы науки и образования. 2019. № 1. ;URL: https://science-education.ru/ru/article/view?id=28443 (дата обращения: 21.04.2026).



