Несмотря на широкое внедрение современных медицинских технологий и усовершенствование методов диагностики, проблема острого аппендицита остается нестареющей и широко обсуждаемой среди врачей. В ургентной хирургии острый аппендицит занимает лидирующие позиции: ежегодно в России выполняется более миллиона аппендэктомий, одна треть из них - по поводу катарального аппендицита [1-4].
В среднем, по данным отечественной литературы, в РФ послеоперационная летальность после выполнения аппендэктомии наблюдается у 0,2-0,3% оперированных, а в отдельных регионах - в два раза выше - 0,4-0,5% [5]. В исследованиях зарубежных авторов доказано, что при остром катаральном аппендиците отдаленные результаты хирургического вмешательства в 2-2,5 раза хуже, чем при флегмонозной и гангренозной формах, и возникает большее количество послеоперационных осложнений [6]. Летальность при осложненных формах острого аппендицита достигает 4,3-5,8% [3; 4].
Образование внутрибрюшных спаек является одним из распространенных поздних послеоперационных осложнений в абдоминальной хирургии. Адгезивный процесс в брюшной полости наблюдается после первого хирургического вмешательства у 44% пациентов, а после повторного - у 96% больных. Ежегодно по поводу спаечного процесса в брюшной полости обследуются и лечатся около 1% больных, у 55-75% из них возникает острая спаечная кишечная непроходимость с послеоперационной летальным исходом у 13-55% оперированных [7; 8].
Целью работы является оптимизация лечебной тактики у больных острым аппендицитом путем прогнозирования и профилактики развития послеоперационных внутрибрюшных сращений.
Материал и методы. В работе представлен анализ исходов лечения 144 больных острым аппендицитом, находившихся на лечении в хирургическом отделении ГБУЗ «Городская клиническая больница № 2» г. Ставрополя.
Критерий исключения из исследования: больные острым аппендицитом, осложненным распространенным перитонитом.
Для ускоренного восстановления после операций (Fast-Track surgery) мы применяли комплекс мер в пред-, интра- и послеоперационном периодах, которые уменьшали сроки реабилитации больных, а также снижали вероятность развития внутрибрюшных спаек.
По половому и возрастному признакам наблюдаемые больные распределились следующим образом: мужчин было 46 (31,9%), женщин – 98 (68,1%). Подавляющее число пациентов находились на лечении в трудоспособном возрасте (20-39 лет) – 84 (58,3%) пациента.
При анализе форм острого аппендицита выявлено, что среди 144 пациентов преобладали больные с флегмонозной формой заболевания – 98 чел. (68,0%), катаральная форма заболевания наблюдалась у 27 (18,8%), гангренозная – у 19 больных (13,2%).
Следует отметить, что все пациенты были оперированы в экстренном порядке. До 6 ч от начала заболевания поступили 70 (48,6%) больных, обращение до 12 ч зарегистрировано у 30 (20,8%) пациентов, до 1 сут. – у 28 (19,4%). Были отмечены случаи позднего обращения за медицинской помощью - через несколько суток после начала заболевания - 16 (11,1%) пациентов с острым аппендицитом.
Анализ места жительства показал следующие данные: среди госпитализированных с диагнозом острый аппендицит 116 (80,6%) пациентов были городскими жителями, 28 чел. (19,4%) - жителями сельской местности.
В связи с тем, что в развитии послеоперационного спаечного процесса в брюшной полости большое значение имеют сопутствующая патология, фенотипические проявления соединительнотканной дисплазии и тип ацетилирования [4; 5], нами проведен анализ этих данных у изучаемых пациентов.
У 87 (60,4%) больных с диагнозом острый аппендицит мы наблюдали 111 сопутствующих заболеваний. Заболевания пищеварительного тракта имели место у 27 (18,8%) пациентов. Расстройства функции органов пищеварительного тракта проявлялись явлениями дискомфорта в правой половине живота у 15 чел. (10,4%), расстройством стула - у 6 (4,2%) пациентов. Системные заболевания соединительной ткани наблюдались у 30 (20,8%) больных: у 21 был ревматизм, у 9 - аутоиммунный васкулит. У 42 (29,2%) пациентов диагностированы гипертрофические рубцы, у 30 (20,8%) оперированных - лекарственная и пищевая аллергия.
Наиболее характерные внешние фенотипические признаки соединительнотканной дисплазии наблюдались у 54 (37,5%) больных. Распределение их по стигмам было следующим: малые и приросшие мочки – у 9 (6,3%) пациентов, носовые кровотечения – у 15 (10,5%) чел., кривые мизинцы – у 6 (4,2%) оперированных, варикозное расширение вен нижних конечностей и сколиоз – по 12 (8,3%) чел., множественные пигментные пятна – у 3 (2,1%) пациентов, короткая шея - у 15 (10,4%) больных, астеническая конституция встречалась в 9 (6,3%) случаях.
Методика определения ацетиляторной активности основана на определении содержания свободного изониазида в моче. Тест-препарат принимался пациентом однократно per os в дозе 0,3 г. Мочу собирали в течение 8-12 ч. Быстрый тип ацетилирования диагностировали при экскреции с мочой менее 10% свободного изониазида за сутки, медленный – более 10%. При изучении ацетилирующей активности у наблюдаемых нами больных 84 (58,3%) из них были медленными и 60 (41,7%) – быстрыми ацетиляторами. Ацетиляторная активность не зависела от пола и возраста оперированных. У пациентов с медленным типом ацетилирования наблюдали следующие клинические формы острого аппендицита: у 8 (9,5%) катаральный аппендицит, у 64 (76,2%) – флегмонозный, у 12 (14,3%) – гангренозный. У быстрых ацетиляторов соответственно: у 19 (31,7%) катаральный аппендицит, у 34 (56,7%) – флегмонозный, у 7 (11,7%) – гангренозный. Лабораторные показатели процента ацетилирования у быстрых ацетиляторов были от 3,1 до 7,9%, в среднем - 6,12 ± 0,11%; при медленном типе ацетилирования этот показатель находился в диапазоне от 11,3 до 77,1%, в среднем - 39,4 ± 2,28% (Р < 0,05).
Анализ результатов определения ацетиляторной способности организма указывает на то, что адгезивный процесс в брюшной полости чаще возникает у пациентов с острым катаральным аппендицитом – 19 (70,4%), в то время как при остром флегмонозном и гангренозном аппендицитах преобладали больные с медленным типом ацетилирования – 64 (76,2%) и 12 (14,3%) соответственно (таблица).
Ацетиляторная активность у больных с различными формами острого аппендицита
|
Форма острого аппендицита |
Тип ацетилирования |
Р |
|
|
быстрый |
медленный |
||
|
Катаральный |
19 (70,4%) |
8 (29,6%) |
< 0,001 |
|
Флегмонозный |
34 (34,8%) |
64 (65,2%) |
< 0,001 |
|
Гангренозный |
7 (36,8) |
12 (63,2%) |
< 0,001 |
|
Всего: |
60 |
84 |
144 |
Таким образом, из 144 больных острым аппендицитом по результатам обследования (сопутствующая патология, тип ацетилирования, признаки соединительнотканной дисплазии) у 82 (56,9%) выявлена предрасположенность к развитию послеоперационного спаечного процесса, из них 60 пациентов были с быстрым типом ацетилирования и 22 больных - с медленным типом ацетилирования, но у которых одновременно сочетались такие факторы риска развития внутрибрюшных сращений, как сопутствующая патология и отсутствие внешних фенотипических проявлений соединительнотканной дисплазии.
На кафедре общей хирургии совместно с сотрудниками Ставропольского противочумного института для прогнозирования развития выраженного адгезивного процесса в брюшной полости была сконструирована тест-система на основе магноиммуносорбентов (МИС) [9]. Белковым лигандом ее служил антигенный спаечный комплекс (АСК), выделенный из внутрибрюшных спаек оперированных больных. Диагностическим разведением сывороток больных являлся титр 1:80. МИС также позволяет контролировать эффективность проводимой противоспаечной терапии по результатам иммуноферментного анализа (ИФА) сывороток больных с тест-системой. Снижение количества положительных реакций агглютинации свидетельствует о положительном результате проводимой противоспаечной терапии. Реакция сывороток этих 82 пациентов с МИС тест-системой была положительной в диагностическом разведении. Результаты ИФА сывороток остальных 62 пациентов были отрицательными, так как реагировали с МИС с иммобилизированными антигенными комплексами из спаек в недиагностических разведениях.
Все больные разделены на 2 группы, равнозначные по возрасту, полу, патологии, прогностическим критериям, определяющим развитие адгезивного процесса, сопутствующей патологии, ацетиляторной активности организма. Группы были рандомизированы случайным порядком слепым методом. Первая группа (контрольная) – это 41 пациент, которым для профилактики развития послеоперационного адгезивного процесса проводилась противоспаечная терапия. Вторую (основную) группу составил 41 больной, лечение которых дополнялось элементами Fast-Track.
В контрольной группе у 41 больного выполнялась аппендэктомия традиционно. Для обезболивания применяли местную инфильтрационную анестезию 0,5%-ным раствором новокаина, внутривенный наркоз или, по показаниям, проводили эндотрахеальный наркоз. Хирургический доступ по Волковичу–Дьяконову обеспечивали скальпелем и ножницами. Кровотечение останавливали путем перевязывания сосудов. При выполнении аппендэктомии культя червеобразного отростка перевязывалась кетгутом с последующим ее погружением кисетным швом в купол слепой кишки. При гангренозном аппендиците у 10 (24,4%) пациентов для дренирования брюшной полости использовали полихлорвиниловые трубки. Ушивание послеоперационной раны осуществляли послойно: брюшина, мышцы, подкожная клетчатка - кетгутом, апоневроз и кожа - отдельными лавсановыми швами. В послеоперационном периоде с целью обезболивания использовали опиоидные анальгетики.
При лечении больных основной группы, наряду с профилактической противоспаечной терапией, применяли элементы мультимодального подхода к лечению (Fast-Track), о которых больных информировали до операции. Кожные покровы в зоне хирургического вмешательства обрабатывались субэритемными дозами ультрафиолетового облучения за 10-15 мин. до операции. Антибиотикопрофилактика осуществлялась с помощью непрямого эндолимфатического введения подкожно в области стопы 1,0 г цефазолина + 300 мг метронидазола + 4 мл 2%-ного раствора лидокаина.
В обязательном порядке на протяжении всего оперативного вмешательства обеспечивалась нормотермия, так как интраоперационная гипотермия влечет за собой ухудшение гемостаза с увеличением кровопотери и повышение потребления кислорода с высоким риском ишемии тканей.
Интраоперационное обезболивание осуществлялось проведением тотальной внутривенной анестезии: 1%-ный р-р пропофола 4-8 мг мг/ч в сочетании с 5%-ным раствором кетамина 3-4 мг/кг массы тела. Спинномозговую анестезию применяли по показаниям, в основном больным с выраженной патологией со стороны сердечно-сосудистой системы, а также пациентам старше 60 лет. С этой целью использовали 15-20 мг 0,5%-ного раствора наропина. Применяли классический хирургический доступ по Волковичу-Дьяконову, пользуясь монополярным электроножом «Сургитрон».
С целью минимизации воспалительной реакции в кишечной стенке и окружающих тканях, предупреждения оставления замкнутой полости при выполнении аппендэктомии культю червеобразного отростка, не перевязывая, погружали в купол слепой кишки кисетным швом. От дренирования брюшной полости отказались. При закрытии раны передней брюшной стенки не производили ушивания париетальной брюшины, так как при ушивании брюшины нарушается кровоснабжение, что приводит к развитию ишемии, что способствует развитию сращений в брюшной полости. Шов апоневроза и внутрикожный шов кожной раны осуществляли мононитью Prolen, минимизируя нарушение кровообращения в тканях. Перед наложением внутрикожного шва осуществляли профилактику гнойно-септических осложнений в ране, промывая ее в течение трех минут 3%-ной перекисью водорода с последующей обработкой 0,5%-ным раствором хлоргексидина.
В послеоперационном периоде обезболивание проводили внутривенным капельным или внутримышечным введением 5%-ного кетопрофена 100 мг х 2 раза в сутки, избегая применения опиоидных анальгетиков. По показаниям, для усиления анальгетического эффекта, однократно внутримышечно вводили 100 мг 5%-ного трамадола.
Энтеральное питание начинали спустя 6 ч после операции. Для профилактики развития внутрибрюшных сращений осуществляли раннюю активацию больных (в течение первого дня после операции до 6 ч вне кровати), стимуляцию кишечной перистальтики.
Противоспаечная терапия пациентам обеих групп включала несколько этапов.
В течение первых трех суток послеоперационного периода внутривенно вводили озонированный физиологический раствор хлорида натрия в концентрации 1,3 мг/л. В связи с тем, что у пациентов, склонных к формированию внутрибрюшных спаек, наблюдается статистически значимое состояние умеренной гиперкоагуляции, то со 2-3-х суток после хирургического вмешательства они получали фрагмин 0,3 мл/сут. (клексан 0,4 мл/сут.). Начиная с пятого дня после операции 1 раз в 3 сут. вводили 3000 ЕД препарата лонгидаза (бовгиалуронидаза), которая снижает вязкость гиалуроновой кислоты и доступность коллагена для фиброкластов и, как следствие, препятствует формированию спаек.
Физиотерапевтический комплекс включал комбинированное применение магнито- и лазеротерапии: начиная с 4-5-х суток после операции выполнялась терапия импульсным магнитным полем, затем – лазеротерапия. Через 3-4 нед. после операции амбулаторно пациенты получали электрофорез с лонгидазой 500 ЕД на буферном растворе по классической методике № 5-7 от аппарата «Поток-1», продолжительность воздействия составляла 15 мин.
Статистическая обработка полученных результатов проводилась методом вариационной статистики и корреляционного анализа с помощью программы Microsoft Excel 2007 (Windows). Анализ проводился с использованием программы STATISTICA 6,0.
Результаты исследования и заключение. Прослежена динамика взаимодействия антител сывороток крови больных после аппендэктомии на 5, 14 и 28-е сутки послеоперационного периода с АСК МИС. Часть исследований выполнена в амбулаторных условиях.
В контрольной группе у 41 пациента в диагностическом разведении во все периоды исследования реакция агглютинации была положительной. По мере удлинения сроков, прошедших после аппендэктомии, увеличивалось количество положительных реакций в больших разведениях – 1:160, 1:320 и 1:640 (рис. 1).

Рис. 1. Динамика изменений числа реакций агглютинации сывороток крови больных контрольной группы с МИС в разные сроки исследования
Проведенные исследования показали, что у пациентов контрольной группы, по мере увеличения сроков послеоперационного периода, нарастает количество больных, сыворотки которых, даже в больших разведениях, вступали в реакцию агглютинации с АСК МИС.
Изучена динамика изменений числа реакций агглютинации разных разведений сывороток крови 41 пациента основной группы с МИС в те же сроки исследования (рис. 2).
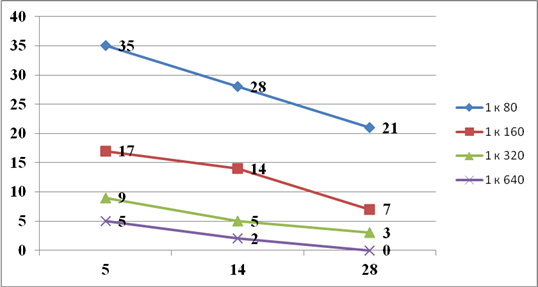
Рис. 2. Динамика изменений числа реакций агглютинации сывороток крови больных основной группы с МИС в разные сроки исследования
На фоне применения в лечении больных с острым аппендицитом элементов мультимодального подхода в сочетании с противоспаечной терапией, по мере удлинения сроков послеоперационного периода, отмечалось однонаправленное снижение числа реакций агглютинации во всех разведениях сыворотки пациентов с АСК МИС. Только у 2 (4,9%) больных через 2 нед. регистрировалась реакция агглютинации с титром сыворотки крови 1:640, а через 4 нед. таких реакций не было. К 28 суткам сыворотки крови 20 (48,8%) пациентов даже в диагностическом титре 1:80 не вступали в реакцию агглютинации с АСК МИС.
Выводы
1. Факторами риска развития внутрибрюшных спаек после аппендэктомии являются патология органов пищеварения, соединительной ткани, аллергия и фенотип быстрого ацетилирования.
2. По динамике изменений количества реакций АСК + антитело в разных титрах сыворотки крови больных после аппендэктомии можно судить о степени активности процессов, происходящих в формирующихся патологических спайках и эффективности проводимой противоспаечной терапии.
3. Проведение противоспаечной терапии в сочетании с элементами Fast-Track хирургии дает более выраженный эффект в предупреждении формирования внутрибрюшных сращений.
Библиографическая ссылка
Лаврешин П.М., Гобеджишвили В.К., Гобеджишвили В.В., Кочкаров Э.В., Байчоров Х.М. ПРОГНОЗИРОВАНИЕ И ПРОФИЛАКТИКА РАЗВИТИЯ ВНУТРИБРЮШНЫХ СПАЕК ПОСЛЕ АППЕНДЭКТОМИИ // Современные проблемы науки и образования. 2018. № 1. ;URL: https://science-education.ru/ru/article/view?id=27436 (дата обращения: 17.05.2026).



