Рак молочной железы (РМЖ) на протяжении многих лет в структуре онкологической заболеваемости и смертности среди женского населения Российской Федерации продолжает занимать лидирующую позицию [1]. На 2013 год абсолютное число заболевших злокачественными новообразованиями в мире 12,7 млн, и РМЖ занял второе место после рака легкого [2]. С 1980 по 2012 г. абсолютное число заболевших злокачественными новообразованиями на территории Российской Федерации составило 59,5 на 100 тыс. человек [3]. По мнению некоторых ученых, рост заболеваемости РМЖ связан с изменениями факторов репродуктивного риска, увеличением продолжительности жизни, пагубными привычками [4; 5]. В настоящее время диагностика и лечение РМЖ достигли высокого уровня, однако прогрессирование опухолевого процесса и отдаленное метастазирование свидетельствуют о неблагоприятном прогнозе для этих больных. Последние годы ознаменовались появлением новых современных методов, использование которых позволяет осуществлять раннюю диагностику этой патологии. Диагноз метастатического поражения зачастую устанавливается после появления симптоматики и подтверждается с помощью таких современных методов, как мультиспиральная компьютерная томография (МСКТ), магнитно-резонансная томография (МРТ), позитронно-эмиссионная томография (ПЭТ-КТ). Главной причиной летального исхода большинства онкологических больных является развитие рецидива и отдаленных метастазов, ежегодно выявляемых в 30-40% наблюдений, при этом метастатический РМЖ является наиболее частой причиной смертности среди женщин моложе 55 лет [6]. Особенностью РМЖ является достаточно высокий процент гематогенного и лимфогенного метастазирования. Частота метастазирования в значительной степени зависит от особенностей гистологического типа первичной опухоли. Так, частота гематогенного церебрального метастазирования рака молочной железы c гиперэкспрессией HER2/neu достигает 28-43%, при отрицательном статусе стероидных гормонов и без экспрессии белка HER2/neu - 55%, при гормон-позитивном типе опухоли - 11%, а легочные метастазы при РМЖ по частоте возникновения занимают второе место и обнаруживаются в 29,4% наблюдений [2].
Порог двухлетней выживаемости преодолевают лишь 8% больных с церебральными метастазами РМЖ, а пятилетняя выживаемость немногим превышает 2%. Значимую роль в прогнозе выживаемости носит характер метастазирования, определяющий эффективность химиотерапевтического лечения. Однако качество жизни данной категории пациентов в течение всего периода времени в существенной степени зависит от выбранной тактики лечения [7]. Методами локального лечения являются хирургическое удаление метастазов и лучевая терапия, а системным – химиотерапия. На сегодняшний день остается неопределенной роль хирургического компонента в лечении больных РМЖ с внутрилегочными метастазами и метастазами в головной мозг. Наиболее значимыми прогностическими факторами при лечении данной категории больных с использованием хирургического метода являются: количество метастазов, характер оперативного вмешательства, длительность безрецидивного периода, состояние внутригрудных лимфатических узлов и локализация вне жизненно важных зон головного мозга [8]. Целесообразность лечения метастазов РМЖ в головной мозг и легкие не подвергается никакому сомнению, несмотря на его паллиативный характер, так как удается продлить жизнь больных более чем на 6 месяцев [9]. Стандартное лечение метастазов рака молочной железы в головной мозг включает лучевую терапию, неи?рохирургическое лечение, химиотерапию и зависит от гистологического типа первичного источника метастазирования. Появление таких новейших методов лечения, как гамма-нож (облучение четко ограниченным сфокусированным пучком), существенно улучшает прогноз заболевания [10]. В настоящее время чередование различных схем цитотоксической, гормональной, таргетной терапии и применение новых хирургических технологий позволяют добиться улучшения непосредственных и отдаленных результатов лечения и сохранения удовлетворительного качества жизни [11]. Оптимальная продолжительность терапии у больных метастатическим РМЖ с объективными регрессиями или стабилизацией до сегодняшнего дня не определена. Считалось, что поддерживающая пролонгированная терапия может улучшить качество жизни и увеличить время до прогрессирования заболевания, однако не влияет на выживаемость [12].
Концепция неизлечимости метастатического РМЖ в наши дни определяет выбор тактики лечения этого заболевания, главной целью которого являются максимальное продление жизни пациентки и облегчение симптомов болезни.
Представляем клинический случай больной раком молочной железы с метастатическим поражением головного мозга, множественными метастазами обоих легких.
В октябре пациентка А., 46 лет обратилась в поликлинику по месту жительства с жалобами на новообразование в правой молочной железе, обнаруженное самостоятельно. Больная направлена на консультацию к онкологу. При осмотре: молочные железы симметричные; в левой молочной железе фиброзно-кистозные изменения; в верхнем наружном квадранте правой молочной железы по передней аксиллярной линии груднои? клетки определяется округлой формы, плотное, ограниченно смещаемое новообразование диаметром 2 см; симптомы площадки, умбиликации и Ке?нига – отрицательные. Регионарные лимфатические узлы не пальпируются.
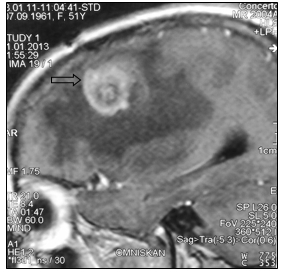
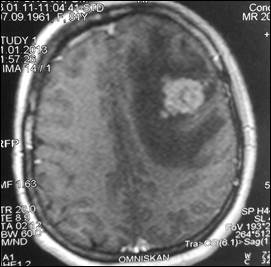
При маммографии молочные железы полусферическои? формы, симметричные. Контуры кожи и соски желез не изменены. Ретромаммарное пространство не затемнено. В верхненаружном квадранте правой молочнои? железы лоцируется округлой формы без четких контуров образование размером 2,0 см - диагностическая категория BI-RADS (Breast Imaging Reporting and Data System): справа – 4; слева – 1. По данным ультразвукового исследования молочных желез, в правой молочнои? железе по переднеи? аксиллярнои? линии в проекции VII межреберья визуализируется очаговое образование сниженнои? эхогенности, неоднороднои? структуры, без четких контуров, с признаками инфильтративного роста, с вертикальнои? ориентациеи? максимальнои? оси размером 19,0х20,0 мм. Кровоток интранодулярныи?, визуализируется единичныи? питающии? сосуд (Ri (resistive index) – 0,63). В правой подмышечной области лоцируется группа измененных лимфатических узлов, максимальным размером 14 мм. При ультразвуковом исследовании органов брюшной полости и малого таза данные о метастазах не выявлены. Выполнена тонкоигольная аспирационная биопсия новообразования правой молочной железы. По данным цитологического исследования – инвазивный рак молочной железы. Установлен диагноз: рак правой молочной железы сT1cN1M0, IIa. Пациентке 1 ноября 2007 г. выполнена радикальная мастэктомия правой молочной железы по Madden с лимфодиссекцией D2. В послеоперационном периоде выполнено иммуногистохимическое исследование. Сформулирован окончательный диагноз: инвазивный дольковый солидно-альвеолярный рак правой молочной железы pT1cN1M0, IIa, умеренной степени злокачественности - 7 баллов, ER- (0), PR- (0), HER2/neu-(3+). Назначено комплексное лечение: системная терапия по схеме FAC 6 курсов (фторурацил 500 мг/м2, доксорубицин 50 мг/м2, циклофосфамид 500 мг/м2 1 раз в 21 день) и курс лучевой гамма-терапии на зоны регионарного метастазирования (СОД 49,5 Гр) и послеоперационный рубец (СОД 50 Гр). С декабря 2007 по январь 2013 года больная находилась под диспансерным динамическим наблюдением у онколога в поликлинике по месту жительства. При проведении очередного контрольного обследования в январе 2013 г. при МРТ головы отмечено прогрессирование заболевания в виде появления единичных метастатических поражений левой лобной доли головного мозга и нижней доли правого легкого (рис. 1, 2).
 а
а
 б
б
Рис. 1. МР-томограммы больной А., 51 год, с метастазом в левую лобную долю (стрелка):
а – сагиттальная плоскость; б – горизонтальная плоскость (объяснение в тексте)
 а
а
 б
б
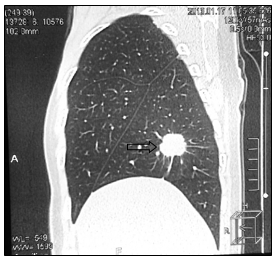
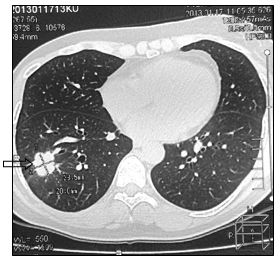
Рис. 2. КТ-картина метастаза в нижнюю долю правого легкого (стрелка):
а – сагиттальная плоскость; б – горизонтальная плоскость (объяснение в тексте)
Консилиумом врачей принято решение об оперативном лечении. 06.02.2013 г. выполнена костно-пластическая трепанация черепа, удаление опухоли левой лобной доли головного мозга. Гистологическое заключение удаленного препарата: метастаз низкодифференцированной аденокарциномы (рис. 3)
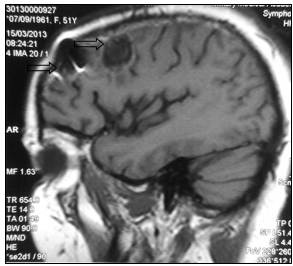 а
а
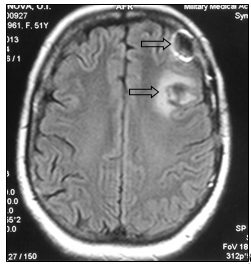 б
б
Рис. 3. МР-картина послеоперационных отечно-глиозных изменений в левой лобной доле (стрелка): а – сагиттальная плоскость; б – горизонтальная плоскость (объяснение в тексте)
Далее проведена системная химиотерапия доцетакселом (80 мг/м2). На фоне 2 циклов 2 линии в мае 2013 г. установлено прогрессирование заболевания в виде увеличения размеров существующего метастаза в нижней доле правого легкого с 20х24х21 до 22х28х25 мм и появления нового метастаза нижней доли левого легкого 7х11х8 мм (рис. 4).
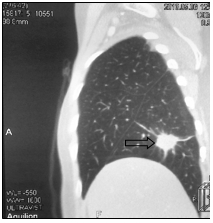 а
а
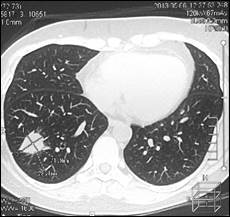 б
б
 в
в
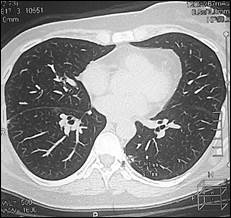
Рис. 4. Компьютерная томография от 05.06.2013 г., признаки прогрессирования в виде увеличения размеров метастазов в нижней доле правого легкого и нижней доле левого легкого: а – метастаз в нижнюю долю правого легкого (стрелка), сагиттальная плоскость; б – горизонтальная плоскость; в - метастаз в нижнюю долю левого легкого (объяснение в тексте)
В связи с неэффективностью проводимой системной терапии принято решение о назначении 3 линии ПХТ (капецитабин 1250 мг/м2+герцептин 2 мг/кг). На фоне 12 циклов 3 линии химиотерапии достигнута стабилизация процесса. Однако при контрольном обследовании спустя год отмечено прогрессирование в виде увеличения размеров метастазов в нижней доле правого легкого с 22х28 до 32х28 мм и нижней доле левого легкого с 7х11 до 11х11 мм (рис. 5).
а, б, в
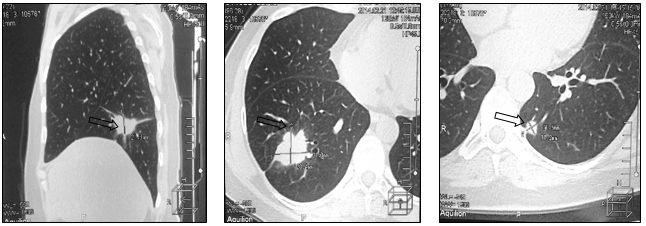
Рис. 5. Компьютерная томография больной А., 52 года, прогрессирование заболевания в виде увеличения размеров опухоли (стрелка): а – метастаз в нижнюю долю правого легкого, сагиттальная плоскость; б – горизонтальная плоскость; в - метастаз в нижнюю долю левого легкого (объяснение в тексте)
В связи с прогрессированием заболевания произведена смена системной химиотерапии на гемцитабин 1250 мг/м2. 4 линия ПХТ позволила стабилизировать онкологический процесс на протяжении 6 месяцев. При контрольном обследовании в июле 2014 г. выявлено новое метастатическое поражение верхней доли левого легкого, размеры других образований не изменились по сравнению с предыдущим исследованием (рис. 6).
а, б, в, г
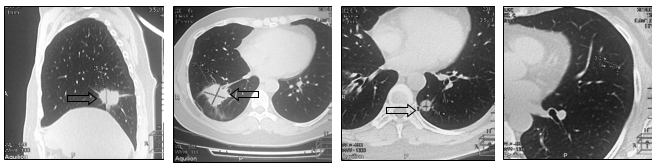
Рис. 6. Компьютерная томография (07.2014 г.), прогрессирование в виде метастатического поражения верхней доли левого легкого, размеры других образований не увеличились (стрелка): а – метастаз в нижнюю долю правого легкого, сагиттальная плоскость;
б – горизонтальная плоскость; в - метастаз в нижнюю долю левого легкого; г – метастаз в верхнюю долю левого легкого (объяснение в тексте)
Произведена очередная смена системной химиотерапии. Назначена монохимиотерапия по схеме паклитаксел (260 мг/м2). Проведено 38 циклов с частичным регрессом заболевания - уменьшение размеров метастазов легких. В настоящее время пациентка продолжает получать назначенное лечение. Общая продолжительность жизни составляет 10 лет (рис. 7, 8).
 а
а
 б
б
 в
в
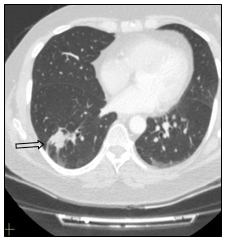
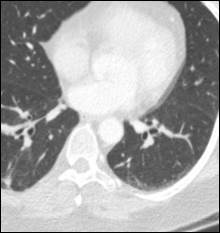
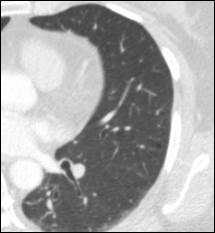
Рис. 7. Компьютерная томография больной А., 55 лет, с метастазами в легкие (стрелка): а – горизонтальная плоскость; б – очаговое уплотнение легочной ткани нижней доли левого легкого; в – уменьшение очагового уплотнения легочной ткани верхней доли левого легкого (объяснение в тексте)
 а
а
 б
б
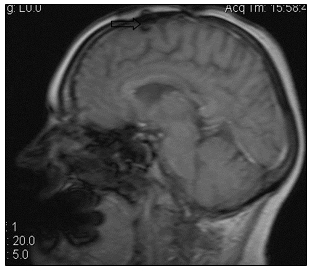
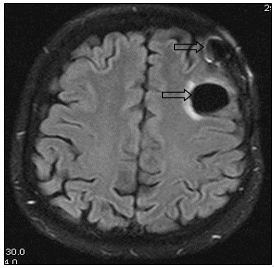
Рис. 8. МР-томограммы больной А., 55 лет, МР-картина послеоперационных кистозно-глиозных изменений в левой лобной доле (стрелка): а – сагиттальная плоскость; б – горизонтальная плоскость (объяснение в тексте)
Заключение
Метастазирование злокачественных опухолей является одной из важнейших проблем современной онкологии. По данным литературы, пятилетняя выживаемость при метастатическом раке молочной железы составляет 0,6–5%, а десятилетняя 0,3–1,2%. Лекарственное лечение РМЖ является ключевым составляющим комплексной терапии. При раннем операбельном РМЖ применение адъювантной системной терапии позволяет улучшить результаты лечения, повышая при этом общую и безрецидивную выживаемость больных, а при метастатическом РМЖ является основным методом лечения, способствующим добиться выраженного клинического эффекта в виде полной или частичной ремиссии различной продолжительности у 40-70% больных. Но и при достижении полной клинической ремиссии в случае метастатического РМЖ остается риск рецидива заболевания и возникновения лекарственной персистентности. В свою очередь сложность лечения рецидивов и метастазов РМЖ осложняется результатами ранее проведенной терапии, включающей облучение, неоадъювантную и адъювантную терапию, что приводит к развитию резистентности опухолевых клеток к цитостатическим препаратам и к снижению функциональных резервов печени, сердечно-сосудистой системы, костномозгового кроветворения.
Данное наблюдение демонстрирует возможность комплексного лечения инвазивного долькового солидно-альвеолярного рака молочной железы с локализацией метастазов в головной мозг и легкие. В описанном клиническом случае создается одна из наиболее важных и трудных для врача проблема выбора терапии. Следует отметить, что значительным моментом является наличие большого числа противоопухолевых препаратов и различных схем полихимиотерапии, обладающих различной степенью активности.
Сегодня метастатический РМЖ продолжает оставаться неизлечимым заболеванием и рассматривается как хронический процесс, который требует достаточно длительного лечения с периодической сменой одного вида терапии на другой. У части больных появилась возможность увеличения длительности ремиссии, выживаемости и улучшения ее качества посредством комбинации методов противоопухолевого лечения. Характерной чертой современных исследовании? продолжает оставаться стремление к индивидуализации терапии, в истоках которой лежит более глубокое понимание молекулярно-биологических основ канцерогенеза и применение новейших достижении? науки, в том числе нанотехнологии?. Поэтому представляет интерес поиск критериев отбора больных распространенным раком молочной железы, чувствительным к проведению противоопухолевого лечения.
Библиографическая ссылка
Баховадинова Ш.Б., Дзидзава И.И., Жильцова Е.К., Ионцев В.И., Фуфаев Е.Е., Марьева О.Г., Баринов О.В., Коваленко Н.А., Старков И.И. КЛИНИЧЕСКИЙ СЛУЧАЙ ЛЕЧЕНИЯ МЕТАСТАТИЧЕСКОГО РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ // Современные проблемы науки и образования. 2018. № 1. ;URL: https://science-education.ru/ru/article/view?id=27377 (дата обращения: 27.05.2026).



