Проблема загрязнения окружающей среды тяжелыми металлами (ТМ) становится все более и более актуальной. Многие из этих металлов обладают высоким сродством к серосодержащим лигандам и образуют с ними прочные соединения. Поэтому, попадая в клетки, они взаимодействуют с SH-группами, инактивируя многие ферменты [1]. Это вызывает разнообразные нарушения метаболизма клеток, с чем связана высокая токсичность тяжелых металлов.
В период прорастания семян закладываются зачатки генеративных и вегетативных органов, поэтому изменение физиологических процессов этого этапа, вызванное стрессором, отразится на протекании всех последующих этапов онтогенеза, на росте и продуктивности растений [2].
Целью данной работы является определение диапазонов концентраций ионов тяжелых металлов, при которых они оказывают стимулирующее и ингибирующее действие на процесс формирования проростков растений семейства Brassicaceae. В работе в качестве тест-культуры использовались семена редиса Федерального государственного унитарного предприятия «Башсортсемовощ». Данная культура рекомендована для применения в целях биотестирования [3]. Кроме того, данный выбор обусловлен биопродуктивными свойствами редиса и его холодостойкостью. Семена редиса прорастают уже при температуре 3-4 °С. Наиболее благоприятная температура для роста редиса 12-15 °С с момента посева и до начала формирования корнеплода, а затем 15-18 °С. Редис обладает чрезвычайно коротким периодом вегетации и не предъявляет особых требований к почве и климату. Основные характеристики семян приведены в таблице 1.
Таблица 1
Характеристика семян, использованных для биотестирования
|
Общепринятое/научное названия |
Семейство |
Сорт |
Сортовая чистота, % |
Всхо- жесть, % |
Влаж- ность, % |
|
|
Редис |
Raphanus sativus |
Brassicaceae |
Жара |
99,4 |
94,0 |
9,0 |
По 50 штук семян редиса укладывались равномерно на фильтровальную бумагу в чашке Петри диаметром 10 см. В одну чашку Петри наливалось 5 мл раствора ТМ, в другую – 5 мл дистиллированной воды. Уровень жидкости в чашках должен быть ниже поверхности семян. Проращивание проводилось в условиях контролируемой температуры и влажности воздуха. Эксперимент заканчивается через 72 часа измерением длины корешков.
Для эксперимента были взяты соли меди, марганца и кобальта в разных концентрациях. Выбор конкретных тяжелых металлов обусловлен их биологической ролью и токсичностью [4].
Медь относится к группе ультрамикроэлементов, входящих в элементарный химический состав клетки, она участвует во многих физиологических процессах. Среднее содержание меди в живом веществе 2·10-4%, известны организмы - концентраторы меди. По биохимическим свойствам и функциям медь сходна с железом, способна образовывать стабильные комплексы и изменять валентность (Cu2+ ↔ Cu+). В растениях до 98-99% меди содержится в виде комплексных форм. Медь характеризуется большим сродством к аминокислотам, чем к органическим кислотам. Основная биохимическая функция меди - участие в ферментативных реакциях в качестве активатора или в составе медьсодержащих ферментов. Важнейшими Cu-ферментами являются пластоцианин, цитохромоксидаза, полифенолоксидаза, супероксиддисмутаза, диаминооксидаза [5].
Количество меди в растениях колеблется от 0,0001 до 0,05% (на сухое вещество) и зависит от вида растения и содержания меди в почве. Так, например, содержание меди во мхах и лишайниках составляет в среднем 5-9 мг/кг сухого вещества. В оптимальных концентрациях медь повышает холодостойкость растений, способствует их росту и развитию.
Недостаточное содержание меди в почвах отрицательно влияет на синтез белков, жиров и витаминов и способствует бесплодию растительных организмов. Медь участвует в процессе фотосинтеза и влияет на усвоение азота растениями. Вместе с тем избыточные концентрации меди оказывают неблагоприятное воздействие на растительные и животные организмы. Для большинства видов критический уровень меди составляет 20-30 мг/кг сухой массы растений. Нарушается интеграция мембран, что приводит к утечке содержимого клеток, особенно у чувствительных видов и экотипов растений. В присутствии кальция (иона-антагониста) повреждающее действие меди уменьшается. Предельно допустимая концентрация для почвы (с учетом фона) равна 55 мг/кг [6]. Реакцией проростков семян редиса на внешние факторы окружающей среды являются: изменения морфологических признаков, снижение всхожести, физиологические сдвиги и т.д.
Кобальт в тканях растений находится в ионной (Co2+, Co3+) и комплексной формах [7]. В оптимальных концентрациях этот микроэлемент способствует увеличению толщины и объема мезофилла в листьях. Кобальт влияет на формирование и функционирование фотосинтетического аппарата растений. Этот микроэлемент способствует концентрированию хлоропластов и пигментов в листьях, что связано с возрастанием объема пластидного аппарата за счет репликации и роста органелл [8].
Кобальт может активировать биосинтез хлорофилла, стимулируя синтез белка цитоплазмы и хлоропластов. Под влиянием кобальта фотохимическая активность хлоропластов возрастает параллельно увеличению содержания в них белка. Связь кобальта с синтезом белка может осуществляться через регуляцию структуры и устойчивости рибосом, а также функционирования РНК.
Критический уровень кобальта у большинства растений колеблется от 0,4 до нескольких миллиграммов на 1 кг сухой массы [9]. Однако повышенные концентрации соединений кобальта являются токсичными. В избыточных концентрациях кобальт тормозит поглощение железа и марганца. ПДКс.с. = 0,0004 мг/м3, класс опасности 2.
Марганец содержится в тканях всех растений, хотя количественные характеристики у разных систематических групп сильно различаются. Максимальное количество марганца содержится в цитоплазме растительных клеток, из органелл – в хлоропластах.
Основные функции марганца в растительных клетках: 1) катализирующая, 2) участие в окислительно-восстановительных реакциях и фотосинтезе.
Известно более 35 ферментов, активируемых марганцем. Большинство из них катализируют реакции окисления-восстановления, декарбоксилирования, гидролиза. В настоящее время особенно выделяют два марганцесодержащих фермента: Mn-белок и супероксиддисмутаза (MnСОД). MnСОД участвует в детоксикации супероксидного радикала, находится главным образом в митохондриях и пероксисомах [10].
Марганец способствует утилизации CO2 растениями, чем повышает интенсивность фотосинтеза, участвует в процессах восстановления нитратов и ассимиляции азота растениями. Марганец способствует переходу активного Fe(II) в Fe(III), что предохраняет клетку от отравления, ускоряет рост организмов и т.д. При избытке марганца в среде нарушается гормональный обмен растений. Нарушения в гормональном обмене сопровождаются подавлением растяжения клеток.
При недостатке марганца в почвах возникают заболевания растений, характеризующиеся в общем появлением на листьях растений хлоротичных пятен, которые в дальнейшем переходят в очаги некроза. Обычно при этом заболевании происходит задержка роста растений и их гибель [11].
Результаты опытов по исследованию воздействия водных растворов солей меди, кобальта и марганца на рост корешков редиса приведены на рисунке 1. Пунктирными линиями на рисунке изображены результаты двух контрольных опытов по проращиванию семян редиса в дистиллированной воде. В «контрольных» вариантах взят усреднённый диапазон значений длины корешков, полученный в результате проведения двух параллельно заложенных контрольных экспериментов [12]. На рисунке 1 этот диапазон ограничен двумя пунктирными линиями.
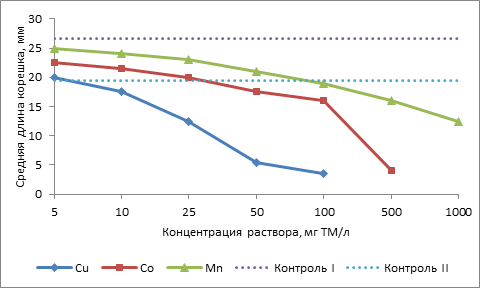
Рис. 1. Влияние различных концентраций ТМ на рост корешков редиса
Из рисунка 1 видно, что растворы с концентрацией ионов меди 5-10 мг/л не проявляют ярко выраженного токсического эффекта. Раствор с концентраций ионов меди 25 мг/л является граничным. При дальнейшем увеличении в растворе концентрации ионов меди в диапазоне от 25 до 100 мг/л наблюдается выраженное угнетающее действие.
Анализ результатов показывает, что ни одна из концентраций кобальта в водном растворе не обладает выраженным стимулирующим эффектом, но в то же время многие из них не оказывают выраженного отрицательного эффекта, поскольку укладываются в область возможных значений, определенных как «контрольные». Можно считать, что диапазон концентраций, при которых редис не получает токсическое воздействие, от 0 до 50 мг/л ионов Co2+. Выраженным ингибирующим воздействием обладает водный раствор с концентрацией тяжелого металла 500 мг/л. Рост корешков в этих условиях возможен, но растение сильно угнетается.
Анализируя график, можно сделать вывод о том, что марганец при высоких концентрациях (500-1000 мг/л) оказывает ингибирующее действие на семена редиса. При меньших концентрациях марганца (1-100 мг/л) рост корешков редиса подобен их росту на дистиллированной воде.
Для оценки комбинированного действия тяжелых металлов в работе по вышеописанной методике было проведено проращивание семян редиса в бинарных растворах металлов Mn и Co, Mn и Fe, Mn и Cu, Mn и Zn, Mn и Ni (рис. 2).
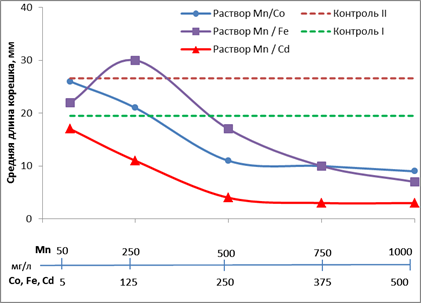
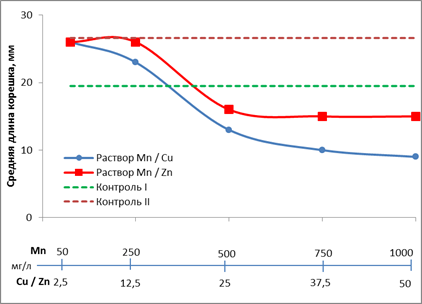
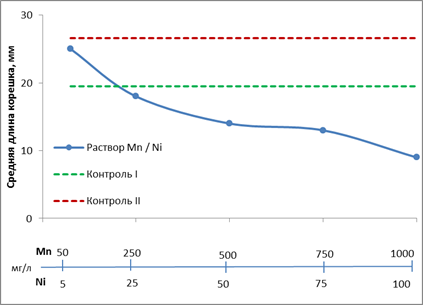
Рис. 2. Влияние различных концентраций смеси ТМ на рост корешков редиса
Из графика видно, что в смеси 300 Mn / 150 Cо мг/л рост корешков редиса подобен их росту в дистиллированной воде, при более высоких концентрациях рост корешков угнетается. Смесь марганца и меди более токсична, т.к. только в сочетании 350 Mn / 15 Cu мг/л средняя длина корешков редиса соответствует контрольным значениям, весь остальной исследуемый диапазон является областью токсического действия. Сравнение смесей марганца с цинком и с медью свидетельствует о большей токсичности последней.
Стимулирующий эффект оказывает раствор Mn и Fe в области концентраций от 80 Mn / 48 Fe до 300 Mn / 180 Fe мг/л, при увеличении концентраций выше 500 Mn / 250 Fe мг/л наблюдается угнетение проростков.
Наиболее токсичным оказался раствор Mn и Сd, так как длина корешка даже при самой низкой из анализируемых концентраций уже была ниже величин контрольного диапазона, а при концентрации раствора 500 Mn / 250 Cd мг/л она составила всего 4 мм.
Полученные данные позволяют выделить три диапазона концентраций бинарных смесей ТМ, оказывающих разное воздействие на проращивание: области стимулирующего, нейтрального и угнетающего действия (табл. 2).
Таблица 2
Диапазоны концентраций ТМ, оказывающих разное воздействие на рост корешков редиса
|
Область концентраций |
Начало области концентраций ТМ, мг/л |
|||||||||||
|
Mn / Co |
Mn / Fe |
Mn / Cd |
Mn / Cu |
Mn / Zn |
Mn / Ni |
|||||||
|
Стимулирующая |
- |
- |
80 |
48 |
- |
- |
- |
- |
- |
- |
- |
- |
|
Нейтральная |
50 |
5 |
300 |
180 |
- |
- |
50 |
2,5 |
50 |
2,5 |
50 |
5 |
|
Угнетающая |
240 |
144 |
500 |
250 |
5 |
50 |
300 |
15 |
370 |
18,5 |
150 |
15 |
Таким образом, прорастание семян редиса оказалось достаточно устойчиво к действию ТМ. Установлено, что наиболее выраженное угнетение прорастания корешков редиса наблюдалось в растворе солей меди, в меньшей степени этот эффект был выражен при проращивании в растворах солей марганца и кобальта. Эксперимент по проращиванию семян в растворе, содержащем смеси солей металлов, показал, что при совместном присутствии в растворе солей марганца и кобальта наблюдается снижение токсичности кобальта. Так, при прорастании семян только в присутствии кобальта зона токсического действия начиналась при его концентрации 50 мг/л, при воздействии кобальта вместе с марганцем, рост корешков начинал угнетаться при концентрациях выше 350 Mn / 150 Cо мг/л. То есть можно предположить наличие антагонистического взаимодействия между этими ионами.
Согласно данным работы [13] подобная тенденция наблюдается и в почве: установлено, что поглощение элементов растениями зависит от содержания в почве элемента-конкурента. Эта связь является прямой пропорциональной при низком содержании элемента-конкурента в почве (синергизм) и превращается в обратную (антагонизм) при высоком содержании в почве элементов-конкурентов [14]. В данном исследовании медь и марганец подобного взаимного влияния не обнаружили, так как область токсического действия меди совпадает при проращивании отдельно и в смеси солей металлов. В обоих экспериментах по проращиванию семян в смеси солей металлов токсическое действие проявлялось при более низкой концентрации марганца (300-350 мг/л в смеси, 500 мг/л отдельно).
Проведённые эксперименты по определению диапазонов ТМ, при которых они оказывают стимулирующее, нейтральное и угнетающее действие на процесс формирования проростков растений, свидетельствуют о возможности использования метода биотестирования для определения пригодности конкретных растений для фиторемедиации почв в зависимости от уровня их загрязненности тяжелыми металлами.
Работа выполнена при поддержке гранта РФФИ № 17-44-020574.
Библиографическая ссылка
Елизарьева Е.Н., Янбаев Ю.А., Редькина Н.Н., Кудашкина Н.В., Байков А.Г., Смирнова А.П. ВЛИЯНИЕ СОЕДИНЕНИЙ НЕКОТОРЫХ ТЯЖЕЛЫХ МЕТАЛЛОВ НА ПРОЦЕСС ФОРМИРОВАНИЯ ПРОРОСТКОВ РЕДИСА // Современные проблемы науки и образования. 2017. № 6. ;URL: https://science-education.ru/ru/article/view?id=27181 (дата обращения: 16.05.2026).



