Инвалидизация и смерть жителей России по-прежнему в значительной степени обусловливаются сердечно-сосудистыми заболеваниями (ССЗ) [9]. Облитерирующие поражения артерий нижних конечностей (НК) верифицируются в 5–15% от численности жителей всех стран и континентов, составляя в структуре патологии сердечно-сосудистой системы (ССС) группу, по удельному весу превышающую 20% [3; 4].
Основная причина поражения артерий НК – атеросклероз (АТС). Почти в 50% наблюдений АТС-поражений артерий НК верифицируются нарушения кровообращения в зоне круро-поплитеальных сегментов [7]. Хирургическое пособие остается преимущественным методом лечения пациентов с данной патологией, а ведущим критерием при принятии решения по реваскуляризации НК может быть только выраженность ишемии [5; 7].
Оценка степени поражения сосудистого русла НК осуществляется на основе классификаций Покровского-Фонтейна [5] и Рутерфорда [8; 12] посредством специальных алгоритмов [6; 8]. Тем не менее ряд авторов полагает, что данные порядки оказания МП не всегда сопровождаются оптимальными результатами [12; 13]. Специалисты в области сосудистой хирургии порой игнорируют неудобные верификационные схемы и предпочитают ориентироваться на личные впечатления в оказании МП больным с АТС-поражением сосудов НК [6]. В настоящее время, используя прикладные компьютерные программы, можно успешно диагностировать заболевания и прогнозировать их исход [1; 2]. Создавая в конечном итоге модели оценки состояния артериального русла НК и используя данные моделирования, можно объективно выявлять степень влияния морфологических изменений сосудистой стенки на состояние гемодинамики и перфузии сегментов НК кислородом. Эта задача актуальна для исследователей не только медико-технических специальностей, но и хирургов (ангиохирургов), т.к. модельные технологии оценки кровотока позволяют не только прогнозировать течение патологического процесса, но и выбирать наиболее эффективный способ реваскуляризации НК.
Цель работы: используя биомеханические методы моделирования кровообращения в нижних конечностях, обосновать возможность объективной оценки степени выраженности атеросклеротического поражения артериальных сосудов ног.
Материалы и методы
В качестве объектов исследования выбраны подколенная и берцовые артерии. Для их моделирования модифицирована геометрия сосудов посредством введения ряда упрощений: жесткое закрепление артерии; избрание идеально изолированной стенки сосуда в качестве поверхности, контактирующей с текучей средой; представление крови – «неньютоновской жидкостью»; давление на входе в подколенную артерию – 10 кПа; скорость кровотока в сосуде – 40 см/cек.
Геометрическая модель артерий НК выстраивалась посредством программы SolidWorks-2013 в следующей последовательности: 1) введение геометрических примитивов; 2) создание из последних элементарных моделей подколенной артерии (ПкА), передней и задней большеберцовых артерий (ПББА и ЗББА), малоберцовой артерии (МБА); 3) сборка исследуемого объекта (рис. 1).
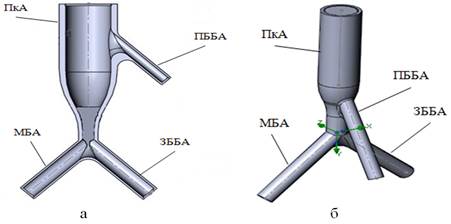
Рис. 1. Модельные изображения артерий НК: а – схематическое, б – объемное
Построение модели артерий НК осуществлялось при значениях геометрических параметров. ПкА: диаметр (Dж)= 7 мм, толщина стенки сосуда (hс)=1 мм, ее длина (L)=25 см; ПББА: Dж=3 мм, hс=1 мм, L=20 см; ЗББА: Dж=3 мм, hс=1 мм, L=20 см; МБА: Dж=1,6 мм, hс=1 мм, L=20 см. Параметры получены при анализе данных обследования 10 человек посредством инструментальных методов (компьютерная томография, УЗИ сосудов НК). Кровоток в неизмененных артериях НК смоделирован с применением указанных допущений и свойств, с использованием данной гемодинамической модели в дальнейшем в качестве эталона (рис. 2).
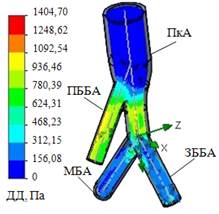
Рис. 2. Эпюра с количественными показателями гемодинамики (артерии НК интактны)
Гемодинамические показатели оценены в артериях круро-поплитеального сегмента НК при разной локализации и выраженности АТС-поражения. Степень стенотических изменений в сосудах стандартизирована: стеноз 20, 50 и 75% просвета артерии, ее окклюзия. Локализация АТС-бляшек (АТСБ) в сосудах оценивалась как в приустьевом, так и в дистальных отделах артерии. Изучены также особенности изменений кровотока, возникающие при множественном поражении артериальных сосудов.
Данные об оценке гемодинамических показателей при вариантах АТС-поражения ПББА
Кровоток смоделирован при изолированной локализации АТСБ в устье ПББА (рис. 3а). Изменения кровотока в просвете артерий голени оценивались по эпюрам для динамического давления (рис. 3 б-г).
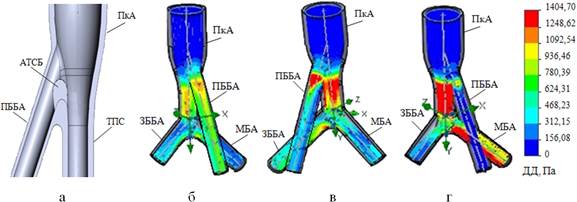
Рис. 3. Модели кровотока в зоне отхождения ПББА от ПкА (а) при степенях стеноза 20% (б), 50% (в), 75% (г)
По показателям динамического давления (ДД) можно полагать, что при увеличении степени атеросклеротического поражения ПББА кровоток в ней уменьшается с компенсаторным его увеличением в ЗББА. Параметры кровотока в МБА и ПкА при этом практически не изменяются. Данные оценки динамики в показателях статического давления (СД) и скорости кровотока в артериях голени отражены на рис. 4.
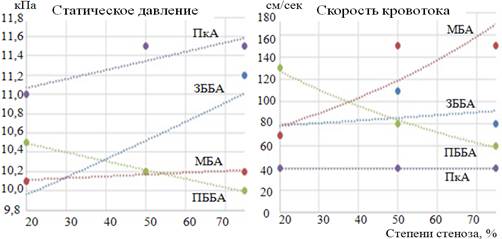
Рис. 4. Параметры СД и СК при локализации АТС в месте отхождения ПББА от ПкА
При оценке изменений СД отмечается его рост в ПкА и ЗББА на фоне снижения в ПББА. При увеличении выраженности стеноза в устье ПББА скорость кровотока (СК) за счет наименьшего диаметра увеличивается в МБА (в ЗББА и ПкА остается практически неизменной), а в ПББА – снижается.
Кровоток в своих особенностях при локализации АТСБ в дистальных отделах ПББА несколько отличался от ее проксимального поражения (рис. 5).
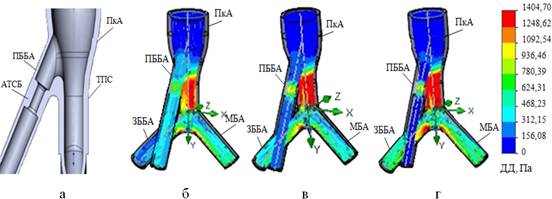
Рис. 5. Модели кровотока при АТС-поражении ПББА (а) с разными степенями сужения: 20% (б), 50% (в), 75% (г)
С нарастанием явления стенотического поражения ПББА в месте бифуркации тибиоперонеального ствола (ТПС) на ЗББА и МБА происходит существенное увеличение показателей ДД (рис. 5 б–г).
Кровоток в ПББА при увеличении степени стеноза падает. Исследование СД и СК проведено на основе моделей разных степеней АТС-поражения ПББА (рис. 6).
Рост АД при увеличении степени АТС-поражения ПББА отмечается во всех сосудах (наибольший – в ПкА). Скорость кровотока в ЗББА и МБА снижается незначительно, в то время как при нарастании стеноза в ПББА отмечается ускорение движения крови. В ПкА скорость кровотока остается постоянной.
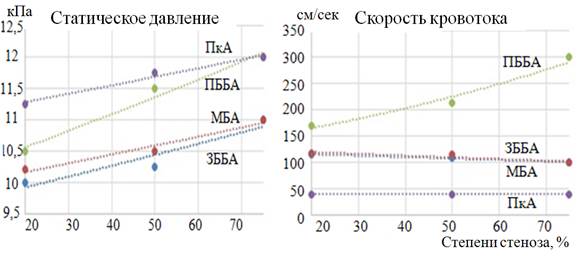
Рис. 6. Параметры СД и СК при разных стадиях АТС-поражения ПББА
Кровь в случаях окклюзии ПББА направляется в ТПС, откуда ее распределение преимущественно происходит в самый крупный сосуд (ЗББА). Следовательно, наибольшее изменение ДД возникает в этой артерии (>1400 Па). Показатели кровотока в МБА несколько увеличены, однако параметр ДД не превышает 800 Па (рис. 7а).
Значительно СК нарастает в ЗББА (до 180 см/сек), в ПкА и МБА она остается практически неизменной (рис. 7б).
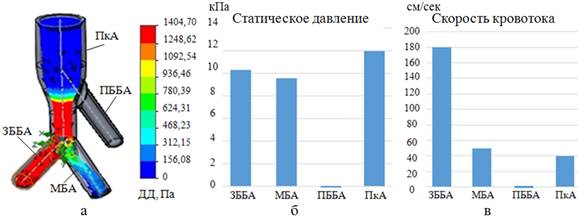
Рис. 7. Параметры динамического (а) и статического давления (б), скорости кровотока (в) при окклюзии ПББА
Показатели давления в ПкА при окклюзии ПББА несколько увеличиваются (12 КПа) по сравнению с принятой нормой (10 КПа), однако эти изменения не могут расцениваться гемодинамически значимыми.
Данные об оценке гемодинамических показателей при вариантах АТС-поражения ветвей ТПС
Изучены данные о показателях кровотока на модели локализации АТСБ в области бифуркации ТПС (рис. 8).
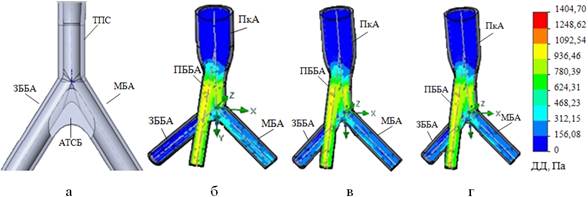
Рис. 8. Варианты показателей кровотока в гемодинамической модели при локализации АТСБ в области бифуркации ТПС (а) со стенозированием: 20% (б), 50% (в), 75% (г)
Очевидно, что ДД, на основании анализа вариантов эпюр, остается почти неизменным во всех артериях при любой стадии АТС-поражения. На диаграммах СД и скорости кровотока также демонстрируются весьма небольшие изменения (рис. 9).
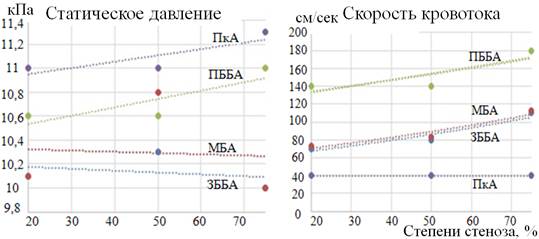
Рис. 9. Показатели СД и СК при разных стадиях формирования АТСБ в артериях НК (между ЗББА и МБА)
При нарастании явлений стеноза СД в ЗББА и МБА остается практически неизменным, а в ПББА и ПкА – увеличивается на 400 и 300 Па (3 и 2,3 мм рт. ст. соответственно), т.е. также – ничтожно. В этих случаях скорость кровотока увеличивается во всех артериях, кроме ПкА.
Итоговые оценки параметров гемодинамики при изолированных поражениях ЗББА и МБА оказываются идентичными, несмотря на некоторые отличия в диаметре внутреннего просвета этих сосудов – 3,0 и 1,6 мм соответственно (рис. 10 и 11).
При изолированном поражении ЗББА или МБА ДД в пораженной артерии падает, а при стенозировании просвета сосуда более 75% интенсивность кровотока практически отсутствует. В ПкА характер тока крови не изменяется, а в ПББА и непораженной ветви ТПС происходит компенсаторное увеличение кровотока.
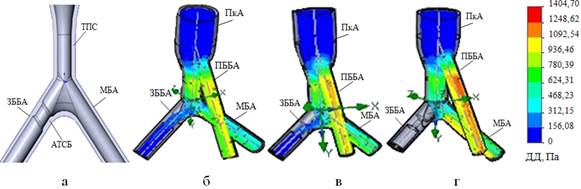
Рис. 10. Варианты модели кровотока в НК при АТС-поражении ЗББА (а) со стенозированием: 20% (б), 50% (в), 75% (г)
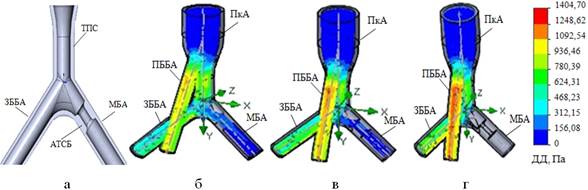
Рис. 11. Варианты модели кровотока НК на разных стадиях развития АТСБ в МБА (а): 20% (б), 50% (в), 75% (г)
Изменения в параметрах СД и СК при увеличении стенозирования в ЗББА и МБА также идентичны (рис. 12). Неизменным СД остается во всех интактных артериях, его падение отмечается только в пораженной артерии, при этом в случаях стеноза просвета сосуда более 65% оно приближается к нулю. Скорость кровотока в ПкА и ПББА также остается стабильной. Изменения касаются только ветвей ТПС: в пораженной артерии происходит падение скорости кровотока, а в интактном сосуде – увеличение.
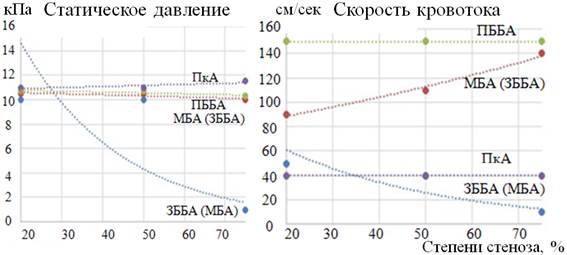
Рис. 12. Показатели СД и СК при разных стадиях АТСБ в ЗББА (МБА)
В случаях сочетанного АТС-поражения ЗББА и МБА (рис. 10 и 11) характер гемодинамических изменений в целом соответствует таковым при АТС-поражении ПББА, что отражено на рис. 6.
Изучены параметры гемодинамической модели взаимного влияния АТСБ на показатели кровотока в ПББА (рис. 5) и ЗББА (рис. 10) при разной степени стенозов (рис. 13).
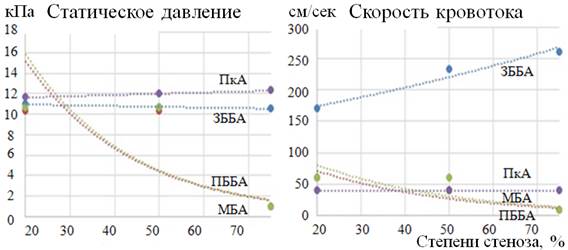
Рис. 13. Показатели СД и СК в при разной степени сочетанного АТС-поражения ПББА и ЗББА
При одновременном увеличении стенотического поражения ПББА и ЗББА СД в них стремится к нулю, в то время как в ПкА и МБА оно остается стабильным. Скорость кровотока при данном варианте модели умеренно увеличивается в МБА, в ПкА остается на прежнем уровне, а в ЗББА и МБА интенсивность кровотока значительно уменьшается, приближаясь к «0».
Сведения по оценке показателей гемодинамики с учетом взаимного влияния атеросклеротических бляшек в ПББА и МБА (рис. 5 и 11) представлены на рис. 14.
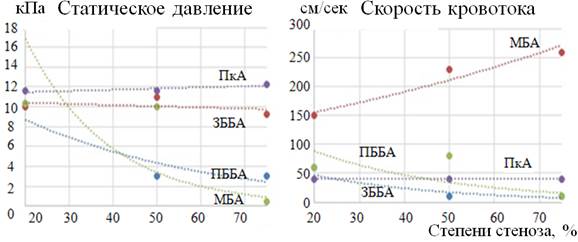
Рис. 14. Показатели СД и СК при разных стадиях АТС в ПББА и МБА
Взаимосвязь показателей СД и СК со степенями стенозов, приведённая на рис. 14, отражает тот факт, что при увеличении степени стенотического поражения ПББА и МБА скорость кровотока в них существенно снижается и значительно возрастает в ЗББА. Статическое давление в МБА и ПББА при нарастании стеноза также стремится к нулю. В ПкА и ЗББА оно остается постоянным.
На рис. 15–16 представлены гемодинамические модели сосудов НК при окклюзии задней большеберцовой и малоберцовой артерий.
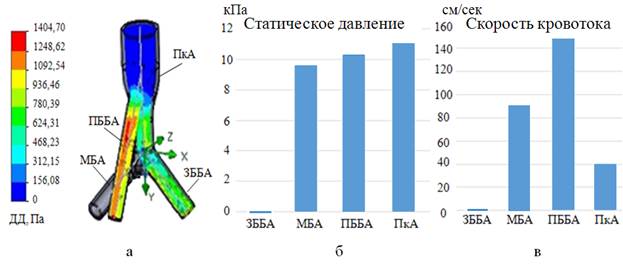
Рис. 15. Параметры ДД (а), СД (б) и СК (в) при окклюзии ЗББА
Изменения в показателях ДД при окклюзии ЗББА возникают в большей степени в ПББА с повышением его до 1,0–1,2 кПа, самые высокие параметры СД при этом отмечаются в ПкА (11 кПа). Наивысшие параметры СК отмечаются в ПББА (до 150 см/сек).
При АТС-окклюзии МБА констатируются изменения ДД, практически аналогичные таковым при окклюзии ЗББА (рис. 16).
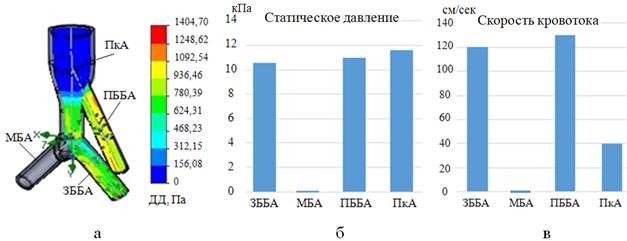
Рис. 16. Показатели гемодинамики (а), давление (б) и скорость кровотока (в) в артериях НК при окклюзии МБА
При окклюзии МБА показатели ДД в ПББА составляют 1,0-1,2 кПа, в ТПС и ЗББА они идентичны и колеблются от 0,6 до 0,9 кПа. Во всех неизмененных артериях СД находится примерно на одинаковом уровне, а скоростные показатели также выше в ПББА.
Выводы
По результатам можно сформулировать ряд выводов: СК при сужении артерий НК увеличивается; стенозирование ЗББА или МБА более 65% значимо обедняет кровоток в их бассейне; в ПББА поступление крови практически прекращается при стенозе сосуда, превышающем 75%; в случаях множественного АТС-поражения артерий значимое нарушение кровотока отмечается уже при стенозе сосудов, превышающем 50%. Атеросклеротическое поражение артерий не только ухудшает кровоток в них, но и оказывает отрицательное влияние на показатели гемодинамики в смежных артериальных коллекторах. При окклюзии ПББА скорость кровотока в ЗББА может увеличиваться до 4,5 раз, а отсутствие кровотока в ЗББА или МБА ускоряет ток крови в ПББА до 3,5 раз. Такие изменения гемодинамики, очевидно, самым негативным образом влияют на функцию сосудов, обусловливая гипоксию тканей нижних конечностей.
Библиографическая ссылка
Артюшин Б.С., Мовчан К.Н., Лебедева Е.А., Бондаренко М.А., Русакевич К.И., Исхаков Р.Б. ПЕРСПЕКТИВЫ СОЗДАНИЯ МАТЕМАТИЧЕСКОЙ МОДЕЛИ КРОВООБРАЩЕНИЯ В АРТЕРИЯХ НИЖНИХ КОНЕЧНОСТЕЙ ПРИ АТЕРОСКЛЕРОЗЕ // Современные проблемы науки и образования. 2017. № 2. ;URL: https://science-education.ru/ru/article/view?id=26321 (дата обращения: 05.04.2026).



