Иммуногистохимия (ИГХ) — это метод выявления точной локализации того или иного клеточного или тканевого компонента (антигена) благодаря связыванию его с мечеными антителами. Albert Coons в 1941 г. впервые получил меченные флюоресцеином антитела и применил их в диагностических целях. В 1970 г. Ludwig Sternberger изобрёл пероксидаза-антипероксидазный метод, а в 1975 г. Georges Kцhler и Cйsar Milstein впервые добились слияния короткоживущих лимфоцитов, продуцирующих антитела, и постоянно растущих клеток плазмоцитомы, и полученные, теоретически «бессмертные», культивируемые клоны гибридных клеток позволили получать разнообразные моноклональные антитела в больших количествах. В 1990-х было обнаружено, что возможен поиск нереактивных антигенов в тканях, фиксированных формалином и заключённых в парафин, путём их нагрева в буферных растворах. Это расширило возможности метода и повысило его чувствительность [1].
В последнее десятилетие ИГХ-анализ обрёл широкое применение в каждодневной диагностической практике, перестал быть методом сугубо научных исследований.
На сегодняшний день существуют различные иммуногистохимические методы, однако в практической деятельности наиболее широко распространено непрямое иммуноокрашивание с использованием биотинавидинового комплекса. Непрямой метод предполагает использование двух различных антител.
Первичные антитела реагируют с антигенами ткани. Связанные с меткой вторичные антитела специфически взаимодействуют с первичными, которые для вторичных антител являются антигеном. Метод значительно чувствительнее прямого, т.к. с каждой молекулой первичных антител связывается несколько молекул вторичных антител, содержащих метку. Биотин (витамин H) — соединение, стойкое к действию высоких температур, к кислой и щелочной среде, хорошо растворяется в воде и спирте. Он является коферментом во многих реакциях присоединения (карбоксилирования). Биотин легко может вступать в стойкое соединение с различными белками, в том числе с ферментами и иммуноглобулинами. Авидин образует с биотином чрезвычайно стойкий комплекс. Разрушить такой комплекс можно только при температурной обработке, т.к. авидин разрушается при нагревании. Авидин имеет 4 места связывания, к которым можно присоединить биотин или белки. Таким образом, комплекс биотинавидин используется связующим мостиком между антителами и ферментами. Для этого готовится комплекс, состоящий из фермента, связанного с биотином, и авидина [2].
В настоящее время все большее распространение иммуногистохимическое исследование приобретает в исследовании щитовидной железы. Данное исследование позволяет оценить степень пролиферативной активности клеток щитовидной железы.
Цель исследования
Целью работы явилось исследование пролиферативной активности ткани щитовидной железы на основе экспрессии белков Ki67 (клон MIB-1), p53 (клон DO-7), Тиреоидного фактора транскрипции TTF-1 (клон 8G7G3/1), тиреоглобулина (клон DAK-Tg6) и их взаимосвязи с возможностью рецидива зоба после оперативного лечения. Это позволяет прогнозировать возможность либо отсутствие рецидива, помогает в выборе более щадящей операции.
Материалы и методы исследования
Иммуногистохимические реакции проводились на фиксированных 10%-ным фосфатным забуференным формалином, залитых в парафин срезах. Использовались моноклональные антитела к белкам Ki67 (клон MIB-1), p53 (клон DO-7), Тиреоидному фактору транскрипции TTF-1 (клон 8G7G3/1), тиреоглобулину (клон DAK-Tg6). Для восстановления антигенных детерминант применялся метод нагревания в цитратном буфере при 95 градусах Цельсия в течение 20 минут на водяной бане. Использовалась высокочувствительная полимерная система детекции, меченная пероксидазой хрена. В качестве хромогена использовался диаминобензидин (продукт реакции имеет различные оттенки коричневого цвета, от желтоватого до почти чёрного, в зависимости от концентрации антигена в исследуемой ткани). В целях визуализации морфологии ткани срезы докрашивались гематоксилином Майера в течение 30 секунд до слабой сине-фиолетовой окраски ядер клеток. В дальнейшем готовые препараты изучались при помощи микроскопа в проходящем свете. Диапазон увеличений от 50 до 1000.
В исследовании было проведено 30 иммуногистохимических исследований препаратов щитовидной железы, удаленных у пациентов хирургического отделения БУЗ МЗ «Первая республиканская клиническая больница МЗ УР» г. Ижевска с диффузными токсическими и диффузно-узловыми формами зоба в период с 01.02. 2015 г. по 01.02.2016 г.
Результаты исследования
При исследовании операционного материала производили его распределение по морфологическим признакам: диффузный зоб, узловой зоб, смешанный зоб (включая кистозный и кистозно-узловой).
Таблица 1
Распределение зоба по морфологическому строению
|
|
Диффузный зоб |
Узловой зоб |
Смешанный зоб |
Всего |
|
количество |
6 |
21 |
3 |
40 |
|
20% |
70% |
10% |
100% |
Таблица 2
Распределение факторов пролиферативной активности у пациентов при иммуногистохимическом исследовании
|
|
До 20% |
20-55% |
Более 55% |
|
Ki67 |
18 |
10 |
2 |
|
|
60% |
33% |
7% |
|
|
До 30% |
30-50% |
Более 50% |
|
p53 |
23 |
6 |
1 |
|
|
77% |
20% |
3% |
У пациентов с макрофолликулярными формами зоба отмечается низкий индекс пролиферации фолликулярного эпителия (до 1% позитивных клеток) - экспрессия Ki67. При микрофолликулярных формах зоба отмечается более высокий индекс пролиферации фолликулярного эпителия (до 5% позитивных клеток). Белок p53 является проапоптотическим белком, участвует в одном из основных сигнальных путей, регулирующих запрограммированную гибель клетки (апоптоз) – ядерный путь апоптоза. Он экспрессируется в ядрах большинства нормальных клеток, при этом определяемая степень экспрессии слабая (желтоватое или бледно-коричневое окрашивание ядер) – так называемый дикий тип гена. При мутации гена, кодирующего белок р53, функция белка нарушается, ядерный путь апоптоза блокируется, клетки становятся «бессмертными», что может впоследствии служить основой для развития опухоли. Мутантный ген также обладает свойством гиперэкспрессии – производится большое количество белка р53, не обладающего функциональной активностью. Продукт мутантного гена накапливается в ядрах клеток, что иммуногистохимически выявляется в виде тёмно-коричневого окрашивания ядер, более яркого, чем окраска ядер соседних клеток, несущих ген «дикого» типа (рисунок).
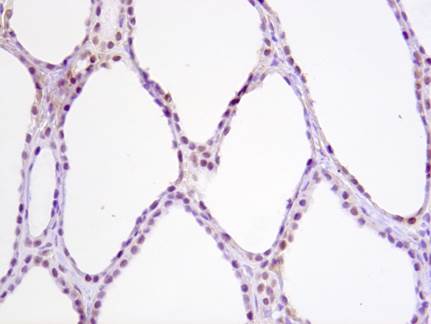
Экспрессия белка р53 в нормальной ткани щитовидной железы. Слабое желтовато-коричневое окрашивание ядер на сине-фиолетовом фоне. «Дикий тип» экспрессии гена р53
У пациентов с пролиферативными формами зоба наблюдалось более интенсивное коричневое окрашивание ядер, что указывает на гиперэкспрессию гена р53 в участках микрофолликулярной пролиферации и косвенно свидетельствует о возможной мутации гена р53. У 2 пациентов наблюдалась гиперэкспрессия мутантного гена р53 в участке микрофолликулярной пролиферации эпителия с морфологическими (ядерными) признаками тяжёлой дисплазии, что говорит о высоком потенциале опухолевой трансформации этой клеточной популяции [3].
Тиреоглобулин – белковый продукт фолликулярного эпителия щитовидной железы, выявляемый в цитоплазме фолликулярных клеток, в коллоиде фолликулов щитовидной железы. Позитивная реакция определяется по различным оттенкам коричневого окрашивания вышеназванных структур. У пациентов с макрофолликуляным зобом наблюдается умеренная интенсивность реакции в коллоиде фолликулов. У пациентов с тиреотоксическими формами зоба наблюдалась интенсивная реакция в коллоиде фолликулов и в цитоплазме фолликулярного эпителия, что свидетельствует о высокой функциональной активности ткани железы. У пациентов с микрофолликулярными формами зоба структуры в цитоплазме практически не содержат коллоида, что говорит о функциональной незрелости данного участка железистой ткани. Тиреоидный фактор транскрипции TTF-1 – белковый продукт, локализующийся в ядрах клеток фолликулярного эпителия щитовидной железы, С-клеток щитовидной железы, альвеолярного эпителия и нейроэндокринных клеток лёгкого. Этот белок является индуктором транскрипции (экспрессии) групп генов, ответственных за дифференцировку вышеназванных клеточных типов, имеющих общее происхождение в эмбриогенезе. Позитивная реакция определяется по коричневому окрашиванию ядер клеток.
При всех вариантах зоба наблюдалась интенсивная экспрессия TTF-1 в фолликулярном эпителии.
После проведенных иммуногистохимических исследований все случаи были распределены в 3 группы в соответствии со степенью выявленной пролиферации ткани щитовидной железы [4].
I степень пролиферации:
- индекс пролиферации Ki-67 составляет 15-20%;
- экспрессия протеина Р53 составляет 25-30%;
- пролиферация фолликулярного и парафолликулярного эпителия, занимающих 30-35% фолликулов.
II степень пролиферации:
- индекс пролиферации Ki-67 составил 50-55%;
- экспрессия протеина Р53 составляет 55-60%;
- пролиферация фолликулярного и парафолликулярного эпителия, занимающих 50% фолликулов.
III степень пролиферации:
- пролиферация фолликулярного и парафолликулярного эпителия, занимающих 70-75% фолликулов;
- индекс пролиферации Ki-67 составил 70%;
- экспрессия протеина Р53 75-80%.
Результаты исследования
После проведенных иммуногистохимических исследований все случаи были распределены в 3 группы в соответствии со степенью выявленной пролиферации ткани щитовидной железы. В 60% случаев была выявлена I степень пролиферации, что позволяет в данных случаях выполнять органосохраняющие операции. В 33% случаях была выявлена II степень пролиферации ткани щитовидной железы, что может говорить о высоком риске рецидивирования, в данном случае будут оправданы радикальные операции. В 7% случаев была выявлена III степень пролиферации, что подразумевает риск малигнизации, данные пациенты должны быть оперированы в условиях онкологического диспансера [5].
Выводы
Первая степень зобной пролиферации не является фактором риска рецидива зоба после оперативного удаления одной доли (гемиструмэктомии) или резекции щитовидной железы. Вторая степень зобной пролиферации служит фактором риска рецидива зоба. Третья степень пролиферации служит достоверным признаком рецидива зоба и возможной малигнизации узлов-регенератов. Эта стадия должна рассматриваться как предраковая и оцениваться как дисплазия III степени.
Заключение
При выявлении первой степени пролиферации зоба оправданными были органосохраняющие операции, гемитиреоидэктомия или резекция щитовидной железы, поскольку риск рецидивирования отсутствует. При выявлении второй степени пролиферации целесообразнее выполнять субтотальную тиреоидэктомию, так как существует риск рецидивирования. При выявлении третьей степени пролиферации должно проводиться радикальное оперативное лечение в условиях онкологического диспансера.
Библиографическая ссылка
Стяжкина С.Н., Порываева Е.Л., Климентов М.Н., Леднева А.В. ВОЗМОЖНОСТИ ИММУНОГИСТОХИМИЧЕСКОГО ИССЛЕДОВАНИЯ ДЛЯ ОЦЕНКИ ПРОЛИФЕРАТИВНОЙ АКТИВНОСТИ ТКАНИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ // Современные проблемы науки и образования. 2017. № 2. ;URL: https://science-education.ru/ru/article/view?id=26185 (дата обращения: 28.04.2026).



