За последние десятилетия отмечается неуклонный рост больных с узловой патологией щитовидной железы (ЩЖ) [1; 2]. Это связано, прежде всего, с неблагоприятной экологической обстановкой, увеличением стрессовых ситуаций, наличием наследственной и регионарной предрасположенности к тиреоидной патологии, связанной с йодным дефицитом, а также улучшением качества диагностики патологии ЩЖ [1]. Рак ЩЖ является наиболее частой формой всех злокачественных новообразований эндокринной системы и составляет от 0,4% до 6% [1; 2; 7].
Клиническая значимость узловых образований ЩЖ основывается, прежде всего, на необходимости исключить рак ЩЖ. В амбулаторной практике мультипараметрическое ультразвуковое исследование (УЗИ), тонкоигольная аспирационная пункционная биопсия (ТАПБ) под контролем УЗИ являются «золотым стандартом» определения тиреоидной патологии [3-5; 11]. При пальпации ЩЖ обнаруживается только одна десятая часть этих узлов [6]. Почти у 50% пациентов с пальпируемым узлом имеются дополнительные узловые образования, обнаруженные при УЗИ [3]. В свою очередь, однофотонная эмиссионная компьютерная томография (ОФЭКТ) позволяет получить данные функциональной оценки патологических процессов ЩЖ [9; 10].
Однако одинаковая сонографическая картина может встречаться как при доброкачественных, так и злокачественных узлах ЩЖ. Поэтому классификация ультразвуковых признаков узлов ЩЖ по системе TIRADS, разработанная в 2009 году E. Horvath и др. и модифицированная J.Y. Kwak и др. в 2011 г., дала новые возможности в выявлении риска злокачественности узлов ЩЖ.
В связи с этим целью нашего исследования явилась оптимизация раннего выявления рака щитовидной железы (РЩЖ) в дооперационном периоде по Чувашской Республике с внедрением в алгоритм комплексной лучевой диагностики классификации узлов по системе TIRADS по данным ультразвуковых изображений с одновременным применением ТАПБ под контролем УЗИ и ОФЭКТ.
Методы и материалы исследования
В основу работы взяты результаты исследования 104 пациентов в дооперационном периоде, обратившихся за медицинской помощью в Бюджетное учреждение «Республиканский клинический онкологический диспансер» Министерства здравоохранения Чувашской Республики с 2007 по 2015 год. Возраст пациентов варьировал от 18 лет до 85 лет. Женщин среди них было 81 (77,8%), мужчин – 23 (22,2%).
В контрольную группу (N2) были включены 30 здоровых пациентов, которые дали добровольное и информированное согласие на исследование ЩЖ.
Все диагностические исследования, которые проводились пациентам в основной группе (N1), производились и пациентам в контрольной группе (N2) с соблюдением принципов конфиденциальности и добровольности в соответствии с «Основами законодательства РФ об охране здоровья граждан» (Указ Президента РФ от 24.12.1993 № 2288), Федеральным законом РФ № 323-ФЗ от 21.10.2011 «Об основах охраны здоровья граждан в РФ».
В ходе нашего исследования всем 104 больным (100%) проводилось мультипараметрическое УЗИ на ультразвуковом аппарате Aplio XG (Toshiba, Япония) с линейным датчиком частотой сканирования 7-14 МГц с использованием современных методик и технологий (В-режима, цветового и энергетического доплеровского картирования). Важными ультразвуковыми характеристиками по классификации TIRADS, которые учитывались при анализе результатов, были эхогенность структуры узлового образования (анэхогенное/ гипоэхогенное/ изоэхогенное/ гиперэхогенное), контуры (четкие/нечеткие, ровные/неровные), наличие микрокальцинатов, особенности васкуляризации обнаруженных узлов.
Для морфологический верификации узлов ЩЖ больным проводилась ТАПБ под контролем УЗИ. Данные протоколов УЗИ сопоставлялись с данными цитологического и морфологического заключений.
ОФЭКТ исследование проводилось пациентам с помощью комбинированной системы Precedence (Philips, Нидерланды), состоящей из двух гамма-детекторов и компьютерной 16-слойной томографической приставки. В диагностических целях использовали радиофармпрепарат - 99mTс-Пертехнетат, который приготовлен по инструкции производителя. Пациенту 99mTс-Пертехнетат вводился внутривенно, активность его составляла 100-300 МБк. Далее через 20 минут после этого проводилось ОФЭКТ. Пациента располагали под детектором гамма-камеры томографа в положении лежа и таким образом, чтобы в поле зрения попадали обе доли щитовидной железы. Результаты накопления радиофармпрепарата в исследуемых зонах оценивались количественно и визуально. Вид излучения, испускаемый 99mTс-Пертехнетатом, относится к классу фотонного (гамма-кванты) с низкой энергией 140 кэВ и периодом полураспада 6 часов. В связи с этим лучевые нагрузки, получаемые нашими пациентами, являлись минимальными и не оказывали существенного (детерминированного) воздействия на организм.
В случае выявления «холодных» узлов пациентам дополнительно проводилось исследование с 99mTс-Технетрилом (МИБИ), приготовленным тоже по инструкции производителя. 99mTс-Технетрил пациенту также вводился внутривенно, активность его составляла 750 МБк. Через 2 часа после введения радиофармпрепарата (РФП) оценивалось накопление РФП в узле.
Расчёты статистических показателей выполнены с использованием стандартных методов. Различия считали статистически значимыми при p <0,05.
Результаты и обсуждения
В настоящее время мультипараметрическое УЗИ является одним из самых информативных методов лучевой диагностики для обследования пациентов с патологией ЩЖ на амбулаторном этапе [3]. Несмотря на это, нет достоверных самостоятельных ультразвуковых критериев для морфологической принадлежности узлов ЩЖ. Врачи пользуются лишь совокупностью сонографических признаков, позволяющей предположить морфологическую структуру узла ЩЖ. Так, для рака ЩЖ характерны нечеткость и неровность контуров, гипоэхогенность структуры, наличие микрокальцификатов, хаотическая внутриузловая васкуляризация узлового образования, регионарная шейная лимфаденопатия с признаками злокачественности. Сочетание этих ультразвуковых признаков с большой степенью вероятности позволяет заподозрить рак ЩЖ.
Однако одинаковая ультразвуковая картина может встречаться и при доброкачественных, и при злокачественных узлах, что создает трудности в дифференциальной диагностике. Поэтому классификация ультразвуковых признаков узлов ЩЖ по системе TIRADS, разработанная в 2009 году E. Horvath и соавт. и модифицированная J.Y. Kwak и соавт. в 2011 г., дала новые возможности в выявлении риска злокачественности узлов ЩЖ. Согласно этой классификации, все узловые образования ЩЖ по данным УЗИ делятся на 7 типов: TIRADS 1 (патологии не выявлено), TIRADS 2 (доброкачественное образование), TIRADS 3 (вероятно доброкачественное образование), TIRADS 4А (неопределенное), TIRADS 4В (подозрительное), TIRADS 5 (соответствует злокачественному), TIRADS 5 (злокачественное) [12].
В исследовании мы оценивали по классификации TIRADS подозрительные на злокачественный процесс солидные узловые образования: гипо-, изо- и гиперэхогенной структуры, с ровными и неровными или неровными и нечеткими контурами, с наличием гиперэхогенных включений (микрокальцинатов), гиперваскуляризации узла. По классификации TIRADS узлы относились к группе 4А и 4В.
Изучены характеристики изображений, полученных при УЗИ. По визуальным характеристикам выделены две группы пациентов. У всех здоровых пациентов в контрольной группе (N2) по данным УЗИ ЩЖ была нормальной эхогенности без узловых образований (TIRADS 1). В зависимости от ультразвуковых признаков выявленных узлов пациенты основной группы (N1) нами были распределены на 6 подгрупп, результаты которых представлены в таблице 1.
Таблица 1
Распределение больных основной группы (N1=100) по ультразвуковым признакам выявленных узлов щитовидной железы (ЩЖ) по классификации TIRADS
|
Подгруппа |
УЗИ признаки узлов ЩЖ |
TIRADS |
|
n1=37 |
Гипоэхогенный узел с четкими контурами с наличием кальцинатов, периферический кровоток |
4А |
|
n2=15 |
Гипоэхогенный узел с четкими контурами с наличием микрокальцинатов, смешанный кровоток |
4А |
|
n3=16 |
Гиперэхогенный узел с капсулой с содержанием микрокальцинатов, кровоток смешанный |
4А |
|
n4=10 |
Изоэхогенный узел с четкими контурами с наличием кальцинатов, смешанный кровоток |
4А |
|
n5=21 |
Гипоэхогенный узел с нечеткими контурами с наличием микрокальцинатов, смешанный кровоток |
4В |
|
n6=5 |
Гипоэхогенный узел с нечеткими, неровными контурами с наличием микрокальцинатов, центральный кровоток |
4В |
Всем пациентам с солидными узлами ЩЖ (основная группа N1), имеющими вышеперечисленные сонографические признаки, проводилась ТАПБ под контролем УЗИ. ТАПБ является единственным и высокоинформативным методом морфологической оценки характера узла на дооперационном этапе. Международные стандарты определяют показание к ТАПБ при размере образования не менее 10 мм. ТАПБ узлов ЩЖ менее 10 мм рекомендуется проводить только в тех случаях, когда клиническая информация или ультразвуковые признаки указывают на возможное наличие злокачественного образования [8]. Правильно выполненная ТАПБ является абсолютно безвредной, безопасной, не дающей осложнений. Благодаря применению ТАПБ в клинической практике в несколько раз сократилось количество «неоправданных» операций на ЩЖ.
По цитологическим результатам, доброкачественный пунктат выявлен у 36 больных, фолликулярная неоплазия – у 21, подозрительный раком пунктат – у 31, злокачественный пунктат – у 10, неинформативный пунктат – у 6 пациентов (рис. 1).
В подгруппе пациентов n1=37 в случае, если был выявлен при УЗИ гипоэхогенный узел с четкими контурами с наличием кальцинатов и периферическим кровотоком, по результатам ТАПБ в 15% случаев определялся доброкачественный пунктат, в 10% - фолликулярная неоплазия, в 8% - подозрительный раком пунктат, в 2% - неинформативный пунктат.
В подгруппе пациентов n2=15 во всех случаях на УЗИ был выявлен гипоэхогенный узел с четкими контурами с наличием микрокальцинатов и смешанным кровотоком. По результатам ТАПБ в этой подгруппе в 7% случаев определялся доброкачественный пунктат, в 3% - фолликулярная неоплазия, в 2% - подозрительный раком пунктат, в 1% - злокачественный узел, в 1% - неинформативный пунктат (рис. 2).
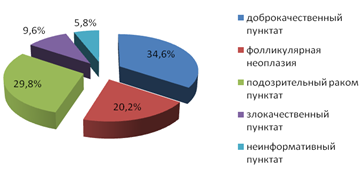
Рис. 1. Распределение пациентов основной группы (N1=100) по результатам ТАПБ
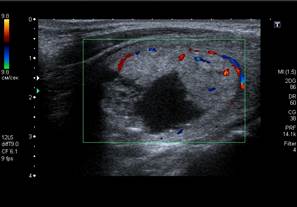
Рис. 2. Узел в левой доле с ровными четкими контурами, неоднородной структуры, со смешанным типом кровотока
В подгруппе пациентов n3=16 если был выявлен при УЗИ гиперэхогенный узел с капсулой с содержанием микрокальцинатов и смешанным кровотоком, то в 5% случаев по результатам ТАПБ определялся доброкачественный пунктат, в 2% - фолликулярная неоплазия, в 5% - подозрительный раком пунктат, в 2% - злокачественный узел, в 1% - неинформативный пунктат.
В подгруппе пациентов n4=10 если был выявлен при УЗИ изоэхогенный узел с четкими контурами с наличием кальцинатов и смешанным кровотоком, то в 4% случаев по результатам ТАПБ определялся доброкачественный пунктат, в 2% - фолликулярная неоплазия, в 4% - подозрительный раком пунктат.
В подгруппе пациентов n5=21 во всех случаях на УЗИ был выявлен узел с гипоэхогенной структурой с нечеткими контурами с наличием микрокальцинатов и смешанным кровотоком. По результатам ТАПБ в 3% случаев определялся доброкачественный пунктат, в 2% - фолликулярная неоплазия, в 10% - подозрительный раком пунктат, в 4% - злокачественный узел, в 2% - неинформативный пунктат.
В подгруппе пациентов n6=5 если был выявлен при УЗИ гипоэхогенный узел с нечеткими, неровными контурами с наличием микрокальцинатов и центральным кровотоком, то по результатам ТАПБ в 2% - подозрительный раком пунктат, в 3% - злокачественный узел.
ОФЭКТ является современным методом диагностики в ядерной медицине. Благодаря этому методу появилась возможность более детальной дифференциальной диагностики патологии ЩЖ. Применение ОФЭКТ/КТ дает возможность получать как совмещенные снимки ОФЭКТ и КТ исследований, так и независимые КТ, ОФЭКТ или планарные изображения. Поэтому несравненное диагностическое преимущество метода заключается в объединении морфологической и функциональной оценки патологических процессов ЩЖ.
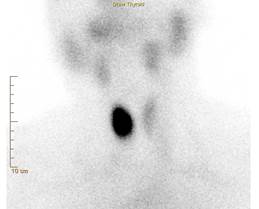
Клиническими показаниями к проведению ОФЭКТ ЩЖ на дооперационном периоде являлись: любое узловое изменение в области щитовидной железы диаметром 1 см или более, эктопическое расположение щитовидной железы, подозрение на диффузную или фокальную автономию, для оценки эндокринной активности нелеченной автономии в динамике, для выявления раннего рецидива тиреотоксикоза. Метод позволяет не только подтвердить или опровергнуть факт наличия загрудинно расположенной тиреоидной ткани, но и оценить ее размеры, в том числе в случаях так называемых холодных узлов.
|
Рис. 3. Сцинтиграфические признаки функционально автономного узла (токсической аденомы) правой доли щитовидной железы |
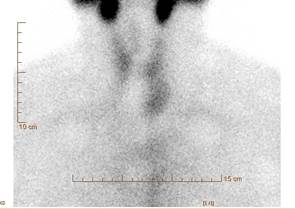
Рис. 4. Сцинтиграфические признаки левостороннего загрудинного зоба |
В ходе проведенных исследований установлено, что из 104 пациентов ОФЭКТ проводилась у 96 – для определения функционального состояния узловых образований при узловом зобе («теплые», «холодные», «горячие» очаги), у 7 – для подтверждения токсической аденомы (функционирующие «горячие» очаги) (рис. 3), у 1 – для выявления загрудинного зоба (рис. 4). В 29 случаях были выявлены «холодные узлы». При проведении ОФЭКТ с 99mTс-Технетрилом в 10 случаях определялось высокое накопление РФП в узлах, что свидетельствовало о раке ЩЖ.
По результатам нашего исследования мы определили следующие рекомендации по наблюдению и ведению пациентов в зависимости от заключений УЗИ, ТАПБ и ОФЭКТ (табл. 2).
Таблица 2
Рекомендации для пациентов основной группы N2 по результатам УЗИ, ТАПБ, ОФЭКТ
|
УЗ-семиотика |
ТАПБ |
ОФЭКТ |
Рекомендации |
|
4А (неопределенные узлы с риском злокачественности 5-10%) 4В (подозрительные узлы с риском злокачественности 10-80%). |
Неинформативный пунктат |
«Теплый узел» «Горячий узел» «Холодный узел» без накопления МИБИ в узле |
Повторная ТАПБ |
|
4А (неопределенные узлы с риском злокачественности 5-10%) |
Доброкачественный пунктат |
«Теплый узел» «Холодный узел» без накопления МИБИ в узле
|
Динамическое наблюдение, УЗИ через 12 месяцев, если узел растет, ТАПБ и ОФЭКТ повторить, продолжить наблюдение |
|
4А (неопределенные узлы с риском злокачественности 5-10%) 4В (подозрительные узлы с риском злокачественности 10-80%). |
Фолликулярная неоплазия |
«Горячий узел» «Холодный узел» без накопления МИБИ в узле |
Гемитиреоидэктомия, CITO морфология |
|
4А (неопределенные узлы с риском злокачественности 5-10%) 4В (подозрительные узлы с риском злокачественности 10-80%). |
Подозрительный раком пунктат |
«Горячий узел» «Холодный узел» без накопления МИБИ в узле |
Тиреоидэктомия |
|
4А (неопределенные узлы с риском злокачественности 5-10%) 4В (подозрительные узлы с риском злокачественности 10-80%). |
Злокачественный пунктат |
«Горячий узел» «Холодный узел» с высоким накоплением МИБИ в узле |
Тиреоидэктомия |
Выводы
1. Предложенная классификация TIRADS позволяет стандартизировать протокол УЗИ ЩЖ, а также минимизировать субъективный фактор в интерпретации сонографической картины узловых образований ЩЖ.
2. Внедрение классификация TIRADS по ультразвуковым данным в алгоритм ранней лучевой диагностики рака ЩЖ по Чувашской Республике является перспективной методикой в выявлении риска злокачественности узлов ЩЖ.
3. Комплексное применение УЗИ, ТАПБ, ОФЭКТ на догоспитальном этапе дает достоверную информацию о нодулярном образовании ЩЖ. Независимо от размеров узлов ЩЖ рациональное применение этих методов амбулаторным больным с тиреоидной патологией позволяет своевременно определить злокачественный характер узла и формировать дальнейшую тактику ведения пациента.
Библиографическая ссылка
Тимофеева Л.А., Алешина Т.Н. ОПЫТ ПРИМЕНЕНИЯ СОВРЕМЕННЫХ МЕТОДОВ ЛУЧЕВОЙ ВИЗУАЛИЗАЦИИ В РАННЕЙ ДИАГНОСТИКЕ РАКА ЩИТОВИДНОЙ ЖЕЛЕЗЫ ПО ЧУВАШСКОЙ РЕСПУБЛИКЕ // Современные проблемы науки и образования. 2017. № 1. ;URL: https://science-education.ru/ru/article/view?id=26069 (дата обращения: 13.05.2026).