В связи с интенсивным развитием биотехнологии актуальным становится поиск новых эффективных продуцентов липолитических ферментов. Ксилотрофные базидиомицеты обладают развитым ферментативным аппаратом, позволяющим им разлагать различные органические вещества природного происхождения. [19]. Наиболее изучены окислительные ферменты (лакказы, КФ 1.10.3.2; лигнинпероксидазы, КФ 1.11.1.14; марганецпероксидазы, КФ 1.11.1.13), ответственные за расщепление лигнина [9]. Для предобработки растительного сырья с целью получения биоэтанола интересны базидиомицеты Ceriporiopsis subvermispora (Pilát) Gilbn. & Ryv. и Pycnoporus cinnabarinus (Jacq.) P.Karst., способные удалять лигнин без разрушения целлюлозы [7, 11]. Лакказы грибов рода Trametes благодаря широкой субстратной специфичности применяются не только для предобработки лигноцеллюлозной биомассы, но и для биоремедиации почв и воды, загрязненных различными ксенобиотиками (в том числе полициклическими ароматическими углеводородами и промышленными красителями) [8, 12, 21].
Помимо оксидаз базидиомицеты также продуцируют большое количество гидролитических ферментов. Высокая активность амилаз (КФ 3.2.1.1) отмечена у грибов Flammulina velutipes (Curtis) Singer, Hericium erinaceus (Bull.) Pers. и Pleurotus ostreatus (Jacq.) P.Kumm., протеаз (КФ 3.4) – у грибов Piptoporus betulinus (Bull.) P.Karst. и Grifola frondosa (Dicks.) Gray [15]. Наличие липаз отмечено как у ксилотрофных базидиомицетов (Pleurotus sapidus Quél., Schizophyllum commune Fr.), так и у почвенных сапрофитов (Agaricus bisporus (J.E. Lange) Imbach), однако их активность и условия продуцирования исследованы недостаточно [10, 20, 22].
Липазы (триацилглицерин гидролазы, К.Ф.3.1.1.3.) представляют собой важную группу биокатализаторов для биотехнологических процессов. Липолитические ферменты способны осуществлять как гидролиз ацилглицеридов до глицерина и свободных жирных кислот, так и синтетические реакции алкоголиза, ацидолиза и этерификации в среде органических растворителей и водно-органических системах [13, 18]. Благодаря широкой субстратной специфичности липазы находят применение в процессах очистки сточных вод, в фармацевтической, пищевой и косметической промышленностях, а также для синтеза биополимеров и биодизельного топлива [13, 14, 16].
Цель настоящей работы – проведение скрининга продуцентов липаз среди грибов, относящихся к виду Fomes fomentarius (L.) Fr., а также выявление закономерностей биосинтеза липолитических ферментов наиболее перспективным штаммом при погруженном культивировании.
Методика
Реактивы
Трибутирин и глицерин были приобретены у «Sigma-Aldrich» (США), фосфорная кислота, гидрофосфат калия, дигидрофосфат калия были приобретены у «CarlRoth» (Германия), гуммиарабик, олеиновая кислота, сульфат аммония и сульфат магния были приобретены у ООО «Русхим» (Россия), агар-агар, глюкоза, ферментативный пептон и дрожжевой экстракт были приобретены у ООО «НТК ДИАЭМ». В работе использовали полуобезжиренную соевую муку, молочную сыворотку, жидкое сусло (4° по Баллингу) и подсолнечное масло пищевого качества.
Штаммы
Штаммы F. fomentarius 12.02, F. fomentarius 12.03, F. fomentarius 12.09, F. fomentarius 12.13, F. fomentarius 12.14 и F. fomentarius 12.23 выделены из плодовых тел, собранных на территории Московской области. Выделение мицелиальных культур проводили по общепринятым методикам на плотной среде, содержащей (г/л водопроводной воды): агар-агар – 15,0; жидкое сусло – 30,0 и ферментативный пептон – 3,0 [2, 3]. Принадлежность выделенных культур к базидиомицетам подтверждалась методом световой микроскопии по наличию пряжек на мицелии. Для установления таксономической принадлежности плодовых тел использовали определители базидиальных грибов [4, 5]. Рабочие культуры базидиомицетов хранили на скошенном сусловом агаре при +4 °С.
Скрининг продуцентов липаз
Скрининг проводили диффузионным методом на среде, содержащей (г/л водопроводной воды): агар-агар – 15,0; трибутирин – 10,0; пептон – 5,0 и дрожжевой экстракт – 3,0. Трибутирин предварительно эмульгировали в воде ультразвуком в течение 1 мин (выходная мощность 85 Вт; ультразвуковой излучатель S-450D, «Branson», США). Чашки Петри засевали агаровыми блоками с 10-дневными культурами базидиомицетов (диаметр 1 мм) и инкубировали при 25 °С в течение 96 ч, после чего проводили измерение диаметров колоний (d) и зон просветления вокруг них (D). Штамм с наибольшей величиной «гало» (D-d) был выбран для дальнейших исследований.
Подбор компонентов питательной среды
Штамм F. fomentarius 12.13 выращивали в течение 120 ч при 25 °С на 42 плотных средах, различающихся сочетаниями источников углерода и азота, после чего вырезали агаровые блоки с мицелием (7 мм × 4 мм) и помещали в центр чашек Петри со средой, содержащей (г/л фосфатного буферного раствора, рН 6,5): агар-агар – 15,0; трибутирин – 10,0. Чашки Петри инкубировали при 37 °С в течение 48 ч. Липолитическую активность оценивали по величине зоны просветления по шкале от «-» (нет активности) до «++++» (высокая активность). В качестве источников углерода использовали глюкозу, жидкое сусло, крахмал, этанол, глицерин, подсолнечное масло, олеиновую кислоту в концентрациях, эквивалентных 20 г/л глюкозы, в качестве источников азота – дрожжевой экстракт, пептон, соевую муку, молочную сыворотку, кукурузный экстракт и нитрат аммония в концентрациях, эквивалентных 10 г/л пептона. Для каждой среды отмечали ростовой коэффициент [3].
Условия культивирования
Погруженное культивирование проводили в колбах Эрленмейера емкостью 750 мл, содержащих 100 мл среды, при 220 об/мин и температуре 28 °C. Объем посевного материала составлял 10% объема ферментационной среды. В качестве посевного материала использовали 6-суточную культуру базидиомицета, выращенную в описанных выше условиях на среде, содержащей (г/л водопроводной воды): глюкозу – 20,0; соевую муку – 10,0; дигидрофосфат калия – 2,5 и сульфат магния – 0,25 [1, 6].
Биомассу отделяли от культуральной жидкости фильтрованием через лавсановую ткань, фильтрат использовали для дальнейших исследований. Биомассу высушивали при 50 °C в течение суток.
Определение липазной активности
Липолитическую активность определяли газохроматографическим методом с использованием эмульсии трибутирина в качестве субстрата. Субстрат готовили добавлением трибутирина (10 % вес.) в водный раствор гуммиарабика (1 %вес.) и обработкой смеси ультразвуком в течение 2 мин. К 400 мкл раствора субстрата добавляли 400 мкл фильтрата культуральной жидкости или 10 мг высушенного мицелия в 400 мкл фосфатного буфера (рН 6,5) и инкубировали смесь при 37 °С в течение 24 часов при постоянном перемешивании. Реакцию ферментативного гидролиза прерывали добавлением 30 мкл фосфорной кислоты (85 %). Реакционную смесь центрифугировали в течение 10 мин при 10000 g, концентрацию масляной кислоты в водной фазе определяли на газовом хроматографе Кристалл-5000.2 («Хроматек», Россия). За единицу активности (U) принимали количество масляной кислоты (µмоль), образующееся при каталитическом воздействии липаз, приходящихся на 1 мл фильтрата культуральной жидкости или 1 мг мицелия.
Результаты и их обсуждение
Из плодовых тел, собранных с различных природных субстратов, выделено 6 штаммов базидиомицета F. fomentarius. Методом фазово-контрастной микроскопии на мицелии всех штаммов были выявлены пряжки – структуры, характерные для представителей отдела Basidiomycota (рис. 1, 2).
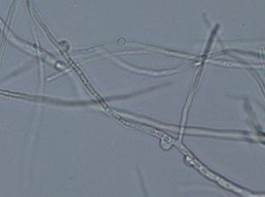
Рис. 1. Микрофотография мицелия F. fomentarius 12.13 (×400)
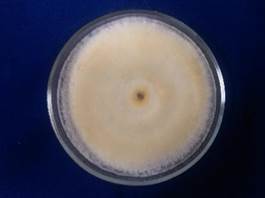
Рис. 2. Культура F. fomentarius 12.13 на сусловом агаре
Скрининг продуцентов липолитических ферментов среди выделенных штаммов проводили диффузионным методом на среде, содержащей трибутирин. В результате ферментативного гидролиза трибутирина вокруг растущих колоний (96 ч культивирования) образовывались зоны гидролиза, размер которых варьировал от 7,25 до 14,75 мм (рис. 3). Полученные данные свидетельствовали о способности всех выделенных штаммов продуцировать липазы. Наибольшая зона просветления была отмечена у штамма F. fomentarius 12.13.

Рис. 3. Скрининг продуцентов липаз диффузионным методом
Исследование роста и липолитической активности F. fomentarius 12.13 на 42 питательных средах различного состава показало, что источник углерода не оказывает существенного влияния на продуцирование липаз базидиомицетом (табл. 1).
Таблица 1
Влияние источников углерода и азота в питательной среде на липолитическую активность fomentarius 12.13
|
Дрожжевой экстракт |
Пептон |
Соевая мука |
Молочная сыворотка |
Кукурузный экстракт |
Нитрат аммония |
|
|
Глюкоза |
- |
+++ |
- |
+++ |
- |
- |
|
Сусло |
- |
++++ |
- |
+++ |
- |
- |
|
Крахмал |
+ |
+++ |
- |
+++ |
- |
- |
|
Этанол |
- |
++ |
- |
++ |
- |
- |
|
Глицерин |
+++ |
+++ |
- |
+++ |
- |
- |
|
Подсолнечное масло |
- |
++ |
- |
+++ |
+ |
- |
|
Олеиновая кислота |
++ |
++ |
- |
+++ |
- |
- |
Липолитическая активность в баллах: «-» – диаметр зоны просветления 0-11,9 мм; «+» – 12,0-14,9 мм; «++» – 15,0-17,9 мм; «+++» – 18,0-19,9 мм; «++++» – более 20 мм
Высокая липолитическая активность была отмечена на средах как с липидными, так и углеводными источниками питания, максимальный ростовой коэффициент был получен на средах, содержащих сусло и крахмал (табл. 2). Среди исследованных источников азота синтезу липаз способствовали пептон и молочная сыворотка, более активному росту базидиомицета – кукурузный экстракт и соевая мука.
Таблица 2
Ростовые коэффициенты базидиомицета F. fomentarius 12.13 на плотных средах через 120 ч культивирования
|
Дрожжевой экстракт |
Пептон |
Соевая мука |
Молочная сыворотка |
Кукурузный экстракт |
Нитрат аммония |
|
|
Глюкоза |
12,45 |
5,55 |
17,10 |
1,15 |
16,50 |
0,50 |
|
Сусло |
15,90 |
8,25 |
25,20 |
11,70 |
22,20 |
15,90 |
|
Крахмал |
10,65 |
4,05 |
25,65 |
1,33 |
17,11 |
0,50 |
|
Этанол |
8,10 |
3,45 |
16,65 |
0,58 |
3,75 |
0,50 |
|
Глицерин |
10,65 |
4,05 |
19,65 |
0,83 |
13,30 |
0,50 |
|
Подсолнечное масло |
10,05 |
4,40 |
2,78 |
1,35 |
2,25 |
0,50 |
|
Олеиновая кислота |
10,8 |
0,90 |
2,85 |
1,43 |
2,95 |
0,53 |
Изучение липолитической активности погруженной культуры базидиомицета проводили, выращивая продуцент на среде с суслом и пептоном в качестве источников углерода и азота, обеспечивших максимальный выход ферментов при культивировании на плотной среде. В табл.3 представлена динамика накопления внеклеточных и внутриклеточных липаз при погруженном культивировании F. fomentarius 12.13 в течение 168 ч. Максимальный выход внеклеточных ферментов был отмечен через 120 ч культивирования (107,1 мU/мл культуральной жидкости), при дальнейшем культивировании базидиомицета содержание липаз в среде резко снижалось. Полученные данные сопоставимы с результатами исследования липолитической активности плесневых грибов. Например, оптимальное время культивирования Penicillium melinii UzLM-4 составило 96 ч [17]. В случае внутриклеточных липаз F. fomentarius 12.13 максимальная липолитическая активность была получена через 144 ч культивирования (4,90 мU/мг мицелия), что соответствовало точке максимума накопления биомассы (0,51 г/100 мл).
Таблица 3
Динамика накопления биомассы, внутриклеточных и внеклеточных липаз при погруженном культивировании базидиомицета F. fomentarius 12.13
|
Время культивирования, ч |
Содержание воздушно-сухой биомассы, г/100 мл |
Активность внеклеточных липаз, мU/мл культуральной жидкости |
Активность внутриклеточных липаз, мU/мг мицелия |
|
24 |
0,13±0,03 |
11,55±1,71 |
0,35±0,09 |
|
48 |
0,21±0,01 |
14,87±4,62 |
1,12±0,07 |
|
72 |
0,29±0,01 |
17,57±0,97 |
1,92±0,15 |
|
96 |
0,46±0,03 |
23,01±3,72 |
2,44±0,13 |
|
120 |
0,48±0,02 |
107,07±4,86 |
2,99±0,23 |
|
144 |
0,51±0,03 |
56,52±1,66 |
4,90±0,55 |
|
168 |
0,48±0,02 |
36,32±0,82 |
4,10±0,48 |
Заключение
Таким образом, установлена способность ксилотрофных базидиомицетов, относящихся к виду F. fomentarius, продуцировать липолитические ферменты. Из 6 штаммов, выделенных из плодовых тел, собранных в природе, был отобран F. fomentarius 12.13, характеризующийся высокими показателями скорости роста в погруженной культуре и активности как внутриклеточных, так и внеклеточных липаз. Полученные данные позволяют рассматривать штамм F. fomentarius 12.13 как перспективный продуцент ферментов для биотехнологических процессов.
Работа выполнена при финансовой поддержке РФФИ, проект 16-38-00904 мол_а.
Библиографическая ссылка
Альмяшева Н.Р., Голышкин А.В. ЗАКОНОМЕРНОСТИ БИОСИНТЕЗА ЛИПОЛИТИЧЕСКИХ ФЕРМЕНТОВ КСИЛОТРОФНЫМ БАЗИДИОМИЦЕТОМ FOMES FOMENTARIUS // Современные проблемы науки и образования. 2016. № 6. ;URL: https://science-education.ru/ru/article/view?id=25835 (дата обращения: 07.05.2026).
DOI: https://doi.org/10.17513/spno.25835



