Актуальность. При коронарных вмешательствах в условиях искусственного кровообращения (ИК) в большинстве случаев требуется использование аутовен [6]. Длительность функционирования этих шунтов во многом определяется малотравматичной их эксплантацией для лучшего сохранения нативных свойств вен в условиях коронарной имплантации [3]. В этом отношении не до конца выяснены морфологические критерии сохранения нативных свойств аутовены при использовании щадящих методик [3]. Таким образом, дальнейшее изучение морфологических характеристик различных методов эксплантации аутовены для коронарного шунтирования (КШ) является актуальной фундаментальной и клинической задачей. В нашем исследовании проведена такая сравнительная морфологическая оценка традиционного метода эксплантации аутовены и разработанного нами метода.
Цель – дать морфологическое обоснование оптимального сохранения нативных свойств аутовен для коронарного шунтирования у больных с ИБС.
Материалы и методы. В клинике госпитальной хирургии ЮУГМУ на базе ФЦ ССХ г. Челябинска и в Самарском межобластном кардиохирургическом центре с 2006 по 2016 гг. была использована разработанная нами новая технология малотравматичной эксплантации аутовен для КШ у пациентов с ИБС. Для оценки морфологических изменений, возникающих при эксплантации аутовены по предложенной нами технологии и по традиционной методике, было использовано 30 фрагментов большой подкожной вены бедра (БПВ) пациентов. Из них 17 фрагментов было эксплантировано по классической методике, а 13 – по предложенной нами малотравматичной технологии. Классическая методика эксплантации аутовены осуществлялась с помощью скальпеля, ножниц и электрокоагулятора, при этом проводилась полная ее скелетизация.
Выделение БПВ по разработанной нами технологии выполняли с сохранением периваскулярных тканей по 0,5 см с обеих сторон и с применением гармонического ультразвукового скальпеля Harmonic Ultracision (Ethicon, США). Основой его действия является энергия ультразвука, которая позволяет производить выделение аутовены с минимальным термическим воздействием (50–100ºС) на периваскулярные ткани, что позволяет добиться минимальной травматизации.
Для сравнения травматичноcти обеих методик мы использовали световую и электронную микроскопию фрагментов аутовен. Проведено морфологическое исследование 30 фрагментов БПВ: 17 фрагментов, взятых по классической методике, и 13 – по разработанной нами технологии. Окраску микропрепаратов для световой микроскопии производили гематоксилином и эозином для общей оценки состояния сосудистой стенки, пикрофуксином по ван Гизону – для выявления коллагеновых волокон, по Харту – для идентификации эластических волокон. Анализ материала производили с помощью светового микроскопа ЛОМО Микмед-2 при увеличении х100, х200 и х400. Фотосъемку проводили с помощью светового микроскопа Axioscop 40 камерой Pixera Pro 150ES (Германия). Морфометрию выполняли с помощью программы Морфология 5.2 (Россия).
С помощью электронной микроскопии было изучено 5 фрагментов аутовен. Из них 3 фрагмента было получено от аутовен, выделенных по нашей малотравматичной методике, и 2 фрагмента были выделены традиционно. Материал для электронной микроскопии фиксировали в 2%-ном параформальдегиде и 2,5%-ном глутаральдегиде на какодилатном буфере (по Карновскому) с 5%-ной сахарозой, затем дофиксировали в 2%-ном тетраоксиде осмия, контрастировали ацетатом урана «в блоке» и заливали в смолу, эпоксидные блоки полимеризовались при температуре 640С. Полутонкие срезы толщиной 900 нм с эпоксидных блоков окрашивали толлуидиновым синим с добавлением 1% буры и просматривали в световом микроскопе. Ультратонкие срезы толщиной 60 нм контрастировали по методу Рейнольдса уранилацетатом и цитратом свинца. Сетки изучали в трансмиссионном электронном микроскопе Libra-120 («Carl Zeiss & MT», Германия) с цифровой SSCCD камерой UltraScan 950 (4 мпикс) в диапазоне увеличения 1200–20000.
Полученные данные были классифицированы в соответствии со степенью выраженности морфологических изменений в них и наличием микроскопических дефектов. Для оценки уровня травматического воздействия на стенку вены мы использовали известные критерии степеней выраженности травматизации аутовены по морфологическим изменениям [2].
Для расчета показателей описательной статистики, статистических критериев, вероятности «Р», а также построения графиков был использован пакет программ IBM SPSS Statistics 21 и Microsoft Excel 2013.
Результаты
Распределение выраженности повреждения в 30 изученных нами фрагментах аутовен по вышеуказанным критериям представлено в таблице 1.
Таблица 1
Морфологические критерии выраженности повреждений аутовен при различных способах их эксплантации
|
Степень изменений сосудистой стенки |
Малотравматичная технология эксплантации аутовен (n=13) |
Классический способ эксплантации аутовен (n=17) |
P |
|
Норма |
3 (23,0%) |
0 (0%) |
0,07 |
|
Слабо выраженные изменения |
6 (46,1%) |
2 (11,7%) |
0,049 |
|
Умеренно выраженные изменения |
3 (23,0%) |
10 (58,8%) |
0,07 |
|
Выраженные изменения |
1 (7,69%) |
5 (29,4%) |
0,196 |
|
Общее количество изменений |
10 (76,92%) |
17(100%) |
0,07 |
Исходя из данных таблицы становится очевидным, что, несмотря на отсутствие достоверных различий в изменениях между двумя способами эксплантации аутовен для КШ, малотравматичный способ выделения аутовены является более щадящим по общим морфологическим критериям. Недостоверность данных может быть связана с небольшим количеством морфологического материала.
Вместе с тем для хорошего и длительного функционирования аутовенозных коронарных шунтов большое значение имеет состояние их эндотелия и сохранности vasa vasorum сразу после их эксплантации [3]. Поэтому для оценки выраженности эндотелиальных повреждений аутовены и сохранности vasa vasorum в зависимости от различных способов ее эксплантации нами проведено дополнительное исследование интимы и адвентиции во всех 30 фрагментах вен. Для этого оценивались отдельные структурные повреждения: очаговая десквамация эндотелия, расслоение стенки вены без визуальных повреждений, надрыв внутреннего слоя сосудистой стенки горизонтального или вертикального направления, локальный или диффузный отек сосудистой стенки, адгезия форменных элементов крови к поверхности эндотелия, формирование пристеночных тромбов и паравазальная коагуляция мягких тканей, количество сохранившихся vasa vasorum в сосудистой стенке и прилежащих тканях.
Частичное отсутствие эндотелиальной выстилки чаще отмечалось в венах, выделенных классическим способом. Протяженность таких участков обычно не превышала 250 мкм. В отдельных случаях отмечалась адгезия форменных элементов крови на участках десквамации эндотелия как результат компенсаторных механизмов закрытия поверхностных повреждений стенки сосуда. При этом формирования пристеночных тромбов в исследуемых препаратах не отмечали. Особенности структурных повреждений эндотелия в исследуемых фрагментах представлены в таблице 2.
Таблица 2
Морфологические критерии выраженности повреждений аутовен при различных способах их эксплантации
|
Виды повреждений стенки |
Фрагменты вены, эксплантированные малотравматичным способом (n=13) |
Фрагменты вены, эксплантированные классическим способом (n=17) |
P |
|
Очаговая десквамация эндотелия |
2 (15,3%) |
6 (35,3%) |
0,407 |
|
Расслоение стенки вены без поверхностных повреждений ее |
3 (23,08%) |
11 (64,7%) |
0,048 |
|
Надрыв внутреннего слоя сосудистой стенки вертикального или горизонтального направления |
3 (23,08%) |
12 (70,59%) |
0,028 |
|
Локальный или диффузный отек сосудистой стенки |
10 (76,9%) |
17 (100%) |
0,141 |
|
Адгезия форменных элементов крови на поверхности эндотелия |
4 (30,7%) |
3 (17,6%) |
0,666 |
|
Формирование пристеночных тромбов |
0 |
0 |
1,000 |
|
Паравазальная коагуляция мягких тканей |
1 (7,69%) |
5 (29,4%) |
0,196 |
|
Сумма всех повреждающих факторов |
24 |
54 |
<0,0001 |
Как видно из таблицы, уровень суммарных альтеративных изменений аутовен при классическом способе их эксплантации был достоверно выше.
Во фрагментах вен, эксплантированных классическим способом, были отмечены участки десквамации эндотелия, отек компонентов сосудистой стенки (рис. 1), а также ее надрывы как в циркулярно-продольном, так и в перпендикулярно-продольном направлении (рис. 2). Глубина их не превышала 15% от общей толщины стенки и не достигала среднего слоя стенки. Наиболее вероятно, эти надрывы являются следствием механического повреждения стенки вены во время ее выделения и подготовки к аутотрансплантации.
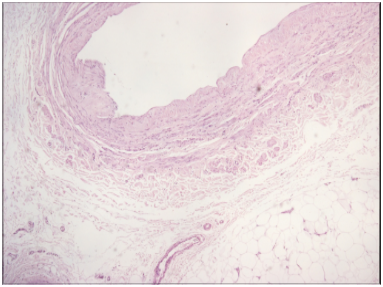
Рис. 1. Морфологическая характеристика БПВ, эксплантированной классическим способом
Очаговая десквамация эндотелиоцитов, умеренный отек компонентов сосудистой стенки, единичные капилляры системы vasa vasorum; нервные стволики отсутствуют.
Окраска гематоксилином и эозином, х200.

Рис. 2. Отек стенки сосуда с расщеплением эластической компоненты БПВ Электронограмма, х1600
Во фрагментах вен, эксплантированных с помощью разработанного нами малотравматичного способа, очаговая десквамация эндотелия была выявлена только в 2 случаях, в остальных венах интима и другие элементы сосудистой стенки были структурно сохранны (рис. 3, 4).
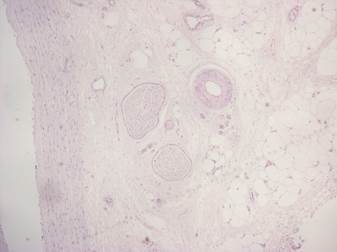
Рис. 3. Структурная сохранность интимы и других элементов сосудистой стенки, значительное представительство vasa vasorum и нервных стволиков, осуществляющих трофику сосудистой стенки. Окраска гематоксилином и эозином, х200
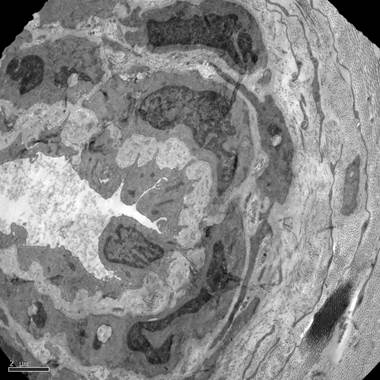
Рис. 4. Структурная сохранность эндотелиоцитов БПВ. Электронограмма, х1260
Во фрагментах вен, выделенных по классической методике, расслоение стенки аутовены на границе внутреннего и среднего слоев обнаружено в 11 случаях. Протяженность его не превышала четверти окружности сосуда. Локальный или диффузный отек стенки вены отмечался во всех случаях классического хирургического выделения БПВ (рис. 5) и в большинстве случаев выделения ее с сохранением паравазальной клетчатки. Возникновение его связано с различными повреждениями сосудистой стенки, возникающими в ходе процедуры выделения сосуда.
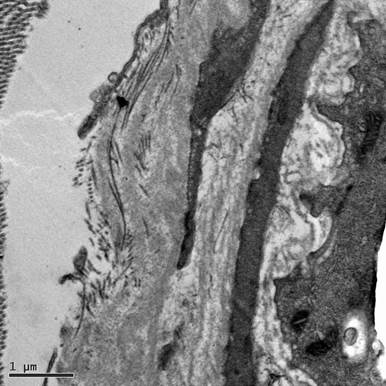
Рис. 5. Отек эластической части сосуда и фрагментация коллагена БПВ, забор которой осуществлялся по традиционной методике. Электронограмма, увеличение х4000
В отдельных случаях имели место изменения паравазальной клетчатки с развитием коагуляционного некроза, связанные с самим хирургическим вмешательством. Эти случаи в обеих группах были весьма немногочисленны.
Отдельно оценивалось количество сохранных vasa vasorum в сосудистой стенке и в паравазальных тканях. Во фрагментах аутовен, эксплантированных по предложенной нами малотравматичной технологии, наблюдались значительное количество и высокая сохранность vasa vasorum (рис. 3). Указанные сосуды капиллярного типа имели расширенный просвет, в отдельных случаях – с набухшим эндотелием; лишь в случаях выраженного диффузного отека сосудистой стенки просвет их был щелевидным. В отдельных случаях отмечалась адгезия форменных элементов крови на поверхности их эндотелия. Количество сохранных vasa vasorum оценивалось с учетом толщины адвентициального и интимального слоя сосудистой стенки (табл. 3).
Таблица 3
Морфометрическая характеристика системы vasa vasorum, толщины интимы и адвентиции аутовен при различных способах их эксплантации
|
Наименование параметров |
Малотравматичная технология эксплантации аутовен (n=13) |
Классический способ эксплантации аутовен (n=17) |
P |
|
Vasa vasorum; |
140±16 |
82,5±18 |
0,024 |
|
Толщина интимы (мкм) |
15,90±1,5 |
10,79±1,7 |
0,032 |
|
Толщина адвентиции (мкм) |
73,99±3,6 |
46,59±11,3 |
0,028 |
Из данных таблицы видно, что число структурно сохранных сосудов из системы vasa vasorum аутовен, удаленных с помощью малотравматичной технологии, достоверно превышает одноименный показатель в группе классического забора БПВ, что подтверждается и достоверно большей толщиной адвентиции сосудов у пациентов, оперированных по нашей методике.
Утолщение интимального и адвентициального слоя в обеих группах было связано как с диффузным или локальным отеком их, так и с развитием в их толще фиброза (преимущественно во фрагментах аутовен, выделенных по классической методике).
Таким образом, выделение БПВ при операции аортокоронарного шунтирования с сохранением паравазальной клетчатки приводит к меньшему количеству структурных повреждений сосудистой стенки, чем выделение вены традиционным способом. Выявленные изменения касаются в основном внутреннего слоя сосудистой стенки и лишь в единичных случаях захватывают средний слой. Полагаем, что предложенный нами способ малотравматичного выделения БПВ позволяет сохранить существенно большее число vasa vasorum, которые способствуют лучшему питанию сосудистой стенки и лучшему сохранению ее жизнеспособности.
Обсуждение
Неудовлетворенность длительностью функционирования аутовенозных КШ у больных ИБС обусловлена отличием их строения от артерий и методов эксплантации аутовен [1]. Функционирование аутовены в атипичных условиях часто приводит к фиброзу аутовенозных шунтов и сокращению сроков их проходимости [5].
В настоящее время доказано, что длительность функционирования аутовенозных шунтов во многом зависит от сохранения нативных свойств аутовены, что может быть обеспечено применением малотравматичных методик при ее эксплантации [7]. Морфологические данные свидетельствуют о том, что в сохранении нативных свойств аутовенозного шунта большое значение имеет сохранение васкуляризации его стенки, что способствует уменьшению посттравматического фиброза, развивающегося при изъятии аутовены из естественных условий функционирования [3]. В связи с этим одним из привлекательных направлений в этом плане является оптимизация щадящих методов выделения, лигирования ветвей и сохранения периваскулярной ткани аутовены.
Полагаем, что важнейшими преимуществами разработанной нами методики эксплантации аутовены являются сохранение периваскулярной ткани и применение ультразвукового гармонического скальпеля. Последнее обстоятельство обеспечивает минимальное термическое воздействие на аутовену и снижает повреждающее воздействие электрокоагуляции, так как температурный спектр такого скальпеля находится в пределах 50–100ºС, а электрокоагуляции — 150–400ºС. При классической методике эксплантации аутовены происходит травмирование ее стенки, что вызывает повреждение структуры эндотелия и, как следствие, нарушение его функциональных свойств [4]. Сохранение окружающей клетчатки вокруг аутовены минимизирует риск возникновения спазма и тем самым устраняет необходимость производить гидравлическую подготовку.
Выводы:
1. В отличие от классического метода эксплантации аутовены предложенная нами малотравматичная технология по морфологическим данным приводит к существенному снижению травматизации сосуда.
2. Для лучшего сохранения нативных свойств аутовены в коронарной позиции при ее эксплантации необходимо использовать ультразвуковой скальпель и сохранять паравазальную клетчатку по всей окружности аутовены.
3. Минимальная травматизация интимы при эксплантации аутовен достигается за счет отказа от увеличения ее диаметра гидравлическим способом.
Библиографическая ссылка
Казачков Е.Л., Семагин А.А., Анненская Е.А., Андриевских И.А. МОРФОЛОГИЧЕСКОЕ ОБОСНОВАНИЕ МАЛОТРАВМАТИЧНОГО СПОСОБА ЭКСПЛАНТАЦИИ АУТОВЕНЫ ДЛЯ КОРОНАРНОГО ШУНТИРОВАНИЯ // Современные проблемы науки и образования. 2016. № 6. ;URL: https://science-education.ru/ru/article/view?id=25817 (дата обращения: 15.05.2026).



