Атеросклероз, как самое распространённое системное заболевание сердечно-сосудистой системы, постоянно находится в сфере внимания патофизиологов и клиницистов. Патогенез этого заболевания в целом достаточно хорошо изучен [10; 13; 14; 21; 27]. Однако, несмотря на то что проведено множество экспериментальных, клинических, психофизиологических и социологических исследований по изучению факторов риска развития атеросклероза, проблемы этиологии заболевания, ранней его диагностики и выявления предикторов развития на донозологической стадии остаются по-прежнему актуальными. Атеросклероз «молодеет» – фиброзные бляшки обнаруживают у лиц 15-20 лет.
Один из парадоксов современной кардиологии состоит в том, что лечить болезни, связанные с атеросклерозом, стали лучше, но количество этих больных увеличивается. Очевидно, что исходя из современных способов профилактики и лечения атеросклероза, остановить пандемию связанных с ним заболеваний (ИБС, гипертония, сахарный диабет II типа, метаболический синдром) в полной мере не удается. Сделать это возможно на основе новых представлений о сущности этих заболеваний и системного подхода к решению данных проблем, исходя из принципов многомерной биологии, позволяющей оценить предрасположенность, механизмы развития заболеваний, различные их проявления, способы лечения и профилактики [23; 24].
Формирование атеросклеротических изменений в сосудистой стенке с возрастом нарастает. Для выявления ранних стадий атеросклероза необходим обширный комплекс клинических, биохимических, физиологических, иммунологических показателей, поскольку, особенно в молодом возрасте, заболевание протекает бессимптомно и без клинических проявлений [3]. В крови пациента определяют содержание маркеров эндотелиальной функции: эндотелин, тромбомодулин, оксид азота, С-реактивный белок, параметры свертывающей системы крови и многие другие показатели. Кроме того, исследуют толщину интимы-медии стенки магистральных сосудов, определяют эластические характеристики артерий [2; 9; 20; 37]. Однако, по сути, перечисленные маркеры эндотелиальных нарушений, артериальная гипертензия, дисфункция надпочечников, печени, вилочковой железы и др. – все это производные системных сдвигов в различных звеньях нейро-метаболического баланса организма, способные проявиться или не проявиться как следствие в развитии атеросклероза (рис. 1).
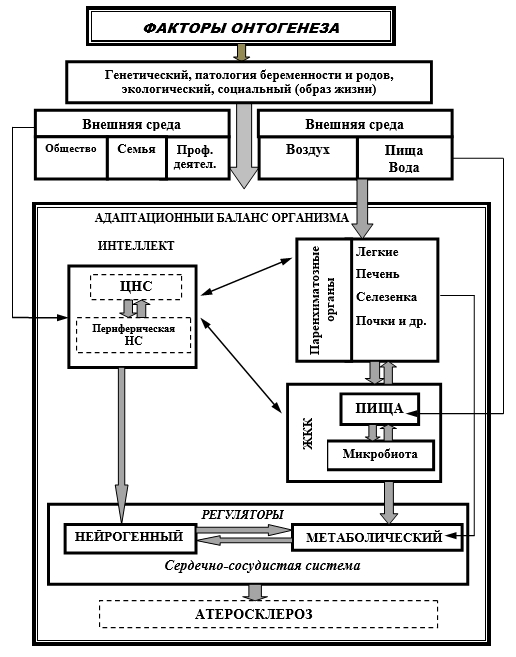
Рис. 1. Звенья онтогенетической цепи развития атеросклероза
Традиционно атеросклероз рассматривают как многофакторное заболевание, относя к факторам риска артериальную гипертензию, гиперхолестеринемию, стресс, курение, возраст, несбалансированное питание, избыточный вес, гиподинамию, а также наследственный фактор.
Схема, приведенная на рис. 1, отражает общеизвестные звенья патогенетической цепи факторов, участвующих в развитии атеросклероза. В каждом индивидуальном случае может доминировать отдельный фактор или, чаще всего, их сочетание. В целом эта схема может быть отнесена ко многим заболеваниям, если заменить конечное звено – «мишень» результирующего действия, т.е. атеросклероз, на другую патологию.
Среди базовых механизмов формирования сосудистых нарушений в организме на первый план можно выделить из них два обобщённых: метаболический и психо-нейрогенный, причем они находятся в теснейшей взаимосвязи целостной системы организма, а точнее надорганизма, включающего собственно организм человека и его микробиоту [23; 26]. В процессе ноосферогенеза (сферы человеческого разума), активно формируемого человеком и ставшего в ХХI веке значимой геологической силой, произошли качественные изменения взаимодействия человека с окружающей природой – системой Земля и микробиотой [6; 11]. Неблагоприятные внешние (вода, почва, воздух, климат) и внутренние (эндоэкология, система регуляции симбиоза, оксидантно-антиоксидантная система) влияния закономерно вызывают изменения вторичного уровня регуляции, связанного с нервной, гормональной, иммунной системами [32]. Эти факторы в процессе ноосферогенеза приводят к развитию заболеваний человека по трем принципиальным направлениям, связанным с нервной системой, инфекциями и различными нарушениями метаболизма.
Ранее была выдвинута теория «терапевтических инфекций»: слабовирулентной и слабопатогенной микрофлоры, сосуществующей в организме хозяина по принципам мутуализма или комменсализма, но способной при наличии дополнительных факторов риска к формированию заболеваний. Подтверждением этого, на наш взгляд, является изменение спектра заболеваний человека с началом эры антибиотиков. В частности, распространение инфаркта миокарда, описанного В.П. Образцовым и Н.Д. Стражеско в 1908 году как казуистика, примерно через сорок лет приобрело характер пандемии, что четко совпало с началом широкого применения антибиотиков, изменивших микробиоту человека и ее регуляторные свойства [25].
Атеросклероз – болезнь, возникающая вследствие постепенно формирующихся нарушений, происходящих в нервной и нервно-эндокринной регуляции паренхиматозных органов и сердечно-сосудистой системы. При рассмотрении этиологии атеросклероза несомненным моментом, на наш взгляд, является необходимость анализа факторов онтогенеза начиная с периода эмбриогенеза.
Наследственный фактор. Генетика – неотъемлемая составляющая здоровья и болезни во всех периодах онтогенеза любого живого существа. При этом следует учитывать, что человек с общебиологических позиций является надорганизмом, включающим геном, метаболом и протеом микроорганизмов эндогенного биоценоза, количество генетического материала которого примерно на два порядка превышает геном человека [26].
Относительно факторов риска атеросклероза известно, что большая их часть в той или иной мере генетически зависима, а это позволяет говорить о наличии наследственной предрасположенности к развитию данного заболевания [10]. Так, например, частый генетический дефект – мутация гена цистатионин-β-синтетаза служит причиной гипергомоцистеинемии, являющейся значимым фактором риска развития атеросклеротических нарушений сосудистого эпителия и тромбоэмболических осложнений [40]. На основе исследований мутации в гене TLR-4 и динамики концентрации циркулирующих противовоспалительных цитокинов и фибриногена предложена рецепторная теория атеросклероза [12].
Последние данные показали, что в период внутриутробного развития нарушения во взаимодействии энзима Ezh2 и гена Six1 могут приводить с возрастом к развитию признаков кардиомиопатии [38]. Предполагается возможность возникновения в эмбриональных прародителях сердечных клеток эпигенетических факторов последующей дизрегуляции и напряжения кардиогомеостаза. Возможно, подобного рода эпигенетические факторы с участием так называемых микро-РНК, состоящих из 19-22 нуклеотидов, играют свою роль в развитии эндотелиальной сосудистой недостаточности и собственно атеросклероза [24].
В целом следует отметить, что генетические факторы в этиологии атеросклероза изучены недостаточно, хотя работы в этом направлении проводились и активно ведутся в настоящее время [8; 17; 38].
Патология беременности и родов. Перинатальный период развития ребёнка, так же как и генетический фактор, накладывает свой очень значимый отпечаток на формирующийся организм. В детской неврологии стало очевидным, что родовые повреждения позвоночника и сочетанные родовые травмы головного и спинного мозга встречаются достаточно часто (иногда даже при кажущемся благополучном исходе родов) и приводят к полиморфным неврологическим нарушениям, которые нередко остаются без внимания [15; 18; 19; 29]. Отмечается, что доминирующим началом во всех проявлениях патологии является гипоксия плода. Многими исследователями показано, что при перинатальных повреждениях шейного отдела позвоночника наиболее страдают позвоночные артерии, из системы которых обеспечивается кровоснабжение бульбарного и спинального дыхательных центров, причем эти нарушения происходят по ишемическому типу. Травматические повреждения в родах патогенетически тесно связаны с патологией дородового периода (крупный плод, токсикозы второй половины беременности и др.) и нередко сопровождаются гипоксией и внутричерепными кровоизлияниями. Следствием этого являются выраженные изменения кровотока в васкуляризуемых вертебробазилярной системой отделах ЦНС. Сдвиги кровоснабжения гипоталамических и лимбико-ретикулярных отделов неизбежно влияют на нейрогуморальный и гормональный статус новорожденных.
Установленная связь перинатальных повреждений позвоночника с развитием различного рода нейрогенно обусловленных заболеваний, разнообразных вегетососудистых пароксизмов, вестибулярных нарушений и др. может проявляться в различные возрастные периоды возникновением локальных или системных нарушений функциональной устойчивости в наиболее слабых звеньях регуляторной цепи паренхиматозных органов и организма в целом.
Метаболизм. До недавнего времени наиболее распространенной концепцией природы атеросклероза являлась теория нарушения обмена липидов, ведущая к гиперхолестеринемии, возникающей вследствие избытка экзогенного холестерина. Однако достоверной связи между количеством потребляемого с пищей холестерина и развитием атеросклероза не выявлено.
Многими предшествующими поколениями ученых различных специальностей была детально изучена роль холестерина и сосудов в развитии атеросклероза. При этом по мере углубления наших знаний произошла подмена понятий: борьбу с атеросклерозом заменили борьбой с холестерином. Однако, анализируя метаболические пути обмена холестерина в организме (рис. 2), следует признать, что печень синтезирует холестерина в 2 раза больше, чем поступает его с пищей и синтезируется микробиотой. Из 150 граммов содержащегося в организме холестерина в крови находится только 8 граммов [32]. Если же холестерин не метаболизируется по основным метаболическим путям, он откладывается в сосудах в виде атеросклеротических бляшек, вызывая вторичные изменения со стороны сердца, сосудов и других органов, которые усугубляются развитием в них оксидативного стресса [22-24]. Таким образом, причинами гиперхолестеринемии являются многие факторы: недостаточная востребованность холестерина клетками тканей, метаболические нарушения внутренних органов, гетеро- и гомозиготные дефекты ЛНП-рецептора, патология печени, дисбиоз, алиментарные факторы.
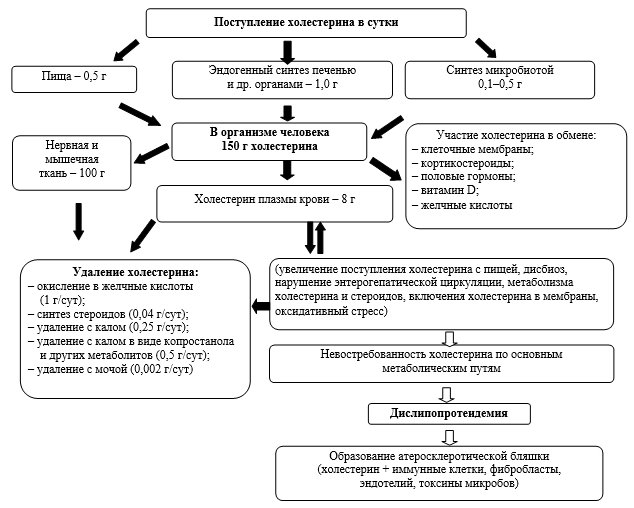
Рис. 2. Метаболические пути холестерина в организме человека (приведено по Ткаченко Е.И., Орешко Л.С., 2013)
Следует отметить, что печень является основным органом обмена холестерина. Она использует экзогенные липиды, доставленные ремнантами хиломикронов для различных целей, в том числе синтеза липопротеидов различной плотности. Печень осуществляет катаболизм холестерина, так как ткани других органов не имеют соответствующих ферментных систем. При этом процессы обмена холестерина могут нарушаться за счет генетических или приобретенных дефектов систем транспорта холестерина, нарушений синтеза холестерина, ферментов, апо-белков, белков-транспортеров, нарушений энтерогепатической циркуляции желчи.
Сдвиг в сторону преобладания прямого транспорта холестерина в клетку с помощью липопротеидов низкой плотности способствует нарушению баланса и накоплению холестерина в интиме стенок артерий.
Атеросклерозу часто предшествует метаболический синдром, проявляющийся комплексом патогенетически взаимосвязанных нарушений липидного, углеводного, пуринового обменов, инсулинорезистентности и артериальной гипертонии. Установлены врожденные и приобретенные причины метаболического синдрома. К врожденным причинам относят наследственную предрасположенность, низкий уровень функциональных резервов, гипертрофию адипоцитов, менопаузу, изменение количества и качества инсулиновых рецепторов, нарушение транспорта глюкозы, снижение активности энзимов. Среди приобретенных причин выделяют: нарушение микробиоты и пищевого поведения, изменение качественного состава пищи и воды, мутации в генах, кодирующих различные виды обмена и физиологические функции, а также вредные привычки, стрессы, экологические и производственные факторы, в том числе социально-психологические [4; 28; 31; 33; 35]. Относительно последних показательным примером могут служить данные В.А. Чепурнова и соавт.: «Наибольший прирост распространенности доклинического атеросклероза у работников нефтеперерабатывающего предприятия происходил в очень молодом возрасте – от работников 21…30 лет к группе лиц 31…40 лет, в среднем на 10 лет раньше, чем в других популяционных исследованиях. У лиц старше 60 лет распространенность бляшек составляла более 90%, что превышает величину этого показателя, опубликованного в литературе» [28].
Пища и микроэлементы. Составу пищи и режимам питания в аспекте развития атеросклероза посвящено великое множество исследований, поэтому останавливаться на общеизвестных истинах в данной работе не имеет смысла. Следует подчеркнуть лишь важную и недостаточно изученную роль в сосудистой патологии входящих в пищевые продукты микроэлементов. К жизненно необходимым относят Fе, J, Zn, F, Sе, Со, Мо, Сr, Ni, V, Мn, Аs, Сu, Si, Li. Доля микроэлементов в организме составляет 10-3-10-5%. Необходимость баланса микроэлементов в организме, начиная с его нахождения в утробе матери, общепризнанна [1; 36]. Тем не менее круг работ, посвященных дифференциальной оценке роли того или иного элемента в развитии атеросклероза и артериальной гипертензии, весьма ограничен. К примеру, существует мнение, что недостаток кремния (Si) в питьевой воде и пищевых продуктах может являться этиологическим фактором в развитии атеросклероза. Известно, что его содержание в стенках артерий новорожденных составляет порядка 0,007%, а у сорокалетних – только 0,0025%, т.е. почти в три раза меньше, при этом в ряде других органов и тканей с возрастом его содержание повышается [7]. Тем не менее глубоких исследований значимости кремния в развитии атеросклероза в доступной литературе авторами не обнаружено. То же самое можно сказать о многих других микроэлементах.
Адаптационный баланс. Заболевание во многом обусловлено образом и условиями жизни современного человека, психоэмоциональными и профессиональными факторами, которые отрицательно действуют на функции нервной, сердечно-сосудистой, эндокринной и пищеварительной систем, приводя к неадекватным метаболическим реакциям и, как следствие, нарушениям трофики сосудистого русла.
Адаптивный гомеостаз биосистемы можно рассматривать как результирующий продукт всех экзогенных и эндогенных факторов, обеспечивающих жизнедеятельность организма хозяина и его симбионтов – специфической бактериальной микрофлоры, содержащейся в желудочно-кишечном тракте. Энтеральная среда выполняет функцию обеспечения химического гомеостаза, срыв которого под воздействием внешних факторов может происходить вследствие ответных нейрогенных реакций (стресс) и системных дисфункций микробиоты и паренхиматозных органов, приводя к развитию той или иной патологии [22; 23; 35]. В аспекте этиологии атеросклероза следует подчеркнуть, что в его развитии важную роль играет кишечная микрофлора, значимость которой отмечал еще И.И. Мечников: «…кишечная стенка постоянно всасывает фенолы, …яды гнилостных бактерий кишечного канала легко всасываются через толстые кишки» [30, с. 633]. Попадая в кровеносное русло, эти «кишечные яды» могут формировать патологию внутренних органов как собственным воздействием, так и через опосредованные ими продукты нарушенного метаболизма (гомоцистеин, инсулин и др.), которые деструктурируют сосудистый эндотелий, формируя его атеросклеротические изменения [30; 39].
Исходя из концепции организма человека как надорганизма (хозяин + микробиота), очевидна роль в рассматриваемых заболеваниях различных микроорганизмов и эндогенного микробиоценоза, находящихся в динамичных кооперативных взаимоотношениях. В частности, установлено, что в развитии атеросклероза принимают участие более 50 видов микроорганизмов (хламидии, хеликобактер, микоплаза, вирусы Коксаки, гепатита С, цитомегаловирусы и другие), выявленные при исследовании атером путем секвестрирования генов 16Sр ДНК и флуоресцентной гибридизации in situ [5]. Установлена способность ряда этих микроорганизмов размножаться в клетках эндотелия, макрофагах, найдены фрагменты бактериальных биоплёнок на бляшках. В частности, показано индуцирующее действие липотейховых кислот грамположительных бактерий, белков теплового шока и белка р70, взаимодействующих с «Толл-лайк»-рецепторами-сенсорами, запускающими ответные защитные реакции: секрецию цитокинов, хемокинов, дефенсинов [5]. При мутации в гене TLR-4 и утрате рецептора TLR-4 снижается концентрация циркулирующих провоспалительных цитокинов и фибриногена, а следовательно, и риск атерогенеза. Эти данные позволили сформулировать рецепторную теорию атеросклероза как побочного эффекта взаимодействия TLR-4 с их экзогенными и эндогенными лигандами на фоне дисбиоза и нарушений метаболизма холестерина [12].
Следует особо подчеркнуть, что при всём многообразии теоретических подходов и вышеперечисленных этиологических факторов адаптационный баланс организма в онтогенезе необходимо рассматривать в совокупности метаболических, психологических и интегративных церебральных взаимодействий, лежащих в основе системных механизмов, ведущих к формированию сердечно-сосудистых заболеваний [16; 34].
Заключение
Системный анализ этиологии атеросклероза в аспекте индивидуального онтогенеза открывает возможность формирования целостной патофизиологической картины развития заболевания с учётом взаимосвязей многочисленных индивидуальных факторов риска и данных о микробиоме, геноме, протеоме и метаболоме больных атеросклерозом. Можно ожидать, что такой системный подход к атеросклерозу, а также к тесно связанным с этим заболеванием метаболическому синдрому, ишемической болезни сердца и гипертонии позволит достичь более эффективных результатов в функциональном управлении единой симбиотической системой «макроорганизм – микробиота» и, следовательно, в профилактике и лечении сердечно-сосудистой патологии.
Библиографическая ссылка
Ткаченко Е.И., Петраш В.В., Орешко Л.С., Ильина Л.В., Литаева М.П. ФАКТОРЫ РИСКА РАЗВИТИЯ АТЕРОСКЛЕРОЗА В ОНТОГЕНЕЗЕ // Современные проблемы науки и образования. 2016. № 6. ;URL: https://science-education.ru/ru/article/view?id=25815 (дата обращения: 30.03.2026).



