Среди «обструктивных уропатии» у детей наиболее часто встречается пузырно – мочеточниковый рефлюкс (ПМР). ПМР представляет собой обратный заброс мочи из мочевого пузыря в мочеточник и чашечно-лоханочную систему почки, вследствие недоразвития замыкательного механизма уретеровезикального соустья [1]. Наличие ПМР приводит к нарушению оттока мочи из верхних мочевых путей, что создаёт условия для частых обострений вторичного пиелонефрита, истончения почечной паренхимы с развитием рефлюкс – уропатии, которая приводит к вторичной артериальной гипертензии и хронической болезни почек [1]. По данным урологического отделения педиатрического корпуса СОКБ им. В.Д. Середавина, в последние годы увеличивается количество детей с ПМР, и составляет 20 – 25% от общего количества пролеченных детей. Это связано с постоянно возрастающей врождённой патологией мочевыделительной системы у детей, а также с хорошей пре- и постнатальной диагностикой [4]. У детей с длительной лейкоцитурией в общем анализе мочи и при отсутствии другой симптоматики, ПМР выявляется в 17 – 35% случаев [2].
В настоящее время предложено много различных методов коррекции ПМР: консервативные, эндоскопические и оперативные. Выбор метода лечения при ПМР зависит от многих факторов, таких как механизм развития ПМР, возраст ребёнка, а также сопутствующей нейрогенной дисфункции мочевого пузыря [3]. Большую роль в выборе метода лечения имеет картина, полученная при проведении цистоскопии, которая позволяет оценить анатомию устьев мочеточника, а также состояние слизистой оболочки мочевого пузыря [5,6,7].
С 1981 года стала активно применяться эндоскопическая коррекция ПМР с помощью синтетических протезов. Предложенный метод лечения отличался своей малоинвазивностью и относительной технической простотой выполнения. За 35 лет предложено большое количество уроимплантов для выполнения эндоскопической коррекции устья мочеточника. В начале использовались препараты животного происхождения (коллаген, плазменный сгусток, фибробласты), затем стали появляться синтетические уроимпланты (ДАММ+, Уродекс, Врудекс). Несмотря на большое разнообразие уроимплантов, в настоящее время нет «золотого стандарта» в выборе одного из них. Ни один из препаратов не отвечает необходимым условиям, таким как высокая устойчивость, отсутствие аллергической реакции и воспаления, биосовместимость и отсутствие миграции [1,5,8,9]. С 2010 года на базе 13ДГКБ им. Н.Ф. Филатова стали применять новое вещество синтетического происхождения Vantris, который представляет собой макрочастицы кополимера полиакрилового поливинилового спирта, растворенного в 40% р-ре глицерола [5,8,9]. Опираясь на положительный опыт применения препарата Vantris нашими коллегами, с 2012 года на базе урологического отделения ПК СОКБ им. В.Д. Середавина мы стали активно внедрять его для проведения эндоскопической коррекции ПМР.
Цель исследования: провести сравнительный анализ эндоскопического лечения пузырно – мочеточникового рефлюкса у детей с использованием препарата Vantris на базе урологического отделения педиатрического отделения СОКБ им. В.Д. Середавина.
Материалы и методы. С 2012-2016 гг., в отделении урологии ПК (заведующий отделением к.м.н. Терёхин С.С.) пролечено 1200 детей с диагнозом пузырно – мочеточниковый рефлюкс. Диагноз поставлен на основании проведения микционной цистографии. Эндоскопическая коррекция рефлюкса препаратом Vantris выполнена 160 детям. Мальчиков 96 (60%), девочек – 64 (40 %). Односторонний рефлюкс выявлен у 128 детей (80%), двусторонний рефлюкс у 32 детей (20%). У 12 детей (10%) отмечался рефлюкс в обе половины удвоенной почки, при полном удвоении. Первичная эндоскопическая коррекция при ПМР выполнена у 120 детей (75%), у 30 детей (19%) эндоскопическая коррекция выполнена после предшествующей эндопластики коллагеном, у 10 детей (6%) эндоскопическая коррекция выполнена после предшествующей внепузырной реимплантации мочеточника. Контрольную группу составили дети (N – 100), которым выполнена эндоскопическая коррекция коллагеном, находившиеся на стационарном лечении в период с 2005 – 2010 гг. Возраст детей составил от 6 месяцев до 14 лет. Средний возраст детей 4 года. Детям с ПМР 1 степени эндопластика не выполнялась. ПМР 2 степени отмечен у 35 детей, ПМР 3 степени – 100 детей, ПМР 4 степени – 25 детей. При ПМР 5 степени эндоскопическая коррекция не выполнялась. Для эндоскопической коррекции ПМР нами были использованы детские цистоуретроскопы фирмы Wolf (Германия) и Storz (Германия) № 8,5 – 17 Ch. Препарат Vantris вводился через иглу № 21 – 23G по методике STING (Subureteral Transurethral Injection), HIT (Hydrodistention Implantation Technique), 2HIT. Методику HIT, 2HIT мы использовали при рефлюксах 4 степени, при остальных степенях рефлюкса предпочтение отдавалось методике STIHG. При полном удвоении почки мы использовали методику STING, с предшествующей ретроградной катетеризацией одного из устьев мочеточника катетериками Ch №3,4. Ретроградная катетеризация устья мочеточника позволяла лучше визуализировать ход мочеточника, для более точного эндоскопического введения болюса. Всем детям однократно вводилось не более 1,0 мл препарата Vantris (в среднем 0,4 – 0,7 мл), что объясняется способностью препарата увеличивать свой объём после введения. В случае введения коллагена, мы вводили одномоментно до 2,0 мл препарата. В случае отсутствия замыкания устья после первого вкола иглы, выполнялся второй вкол иглы, для «поднятия» и замыкания устья (2HIT). Операции выполнялись под общим обезболиванием, с использованием комбинированного интубационного наркоза. Предпочтение отдавалось препаратам с наименьшим нефротоксическим действием (севофлуран, фентанил, пропофол). При проведении вводной анестезии предпочтение отдавалось севофлурану, для детей до 3 лет, детям старшего возраста использовался пропофол. Интраоперационная анальгезия проводилась фентанилом. Данное анестезиологическое пособие приводило к минимальному риску осложнений во время наркоза. Мочевой пузырь в послеоперационном не дренировался. В послеоперационном периоде все дети получали антибактериальную терапию (цефтриаксон, амикацин, нитрофураны), в сроки 5 – 14 дней. Общий анализ мочи всем детям взят на 5 сутки, через 1 и 3 месяца после операции, для оценки купирования инфекции мочевых путей. Ультразвуковое исследование выполнено всем детям на следующий день после введения препарата Vantris и коллаген, через 7 суток, 1 и 3 месяца. Контрольное урологическое обследование для оценки результатов эндоскопической коррекции, заключающееся в проведении микционной цистографии и экскреторной урографии, выполнено всем детям через 6-8 месяцев после операции.
Результаты. В раннем послеоперационном периоде осложнений в виде аллергической реакции, гипертермии, дизурии зафиксировано не было. У двух детей отмечена однократная макрогематурия, в течение первых суток после введения препарата, самостоятельно купированная. Изменения в анализах мочи в виде стойкой лейкоцитурии, бактериурии купировались у всех детей через 1 месяц после операции. У 10 детей с 4 степенью ПМР через 1 месяц после введения препарата Vantris по данным УЗИ появились признаки нарастающей обструкции мочевых путей на стороне введения (расширение чашечно-лоханочной системы и мочеточника более, чем на 30% от исходных размеров). Сразу после введения препарата изменения по УЗИ нами не отмечены. У всех детей размеры ЧЛС по данным УЗИ не отличались от исходного уровня до введения препарата. В случае введения коллагена признаков нарастающей обструкции мочевых путей на стороне введения нами отмечено не было. Обострение вторичного пиелонефрита в послеоперационном периоде у детей не отмечено. Через 6 – 8 месяцев после операции все дети обследованы в отделении урологии педиатрического корпуса СОКБ им. В.Д. Середавина. Контрольное обследование заключалось в проведении экскреторной урографии, микционной цистографии, качественных и количественных анализов мочи. По результатам микционной цистографии выздоровление после введения препарата Vantris отмечалось у 136 детей (85%). Рецидив ПМР выявлен у 8 детей (5%). Степень рефлюкса при рецидиве у всех детей была ниже исходной, что позволило нам выполнить повторную эндопластику препаратом Vantris до полного выздоровления. По данным экскреторной урографии у 10 детей (6%) выявлен обструктивный мегауретер на стороне введения Vantris, при отсутствии рефлюкса. У данных детей эндопластика выполнялась по методике 2HIT, либо STING. Нарастание обструкции протекало бессимптомно (отсутствие почечной колики, обострение вторичного пиелонефрита, изменения в анализах мочи), было отмечено нарастание расширения ЧЛС и мочеточника по данным УЗИ, начиная с 1 месяца после введения препарата. У 2 детей нарастание обструкции после введения Vantris нами отмечено через 1 и 3 года, при отсутствии изменений по результатам проведённого контрольного рентгенурологического обследования через 6 месяцев после операции. Всем 10 детям с обструктивным мегауретером было решено выполнить уретероцистонеоанастомоз по Cohen. Временное эндоскопическое стентирование мочеточника нами не применялось, учитывая высокую устойчивость препарата. Во всех случаях терминальный отдел мочеточника иссечённый во время операции отправлялся на гистологическое исследование, по результатам которого отмечалось отсутствие нервно-мышечных элементов в стенке мочеточника, фиброз и атрофия подслизистого слоя, что свидетельствовало об отсутствии сократительной способности и дисплазии терминального отдела мочеточника. Таким образом, в этих случаях у детей подтверждался диагноз «рефлюксирующий мегауретер», или «рефлюкс – стеноз». После введения препарата Vantris рефлюксирующий компонент устранялся (выздоровление по ПМР), а мочеточник, лишённый нервно – мышечного аппарата и как следствие сократительной способности, с дополнительной нагрузкой в виде болюса не справлялся, что приводило к образованию обструктивного мегауретера. В дальнейшем, для предупреждения развития обструкции, детям с ПМР 4 степени мы выполняли перед операцией ультразвуковое исследование с лазиксной нагрузкой на уретральном дренаже, для исключения «рефлюксирующего мегауретера». Уретральный дренаж устанавливался ребёнку накануне проведения УЗИ, для исключения нейрогенного мочевого пузыря. Доза лазикса для проведения пробы рассчитывалась из расчёта 0,5 мг/кг массы тела ребёнка. Исследование выполнялось через 20, 40 и 60 минут после введения лазикса. Расширение чашечно – лоханочной системы и мочеточника на 30% и более от исходного размера ЧЛС через 60 минут после введения лазикса нами расценивалось, как наличие у ребёнка «рефлюксирующего мегауретера» и являлось противопоказанием к эндопластике. У данных детей мы отдавали предпочтение уретероцистонеоанастомозу по методике Cohen (рисунок).
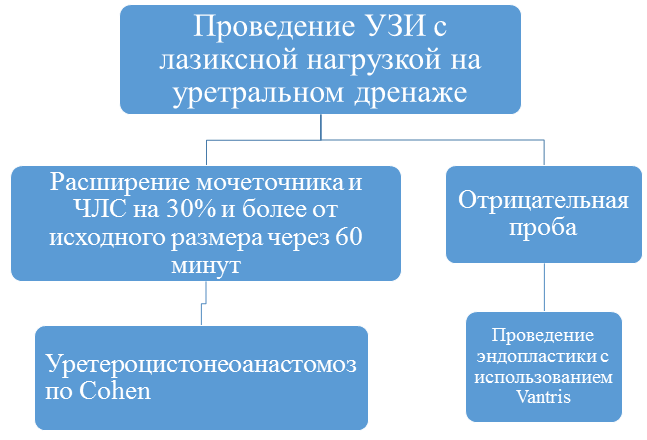
Дооперационная тактика при ПМР с использованием препарата Vantris
Среди детей контрольной группы, которым выполнена эндопластика с использованием коллагена выздоровление отмечено у 65 детей (65%). Рецидивы – у 35 детей (35%). Развитие обструктивного мегауретера после введения коллагена нами отмечено не было. В дальнейшем дети с выздоровлением по ПМР наблюдаются амбулаторно врачом – детским урологом – андрологом поликлиники, с ультразвуковым исследованием мочевыделительной системы, с периодичностью 1 раз в 6 месяцев. Рентгенурологическое обследование проводится 1 раз в 2 – 3 года. Все дети, у которых эндоскопическая коррекция выполнялась препаратом Vantris, находятся на диспансерном учёте. Мы считаем целесообразным наблюдать таких детей до 15 лет, учитывая относительно небольшой опыт применения препарата во всём мире и отсутствие отдалённых результатов применения.
Выводы:
1. Эндоскопическая коррекция ПМР препаратом Vantris позволила добиться полного выздоровления у 85% детей. По сравнению с коллагеном, препарат Vantris имеет ряд преимуществ, таких как высокая устойчивость и отсутствие миграции, что обеспечивает длительный антирефлюксный эффект.
2. Развитие обструктивного мегауретера после введения препарата Vantris является следствием наличия у ребёнка рефлюксирующего мегауретера, не диагностированного до эндопластики. Для предупреждения развития обструкции после эндопластики, детям с ПМР 4,5 степени до введения препарата следует проводить ультразвуковое исследование с лазиксной нагрузкой на уретральном дренаже до введения препарата. Учитывая высокую стойкость препарата Vantris, детям раннего возраста (до 1 – 2 лет) предпочтительно проводить эндоскопическую коррекцию ПМР с использованием менее стойких препаратов (коллаген). Это оправдано, с учётом «дозревания» уретеровезикального сегмента у детей раннего возраста.
3. Отдалённые результаты эндоскопической коррекции с использованием препарата Vantris мало изучены. Учитывая наблюдение за развитием обструктивного мегауретера, спустя 3 года после проведённой эндоскопической коррекции, дети должны находится на диспансерном наблюдении в течение длительного времени.
Библиографическая ссылка
Гасанов Д.А., Барская М.А., Терёхин С.С., Мелкумова Л.Г., Бастраков А.Н., Алексеева И.Н., Завьялкин В.А., Смолин С.Е., Зеброва Т.А. ПОДХОД К ЭНДОСКОПИЧЕСКОМУ ЛЕЧЕНИЮ ПУЗЫРНО – МОЧЕТОЧНИКОВОГО РЕФЛЮКСА У ДЕТЕЙ // Современные проблемы науки и образования. 2016. № 6. ;URL: https://science-education.ru/ru/article/view?id=25724 (дата обращения: 30.03.2026).



