Церебральные аневризмы являются одной из основных причин нетравматического субарахноидального кровоизлияния (САК). Чаще других носителем церебральных аневризм оказывается средняя мозговая артерия (СМА) [4; 6]. Согласно данным разных исследователей, частота встречаемости аневризм СМА (АСМА) колеблется в диапазоне 18-43% от всех внутричерепных аневризм [13], а по данным аутопсий, достигает 32%.
Важную роль в формировании аневризм играет гемодинамический удар, возникающий при повышении артериального давления [2]. Согласно данным Забродской Ю.М. (1996), большую значимость в патогенезе аневризматической болезни приобретают микроскопические изменения сосудистой стенки – происходит гибель гладкомышечных элементов в области развилки сосуда, а затем фиброз средней оболочки сосуда, при этом изменения располагаются не только в области самой развилки, но также распространяются на устья исходящих из бифуркации сосудов [1], что позволяет объяснить преимущественное расположение аневризм (80-90%) в области развилки основного ствола СМА, а также нередко встречающиеся т.н. фузиформноподобные аневризмы данной локализации, т.е. аневризмы с вовлечением артериальных ветвей в шейку и пришеечную область [6].
У больных с аневризмами СМА более отчётлива зависимость от наследственного фактора, поэтому у их родственников следует ожидать более высокий риск кровоизлияния.
В настоящий момент в лечении больных с аневризмами церебральных сосудов применяют два основных метода: микрохирургический, то есть выделение и наложение металлического клипса на шейку аневризмы, и эндоваскулярный – пункция бедренной артерии, катетеризация аневризмы и внутрисосудистое выключение аневризмы из кровотока. Давно ведется спор между приверженцами обоих методов. Сторонники клипирования указывают на большую радикальность выключения аневризмы из кровотока и возможность выполнения реконструктивного клипирования при сложной геометрии аневризматического мешка; приверженцы эндоваскулярного метода указывают на малую инвазивность процедуры, возможность окклюзии аневризмы у больных, находящихся в тяжелом состоянии (H&H IV –V) и другие факторы.
Аневризмы СМА традиционно считаются более подходящими для открытой операции вследствие анатомических особенностей (сравнительно поверхностная топография СМА, благоприятная для внутричерепного доступа, отсутствие выраженных коллатералей, повышающее эффективность временного клипирования), а также частой неблагоприятной геометрии аневризм данной локализации: широкая шейка, вовлечение в состав мешка аневризмы одного или более М2 сегментов. Эти обстоятельства препятствуют тотальной эмболизации и обусловливают высокий риск ишемических осложнений [7]. По мнению Rodriguez-Hernandez A. (2013), J.M.C. Van Dijk (2011) и многих др. исследователей, микрохирургическое вмешательство продолжает оставаться операцией выбора и на современном этапе [5; 14].
Следует отметить, что некоторая неудовлетворённость в достижении радикальной внутрисосудистой окклюзии аневризм СМА имела место на этапе развития и отработки методики эмболизации спиралями. C 2003 года стали доступны интракраниальные саморасширяющиеся стенты, которые открывали новые возможности для более эффективного и безопасного лечения «сложных» церебральных аневризм, однако предпочтение отдавалось другим локализациям. Напротив, в последних публикациях возрастает интерес к использованию стент-ассистенции в лечении аневризм СМА. Согласно данным разных авторов применение стентов позволяет добиться радикальности, сопоставимой с микрохирургическим клипированием, при этом укорачивается послеоперационный период и уменьшаются сроки пребывания пациента в стационаре [11]. Стент-ассистенция все чаще применяется в геморрагическом периоде (JohnsonA.K. et al., 2013), однако данная методика имеет ряд ограничений в связи с необходимостью применения двойной дезагрегантной терапии, которая повышает риск развития осложнений [8].
Таким образом, представленные литературные данные указывают, что в повышении эффективности лечения АСМА стоят задачи, общие для всех аневризм, однако на их решение существенно влияет и данная локализация. Относительно поверхностное расположение СМА, слабый коллатеральный кровоток, всё же не устраняют недостатки открытого оперативного вмешательства. «Фузиформноподобный» характер и другие морфологические особенности затрудняют радикальную эмболизацию АСМА, однако использование наиболее современного внутрисосудистого инструментария, ассистирующих методик могло бы повысить радикальность малоинвазивной внутрисосудистой операции и способствовать лучшему функциональному результату.
Материал и методы. В настоящее исследование были включены 163 больных с 210 аневризмами, из них 174 аневризмы средней мозговой артерии, оперированных в ФГБУ «Российский научно-исследовательский нейрохирургический институт им. проф. А.Л. Поленова» с января 2010 по март 2014 г. включительно. Средний возраст больных составил 48,8±0,9 года, соотношение мужчин и женщин – 1:2. Заболевание проявило себя кровоизлиянием у 90 (55,2%) пациентов, другими неврологическими симптомами – у 24 (14,8%). С множественными аневризмами было 38 (23,3%) пациентов. Из них у 31 выявлено 2 аневризмы, у 5 - 3; 4 аневризмы встретились в 2 случаях. У 8 пациентов аневризмы располагались на СМА с одной стороны, зеркальные аневризмы СМА были у 3 пациентов, сочетание аневризмы СМА с аневризмой другой локализации у 27 пациентов.
На основании дооперационной ангиографической картины, анализа геометрии аневризм мы разделили их на мешотчатые, фузиформные (веретенообразные) и «фузиформноподобные» аневризмы (рис. 1).
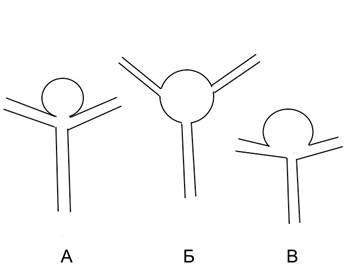
Рис. 1. Виды аневризм: А — мешотчатая, Б — фузиформная, В — фузиформноподобная
К фузиформноподобным мы отнесли те случаи, когда ветви СМА были вовлечены в структуру шейки или отходили непосредственно от мешка аневризмы, что снижало радикальность операции и повышало риски развития как интра-, так и послеоперационных осложнений (рис. 2).
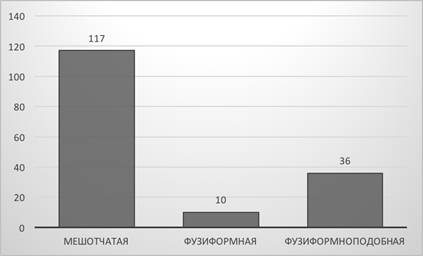
Рис. 2. Распределение аневризм по типу строения
В геморрагическом периоде оперировано 11 (6,7%) больных, в постгеморрагическом – 152 (93,3%). Поздние операции были обусловлены, вероятно, несвоевременным направлением больных в клинику института.
Для проведения сравнительного анализа все пациенты были разделены на две группы: в первую группу вошли пациенты, перенесшие микрохирургическое вмешательство – 71 пациент, во вторую – эндоваскулярное – 92 пациента. Эмболизация аневризм осуществлялась при помощи отделяемых микроспиралей, а в ряде случаев с помощью ассистирующих и потокперенаправляющих стентов. По степени радикальности выделяли тотально-субтотальную эмболизацию – 95-100%, частичную - <95% и попытку вмешательства – 0%, функциональный исход оценивали на момент выписки из стационара по шкале исходов Глазго (GOS).
Результаты
Семидесяти одному больному была выполнена 71 микрохирургическая операция: клипирование аневризмы проведено 58 больным; укрепление стенки аневризмы (окутывание фрагментом мышцы) – 4; клипирование, дополненное окутыванием аневризмы мышцей, выполнено 9 пациентам. Хороший результат (OGS 5–4) был достигнут у 81,7% больных. Неудовлетворительный и плохой результат (OGS 1-2) отмечен у 2,8% (рис. 3).
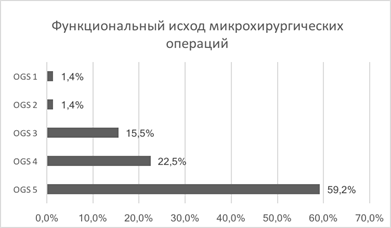
Рис. 3. Функциональный исход микрохирургических операций
При сравнении результатов хирургического лечения в зависимости от типа строения аневризмы было выявлено ухудшение результатов лечения после операций на фузиформных аневризмах. Частота благоприятных исходов (OGS IV-V) при фузиформном строении аневризмы была ниже (66,7%), чем при аневризмах других типов (80-84%). Различие достоверно (p<0,001).
Как и при анализе общих результатов лечения, в оценке эффективности только открытых оперативных вмешательств существенное значение придавали не только клинико-неврологическому исходу, но и определению степени радикальности выключения аневризмы из кровообращения.
Тотального выключения из кровообращения (> 90%) микро-, небольших и больших аневризм достигали чаще, чем гигантских (р=0,02), тогда как попытка клипирования или окутывание аневризмы мышцей (радикальность=0) встречалась чаще при гигантском размере аневризмы. Достоверной зависимости степени радикальности от возраста больного, типа строения аневризмы выявлено не было.
Интраоперационные геморрагические осложнения имели место у 2 (2,8%) больных. Осложнения протекали бессимптомно, неврологическая симптоматика в послеоперационном периоде не наросла, оба больных выписаны с хорошим (OGS V) результатом. Ишемических осложнений отмечено не было. Ретракционная травма была заподозрена, по данным КТ, у 10 (14%) больных. Убедительных неврологических проявлений ретракционной травмы в наших наблюдениях отмечено не было. Послеоперационные эпи- и субдуральные гематомы были выявлены у 2 (2,8%) больных в результате контрольного КТ-исследования. Оба больных были реоперированы, в одном случае пациент умер (OGS I), во втором в последующем произошел частичный регресс неврологической симптоматики (OGS III). Послеоперационные менингиты выявлены у 2 (3%) больных. Послеоперационная летальность в группе составила 1,4%.
Внутрисосудистым методом были оперированы 92 пациента, которым было выполнено 96 внутрисосудистых операций. Хороший исход лечения (OGS 5–4) к моменту выписки имели 79,3% больных. Удовлетворительный (OGS 3) результат лечения был достигнут у 11% больных. Неудовлетворительный результат (OGS1–2) отмечен у 9,7% больных с летальностью 5,4% (рис. 4).
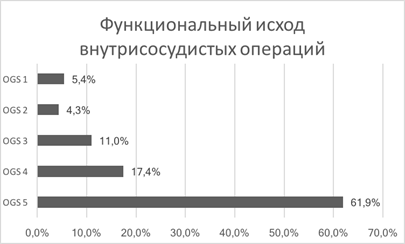
Рис. 4. Функциональный исход внутрисосудистых операций
Нами была выявлена определённая зависимость между функциональным исходом лечения и типом строения мешка аневризм. Неудовлетворительный функциональный исход встречался достоверно чаще после операций на аневризмах с фузиформноподобным типом строения - частота неблагоприятных исходов (OGS I-II) (21%) была выше, чем при операциях на мешотчатых и фузиформных аневризмах (p<0,01). Частота благоприятных исходов (OGS IV-V) была выше у больных с мешотчатыми и фузиформными аневризмами (86,3% и 100% соответственно), чем у больных с фузиформноподобными аневризмами (63,5%). Различие статистически достоверно (p<0,05).
При анализе параметра радикальности достоверной зависимости от типа строения аневризмы выявлено не было.
С использованием стент-ассистенции было прооперировано 16 человек. Радикальность лечения таких аневризм составила 100%, что превысило радикальность лечения без применения стент-ассистенции (84,2%), причем данное различие было достоверным (р<0,05).
Частота хороших и отличных функциональных исходов (OGS 4-5) в группе фузиформных и фузиформноподобных аневризм составила 100% и 63,6% соответственно.
Интраоперационные осложнения имели место у 10 (11%) больных. Ишемические осложнения отмечены у 6 больных (54,5%), геморрагические интраоперационные осложнения - у 4 пациентов (45,5%). К летальному исходу осложнения привели у 3 (21%) больных, к инвалидизации – у 2 (14%).
Среди ишемических интраоперационных осложнений наиболее часто наблюдали миграцию микроспирали из аневризмы в просвет сосуда (50%) и тромбоз несущего сосуда (33,3%). Среди геморрагических осложнений наиболее часто отмечен интраоперационный разрыв аневризмы, у 1 пациента наблюдалось повреждение сосудистой стенки микроинструментом с последующим развитием массивного базального САК. Послеоперационные осложнения отмечены у 14% больных. Повторные кровоизлияния в послеоперационном периоде возникли у 2 больных, при этом исходы были неудовлетворительны (OGS I). Нецеребральные осложнения наблюдали у 7,6% больных. Общая летальность составила 5,4%.
При сравнительном анализе исходов после хирургического вмешательства нами было установлено, что неудовлетворительные результаты лечения (OGS1-2) достоверно чаще встречались у больных, перенесших эндоваскулярную операцию, чем у больных после микрохирургического вмешательства (24% и 0% соответственно), при этом наиболее часто неудовлетворительные исходы (OGS 1-2) были отмечены у группы больных с наиболее сложными, фузиформноподобными аневризмами, а частота хороших и отличных результатов (OGS 4-5) для фузиформноподобных аневризм была выше после микрохирургического вмешательства (80%), чем после эндоваскулярной операции (63,2%).
При сравнении параметра радикальности окклюзии аневризмы в зависимости от типа строения было выявлено, что в отношении фузиформноподобных аневризм показатель радикальности >90% оказался сопоставим для групп микрохирургического и эндоваскулярного вмешательства (86,7% и 84,2% соответственно)
Отдаленные результаты отслеживались у больных в сроки 6-12 месяцев при помощи селективной церебральной ангиографии. Катамнез был отслежен у 69 пациентов (42,3%), из которых 27 пациентов перенесли микрохирургическое вмешательство, 42 - эндоваскулярное. Особое внимание уделялось реканализации и/или росту аневризмы. Так, из 27 пациентов, перенесших микрохирургическую операцию, у 25 (92,6%) реканализации и роста отмечено не было, в двух случаях (7,4%) был отмечен рост аневризмы. Среди пациентов, перенесших внутрисосудистую операцию, реканализация аневризмы была отмечена у 2 пациентов (4,8%), тогда как дальнейший рост аневризмы был выявлен у 5 пациентов (11,9%). Нами была выявлена зависимость частоты роста или реканализации аневризмы от типа строения аневризматического мешка. Так, наиболее часто реканализация и/или рост аневризмы отмечались у пациентов с т.н. фузиформноподобным типом строения аневризмы (55,5%).
Повторные операции по поводу роста и/или реканализации были выполнены 4 (5,9%) пациентам, из них повторная эмболизация микроспиралями была выполнена в 1 случае (25%), в трех случаях (75%) использована реконструкция области развилки СМА с помощью ассистирующих стентов с последующей тотальной эмболизацией заполняющейся части микроспиралями с хорошим функциональным исходом.
Обсуждение. Согласно данным Kim B.M. (2010), расположение устьев ветвей основного ствола СМА в области шейки имеет место у 40,5%, т.е. практически у половины пациентов аневризмы СМА имеют т.н. фузиформноподобное строение, что усложняет операцию и повышает риски развития осложнений, однако хороший клинический результат (OGS 4–5) после внутрисосудистых операций на СМА удается получить у 74-92,5% больных, что сопоставимо с соответствующим показателем для микрохирургических операций (69–95%) [9; 10; 12; 15]. Согласно данным Brinjikji W. с соавт (2011), у больных, оперированных микрохирургически по поводу аневризм СМА, была отмечена более высокая смертность в сравнении с пациентами, прооперированными внутрисосудистым методом [3]. В нашей серии частота неблагоприятных исходов после эндоваскулярных вмешательств превышала таковую для прямого клипирования аневризмы, что мы объясняем относительно частым фузиформноподобным строением аневризм СМА, т.к. это препятствует адекватному расположению микроспиралей в аневризме и повышает риски развития осложнений. Радикальность для микрохирургической и внутрисосудистой операции была сопоставима и соответствовала данным ведущих исследователей [8].
Применение стентов позволило нам значительно повысить радикальность лечения наиболее сложных аневризм (100%), при этом хороший функциональный исход в эндоваскулярной группе удалось получить у 79,3% пациентов, что было сопоставимо с исходами в микрохирургической группе и данными литературы [3].
Выводы:
1. Селективное применение внутрисосудистой и внутричерепной операции повышает эффективность лечения больных с аневризмами средней мозговой артерии; применение эндоваскулярных операций после ранее проведенного внутрисосудистого или микрохирургического вмешательства повышает радикальность, не ухудшая функциональный результат.
2. Микрохирургическая операция может выполняться на большинстве аневризм СМА, не ухудшая функциональный исход и имея высокую радикальность в отдаленном периоде.
3. Селективный отбор больных на эмболизацию или микрохирургическое клипирование полностью не предупреждает развитие интра- и послеоперационных осложнений, при этом повышая радикальность. При внутрисосудистых вмешательствах преобладают тромбозы и тромбоэмболические осложнения, при внутричерепных операциях – геморрагические и инфекционные осложнения.
4. Фузиформноподобное строение аневризмы, т.е. вовлечение артериальных ветвей в шейку аневризмы, препятствует радикальности, а также повышает риск интра- и постоперационных осложнений.
5. Применение стент-ассистенции позволяет повысить эффективность лечения у больных с фузиформноподобными аневризмами средней мозговой артерии.
Библиографическая ссылка
Горощенко С.А., Асатурян Г.А., Иванов А.Ю., Петров А.Е., Рожченко Л.В. РЕЗУЛЬТАТЫ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ АНЕВРИЗМ СРЕДНЕЙ МОЗГОВОЙ АРТЕРИИ // Современные проблемы науки и образования. 2016. № 6. ;URL: https://science-education.ru/ru/article/view?id=25669 (дата обращения: 31.05.2026).



